Seroterapia Antivenenosa
Ventajas del uso de antivenenos del tipo IgG, F(ab´)2 o Fab en picaduras de escorpiones y mordeduras de serpientes
Dr. Rafael Otero
Pediatra Toxinólogo
Investigador y Asesor Programa de Ofidismo / Escorpionismo, Facultad de Medicina, Universidad de Antioquia
Resumen
Actualmente se producen 3 tipos de antivenenos en el mundo: 1) de IgG fraccionada del plasma equino hiperinmune con sulfato de amonio o ácido caprílico; 2) digeridos con pepsina para obtener fragmentos F(ab’)2 ; 3) de origen ovino y digeridos con papaína para obtener fragmentos Fab. Algunos de los factores relacionados con la neutralización veneno – antiveneno in vivo son: a) la dosis y farmacocinética del veneno; b) el intervalo entre la penetración de la toxina y la administración del anticuerpo; c) la dosis, ruta y potencia neutralizante del anticuerpo administrado; y d) la farmacocinética del antiveneno. En este artículo se presenta una revisión de los aspectos farmacocinéticos de los venenos y de los 3 tipos de antivenenos, así como también del estado actual del conocimiento en relación con la eficacia experimental y clínica de los antivenenos y de su seguridad en el tratamiento del accidente ofídico y del envenenamiento escorpiónico. Finalmente, se anexa un listado de de los antivenenos recomendados para Colombia, así como también sus características y potencia neutralizante.
Palabras clave: Antivenenos, venenos, escorpiones, serpientes, envenenamientos.
Abstract
Three types of antivenoms are currently produced in the world: 1) of whole IgG obtained from horse hyperimmune plasma fractionated either by ammonium sulphate or by caprylic acid; 2) pepsin-digested to obtain F(ab´)2 fragments; 3) ovine origin and papain-digested to obtain Fab fragments. Some of the factors involved in the in vivo venom-antibody neutralization are: a) the dose and toxicokinetics of venom; b) the interval between toxin penetration and antibody administration; c) the dose, route and potency of the antibody administered; and d) the pharmacokinetic of the antivenom. In this paper, pharmacokinetic aspects of snake and scorpion venoms and of the 3 antivenom types, are reviewed as well as the current knowledge in relation to the experimental and clinical efficacy and safety of the antivenoms in the treatment of snake bites and scorpion stings. Finally, a list of the antivenoms recommended for Colombia is additioned, as well as their characteristics and neutralizing potency.
Key words: Antivenoms, venoms, scorpions, snakes, envenomations.
Introducción
La seroterapia fue uno de los más importantes descubrimientos científicos a finales del siglo XIX. Transcurridos más de cien años desde su descubrimiento por Calmette (1894) y de la iniciación del tratamiento específico en víctimas humanas de mordeduras de serpientes (1896), la seroterapia continúa siendo la piedra angular del tratamiento de los envenenamientos causados por animales venenosos 1-4. El impacto de la seroterapia para mejorar el pronóstico de las mordeduras de serpientes ha sido apreciable; la mortalidad descendió desde 20% – 25% a comienzos del siglo XX hasta 0.6% y 0.1% en Brasil y USA, respectivamente, a finales del mismo. La mortalidad por picaduras de escorpiones disminuyó del 4% en 1980 a 0.28% y 0.05% a finales de la última década del siglo en Brasil y México, respectivamente5-8.
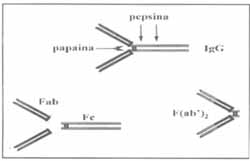
Tres tipos de antivenenos se producen actualmente en el mundo. El primero corresponde a los de IgG total obtenida del plasma equino hiperinmune mediante fraccionamiento con sulfato de amonio (precipitación de la IgG) o con ácido caprílico (ácido octanóico), este último precipita las proteínas no inmunes del plasma (fibrinógeno, albúmina, alfa y beta globulinas) mediante un procedimiento más rápido que permite obtener en el filtrado mayor cantidad de IgG y de mayor pureza 9-10. El segundo corresponde a los antivenenos de fragmentos F(ab´)2 obtenidos mediante la digestión de la IgG con pepsina y el sometimiento del plasma hiperinmune a drásticos cambios de pH, calentamiento y precipitación con sulfato de amonio. Después de la división enzimática de la IgG, la porción Fc es coagulada por calentamiento (57 oC) y los fragmentos F(ab´)2 son purificados con el fin de disminuir la incidencia de reacciones tempranas adversas (RTAs) por activación del complemento . El tercer tipo, de origen ovino, corresponde a los antivenenos de pequeños fragmentos Fab obtenidos mediante digestión enzimática de la IgG con papaína y purificación por cromatografía de afinidad. Los fragmentos Fab están desprovistos de activación del sistema del complemento 10,11 (Figura 1).
Figura No 1: Representación esquemática de los sitios de digestión enzimática de la molécula de IgG para obtener fragmentos F(ab´)2 o Fab. Modificado y adaptado de: Chippaux JP., Goyffon M. Venoms, antivenoms and immunotherapy. Toxicon 1998; 36: 823-846.
Algunos de los factores involucrados en la neutralización in vivo veneno – anticuerpo son: a) la dosis y toxicocinética del veneno; b) el intervalo entre la penetración de la toxina y la administración del anticuerpo; c) la dosis, ruta y potencia del anticuerpo administrado; d) la biodisponibilidad de sitios de unión específicos de alta afinidad (un antiveneno monoespecífico puede ser más eficiente cuando se identifica la serpiente responsable del envenenamiento; cuando no hay certeza de ello, es mejor utilizar un antiveneno poliespecífico); e) la redistribución de las moléculas de la toxina de los compartimentos profundos al compartimento del anticuerpo (vascular); f) la razón eliminación de la toxina / eliminación del anticuerpo; y g) la recirculación del anticuerpo en cada órgano 12,13.
Farmacocinética del Veneno y del Antiveneno
Si nosotros comparamos la IgG con los fragmentos F(ab´)2 y Fab, ellos difieren en: a) su masa molecular (150, 100 y 50 Kda, respectivamente); b) el volumen de distribución (1, 2 y 5 veces el volumen plasmático, respectivamente); c) el pico de concentración (Tmax) es 5-6 veces más rápido para el F(ab´)2 en el tejido superficial (1 hr) y en el tejido profundo (6 hr) que para la IgG (6 y 30 hr, respectivamente); d) la excreción de los fragmentos Fab es a través del riñón mientras que para la IgG y los fragmentos F(ab´)2 se hace a través del tejido inmune (intestino, hígado, bazo, ganglios linfáticos); e) la eliminación de los fragmentos Fab es más rápida (7-10 hr) que la de los fragmentos F(ab´)2 (60 hr) y de la IgG (> 100 hr). Por último, la porción Fc de la IgG activa el complemento por la vía clásica, mientras que los fragmentos F(ab´)2 lo hacen por la vía alterna 11, 12.
En relación con la farmacocinética del veneno y del antiveneno, se ha demostrado que los venenos de escorpiones contienen toxinas de bajo peso molecular (< 10 Kda) que se absorben rápidamente desde los sitios de inyección s.c. o i.m. y se distribuyen muy rápido hacia el compartimento tisular (Tmax = 30-60 min) donde se ejercen principalmente las acciones tóxicas. Así, el antiveneno utilizado debería poseer una rápida capacidad de distribución para neutralizar el veneno. Utilizando veneno de Leiurus quinquestriatus (escorpión amarillo de Arabia Saudita) marcado con I radioactivo, inyectado por vía s.c. en conejos, a los cuales posteriormente se les administró por vía i.v. antivenenos específicos del tipo IgG, F(ab´)2 o Fab, Ismail y Abd-Elsalam (1998) demostraron un rápido pico de concentración del veneno (Tmax= 10 min y 1.8 hr en el tejido superficial y profundo, respectivamente). La IgG alcanzaba un Tmax a los 360 min y 29-30 hr, y el F(ab´)2 a los 60 min y 6 hr, en el tejido superficial y profundo, respectivamente. Los fragmentos Fab tuvieron valores de Tmax intermedios entre la IgG y el F(ab´)2. Por esta razón los autores recomendaron el uso de antivenenos F(ab´)2 para las picaduras de escorpión y aumentar la dosis calculada para acelerar la neutralización del veneno, compensando también la lenta velocidad de distribución del antiveneno en el tejido profundo13.
Capacidad Neutralizante de los Antivenenos
Venenos de escorpiones
El veneno de Buthus occitanus tunetanus (Túnez) inyectado s.c. en conejos alcanza su máxima concentración plasmática en 30-60 min, con una eliminación total en 12-24 hr, dependiendo de la dosis de veneno 4. El antiveneno F(ab´)2 inyectado i.v. 30 min después de la inyección del veneno, produce una completa y definitiva neutralización del veneno circulante desde el fin de la infusión del mismo. La absorción del antiveneno inyectado por la ruta i.m. es incompleta y muy lenta (Tmax = 48hr), induciendo una neutralización parcial y demorada de las toxinas circulantes. Así, la rápida absorción y distribución de las toxinas de escorpiones indica que el envenenamiento escorpiónico es una emergencia médica extrema y que el antiveneno debe inyectarse por la ruta i.v. 4.
El veneno de Centruroides limpidus limpidus (México) tiene también una rápida absorción y distribución. Cuando dicho veneno marcado con I radioactivo se inyecta por vía s.c. en conejos, alcanza su máxima concentración en sangre (Tmax) en 1 hr. Si dos horas más tarde se administra un antiveneno F(ab´)2 específico por vía i.v., hay un incremento significativo en la concentración plasmática del veneno 10 min después, lo cual indica que hay una redistribución de las toxinas del veneno de escorpión desde el compartimento extravascular hacia el espacio vascular (secuestro) donde ellas son neutralizadas. La excreción urinaria de radioactividad indica que más del 90% de las toxinas de escorpiones se eliminan por esta ruta en 24 hr 14.
Datos similares fueron obtenidos con el veneno de Tityus serrulatus (Brasil) inyectado por vía s.c. en ratas (rápida absorción, rápida y alta distribución en los tejidos). Adicionalmente, se comprobó que la severidad del envenenamiento está relacionada con la concentración plasmática del veneno (ELISA), siendo más alta la concentración en pacientes con envenenamiento escorpiónico moderado/grave 7. Los niveles circulantes de antígenos desaparecen 1 hr después de la infusión de un antiveneno F(ab´)2 y altas concentraciones de anticuerpos persisten por lo menos durante 24 hrs, confirmando la eficacia de la inmunoterapia y de los fragmentos F(ab´)2 en las picaduras de escorpiones. Clínicamente, la seroterapia en Brasil también ha demostrado mejoría de los síntomas del envenenamiento desde la primera hora, con desaparición total de ellos 12-48 hr después 7.
Venenos de Serpientes
Se acepta que los venenos de serpientes de la familia Viperidae y algunos de la familia Elapidae, contienen toxinas con un peso molecular que fluctúa entre 10 y 200 Kda. Así, la absorción desde los depósitos tisulares, la distribución y la eliminación no son tan rápidas como ocurre con los venenos de escorpiones. La reabsorción total puede tardar 3 días, con altas concentraciones séricas de veneno circulantes por un largo periodo (7-10 días) tal como ha sido observado con los venenos de Vipera aspis y Naja spp 11. Por otra parte, en casos de envenenamiento por crotálidos se ha demostrado también que las concentraciones séricas de veneno son mayores en los casos graves que en los leves/moderados 15-17. Los efectos locales de los venenos de víboras (edema, hemorragia, mionecrosis) son de rápida instalación después de la inyección del veneno (4-15 min), y continúan siendo uno de los problemas sin completa solución en el tratamiento de las víctimas de estas mordeduras, por la falta de total y eficiente neutralización por parte de los antivenenos . El veneno debe neutralizarse tanto en el compartimento del anticuerpo (en el plasma) como en el compartimento tisular.
En experimentos efectuados en ratones, con princubación de veneno (Bothrops asper de Costa Rica) y antivenenos específicos ( IgG o Fab), ambos neutralizaron totalmente el efecto hemorrágico del veneno de una manera dependiente de la dosis 18. No hubo diferencias significativas en la capacidad neutralizante de ambos antivenenos. Por otra parte, siguiendo el mismo diseño de experimentos, se demostró que un antiveneno monoespecífico del tipo IgG puede tener mayor capacidad neutralizante de los efectos edematizante y desfibrinante del veneno de B. atrox de Colombia, que un antiveneno poliespecífico 19.
En experimentos con administración independiente (i.m.) del veneno (B. asper) y del antiveneno (por vía i.v.) del tipo IgG, Fab2 o Fab, se demostró que todos estos tenían eficacia parcial y similar para neutralizar el daño tisular local (edema, hemorragia, mionecrosis) inducido por el veneno, indicando que los 3 tipos de antivenenos penetraron al compartimento tisular 18,20. No obstante, la neutralización fue mejor cuando el antiveneno se administró i.v. inmediatamente después de la inyección del veneno.
Todo parece indicar que el daño inducido por el veneno en la microvasculatura favorece una extravasación similar e importante de anticuerpos IgG y F(ab´)2 en el compartimento tisular, según se ha demostrado cuantificando su concentración por ELISA en el tejido muscular 21. Cuando el veneno de B. asper se preincubó con CaNa2EDTA para inhibir las metaloproteinasas (hemorraginas) del veneno, hubo también extravasación de IgG específica y F(ab´)2 en el músculo, pero en menor concentración. No hubo diferencias significativas en la concentración de los 2 tipos de anticuerpos 21.
Experimentalmente también se ha demostrado la eficacia de estos productos para neutralizar el efecto letal del veneno. En experimentos llamados de rescate, con administración independiente del veneno de B. asper (i.p.) y del antiveneno del tipo IgG o Fab2 (i.m. o i.v.), estos últimos fueron igualmente efectivos para neutralizar la letalidad en ratones, especialmente cuando se administraron i.v. inmediatamente después de la inyección del veneno 21. Así, no hay duda de que la seroterapia debe ser administrada por vía i.v. y muy pronto después del envenenamiento ofídico para obtener buenos resultados.
Ensayos Clínicos en Mordeduras de Víboras
En varios ensayos clínico-terapéuticos aleatorizados realizados en humanos a través del mundo, se ha demostrado la eficacia de los antivenenos de IgG, F(ab´)2 y Fab para el tratamiento de las mordeduras de serpientes, permitiendo a su vez establecer su dosificación 3,15,22-26. En Colombia por ejemplo, antivenenos del tipo IgG producidos en el Instituto Clodomiro Picado de Costa Rica y en el Instituto Nacional de Salud de Bogotá, y antivenenos de fragmentos F(ab´)2 producidos en el Instituto Butantan de Sao Paulo (Brasil), fueron comparados en 3 ensayos clínico-terapéuticos aleatorizados y se demostró su eficacia para detener la progresión del envenenamiento bothrópico y mejorar algunos signos característicos tales como el edema, la hemorragia local y sistémica, y la alteración de la coagulación sanguínea. La cuantificación de las concentraciones séricas de veneno y antiveneno (ELISA) en diferentes momentos del tratamiento, también permitió hallar una dosificación racional de los antivenenos (2, 4, y 6-9 frascos en los envenenamientos leves, moderados y graves, respectivamente). No se encontraron diferencias significativas en la eficacia de los antivenenos, y los niveles séricos de veneno desaparecían desde la primera hora de la seroterapia, a menos que se hubiera administrado una dosis de antiveneno inferior a la recomendada 17,27,28.
El fenómeno de la recurrencia de signos locales de envenenamiento (edema, hemorragia), de la coagulopatía (hipofibrinogenemia), de la trombocitopenia y de la elevación de los niveles séricos de veneno, se ha descrito en el tratamiento del envenenamiento grave por crotálidos, utilizando cualquiera de los 3 tipos de antivenenos, siendo la recurrencia de la coagulopatía más frecuente (53%) con el uso de antivenenos de fragmentos Fab 15,17,26,28-30. Hay varias explicaciones posibles para el fenómeno de la recurrencia: 1) la disparidad en la cinética y dinámica del veneno y del antiveneno; 2) el antiveneno falla en neutralizar todo el veneno inicialmente; 3) el veneno no neutralizado en los depósitos tisulares puede absorberse hacia el torrente circulatorio de tal manera que eventualmente hay una concentración sérica de antiveneno insuficiente para neutralizarlo; 4) la más rápida eliminación de los fragmentos F(ab´)2 o Fab no unidos a los antígenos, en comparación con la eliminación de los componentes del veneno; 5) separación de complejos veneno/antiveneno después de su unión inicial eficaz; y 6) en algunos casos, un exceso de antiveneno no parece prevenir la recurrencia de antigenemia, porque una fracción del antiveneno no es funcional, teniendo pobre avidez por los antígenos o porque forma agregados 15,29,30.
Como el fenómeno de la recurrencia puede ocurrir principalmente en las primeras 72-96 horas del tratamiento con el uso de antivenenos IgG o F(ab´)2, los pacientes con envenenamiento grave serían reevaluados al menos cada 6-12 horas para la progresión del edema y de los signos de sangrado 15,17,31,32. La alteración de la coagulación (Tiempo de Coagulación, concentración de fibrinógeno sérico, TP, TTP) debe ser evaluada a las 6 o a las12, 24, 48, 72 y 96 horas después de la infusión del antiveneno, y el recuento de plaquetas a intervalos de 24 horas 15,31,33. Una dosis suficiente de antiveneno en accidente bothrópico conduce al cese del sangrado en las primeras 6 hrs en más del 80% de los casos, y en 12 hrs en el 100%; el edema cesa en su progresión en 12 hrs en el 80% de los casos y en 24 hrs en el 95%; la coagulación sanguínea se normaliza en 12 hrs en más del 80% de los casos, y en 24 hrs en el 100% 17,27,28. Si hubo trombocitopenia, el recuento de plaquetas se incrementará gradualmente hasta su normalización en 3-4 días, a menos que ocurra sepsis.
En los pacientes tratados con fragmentos Fab (CroFab®), la recurrencia de coagulopatía y trombocitopenia puede ocurrir hasta 14 días después de la seroterapia, siendo también más frecuente durante los primeros 3-4 días. Por la corta vida media de los fragmentos Fab, los pacientes requieren más que una dosis inicial de 6 frascos de antiveneno (dosis adicionales de 2 frascos a las 6, 12 y 18 hrs) para alcanzar una buena neutralización o mejoría de los signos de envenenamiento, y para evitar la recurrencia del edema. Además de la evaluación de la hemostasia arriba recomendada, los pacientes tratados con CroFab® deben ser reevaluados al menos una vez en 5 días después de su egreso del hospital. La administración de 2-3 frascos de cualquiera de los 3 tipos de antivenenos será suficiente en caso de recurrencia temprana o tardía 15,17,30,33.
CLIC AQUÍ Y DÉJANOS TU COMENTARIO