Obstrucción Tubárica Proximal
La anastomosis cornual se realiza en casos de obstrucción cornual. Los resultados de este procedimiento dependen de la etiología del bloqueo. Novy y colaboradores (33) demostraron canulación tubárica histeroscópica en el 50% de casos de falsos positivos de obstrucción tubárica reportados por histerosalpingografía.
La anastomosis tubo cornual bilateral está asociada con tasas de embarazo intrauterino que varían de 50% (34) a 71% (35), con tasas de embarazo ectópico de 0 a 40% (36).
Los intentos de corregir múltiples sitios de obstrucción en la trompa de Falopio (enfermedad tubárica bipolar) han producido resultados muy pobres (37). La obstrucción tubárica múltiple es una indicación para FIV y no se debe realizar tratamiento quirúrgico.
Reversión de la esterilización
La esterilización tubárica sigue siendo uno de los métodos más comunes de contracepción en el mundo; afortunadamente la reanastomosis tubárica puede restaurar la fertilidad. El éxito de la reversión de la esterilización tubárica depende de varios factores: la longitud de cada trompa al terminar el procedimiento, el tipo del procedimiento para la esterilización, la localización de la anastomosis a lo largo de la tuba, la edad de la paciente y la presencia de otro tipo de patología coexistente.
Se ha reportado que la anastomosis ístmico-ístmico es la más exitosa en cuanto a tasas de embarazo (81%), y que la longitud de las tubas en centímetros después del procedimiento, multiplicada por un factor de 10 da una aproximación de la tasa de embarazo a término (38). La esterilización con anillos de Silatic o ganchos produce poco daño a la tuba y por tanto los resultados de la reanastomosis son mejores que cuando ésta es realizada con electro cauterio; esta última técnica produce una mayor incidencia de embarazos tubáricos (39).
Cuando se compara la técnica microquirúrgica con la macroquirúrgica los resultados con la primera son definitivamente mejores cuando se realiza la anastomosis tubárica (62% frente a 44%) y la tasa de embarazo ectópico es menor (2.3% frente a 9.2%) (22). Para la paciente joven en la categoría de buen pronóstico, la anastomosis tubárica microquirúrgica ofrece excelentes resultados y la oportunidad de tener múltiples embarazos. Al contrario, la reversión de la esterilización tubárica es controversial en mujeres mayores de 40 años.
La tasa de embarazo reportada en 1992 por la Sociedad de Tecnología para la Reproducción Asistida (SART) en mujeres de 40 años y mayores sin compromiso del factor masculino fue del 7.2% (partos por ovocitos recuperados) (40). De este modo, cuando existe función ovárica normal, la decisión que se tome acerca del tratamiento debe hacerse después de un análisis cuidadoso de las posibilidades de éxito y riesgos de cada opción; de lo anterior podemos concluir que se debe realizar FIV en todas aquellas pacientes con baja probabilidad para una reanastomosis debido a una inadecuada longitud tubárica, obstrucciones cornuales por fibrosis extensa y fimbriectomía distal.
Se debe tener especial atención en el factor edad, pues con cada año que pase después de los 40 la fecundabilidad decrece drásticamente y la FIV puede ofrecer de forma inmediata una posibilidad de embarazo sin la morbilidad potencial de una cirugía abdominal.
Embarazo Ectópico y Cirugía Tubárica Reconstructiva
La asociación de cirugía tubárica y embarazo tubárico es bien reconocida. El embarazo tubárico resulta de una demora en el tránsito del embrión a través de la trompa de Falopio.
El riesgo de embarazo ectópico después de una cirugía tubárica es variable y depende de la condición previa de la trompa, del tipo de procedimiento realizado, la técnica utilizada y la pericia del cirujano. Reparaciones quirúrgicas imperfectas pueden originar la formación de sacos de mucosa ciegos, lo cual puede ser causa de un atrapamiento del óvulo que predispone a la paciente a un embarazo ectópico. Igualmente, las adherencias peritubáricas, que a menudo suelen ser una secuela de cirugía, pueden restringir la motilidad tubárica y de esta forma interferir con la captación y el transporte del óvulo.
Pacientes con historia de embarazo ectópico tienen un riesgo mayor de recurrencia. El riesgo de embarazo ectópico recurrente después de salpinguectomía en una mujer que desea fertilidad es del 15.4% y el de embarazo uterino de un 36.5% (41).
En la actualidad son utilizados comúnmente procedimientos quirúrgicos que hacen todo lo posible por conservar la trompa de Falopio al momento de remover el embarazo ectópico. La elección del procedimiento en pacientes con embarazo ectópico, hemodinámicamente estables, que desean preservar su potencial reproductivo, es realizar una salpingostomía lineal mediante laparoscopia quirúrgica (42-44). Las tasas de embarazo ectópico recurrente no son diferentes de aquéllas a las que se les realizó salpinguectomía. Son de particular preocupación las mujeres que han tenido embarazos ectópicos múltiples. La alta posibilidad de repetir un embarazo ectópico, y las bajas tasas de embarazo intrauterino en este grupo, nos hacen sugerir con firmeza que el tratamiento de elección es FIV, previa salpinguectomía profiláctica (41-44).
Resultados en Reproducción Asistida
Tasas acumulativas de embarazo
Para dar a las parejas alternativas aceptables de tratamiento, el cirujano ginecólogo debe estar familiarizado con las tasas de éxito de los diferentes procedimientos, y con las variables comprometidas en un estimativo real de las posibilidades de embarazo. Los datos reportados en 1992 por la Sociedad de Tecnología en Reproducción Asistida (SART) FIV-TE (embriones transferidos) (40) muestran que la tasa de partos por aspiración en 37.164 ciclos estimulados para FIV, GIFT y ZIFT fueron 16.8%, 26.7 y 22.8% respectivamente; además, de 5.324 embriones crío-preservados y transferidos se obtuvo una tasa de partos del 11.5%.
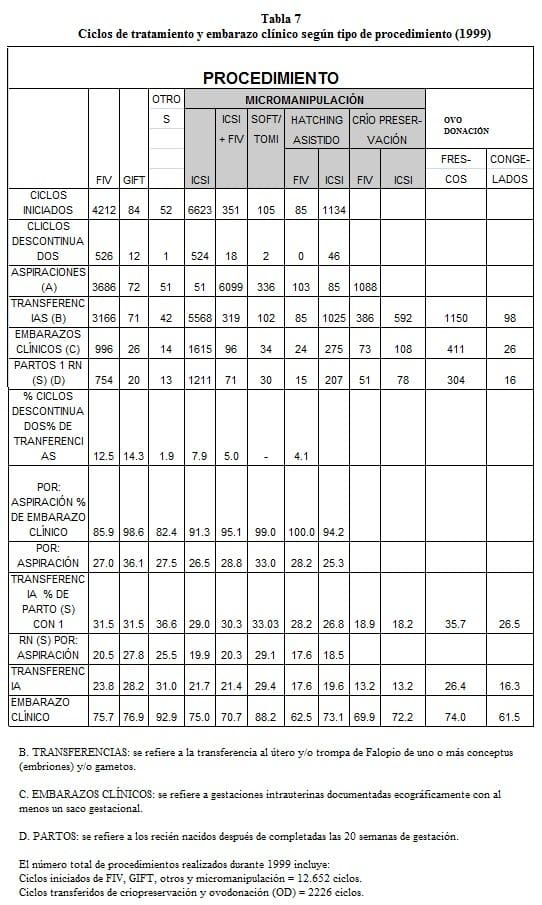
Las tasas de embarazo reportadas por el Registro Latinoamericano de Reproducción Asistida (44) muestran los siguientes resultados (Tabla 7).
A. ASPIRACIONES: se refiere a aspiraciones foliculares transvaginales y laparoscopias, independientemente de la recuperación de ovocitos.
B. TRANSFERENCIAS: se refiere a la transferencia al útero y/o trompa de Falopio de uno o más conceptus (embriones) y/o gametos.
C. EMBARAZOS CLÍNICOS: se refiere a gestaciones intrauterinas documentadas ecográficamente con al menos un saco gestacional.
D. PARTOS: se refiere a los recién nacidos después de completadas las 20 semanas de gestación.
El número total de procedimientos realizados por la Red durante 1999 incluye:
• Ciclos iniciados de FIV, GIFT y otros: 4.348 con tasas de embarazo clínico por aspiración de 27.0, 36.1 y 27.5% respectivamente.
• Ciclos aspirados de ICSI, ICSI + FIV, ICSI + GIF, Hatching Asistido: 8.298 con tasas de embarazos por aspiración de 26.5, 28.8, 33.0 y 26.8% respectivamente.
• Ciclos transferidos de crío preservación y ovodonación (OD): 2.236 con tasa de embarazo del 18.6% por trasferencia de embriones criopreservados, del 35.7% para óvulos donados frescos y 26.5% para óvulos congelados.
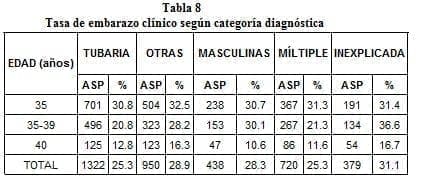
Del reporte de la Red Latinoamericana encontramos que las tasas acumulativas de embarazo clínico de parejas con factor tubárico (34.7%) como causa de infertilidad tratadas con FIV es del 25.3% en 1.322 aspiraciones. Al relacionar las tasas de embarazo con la edad se encontró lo siguiente: pacientes menores de 35 años, 30.8%; entre 35-39 años, 20.8%; de 40 años o más, 12.8% (Tabla 8).
Es importante anotar que el estado de la enfermedad tubo ovárica o la historia de adherencias pélvicas o cirugía tubárica no parece tener un impacto significativo sobre la eficiencia del FIV. No obstante, se observa una disminución significativa en las tasas de embarazo en pacientes con factor tubárico como causa de infertilidad tratadas con FIV cuando se compararon los diferentes grupos de edad.
El factor edad
Uno de los factores pronósticos más importantes de la fertilidad humana es la edad de la mujer (45).
La disminución de la fertilidad de las parejas casadas con el avance de la edad ha sido documentada en forma repetida (46). Con seguridad se puede decir que un tercio de las mujeres que difieren el embarazo hasta mediados o finales de sus 30 años tienen problemas de fertilidad, y por lo menos la mitad de las mujeres por encima de los 40 años de edad experimentan problemas para concebir. Esta disminución en la fertilidad se inicia por lo menos 15 años antes de la menopausia; durante este periodo los ciclos menstruales son regulares, pero se observa un acortamiento estable del ciclo menstrual, debido a una fase folicular corta (47). Con el acortamiento de los ciclos al final de los 30 años se produce un incremento sutil pero real de la FSH, y una disminución de los niveles de inhibina (48). Estos cambios se asocian a menudo a un crecimiento folicular acelerado, aunque al mismo tiempo se desarrollan pocos folículos por ciclo; finalmente ocurre la menopausia porque el abastecimiento de folículos se agota.
La disminución de la fecundidad femenina con la edad se ha observado en FIV y en otras técnicas de reproducción asistida (49-50). Muchos programas de reproducción asistida han establecido una edad límite basados en el pronóstico marcadamente pobre para mujeres por encima de los 40 años a causa de las bajas tasas de embarazo y a un incremento en el riesgo de aborto espontáneo (51).
A diferencia de los hombres, las mujeres están dotadas de un número finito no reemplazable de células germinales que alcanzan el pico máximo a la mitad de la gestación (52).
El número absoluto y la capacidad funcional de los folículos y células germinales comprende lo que podemos llamar la reserva ovárica, lo cual afecta su respuesta a la estimulación y su posibilidad de éxito. Se han descrito varias pruebas para evaluar la reserva ovárica en forma indirecta entre éstas se incluyen:
Pruebas estáticas, que se caracterizan por la determinación en situación basal (día tres del ciclo) de una determinada sustancia (52-60): FSH, estradiol sérico (E2) e inhibina B. Pruebas dinámicas, que se caracterizan por la determinación de FSH y E2 antes y después de someter al eje hipotálamo-hipófisis a un estímulo específico (56-61): El Efort (Exogenous FSH Ovarian Reserve Test) y la prueba del clomifeno. Estas pruebas se deben realizar en todas las mujeres mayores de 35 años, ya que a partir de esta edad existe la mayor proporción de pacientes con baja respuesta a la estimulación ovárica; no obstante, no todas presentaran una baja respuesta a la hiperestimulación ovárica controlada. Por otro lado, la calidad ovocitaria desciende con la edad (62).
Se define como baja respondedora a una mujer con ciclos ovulatorios espontáneos completamente normales (se excluyen todas las que presentan alteraciones menstruales asociadas a un desarrollo folicular anormal, como el síndrome de ovario poliquístico y la premenopausia), que responde a los protocolos habituales de inducción de ovulación con menos de tres a seis folículos en, al menos, dos ciclos consecutivos de estimulación (un sólo ciclo de baja respuesta puede obedecer a motivos ajenos al funcionamiento del ovario). Un estradiol (E2) menor de 500 pg/ml tras finalizar un ciclo de hiperestimulación ovárica controlada, podría indicar un ciclo de baja respuesta, pero en la actualidad es un parámetro poco útil en la clínica.
Determinación de la FSH sérica
La FSH sérica tiene un valor predictivo de los resultados de éxito de la FIV, de manera que mujeres con FSH basal mayor de 20 mUl/ml el día tres del ciclo tiene mal pronóstico (54). Incluso se ha comprobado que la FSH se correlaciona mejor que la edad con la probabilidad de éxito de la FIV (55).
El E2
La elevación del E2 en el día tres del ciclo menstrual es indicador de un pronóstico pobre y se debe al aumento en la secreción de la FSH en la fase lútea del ciclo anterior, lo que produce una foliculogénesis acelerada y, por consiguiente, niveles de E2 mayores de 30 pg/ml.
Debido a la variabilidad entre laboratorios, se recomienda la determinación de estos valores en dos ocasiones diferentes antes de tomar una decisión clínica.
La inhibina B
La inhibina B una glucoproteína secretada directamente por las células de la granulosa del folículo, sus niveles son variables durante el ciclo menstrual, y presenta niveles más bajos en mujeres mayores de 35 años sometidas a hiperestimulación ovárica controlada; por esta razón es indicador sensible de la vitalidad de los folículos en crecimiento (59-60).
Seifer y colaboradores (58) demostraron que las mujeres con niveles séricos basales de inhibina B menores de 45 pg/ml el día tres tenían malas respuestas a la hiperestimulación ovárica controlada que aquéllas con niveles de inhibina B mayores o iguales a 45 pg/ml.
El Efort
Consiste en medir los niveles basales de FSH y E2 administrando a continuación 300 UI de FSH el día tres del ciclo, midiendo de nuevo FSH y E2 sérico a las 24 horas. Si la FSH es mayor de 11 mUI/ml y/o el incremento de E2 es menor de 30 pg/ml se habla de un Efort patológico; pero si la FSH es menor de 11 mUI/ml y/o el incremento de E2 es mayor de 30 pg/ml, se habla de un Efort normal (56). Esta prueba tiene un alto valor predictivo: el 90% de las mujeres con un Efort normal mostraron una respuesta óptima a la estimulación ovárica controlada; por el contrario, con un Efort patológico, el 81% de las pacientes presentaron respuestas bajas (56).
Prueba de clomifeno
Ésta ha sido diseñada para explicar situaciones clínicas confusas, en las que mujeres con respuesta baja a la hiperestimulación ovárica controlada presentan niveles basales de FSH normales o ligeramente elevados (menores de 20 mUI/ml) (53, 57).
La prueba consiste en medir la FSH sérica el día tres del ciclo, y estimular a la mujer con 100 mg/diarios de citrato de clomifeno durante los días cinco al nueve del ciclo, y determinar nuevamente la FSH el día 11 del ciclo. Si la sumatoria de las dos FSH es mayor de 26 mUI/ml se debe considerar que la paciente está en falla ovárica.
La relación entre concentraciones elevadas de FSH y los resultados de la FIV es sorprendente. El efecto se observa en el patrón de la respuesta ovárica a la estimulación, tasas de embarazo y eficiencia en la implantación.
Los resultados de tasas de embarazo por aspiración caen de un 21.1% en mujeres con FSH menores de10 mU/ml el día tres del ciclo a 8.3% en mujeres con niveles basales de FSH por encima de 20 mUI/ml (64).
Parece que el mayor obstáculo para la concepción natural en la mujer mayor está relacionado con una disminución en la implantación del embrión: la tasa de implantación por embrión diminuye de 29% en mujeres menores de 34 años, a 21.8% en mujeres de 34 años, con una disminución lineal hasta 2.2% por embrión transferido a los 44 años (64).
En las mujeres agonadales que reciben embriones de donantes jóvenes su tasa de embarazo es de la más alta observada en reproducción asistida, sugiriendo que la disminución en la tasa de implantación con la edad avanzada está claramente relacionada con la pobre calidad del oocito (65). Hay gran cantidad de evidencia que demuestra que embriones obtenidos de mujeres de 40 años a los cuales se les a realizado diagnóstico genético preimplantación presentan con gran frecuencia aneuploidias (66). Estos hallazgos son consistentes con las observaciones realizadas en pacientes de FIV, quienes presentan alta tasa de abortos espontáneos con la edad avanzada (67).
Debido a la rápida disminución de la fertilidad en mujeres sobre los 40 años de edad, a éstas se les debe realizar una evaluación rápida. La determinación de FSH y E2 el día tres del ciclo es de gran ayuda cuando se trata de aconsejar a la paciente acerca de reales posibilidades de embarazo o de dirigirla con niveles altos de gonadotropinas a recibir óvulos de una donante.
La reparación quirúrgica o laparoscópica de la enfermedad tubárica se debe cuestionar seriamente en aquellas mujeres que están al final de la década de los 30, en quienes (aún cuando los niveles de gonadotropinas estén normales el día tres a la evaluación inicial) la reserva ovárica puede declinar, disminuyendo la posibilidad de un embarazo exitoso. En este grupo particular de pacientes creemos que los esfuerzos se deben dirigir a un método de reproducción asistida que podría proporcionar una mayor posibilidad de éxito en un intervalo de tiempo corto.
Discusión
La infertilidad tubárica debida a causas infecciosas va en aumento, esto ha causado un creciente interés en la cirugía reconstructiva. En la década pasada se observó un cambio en el tratamiento quirúrgico de los desórdenes tuboperitoneales. La laparoscopia quirúrgica y las técnicas microquirúrgicas prácticamente han reemplazado a la laparotomía. Como quiera que sea, la evolución de la microcirugía a la laparoscopia tomó lugar sin estudios prospectivos randomizados. El papel de las técnicas de reproducción asistida en la infertilidad tubárica no ha sido aún determinado de manera prospectiva controlada.
Toda pareja infértil, con factor tubo peritoneal comprometido, debe ser estudiada en forma completa, esto incluye espermograma, evaluación de los niveles basales de FSH el día tres del ciclo, histerosalpingografía y laparoscopia diagnóstica. Estos estudios son decisivos para determinar si la pareja se refiere a programa de cirugía tubárica reconstructiva o al programa de técnicas de reproducción asistida.
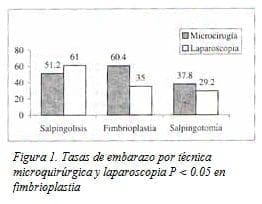
Se ha demostrado el papel de la adhesiolisis en favorecer la fertilidad. Tulandi y colaboradores (11) mostraron que la salpingoovariolisis favorece la posibilidad de embarazo en un factor de tres. No se encontraron diferencias significativas en los resultados después de realizar la salpingoovariolisis por microcirugía o laparoscopia. Las tasas acumulativas de embarazo después de dos años de seguimiento están entre 50 y 60% (Fig. 1).
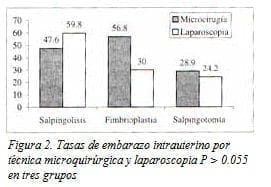
Las tasas de embarazo intrauterino son ligeramente más altas con el manejo laparoscópico, aunque esto no es estadísticamente significativo (Fig. 2).
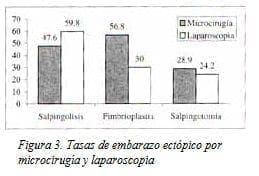
No se encontraron diferencias en las tasas de embarazo ectópico (Fig. 3).
Si las adherencias son el único factor de infertilidad demostrable, la salpingoovariolisis laparoscópica debe ser el tratamiento de elección; no obstante los resultados están relacionados con la extensión de las adherencias. Hulka (21) demostró que pacientes a las que se les realizó salpingoovariolisis microquirúrgica de adherencias laxas (avasculares) alcanzaron una tasa de embarazo del 47% frente a 0% en pacientes con adherencias extensas (densas y vasculares), por tanto estas últimas pacientes deben ir directamente al programa de reproducción asistida.
Cuando existe obstrucción tubárica distal parcial, asociada con aglutinación de la fimbria o fimosis, el procedimiento a realizar es una fimbrioplastia.
En nuestra revisión encontramos un incremento estadístico de embarazo en favor de la fimbrioplastia por microcirugía (Fig. 1).
Los resultados en términos de embarazo intrauterino después de salpingolisis y fimbrioplastia por microcirugía son similares (Fig. 2).
El embarazo ectópico ocurre con una frecuencia tres veces mayor en grupos de fimbrioplastia por laparoscopia (Fig. 3). La razón para esta diferencia no es clara; se podría esperar una tasa grande de embarazo ectópico en los dos grupos por el compromiso endosalpingueal presente en ambos, pero posiblemente la restauración anatómica es mucho más precisa en la microcirugía que en la laparoscopia.
Cuando un hidrosalpinx está presente se debe realizar una salpingoneostomía. Usualmente se encuentra un compromiso severo de la mucosa tubárica, resultando en tasas bajas en embarazo. No se encontraron diferencias en los resultados (tasa de embarazo uterino y ectópico) con el manejo realizado por microcirugía o laparoscopia. Estos resultados dependen del estado anatómico y la integridad funcional de las trompas de Falopio. Muchas clasificaciones toman estos dos factores en cuenta.
Mage y colaboradores (67) clasifican los pacientes de acuerdo con la extensión de las adherencias perianexales y al estado de la tuba. Esta clasificación tiene fundamento en el tipo y grado de compromiso de las adherencias ováricas. La apariencia tubárica es evaluada con base en el aspecto de los pliegues de la mucosa a la histerosalpingografía y el aspecto de la pared salpingueal (puntajes de I a IV, el I es mejor). La clasificación de la American Fertility Society (1988) se basa en la mucosa tubárica, paredes de la tuba, tamaño del hidrosalpinx, tipo de adherencias y área comprometida.
En una serie de 81 pacientes a los cuales se les realizó salpingoneostomía por laparoscopia, Dubuisson y colaboradores (68) encontraron una tasa de embarazo del 60% en el grupo I y 0% en el grupo IV de acuerdo con el puntaje tubárico asignado por Mage y colaboradores (67). Estos autores recomiendan realizar salpingoneostomía en pacientes con daño tubárico mínimo y limitado, mientras que pacientes con daño tubárico severo se les debe aconsejar FIV.
Por otra parte, diversos autores puntualizan que similarmente a la salpingoovariolisis, la severidad de la patología tubárica preexistente y la extensión de las adherencias tubáricas juegan un papel que afecta las tasas de éxito.
El diámetro del hidrosalpinx es también un factor pronóstico importante. Singhal y colaboradores (69) encontraron tasas de nacimiento significativamente bajas en pacientes con hidrosalpinx mayores de 20 mm de diámetro comparado con aquéllos de diámetro menor de 20 mm; de estos resultados se concluyó que este factor negativo es una consecuencia directa de una disminución de las células ciliadas del lumen tubárico distal.
El FIV con transferencia de embriones (TE) es una amplia alternativa disponible a la cirugía tubárica reconstructiva.
La pregunta que persiste es ¿a cuáles parejas se les debe ofrecer cirugía de infertilidad o técnicas de reproducción asistida?
Las tasas de embarazo clínico después de FIV-TE en pacientes con factor tubárico varía entre 30.8 y 12.8%, dependiendo de la edad de la paciente, siendo las mejores tasas en mujeres menores de 35 años y bajas en mujeres de 40 años y más (45).
Benadiva y colaboradores2 estudiaron en forma retrospectiva la tasa de embarazo acumulativo en parejas con factor tubárico como causa de infertilidad; la tasa de parto total en pacientes con factor tubárico como causa exclusiva de infertilidad por transferencia fue de 30.1% en 491 pacientes (673 aspiraciones). Ellos demostraron que otros diagnósticos de infertilidad secundarios (anovulación, endometriosis, factor masculino, inmunológico) no afectan las tasas de embarazo (26% en 371 aspiraciones) en forma significativa después de FIV _TE.
La tasa de embarazo acumulativa después de cuatro ciclos fue mayor del 70% en ambos grupos. Se observó una tasa de aborto del 2.4%.
Se debe tener especial cuidado en pacientes con grandes hidrosalpinx. Los resultados de FIV- ET se ven afectados negativamente por el flujo retrógrado del líquido del hidrosalpinx a la cavidad uterina. La implantación se puede deteriorar por el efecto tóxico sobre el endometrio (70).
Si la cirugía reconstructiva es de mal pronóstico, se debe realizar salpinguectomía o ligadura en estas pacientes antes de iniciar técnicas de reproducción asistida.
Cuando consideramos las tasas acumulativas de embarazo después de cuatro ciclos de técnicas de reproducción asistida o salpingoovariolisis, fimbrioplastia o salpingoneostomía (Fig. 1), la primera da mejores resultados en cada uno de los frentes; sin embargo, podría ser un error pronosticar que la cirugía reconstructiva vaya a ser historia pronto. En primer lugar, si la cirugía es exitosa ésta ofrece la posibilidad de concebir en múltiples ciclos y lograr múltiples embarazos en forma consecutiva. El riesgo de embarazo múltiple es bajo después de tratamiento quirúrgico.
El factor económico también puede pesar al momento de tomar la decisión; en Colombia el costo de un tratamiento de reproducción asistida (FIV-TE) está entre $7.000.000 y $9.000.000, y una cirugía reconstructiva está en el promedio de $4.000.000; el dilema está en seleccionar la paciente que tiene buen pronóstico quirúrgico.
El objetivo principal es determinar la técnica más eficaz con las mínimas complicaciones para cada pareja a fin de obtener un embarazo en el tiempo mínimo posible. La edad de la paciente y los niveles basales de la FSH juegan un papel importante en la decisión.
Los resultados anteriores sugieren que las mujeres jóvenes, con disturbio tuboperitoneal leve o moderado, son candidatas primarias para cirugía tubárica reconstructiva, mientras mujeres de edad mayor con enfermedad severa o pelvis congelada deben ser dirigidas inmediatamente al programa de reproducción asistida.
Resultados comparables se han obtenido en salpingoovariolisis y salpingoneostomías realizadas por laparoscopia o microcirugía, haciendo que el manejo laparoscópico sea el preferible; en el caso de ser necesaria una fimbrioplastia se debe considerar preferentemente realizarla por laparotomía microquirúrgica.
Las anteriores conclusiones se fundamentan en datos retrospectivos. No hay estudios randomizados sobre una base prospectiva, que comparen las tasas de embarazo después de una microcirugía o una laparoscopia quirúrgica y reproducción asistida en parejas con obstrucción tubárica demostrada y espermograma normal.
Referencias Bibliográficas
1. Lilford RJ, Watson AJ. Has in vitro fertilisation made salpingostomy obsolete? Br J Obstet Gynecol 1990; 97: 557-560.
2. Benadiva CA, Kligman I, Davis O, Rosenwaks Z. In vitro fertilisation versus tubal surgery: is pelvic reconstructive surgery obsolete? Fertil Steril 1995; 64: 1051-1061.
3. Speroff L, Glass RM, Kase NG. Female infertility. In: Clinical gynaecologic endocrinology and infertility, 5th Ed. Williams and Wilkins. Baltimore 1994; 809-839.
4. Trimbos _ Kemper T, Trimbos B, Van Hall E. Etiological factors in tubal infertility. Ferti Steril 1982; 37: 384-388.
5. Westron L. Incidence, prevalence and trends of acute pelvic inflammatory disease and its consequences in industrialised countries. Am J Obstet Gynecol 1980; 138: 880-892.
6. Urman B, Gomel V, McComb P, Lee N. Midtubal occlusion: aetiology, management and outcome. Fertil Steril 1992; 57: 747-750.
7. Sulak PJ, Letterie GS, Coddington CC, Hayslip CC, Woodward JE, Klein TA. Histology of proximal tubal occlusion. Fertil Steril 1987; 48: 437-440.
8. Gomel V. Salpingoovariolisis by laparoscopy in infertility. Fertil Steril 1983; 40: 607-611.
9. Fayez JA. An assessment of the role of operative laparoscopy in tuboplastia. Fertil Steril 1983; 39: 476-479.
10. Bowman MC, Cook ID. Comparison of fallopian tube intraluminal pathology as assessed by salpingoscopy with pelvic adhesions. Fertil Steril 1994; 61: 464-469.
11. Tulandi T, Collins JA, Burrows E, Jarrel JF, Mc Innes RA, Wrixon W, Simpson CW. Treatment dependent and treatment independent pregnancy among women with periadnexal adhesions. Am J Obstet Gynecol 1990, 162: 354-357.
12. Frantzen C, Schlosser HW. Microsurgery and post infectious tubal infertility. Fertil Steril 1982; 38: 397-402.
13. Fayez JA, Suliman SO. Infertility surgery of the oviduct: comparison between macrosurgery and microsurgery. Fertil Steril 1982; 37: 73-78.
14. Donnez J, Casanas-Roux F. Prognostic factors of fimbrial microsurgery. Fertil Steril 1986; 46: 200-204.
15. Tulandi T. Salpingoovarilysis: a comparison between laser surgery and electrosurgery. Fertil Steril 1986; 45: 489-491.
16. Watson AJS, Gupta JK, O’ Donovan P, Dalton ME, Lilford RJ. The results of tubal surgery in the treatment of infertility in two non _specialist hospital. Br J Obstet Gynecol 1990; 97: 561-568.
17. Marama R, Rizzi M, Muzii L, Catalano GF, Carvana P, Mancuso S. Correlation between the American Fertility Society Classifications of adhnexal adhesions and distal tubal occlusion, salpingoscopy and reproductive outcome in tubal surgery. Fertil Steril 1995; 64: 924-929.
18. Donnez J, Nisolle M, Casanas-Roux F. CO2 laser laparoscopy in infertility women with tubal occlusion. J Gynecol Surg 1989; 5: 47-53.
19. Siegler AM, Kontopoulos V. An analysis of macrosurgical and microsurgical techniques in the management of the tuboperitoneal factor in infertility. 1979; 32: 377-382.
20. Caspi E, Halperin Y. Surgical management of periadnexal adhesions. Int J Fertil 1981; 26: 49-54.
21. Hulka JF. Adnexal adhesions: a prognostic staging and classification system based of five year survey of fertility surgery results at Chapel Hill, North Carolina. Am J Obstet Gynecol 1982; 144: 141-148.
22. Lavy G, Diamond MP, De Cherney AH. Ectopic pregnancy: its relationship to tubal reconstructive surgery.
23. Dubuisson JB, Bouquet de Jolienere J, Aubriot FX, Darai E, Foulot H, Mandelbrot L. Terminal tuboplasties by laparoscopy: 65 consecutives cases. Fertil Steril 1990; 54: 401-403.
24. Gomel V. Salpingostomy by microsurgery. Fertil Steril 1978; 29: 380-387.
25. Tulandi T, Farag R, Mcinnes RA. Reconstructive surgery for hidrosalpinx and without the carbon dioxide laser. Fertile Steril 1984; 42: 839-845.
26. Mage G, Bruhat MA. Pregnancy following salpingostomy: comparison between CO2 laser and electrosurgery procedures. Fertil Steril 1983; 40: 472-478.
27. Tulandi T, Bugnah M. Operative laparoscopy: surgical modalities. Fertil Steril 1995; 63: 237-245.
28. Rock JA, Katayana KP, Martin EJ. Factors influencing the success of salpingostomy techniques for distal fimbrial obstruction. Obstec Gynecol 1978; 52: 591-596.
29. Young PE, Egan JE, Barlow J. Recostructive surgery for infertility at the Boston Hospital for women. Am J Obstet Gynecol 1970; 108: 1092-1098.
30. Debruyne F, Puttemans P, Boeckx W. The clinical value of salpingoscopy in tubal infertility. Fertil Steril 1989; 51: 339-346.
31. Audibert F, Hedon B, Arnal F. Therapeutic strategies in tubal infertility with distal pathology. Human Reprd 1991; 6: 1439-1445.
32. Marana R, Quagliarello J. Distal tubal occlusion: microsurgery versus in vitro fertilisation a review. Int. J Fertil 1988; 33: 107-114.
33. Novy MJ, Thurmond AS, Patton P. Diagnosis of cornual obstruction by transcervical fallopian tube cannulation. Fertil Steril 1986; 46: 21-27.
34. Kerin JF, Surrey ES, Williams DB. Falloscopic observations of endotubal isthmic plugs as a causal of reversible obstruction and their histological characterisation. J Lparoscopic Surg 1991; 1:103-109.
35. Gomel V. Tubal reanastomosis by microsurgery. Fertil Steril 1977; 28: 59-65.
36. Lavy G, Diamond MP, DeCherney AH. Pregnancy following tubocornual anastomosis. Fertil Steril 1986; 46: 21-27.
37. Patton PE, William TJ, Coulan CB. Results of microsurgical reconstruction in patients with combined proximal and distal tubal occlusion: double obstruction. Fertil Steril 1987; 48: 670-677.
38. Henderson SR. The reversibility of female sterilisation with the use of microsurgery: a report on 102 patients with more than one year of follow _ up. Am J Obstet Gynecol 1984; 149: 57-64.
39. Rock JA, Bergquist CA, Zacur HA. Tubal anastomosis following unipolar cautery. Fertil Steril 1982; 37: 613-620.
40. Society For Assisted Reproductive Technology, The American Fertility Society: Assisted Reproductive Technology in the United States and Canada: 1993 results generates from The American Fertility Society /Society for Assisted Reproductive Technology Registry. Fertil Steril 1994; 62: 1121-1131.
41. Olsner G, Tarlatzis BC, Radical surgery for estrauterine pregnancy. In: Ectopic Pregnancy, De Cherney AH, editorial. Rockville, MD. Aspen Publishers. 1986: 127-132.
42. Bruhat MA, Manhes H, Mage G. Treatment of ectopic pregnancy by means of laparoscopy. Fertil Steril 1980; 33: 411-416.
43. Saavedra JS, Navarro NH, Díaz C. Embarazo ectópico: manejo ambulatorio. Rev Col de Obs y Ginecol 2001; 52: 79-85.
44. Registro Latinoamericano de Reproducción Asistida. Zegers F, Gadalmes V, Balmaceda J. Ciclos de tratamiento y embarazo clínico según tipo de procedimiento 1999.
45. Tietze C. Reproductive span and rate reproduction among Hutterite women. Fertil Steril 1957; 8: 59-64.
46. Menken J, Trussell J, Larsen U. Age and infertility. Science 1986; 233: 1389-1395.
47. Sherman BM, Korenman SG. Hormonal Characteristics of human menstrual cycle throughout reproductive live. J Clin Invest 1975; 55: 699-705.
48. Lenton EA, Dekretser DM, Woodward AJ. Inhibin concentrations throughout the menstrual cycle of normal, infertile and older women compared with those during spontaneous conceptions cycles. J Clin Endocrinol Metab 1991; 73: 1180-1186.
49. Sharma V, Riddle A, Mason BA. An analysis of a clinical pregnancy in an ultrasound based ambulatory in vitro fertilisation program. Fertil Steril 1988; 49: 468-474.
50. Piette C, De Mouzon J, Buchelot A. In vitro fertilisation: influence of women’s age on pregnancy rates. Human Reprod 1990; 5: 56-62.
51. Romeu A, Muasher SJ, Acosta AA. Results of in vitro fertilisation attempts in women 40 years of age and older: The Norfolk experience. Fertil Steril 1987; 47: 130-137.
52. Navot D, Rosenwaks Z, Margalioth EJ. Prognostic assessment of female fecundity. Lancet 1987; 19: 645-651.
53. Toner JP, Philput CB, Jones GS, Muasher SJ. Basal follicle stimulating hormone levels is a better predictor of in vitro fertilisation performance than age. Fertil Steril 1991; 55: 784-791.
54. Muasher SJ, Oehninger S, Simonetti S. The value of basal and/or stimulated serum gonadotropin levels in the prediction of stimulation response and in vitro fertilisation outcome. Fertil Steril 1988; 50: 298-307.
55. Fanchin R. De Ziegler D, Olivennes. Exogenous follicle stimulant hormone ovarian reserve test (Efort): a simple a reliable screening test for detecting poor responders in vitro fertilisation. Human Reprod 1994; 9: 1607-1611.
56. Richard T, Scott Jr MD. Evaluation and treatment of low responders. Sem Reprod Endocrinol 1996; 14: 317-337.
57. Scott RT, Leonardi MR, Hoffman GE. Prospective evaluation of clomiphene citrate challenge test screening in the general infertility population. Obstet Gynecol 1993; 82: 539-545.
58. Seifer DB, Lambert-Messerlian G, Hogan JW, Gardiner AC, Blazar AS, Berk CA. Day 3 serum inhibin_B is predictive of assisted reproductive technologies outcome. Fertil Steril 1997; 67: 110-114.
59. Balash J, Creus M, Fabregues F, Carmona F. Inhibin, follicle stimulant hormone, and age as predictors of ovarian response in invitro fertilisation cycles stimulated with gonadotropin- realising hormone agonist-gonadotropin treatment. Am J Obstet Gynecol 1996; 175: 1226-1230.
60. Loumaye E, Billion JM, Mine JM. Prediction of individual response to controlled ovarian hiperestimulation by means of clomiphene citrate challenge test. Fertil Steril 1990; 53: 295-301.
61. Levy T, Limor R, Villa Y, Eshel A, Eckstein N, Vagman I, Lidor A, Ayalon D. Another look at co-treatment with growth hormone and human menopausal gonadotropins in poor ovarian responders. Human Reprod 1993; 6: 834-849.
62. Battaglia DE, Goodwing P, Klein NA, Soules MR. Influence of maternal age on meiotic spindle assembly in oocytes fron naturally cycling women. Human Reprod 1996; 11: 2217-2222.
63. Benadiva AC, Kleigman I, Rosenwaks Z. Assisted Reproductive Technology versus tubal surgery in Operative Gynaecology Endoscopy. Joseph S, Sanfilipo and Ronald L Levine, editor. 1989; 278-305.
64. Navot D, Bergh PA, Williams MA. Poor oocyte quality rather than implantation failure is a cause of age related decline in female infertility. Lancet 1991; 337: 1375-1381.
65. Munne S, Alikani M, Tomkin G. Embryo morphology, developmental rates and maternal age are correlated with chromosome abnormalities. Fertil Steril 1995; 64: 382-389.
66. Padilla SL, García JE. Effect of maternal age and number of in vitro fertilisation procedures on pregnancy outcome. Fertil Steril 1989; 52: 270-276.
67. Mage G, Pouly JL, Bouquet de Joliniere J, Chabrand J, Riouallon A, Bruhat MA. A preoperative classification to predict the intrauterine and ectopic pregnancy rates after distal tubal microsurgery. Fertil Steril 1896; 46: 807-810.
68. Dubuisson JB, Chapron C, Morice P, Aubriot FX, Foulot H, Bouquet de Joliniere J. Laparoscopic salpinguectomy fertility results according to the tubal mucosal appearance. Human Reprod 1994; 9: 334-339.
69. Singhal V, Li TC, Cooke ID. An analysis of factors that influencing the outcome of 232 consecutives tubal microsurgery cases. Br J Obstet Gynaecol 1991; 98: 628-636.
70. Meyer WR, Beyler SA. Deleterious effects of hidrosalpingues on in vitro fertilisation and endometrial integrin expression. Ass Reprod Rev 1995; 5: 201-203.
CLIC AQUÍ Y DÉJANOS TU COMENTARIO