1Dr. Jorge Luis Zambrano V. 1Dr. Víctor Cotrino B. 1Dra. Claudia
Jiménez E. 1Profesor Asistente. Facultad de Medicina Veterinaria
y de Zootecnia Universidad Nacional de Colombia. 2Dra. Mariana
Romero. 2 Bacteriologa. Laboratorio Médico Veterinario L.M.V.
3Dr. Bernardo Guerrero. 3 Médico Veterinario. Laboratorios Pfizzer.
Resumen
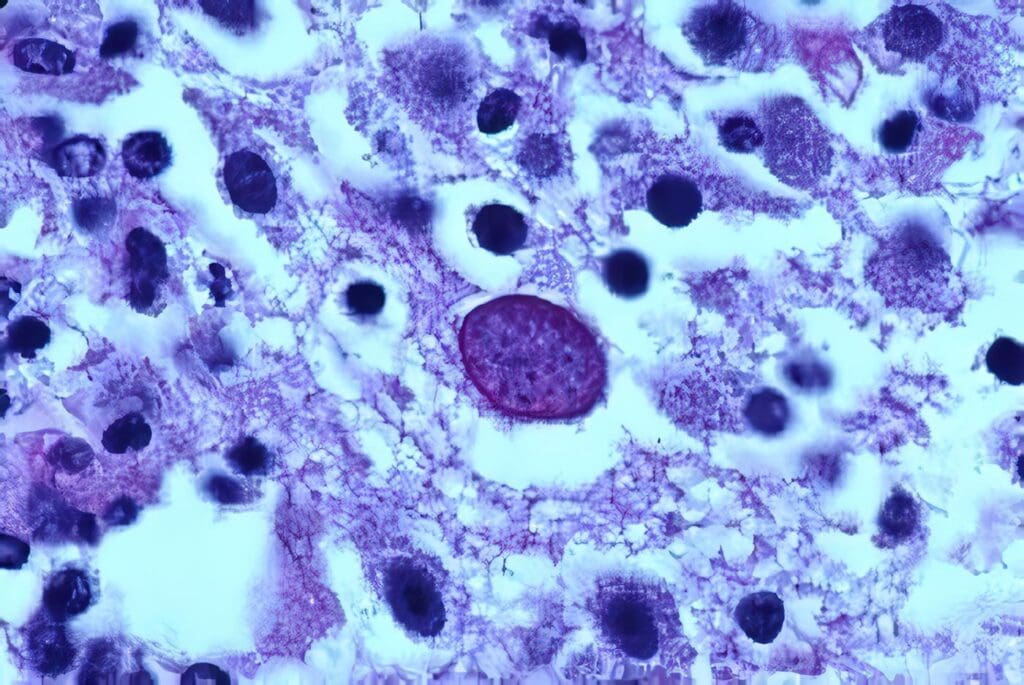
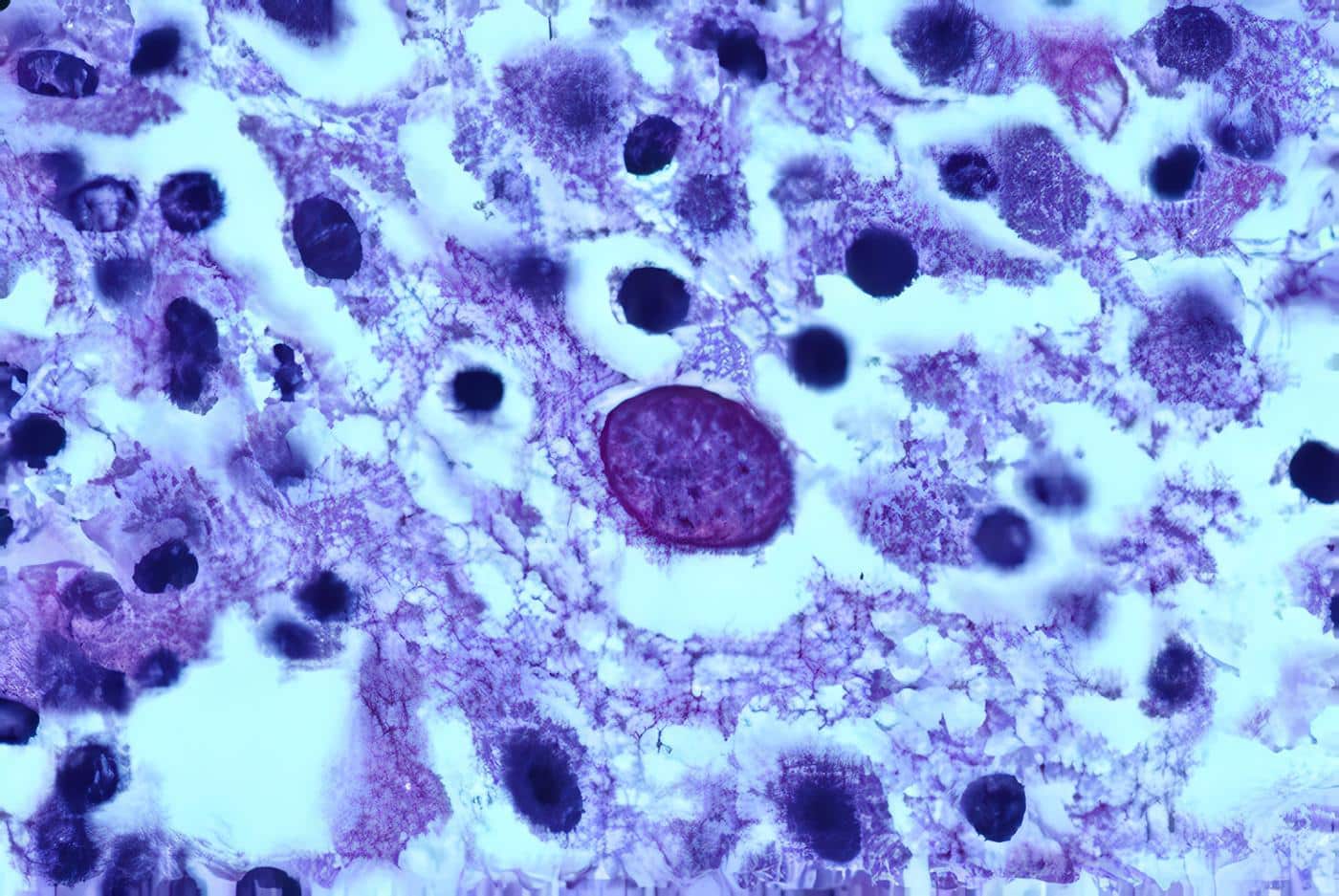
Neospora caninum es un protozoario que ha adquirido gran importancia a nivel mundial al ser implicado en 1989 como una de las principales causas de aborto en bovinos.
Se ha reportado desde entonces en: Australia, Nueva Zelandia, Estados Unidos y la mayoría de los países europeos. También en el Japón (Ogino y col, 1992) e Israel Harmelin y col, 1995.
El Estado de California (USA) es una zona endémica de la enfermedad con prevalencias del 33% en los hatos lecheros y con una variación del 20 al 40% (Anderson y col., 1991). Además se ha identificado en el 24.4% de los fetos abortados sometidos a exámenes histopatológicos en los laboratorios de referencia.
En América Latina solo existe un reporte de actividad serológica en Argentina (Venturini y col, 1995) y otro en México donde adicionalmente se demostró la presencia del parásito (Mendoza, 1997).
El primer aislamiento se produjo solo hasta 1991 (Conrad y col), y en 1988 McAllister y col definen al perro como el huésped definitivo. Es decir en el cuál se cumplen la fase sexual del protozoario.
En este primer reporte nacional, se evaluaron 357 sueros bovinos procedentes de 74 fincas que tenían problemas de tipo reproductivo con aborto en diferentes edades de la gestación y para los cuales no fue posible definir un diagnóstico serológico para entidades como Brucelosis, Leptospirosis, IBR y DVB.
El haber encontrado un 54% de sueros con una reacción positiva a la prueba de ELISA, abre la posibilidad de la presencia de N. Caninum como agente causal de la muerte en bovinos y crea la necesidad de adelantar investigaciones con miras a la demostración o no de esta entidad en nuestro medio.
Lea También: Neospora Caninum en Bovinos en Colombia, Diagnóstico
Revisión de Literatura
Historia
La historia de neosporosis se inicia en 1984 con un reporte de Bjerkas en Noruega de un caso de encefalitis y miocarditis en caninos, producido por un protozoario.
Dubey y col en 1988 propusieron el nombre de Neospora caninum y lograron comprobar los postulados de Koch en esta especie. Thilsted y col en 1989 reporta su participación como causa de aborto en bovinos y un año después Dubey y su grupo demostraron la transmisión transplacentaria en caninos, felinos, ovinos y bovinos.
En el año de 1991 fue considerada como la mayor causa de abortos bovinos en el Estado de California.
En 1993 Conrad y col logran reproducir la enfermedad al inocular taquizoitos en bovinos en forma experimental.
Desde el punto de vista diagnóstico el mismo Bjerkas en 1991 reportó que las cepas aisladas en caninos son idénticas a las aisladas en bovinos.
Con este hallazgo y el desarrollo de técnicas de diagnóstico inmunohistoquímico (Lindsay, 1989) y de ELISA (Bjorkman, 1994) se amplían las herramientas diagnósticas.
A pesar de los estudios realizados quedaban por definir algunos aspectos relacionados con el ciclo de vida del protozoario especialmente referentes con el huésped definitivo de la entidad, y aunque este tema fue elaborado desde 1988 por varios autores como Dubey y col, solamente en 1998 el grupo de McAllister y col. Logran definir al perro como huésped definitivo al haber demostrado la presencia de ooquistes en materia fecal de animales alimentados con tejidos infectados de taquizoitos.
Patogénesis
La Neosporosis es una enfermedad que se ha detectado en la mayoría de las especies domésticas: bovinos, ovinos, caprinos, equinos, ciervos y caninos (Anderson, 1996).
La ruta de transmisión mejor descrita e identificada hasta el momento es la vía transplacentaria la cuál parece ser la forma más importante para mantener la infección en los hatos debido a la eliminación del parásito a través de los fetos abortados o por el nacimiento de terneros congénitamente infectados (Paré y col, 1996).
Thurmond y Hietala, 1998, proponen también la posibilidad de infección postnatal basados en el hecho encontrar que de las terneras nacidas en hatos con seropositividad del 30 – 50% solamente el 1 – 2% de ellas presentaban una infección.
Adicionalmente las terneras nacidas de vacas seronegativas alimentadas con calostro y leche de seropositivas no presentaron seroconversión.
Se documentó que la evidencia de infección post natal es más frecuente desde el sexto mes de vida cuando el animal ya consume una dieta mixta.
Por esta razón y debido a su similitud con el Toxoplasma gondii. Se propone que puede haber transmisión por vía oral a través del consumo de forrajes contaminados con materia fecal de caninos u otros carnívoros que actuarían como huéspedes definitivos.
La transmisión entre carnívoros demostrada por Anderson, 1996, sucede a través del consumo de tejidos bovinos o de otros carnívoros infectados.
Con base en los trabajos realizados por Lindsay y col, en 1993, y la definición por McAllister y col, en 1998 del perro como huésped definitivo:
El ciclo de vida de N caninum comprendería una fase sexual en el intestino del perro con la formación de ooquistes que al ser eliminados en las heces y posteriormente al ser ingeridos por los bovinos daría el inicio de la fase asexual con la formación de quistes tisulares y taquizoitos en los tejidos del huésped intermediario o del feto y que al ser ingeridos por los caninos cerrarían el ciclo epidemiológico con la formación de ooquistes.
Los únicos estados bien conocidos hasta el momento son los taquizoitos y los quistes tisulares que contienen bradizoitos los primeros se encuentran en muchos tejidos de terneros infestados congénitamente y se relacionan con las lesiones microscópicas.
Los quistes tisulares, se han detectado igualmente, en cerebro y medula espinal de los fetos, pero en estos casos no se hallan asociados a lesiones microscópicas (Lindsay y col, 1996).
Los taquizoitos pueden crecer en cultivos celulares y son una fuente de antígeno para el diagnóstico serológico (Veturini Col, 1995).
Los primeros cultivos se hicieron en monocitos bovinos y en células endoteliales de la arteria cardio pulmonar, actualmente se utilizan las células VERO y los fibroblastos humanos en forma rutinaria (Dubey y Lindsay, 1996).
Signos Clínicos
Los abortos pueden ocurrir en cualquier época de la gestación en manera esporádica o en forma de brotes.
Un reporte de Neosporosis, en una finca en Tasmania, describe una tormenta de abortos que afectó a un 23.5% de las vacas gestantes sin diferencia en el número de partos (Obendorf y col, 1994).
Los abortos se presentan entre los 90 y 240 días (158 ± 10 días) de gestación, aunque la mayor presentación (78%) se concentra entre los 4 y los 6 meses (Lindsay y col, 1996).
En los casos reportados, no se han detectado signos clínicos previos al aborto, que se caracteriza por la expulsión de un feto usualmente en estado autolítico y que ocasionalmente presenta grados variables de momificación (Bidfel col., 1994), por lo general cursa sin retención placentaria (Anderson y col., 1994).
Obendorf y col (1994), reportan que el 43.8% de las vacas que abortaron por primera vez, lo volvieron hacer, sin definir si la infección se originó de los quistes existentes en ellas o si se debió a una reinfestación.
Las vacas infestadas con Neospora spp pueden parir terneros congénitamente infestados y que se consideran importantes diseminadores de la enfermedad.
Dichos terneros pueden presentar sintomatología nerviosa o pueden ser portadores de tipo asintomático (Anderson y col., 1994).
Se ha reportado una mayor prevalencia en las ganaderías de leche que de carne, no porque haya una mayor resistencia de los últimos a la enfermedad, sino porque en las ganaderías de leche se manejan mayores densidades de población lo que favorece la diseminación de la enfermedad (Anderson y col., 1994).