La disfagia alta es un síntoma común en los pacientes con SSp, y se debe a la reducción en la producción de saliva, y probablemente a alteraciones en la motilidad esofágica. Estas últimas, han sido motivo de diferentes estudios de manometría, electrofisiología, radiología y de medicina nuclear, al igual que se han tratado de realizar correlaciones con estudios de anatomía patológica. Lo más prominente de estos estudios es que se han encontrado ya sea ausencia o disminución en la contractibilidad principalmente del tercio superior esofágico48.
Síntomas como el dolor epigástrico, náuseas o dipepsia prolongada, son comunes en los pacientes con SSp. Desde el punto de vista endoscópico el hallazgo más común es la gastritis. La anatomía patológica demuestra GASTRITIS ATROFICA con o sin metaplasia49. Los estudios bioquímicos demuestran acloridia o hipocloridia, hipergastrinemia e hipopepsinogenemia50. Se han informado además casos con disminución de la producción de factor intrínseco y bajos niveles sérico de Vitamina B12 al igual que la presencia de niveles altos de anticuerpos anti-célula parietal50.
En el estómago se pueden desarrollar también trastornos linfoproliferativos como los linfomas no Hodgkin.
Manifestaciones hepatobiliares
Alteraciones en alguna de las pruebas de función hepática se observan en el 25% de los casos de SSp sin mayor connotación clínica51-52. Menos del 2% de casos de SSp tiene síntomas relacionados con disfunción hepática como son el prurito, ictericia o eritema palmar. Lo más común es un incremento leve benigno de las ALT, AST y fosfatasa alcalina51. Estudio de anatomía patológica de estos pacientes revelan características histológicas de la Cirrosis Biliar Primaria (CBP), en estadío I53. Algunos casos pueden tener incremento de los anticuerpos antimitocondriales, anti músculo liso y anti priruvato deshidrogenasa, lo que sugiere una posible relación con CBP o con hepatitis autoinmune (HA)54. En la literatura se informan casos de SSp asociado a CBP o con HA, lo que hace pensar mejor que se trata de casos con CBP o HA con SS secundario55. La asociación con cirrosis es prácticamente descartada.
Compromiso vascular
La vasculitis de pequeños vasos puede presentarse hasta en el 30% de los casos5. Se han descrito pacientes con compromiso similar a la poliarteritis nodosa. La piel es el sitio más frecuentemente comprometido, con la presencia de púrpura palpable de localización primordial en miembros inferiores. También se encuentra casos con urticaria vasculítica. El compromiso visceral puede presentarse en el riñón, pulmón, sistema nervioso y a nivel gastrointestinal56.
Lo usual es que los pacientes con vasculitis presenten hipergamaglobulinemia, altos títulos de factor reumatoide, anticuerpos anti Ro e hipocomplementemia. El depósito de complejos inmunes es uno de los componentes patogénicos5.
El fenómeno de Raynaud se presenta entre 38 y 64% de los casos, dependiendo de las series informadas. A diferencia del fenómeno de Raynaud asociado con escleroderma, en el SSp rara vez lleva a necrosis digital o úlceras digitales5.
Manifestaciones hematológicas
El 6% de los pacientes con SSp cursan con anemia leve normocítica normocrómica. En 22% se aprecia leucopenia y es primariamente debida a la reducción de linfocitos T CD4+ circulantes y menos frecuente a neutropenia. El mecanismo es desconocido, pero se involucran los anticuerpos anti-Ro, la apoptosis linfocítica periférica y el secuestro esplénico5. El 70% de los pacientes tienen una velocidad de sedimentación globular elevada. La trombocitopenia es rara. La esplenomegalia se puede encontrar hasta en el 14% de casos y linfadenopatías hasta en el 20%5.
Manifestaciones neurológicas
En una serie de 95 pacientes colombianos con SSp, once de ellos (11,6%) cursaron con alguna manifestación a nivel neurológico: ocho (8.4%), en el sistema nervioso periférico (cinco con síndrome del túnel del carpo y tres con polineuropatía sensitiva distal), y tres (3.2%), en el sistema nervioso central (migraña complicada, esclerosis múltiple con vasculitis y neuritis óptica con epilepsia). Una posible asociación de los casos con afección de sistema nervioso central se observó con la presencia del antígeno HLA-DQB1*030357.
Otras series de casos han informado además la asociación con neuropatías craneales, como la neuropatía del trigémino o vasculitis cerebral con déficit neurológico focal diverso1.
Compromiso linfoproliferativo
La primera descripción de LINFOMA NO HODGKIN asociado a SSp la realizaron Bunim y Talal en 1963, donde se plantea además como causa patogénica, la posible estimulación crónica inmunológica58. El riesgo relativo para presentarse esta neoplasia en pacientes con SSp, la calcularon Kassan et al. en 1978, el cual puede ser del orden de las 44 veces, comparado con la población general59. Puede desarrollarse hasta 20 años después de diagnosticado el SSp. El promedio de tiempo entre el diagnóstico del SSp y el desarrollo de linfoma está alrededor de los 7.2 años. Algunas condiciones han sido asociadas a un mayor riesgo para desarrollar linfomas como son: la parotidomegalia, esplenomegalia, linfadenopatías, crioglobulinemia mixta monoclonal (Tipo II) y la presencia de factor reumatoide monoclonal59.
Los órganos afectados por el SSp, cursan con infiltración de poblaciones de linfocitos activados tanto de tipo T como B, los cuales pueden llegar a tener comportamiento proliferativo de características incluso monoclonales que pueden en un espectro de evolución conducir al desarrollo de linfomas. Existe un espectro de cambios linfoproliferativos, que como en el caso del pulmón, puede presentarse desde una situación benigna a una maligna: neumonitis intersticial linfocítica, pseudolinfoma y linfoma19, 21. En la situación más benigna existe la proliferación linfocítica en forma difusa, con células pequeñas y bien diferenciadas, y en las formas más malignas se presenta una infiltración de tipo nodular, desordenado, infiltrativo con daño de la arquitectura de sitios adyacentes, aparición de imágenes mitóticas, monoclonalidad al igual que la capacidad de diseminación hacia nódulos linfáticos vecinos o distantes60.
Para algunos autores los pseudolinfomas son clasificados como linfomas de bajo grado, basándose en estudios inmunohistoquímicos, de DNA, y moleculares61.
Característicamente los linfomas asociados a SSp, son del tipo no Hodgkin, de células B, de grado bajo de malignidad, de origen tanto nodal como extranodal, con una distribución marginal. Estas células B pueden producir anticuerpos y desarrollar incluso una crioglobulinemia, con títulos altos de factor reumatoideo monoclonal. Algunos tratadistas del tema denominan estas neoplasias “inmunocitomas”1, 60-61.
Los sitios más frecuentes de inicio del proceso neoplásico son las parótidas, siguiéndole en frecuencia sitios extranodales como el pulmón o el estómago62.
El inicio del proceso linfoproliferativo a nivel histológico son los tejidos linfoides asociados a las mucosas o MALT (mucosa associated lymphoid tissues), los cuales tienen la función primordial de protección de las “puertas de entrada” como son los epitelios11. Los tumores derivados de los sistemas MALT, ocasionalmente son referidos como “maltomas”.
En forma ocasional, se informan casos de linfoma de células T, presentándose una condición de alta malignidad62.
La clasificación y el tratamiento de los linfomas asociados a SSp, se enfocan en forma similar a los otros tipos de linfoma no Hogkin.
Otras manifestaciones
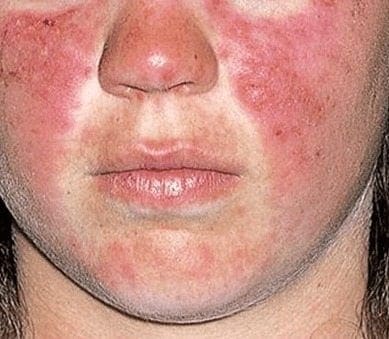
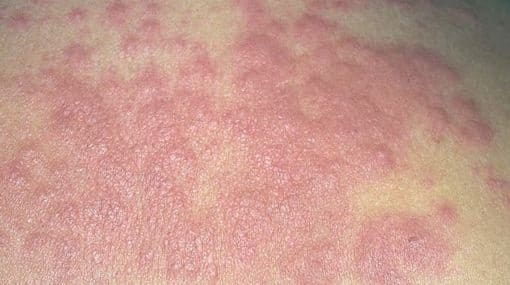
Algunos pacientes pueden presentar eritema anular que afecta principalmente la cara y el tronco63. La fotosensibilidad puede presentarse hasta en el 24% de los casos3. La tiroiditis autoinmune se ha detectado ocasionalmente al igual que hipotiroidismo, que por lo regular es de tipo subclínico64. La dispareunia puede ser una queja importante desde el inicio de la enfermedad, y es ocasionada por la sequedad vaginal65.
Referencias
1. Manoussakis MN, Talal N, Moutsopoulos HM. Sjogren’s syndrome. En Rose NR, Nackay IR (Editores): The autoimmune diseases. Third edition. San Diego, California. Academic press, 1998; 381-404.
2. Cañas C, Jiménez C, Restrepo JF, Rondón F, Peña M, Sánchez A, Iglesias A. Síndrome de Sjögren primario (estudio prospectivo para conocer las características clínicas en nuestro medio). Rev Col Reum 1997; 4: 126-130.
3. Anaya JM, Correa PA, Mantilla RD. Síndrome de Sjögren primario. Características clínicas e inmunogenéticas. Acta Med Col 1999; 24: 127-136.
4. Leroy JP, Drosos AA, Yannopoulos D, Youinou P, Moutsopoulos HM. Intravenous pulse cyclophosphamide therapy in myositis and Sjögren´s syndrome. Arthritis Rheum 1990; 33: 1579-1581.
5. Anaya JM, Talal N. Sjögren´s syndrome and connective tissue diseases associated with other immunologic disorders. En Koopman WJ (Editor) : Srthritis and allied conditions. 13th Edition Baltimore, William & Wilkins, 1997; 1561-1580.
6. Cain HC, Noble PW, Matthay RA. Pulmonary manifestations of Sjogren’s syndrome. Clinics in Chest Medicine 1998; 19: 687-699.
7. Strimlan CV, Rosenow EC III, Divertie MB. Pulmonary manifestations of Sjogren’s syndrome. Chest 1976; 70: 354-361.
8. Constantopoulos SH, Papadimitrio CS, Moutsopoulos HM. Respiratory manifestations in primary Sjogren’s syndrome. Chest 1985; 88: 226-229.
9. Tumiati B, Casoli P, Parmeggiani A. Hearing loss in the Sjögren syndrome. Ann Intern Med 1997; 126: 450-453.
10. Constantopoulos S. H., Drosos A. A. Xerotrachea and interstitial lung disease in primary Sjogren’s syndrome. Respiration 1984; 46: 310-314.
11. Gardiner P. Primary Sjogren’s syndrome. Baillieres Clin Rheumatol 1993; 7: 59-77.
12. Newball H. H., Brahim S.A. Chronic obstructive airway disease in patients with Sjogren’s syndrome. Am Rev Respir Dis 1977; 115: 295-304.
13. Potena A., La Corte R. Increased bronchial responsiveness in primary and secondary Sjogren’s syndrome. Eur Respir J 1990; 3: 548-553.
14. Stalenheim G., Gudbjornsson B. Anti-inflammatory drugs do not alleviate bronchial hyperreactivity in Sjogren’s syndrome. Allergy 1997; 52: 423-427.
15. Hatron P, Wallaert B, Gosset C, Tonnel A, Gosselin B, Voisin C, et al. Subclinical lung inflammation in primary Sjogren’s syndrome. Arthritis Rheum 1987; 30: 1226-1231.
16. Kadota J, Kusano A, Kawakami K, Morikawa T, Kohno A. Usual interstitial pneumonia associated with primary Sjogren’s syndrome. Chest 1995; 108: 1756-1758.
17. Usui Y., Kimula Y. A case of bronchiolitis obliterans organizing pneumonia associated with primary Sjogren’s syndrome who died of superimposed diffuse alveolar damage. Respiration 1992; 59: 122-124.
18. Collins R. D., Jr., Ball G. V. Gallium-67 scanning in Sjogren’s syndrome: concise communication. J Nucl Med 1984; 25: 299-302.
19. Alkhayer M., McCann B. G. Lymphocytic interstitial pneumonitis in association with Sjogren’s syndrome. Br J Dis Chest 1988; 82: 305-309.
20. Ogasawara H., Sekiya M. Very low-dose cyclosporin treatment of steroid-resistant interstitial pneumonitis associated with Sjogren’s syndrome.Clin Rheumatol 1998; 17: 160-162.
21. Gardiner P, Ward C, Allison A, Ashcroft T, Simpson W, Walters H, et al. Pleuropulmonary abnormalities in primary Sjogren’s syndrome. J Rheumatol 1993; 20: 831-837.
22. Joseph J, Sahn S. Connetive tissue disease and pleura. Chest 1993; 104: 262-270.
23. Talal N, Zisman E, Schurt PH. Renal tubular acidosis, glomerulonephritis and immunologic factors in Sjogren’s syndrome. Arthritis Rheum 1968; 11: 774-786.
24. Shearn MA, Tu WH. Nephrogenic diabetes insipidus and other defects of renal tubular function in Sjogren’s syndrome. Am J Med 1965; 39: 312-318.
25. Winer RL. Sjogren’s syndrome. En Grishman E, Churg J, Needle MA, Venkataseshan VS (Editores): The Kidney in collagen vascular diseases. New York. Raven Press, 1993; 724-727.
26. Enestrom S, Denneberg T, Erikksson P. Histopathology of renal biopsies with correlation to clinical findings in primary Sjogren’s syndrome. Clinical Exp Rheumatol 1995; 13: 697-703.
27. Dussol B., Tsimaratos M. Crescentic glomerulonephritis and primary Gougerot-Sjogren syndrome. Nephrologie 1994; 15: 295-288.
28. Goules A., Masouridi S, Tzioufas AT, Ioannidis JPA, Skopouli FN, Moutsopoulos HM. Clinically significant and biopsy-documented renal involvement in primary Sjogren syndrome. Medicine 2000; 79: 241-249.
29. Dabadghao S, Aggarwal A, Arora P, Oandey R, Misra R. Glomerulonephitis leading to end stage renal disease in a patient with primary Sjogren’s syndrome. Clinical Exp Rheum 1995; 13: 509-511.
30. Aguilera S., Lopez R. Distal renal tubular acidosis and nephrolithiasis in 3 cases of primary Sjogren syndrome. Rev Med Chil 1996; 124: 1467-1475.
31. Siamopoulos KC, Elisaf M, Drosos AA, Mavridis AA, Motsopoulos HM. Renal tubular acidosis in primary Sjogren’s syndrome. Clinical Rheumatol 1992; 11: 226-230.
32. Moutsopoulos HM, Balow JE, Lawlwey TJ, Stahl NI, Antonovych TT, Chused TM. Immune complex glomerulonephritis in sicca syndrome. Am J Med 1978; 64: 955-960.
33. Battle DC. Renal tubular acidosis. Med Clin North Am 1983; 67: 859-878.
34. Vitali C, Tavoni A, Sciuto M, Maccheroni M, Moriconi L, Bombardieri S. Renal involvement in primary Sjogren’s syndrome: a retrospective-prospective study. Scand J Rheumatol 1991; 20: 132-136.
35. Matsumura R., Umemiya K. Immunohistochemical identification of infiltrating mononuclear cells in tubulointerstitial nephritis associated with Sjogren’s syndrome. Nippon Rinsho 1995; 53: 2503-2509.
36. DeFranco P. E., Haragsim L. Absence of vacuolar H(+)-ATPase pump in the collecting duct of a patient with hypokalemic distal renal tubular acidosis and Sjogren’s syndrome. J Am Soc Nephrol 1995; 6: 295-301 Chest 1976; 70: 354-361.
37. Cohen E. P., Bastani B. Absence of H(+)-ATPase in cortical collecting tubules of a patient with Sjogren’s syndrome and distal renal tubular acidosis. J Am Soc Nephrol 1992; 3: 264-271.
38. Inagaki Y., Jinno-Yoshida Y. A novel autoantibody reactive with carbonic anhydrase in sera from patients with systemic lupus erythematosus and Sjogren’s syndrome. J Dermatol 1991; 2: 147-154.
39. Brenner B, Mackenzie. Disturbances of renal fuction. En Fauci AS, Braunwald E, Isselbacher KJ. (Editores). Harrison´s Principles of Internal Medicine 14th Edition. McGraw-Hill, New York 1998; 1498-1504.
40. Monte Neto J. T., Sesso R. Osteomalacia secondary to renal tubular acidosis in a patient with primary Sjogren’s syndrome. Clin Exp Rheumatol 1991; 9: 625-627.
41. Michalski J, Daniels T, Talal N, Grey H. Beta-2 microglobulin and lymphocytic infiltration in Sjogren’s syndrome. N Engl J Med 1975; 293: 1228-1231.
42. Daghestani L, Pomeroy C. Renal manifestations of hepatitis C infection. Am J Med 1999; 106: 347-354.
43. Dimitrakov D., Pandeva S. A case of primary Sjogren’s syndrome in combination with chronic mesangiocapillary glomerulonephritis and interstitial nephritis. Folia Med 1998; 40: 29-33.
44. Gamron S., Barberis G. Mesangial nephropathy in Sjogren’s syndrome. Scand J Rheumatol 2000; 29: 65-77.
45. Yoshida K., Suzuki J. Sjogren’s syndrome with membranous glomerulonephritis detected by urine screening of school children. Acta Paediatr Jpn 1996; 38: 533-536.
46. Cortez M. S., Sturgill B. C. Membranoproliferative glomerulonephritis with primary Sjogren’s syndrome. Am J Kidney Dis 1995; 25: 632-636.
47. Khan M. A., Akhtar M. Membranoproliferative glomerulonephritis in a patient with primary Sjogren’s syndrome. Report of a case with review of the literature. Am J Nephrol 1988; 8: 235-239.
48. Tsianos EB, Chiras CD, Drosos AA, Moutsopoulos HM. Oesophageal dysfunction in patient with primary Sjögren syndrome. Ann Rheum Dis 1985; 44: 610-613.
49. Pokorny G, Karacsony G, Lonovics J, Hudak J, Nemeth J, Varró V. Types of atrophic gastritis in patients with primary Sjögren´s Syndrome. Ann Rheum Dis 1991; 50: 97-100.
50. Tsianos E. V. , Moutsopoulos H. M. Sjogren’s syndrome and the gut. Baillieres Clin Rheumatol 1989; 3: 357-370.
51. Whaley K, Williamson J, Dick WC, Goudies RB, Nuki G, Buchaman WW. Liver disease in Sjögren´s Syndrome and rheumatoid arthritis. Lancet 1970; i: 861-863.
52. Skopouli F. N., Barbatis C. Liver involvement in primary Sjogren’s syndrome. Br J Rheumatol 1994; 33: 745-748.
53. Skopoull EN, Barbatis C, Moutsopoulos HM. Liver involvement in primary Sjögren´s Syndrome. Br J Rheum 1994; 33: 745-748.
54. Biasi D., Caramasch P. Sjogren’s syndrome associated with autoimmune hepatitis. A case report. Clin Rheumatol 1997; 16: 409-412.
55. Alarcon-Segovia D, Diaz-Jouanen E. Features of Sjögren´s Syndrome in primary biliar cirrhosis. Ann Int Med 1973; 79: 31-36.
56. Anaya JM, Talal N. Head and neck finding in systemic lupus erythematosus: Sjögren´s syndrome and the eye, ear, and larynx. En Wallace DJ, Hahn BH (Editores): Dubois´ Lupus erythematosus. 5th Edition. Baltimore. Williams & Wilkins, 1996; 783-791.
57. Anaya JM, Villa LA, Vargas SA, Restrepo C, Mantilla RD. Compromiso neurológico asociado al síndrome de Sjögren. Acta Med Col 2000; 25: 179-187.
58. Bunim JJ, Talal N. The association of malignant lymphoma with Sjogren’s syndrome. Trans Assoc Am Physicians 1963; 76: 45-56.
59. Kassan SS, Thomas TL, Moutsopoulos HM, Hoover R, Kimberly RP, Budman DR, et al. Increased risk of lymphoma in sicca syndrome. Ann Inter Med 1978; 89: 888-892.
60. Hansen L. A., Prakash U. B. Pulmonary lymphoma in Sjogren’s syndrome. Mayo Clin Proc 1989; 64: 920-931.
61. De Vita S, Boiocchi M, Sorrentino D, Carbone A, Avellini C, Dolcetti R, et al. Characterization of prelymphomatous stage of B cell lymphoproliferation in Sjogren’s syndrome. Arthritis Rheum 1997; 40: 318-331.
62. Voulgarelis M, Dafni U, Isenberg DA, Moutsopoulos HM, et al. Malignant lymphoma in primary Sjögren´s Syndrome. Arthritis Rheum 1999; 1765-1772.
63. Teratomo N, Katayama I, Arai H, Kamimura K, Ketsuka M, Kondo S, et al. Annular erythema´s possible association with primary Sjögren´s siyndrome. J Am Acad Dermatol 1989; 20: 596-601.
64. Karsh J, Pavlidis N, Neitraub BD, Moutsopoulos HM. Thyroid disease in Sjögren´s syndrome. Arthritis Rheum 1980; 23: 1326-1329.
65. Parke AL. Sjögren´s syndrome: a women´s health problem. J Rheumatol 2000; 27 Suppl 61: 4-5.