Artículo de Revisión
Síndrome de Sheehan: Epidemiología, Clínica, Diagnóstico y Manejo
GUSTAVO GÓMEZ TABARES*, KELLY GUTIÉRREZ**
Introducción
El síndrome de Sheehan es la necrosis de la glándula pituitaria, secundario a una hemorragia posparto; genera hipopituitarismo o disminución/ausencia de las hormonas secretadas por esta glándula1, lo cual sucede por el vasoespasmo, la trombosis y la isquemia de las arterias hipofisarias2.
Se han descrito diferentes grados de disfunción de dicha glándula, la cual es una de las causas más comunes de hipopituitarismo en los países en vía de desarrollo, y muy rara en países desarrollados.
Historia
En 1913, Glinsky publicó el primer reporte de una paciente con necrosis de la glándula pituitaria en el puerperio que experimentó una hemorragia posparto masiva, y murió 9 días después por sepsis tardía3.
En 1914 Simmonds reportó una mujer puérpera que presentó sepsis y murió al quinto día; la autopsia reveló atrofia de la glándula pituitaria4.
Posteriormente, en 1937, Harold Sheehan, patólogo del hospital de maternidad de Glasgow, realizó una serie de autopsias en mujeres que morían en el parto o puerperio tardío; de estas, 12 de 76 presentaban una destrucción extensiva de la adenohipofisis teniendo en común hemorragia posparto; histológicamente se aprecia con fibrosis y tejido intacto, interpretando que esto era consecuencia de espasmo o trombosis; en su momento se denominó síndrome de Sheehan5.
Sheehan, basado en autopsias, se dedicó a estudiar la historia natural de esta patología caracterizando anatómica e histológicamente la glándula pituitaria así como el hipopituitarismo secundario subsecuente. Posteriormente la descripción de dicho síndrome la publicó en textos en 19825.
Epidemiología
Cada vez es menos común en obstetricia la presencia de hemorragia posparto; se estima que ocurre en un 3% a 4% según datos de la OMS6; además el síndrome de Sheehan se presenta en regiones con poca accesibilidad a servicios de salud o aumento de partos en casa.
La incidencia del panhipopituitarismo publicada en un estudio en España mostró que se presentaban 46 casos por cada 100.000 personas, 61% por tumores y solo una fracción del 6% por el síndrome de Sheehan.7. Un estudio retrospectivo en Kashmir, en la India, estimó
una prevalencia del 3,1% de esta patología8. En países en vía de desarrollo se estima que puede encontrarse en 5 de cada 100.000 nacimientos9.
En estudios más recientes, en el 2013, en una población de 405.218 pacientes seguidos por un periodo de 10 años, no se encontraron casos de síndrome de Sheehan, lo cual se explica probablemente por la mejoría de la atención en salud10. (Lea También: Síndrome de Sheehan, Tratamiento )
Por lo tanto, saber con exactitud su incidencia y prevalencia resulta difícil dado que el diagnóstico generalmente es tardío; estudios reportan que se pueden demorar desde 1 hasta 33 años para realizar dicho diagnostico; esto se debe a la poca práctica del personal de salud para analizar el síndrome de Sheehan y a la aparición escalonada de los síntomas de acuerdo a la manifestación de las células hipofisiaria afectadas.
Factores de riesgo
El principal factor de riesgo es el embarazo, debido a los cambios fisiológicos de la glándula pituitaria en la gestación cuando al aumentar de tamaño se torna vulnerable a procesos isquémicos.
La pérdida sanguínea en una mujer no embarazada no causa hipopituitarismo, lo que vuelve al embarazo un factor de riesgo predictivo para sufrir de esta patología11.
Sin embargo, es difícil predecir qué mujeres presentarán hemorragia posparto, pues la mayoría de estas pueden no tener otros factores de riesgo más comunes como la multiparidad, polihidramnios, corioamnionitis, embarazos gemelares, inducción de parto, parto instrumentado, entre otros12.
Se han encontrado, otros factores predisponentes como aumento del tamaño de la glándula y una silla turca pequeña, lo cual generará una restricción en el flujo sanguíneo, así como anormalidades de la coagulación (congénitas o adquiridas)13.
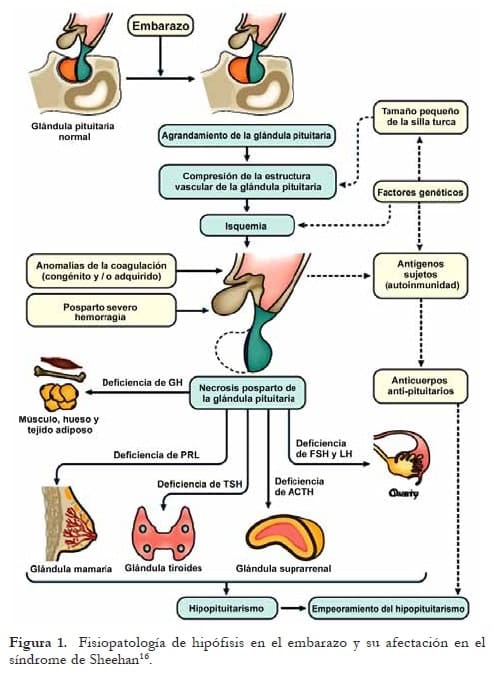
Mecanismos fisiopatológicos
Anatomía de la glándula pituitaria
La glándula pituitaria se perfunde a través de las arterias hipofisarias superiores e inferiores14.
El infundíbulo, la eminencia media y la pars tuberalis es irrigada por la arteria hipofisaria superior, y el lóbulo posterior por la arteria hipofisaria inferior. La pars distalisis recibe flujo venoso del lóbulo posterior de la glándula pituitaria por los vasos portales; esta ruta suma el 30% del flujo sanguíneo del lóbulo anterior de la glándula pituitaria15.
Las hormonas de la adenohipofisis son controladas por factores principalmente estimuladores e inhibitorios (GH y PRL) secretados por el hipotálamo.
En el lóbulo anterior encontramos hormona del crecimiento (GH), prolactina (PRL), hormona folículo-estimulante (FSH) y hormona luteinizante (LH), hormona estimuladora de tiroides (TSH), hormona adrenocorticotrópica ACTH), hormona estimulante de los melanocitos (MSH) y en el lóbulo posterior, vasopresina y oxitocina16.
Durante el embarazo ocurre un aumento del tamaño de la glándula, aproximadamente en un 45% en el primer trimestre hasta un 120 a 136% cerca del término; el tamaño normal es de 4 a 8 mm y en el embarazo alcanza de 10 a 12 mm, debido a que tiene que suplir las demandas hormonales durante el estado de gestación como por ejemplo aumento de los lactotropos.
El aumento de volumen la torna vulnerable a los cambios de flujo sanguíneo por aumento de demanda17.
Fisiopatología
Secundario al sagrado excesivo y baja tensional el paso inicial es la necrosis del lóbulo anterior por infarto o arresto de flujo sanguíneo, siendo muy raro el daño en el lóbulo posterior18.
Debido al choque hipovolémico se produce un vasoespasmo y trombosis con agregación plaquetaria que genera un daño en las células endoteliales. Si ocurre un daño mayor del 70% se puede presentar incluso panhipopituitarismo19.
Posterior a esto ocurre una disfunción progresiva de la glándula, lo cual hace pensar que pueden existir factores contribuyentes, tales como un proceso autoinmune concomitante.
La glándula pituitaria sufre una isquemia que produce necrosis; entonces se encuentra sangre coagulada y células inflamatorias, y en las zonas necróticas hay ausencia total de hormonas; en la fase crónica se forma fibrosis, tornándose la glándula hipotrófica20. El 90% ocurrirá en el lóbulo anterior.
Las hormonas afectadas más frecuentemente y casi en orden cronológico son la prolactina (90-100%) y la GH, mientras otras hormonas, como ACTH y por consiguiente cortisol, las gonadotropinas y la hormona tirotrópica, se ven afectadas en menos pacientes (50-100%) y la deficiencia aparece tardíamente, a veces más de 5 años después del evento hemorrágico35.
Manifestaciones clínicas
Lo más importante es investigar sobre la historia obstétrica; el síntoma inicial es en el posparto inmediato en pacientes que presentaron hemorragia posparto importante12.
La amenorrea posparto y la agalactia son los síntomas iniciales tempranos Posteriormente hay signos y síntomas de hipopituitarismo, tales como, dicultad para lactar, disminución del vello púbico y axilar, hipoglicemia, cambios cognitivos, astenia y diabetes insípida16. Como se dijo anteriormente las hormonas más afectadas son principalmente la GH y PRL (90%), y no tan común y tardía la alteración de TSH y ACTH (50%)21.
Pueden existir formas más severas como crisis adrenal, colapso circulatorio, mixedema e hiponatremia. Las alteraciones hematológicas también son comunes, encontrándose anemia normocítica normocrómica, pancitopenia y deficiencia del factor VIII22.
Es una enfermedad progresiva por lo tanto muchas pacientes presentan síntomas poco específicos, generando demoras en el diagnóstico.
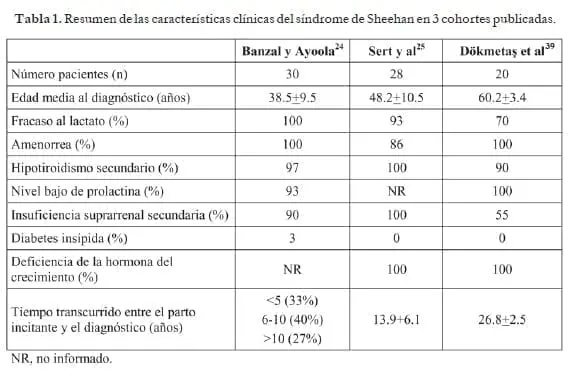
Pacientes con historia de falla en la lactancia, alteración de ciclos menstruales, síntomas de hipotiroidismo o insuficiencia adrenal e involución de caracteres sexuales deben hacer sospechar sobre el síndrome de Sheehan16. La tabla 1 muestra la prevalencia clínica de estos síntomas en tres estudios.
Al examen físico se puede encontrar vello axilar y púbico disminuido, atrofia mamaria, arrugas alrededor de la boca y ojos como signos prematuros de vejez, sequedad en la piel, bradicardia y caída del cabello2. La hiponatremia es el trastorno hidroelectrolítico más común (21 a 59%); el síndrome de Sheehan se considera la segunda causa más común de hipoglicemia asociada a coma después de la diabetes mellitus, como también puede encontrarse hipotiroidismo23.
Diagnóstico
Criterios clásicos24:
- Historia de hemorragia posparto
- Choque severo con transfusión sanguínea
- Ausencia de lactancia
- Alteración menstrual (amenorrea)
- Hipopituitarismo parcial o total
- Silla turca vacía total o parcialmente detectada al TAC o RMN
El déficit temprano y crítico de la prolactina explica el fallo en la lactancia, y este es el síntoma más frecuente y característico. Las gonadotropinas no están afectadas en muchas ocasiones, y hay casos de síndrome de Sheehan que mantienen ciclos menstruales regulares, e incluso algunos con embarazos espontáneos.
La presentación del síndrome de Sheehan puede ser aguda o crónica.
En las formas agudas los datos clínicos incluyen signos de insuficiencia adrenocortical 2, 7,8 como hipotensión, hipotermia, taquicardia, hipoglucemia, hiponatremia, náuseas y vómitos.
En las formas graves puede ocurrir colapso circulatorio, hiponatremia severa, diabetes insípida central, fallo cardiaco congestivo, e incluso psicosis.
Y en las formas crónicas, o de presentación tardía, los síntomas son más variables: amenorrea, esterilidad y disminución del vello axilar y púbico por déficit de gonadotropinas; astenia, debilidad, fatiga y pérdida de masa muscular por déficit de tiroxina y GH; hipoglucemia, intolerancia al frío y envejecimiento prematuro.
Exámenes de laboratorio
La hiponatremia es la alteración electrolítica más frecuente y se observa entre un 33 y 69% de los casos7; en algunos casos clínicos presentados esta era la única alteración inicial. Puede ocurrir tanto en las formas agudas como en las crónicas.
Su causa también es multifactorial y se relaciona con hipovolemia, hipotiroidismo, bajos niveles de cortisol y el desarrollo de un síndrome de secreción inadecuada de hormona antidiurética.
El potasio no se altera en este síndrome porque la producción de aldosterona es parcialmente independiente de la hipófisis.
También encontrarse alteraciones hematológicas como anemia, que es la más frecuente; y se han descrito también casos de pancitopenia y alteraciones en la coagulación36.
Es importante resaltar que la estimulación de ACTH puede ser normal los primeros meses, ya que la corteza adrenal aún no se ha atrofiado25, y los niveles de FSH y LH pueden encontrarse normales.
Los niveles de T3 y T4 libre pueden estar disminuidos con TSH normales (hipotiroidismo subclínico); cuando se administra TRH hay falla para aumentar los niveles de TSH o PRL en pacientes con síndrome de Sheehan26, lo que sugiere que el hipotálamo está funcionando normal.
Como se mencionó anteriormente, el trastorno hidroelectrolítico más común es la hiponatremia, pero puede haber hipocalemia, hipomagnesemia e hipocalcemia.
La explicación para la hiponatremia no se sabe con exactitud, pero se cree que es por un aumento de la ADH, como consecuencia de la disminución del flujo sanguíneo y del gasto cardiaco16.
Imagenología
La RMN es la técnica imagenológica preferida para el diagnóstico diferencial; sin embargo, puede usarse la TAC.
En la imagen se encuentra una glándula pituitaria agrandada con un infarto a nivel central; en el síndrome más avanzado se presenta una atrofia progresiva, hasta finalmente encontrar una silla turca vacía característica del síndrome de Sheehan16.
Se ha demostrado que hasta un 70% de las pacientes con Sheehan presentan una imagen de silla turca vacía. Y el 30%, una imagen de vacío parcial. Cabe aclarar que encontrar silla turca parcialmente vacía no se relaciona con panhipopituitarismo; es decir, se puede tener una silla turca totalmente vacía con hipopituitarismo parcial o viceversa1.
Autores
* GUSTAVO GÓMEZ TABARES. Profesor Titular y Distinguido. Universidad del Valle, Departamento de OB-GIN, Sección Endocrinologia Reproductiva.
** KELLY GUTIÉRREZ. Residente Universidad del Valle Departamento de OB-GIN. Rotante por Endocrinologia Reproductiva.