Menopausia al Día
Una mujer de 27 años de edad presenta sofocos intensos y sudores nocturnos secundarios a Insuficiencia Ovárica Primaria (IOP) y desde la menopausia temprana después de la quimioterapia para el tratamiento del linfoma de Hodgkin ¿Cuál es el mejor enfoque de tratamiento?
Comentario
La mayoría de las mujeres llegarán a la menopausia cuando tengan entre 45 y 55 años (edad promedio en los EE. UU., 52 años). Aproximadamente el 5% de las mujeres, sin embargo, experimentarán la menopausia temprana, que se produce entre las edades de 40 y 45.
En un número aún más pequeño (1%) se presentará la menopausia prematura, que ocurre antes de la edad de 40.1
La menopausia prematura se caracteriza por la pérdida temprana de la función ovárica, que puede atribuirse a la disminución de la cantidad de folículos, la destrucción acelerada del folículo o la disminución de la respuesta folicular a las gonadotropinas.
Los trastornos genéticos y autoinmunes, las infecciones y las causas iatrogénicas secundarias a la quimioterapia, la radiación o la cirugía, se han identificado como las causas más comunes de IOP que conducen a la menopausia temprana.
La menopausia prematura es un efecto adverso conocido a largo plazo del tratamiento del linfoma de Hodgkin. Aunque hay poca información sobre cómo la radioterapia pélvica y la quimioterapia alquilante utilizada para el tratamiento del linfoma de Hodgkin afecta el estado hormonal femenino, hay algunas pruebas de que la menopausia ocurre más rápidamente después de la radioterapia y la quimioterapia en dosis altas, que después de la quimioterapia alquílica sola.2
Esto es una información importante para retransmitir cuando se asesora a los pacientes.
Varias complicaciones de salud resultan de los IOP debido a deficiencias en la producción de hormonas ováricas, específicamente estrógenos (Tabla 1).3

Terapia Hormonal
El Colegio Estadounidense de Obstetras y Ginecólogos (ACOG, por sus siglas en inglés) recomienda dosis de reemplazo total de la terapia hormonal (TH) para controlar los síntomas del hipoestrogenismo y reducir el riesgo de consecuencias para la salud a largo plazo.
La TH sistémica se recomienda para tratar los síntomas de la menopausia, mitigar la pérdida ósea, prevenir los efectos negativos sobre la salud cardiovascular y mejorar la calidad de vida de las mujeres jóvenes con IOP.
Una distinción importante en el tratamiento de mujeres jóvenes con IOP y mujeres en transición a través de la menopausia normal es que el requisito para el reemplazo es diferente.
En mujeres jóvenes con IOP, la terapia de mantenimiento diaria para lograr niveles normales de funcionamiento de ovario de estradiol es la meta. Por lo tanto, a menudo requieren dosis más altas de estrógeno que las mujeres menopáusicas para lograr un reemplazo adecuado y control de los síntomas.
ACOG, la Sociedad Americana de Medicina Reproductiva, la Federación de Menopausia de Asia Pacífico, la Sociedad Endocrina, la Sociedad Europea de Menopausia y Andropausia, la Sociedad Internacional de Menopausia, la Fundación Internacional de Osteoporosis, la Sociedad Médica Británica y la Sociedad Norteamericana de Menopausia, acuerdan que el tratamiento debe continuar hasta la edad natural de la menopausia si no hay contraindicaciones.
Suplementos de Estrógenos
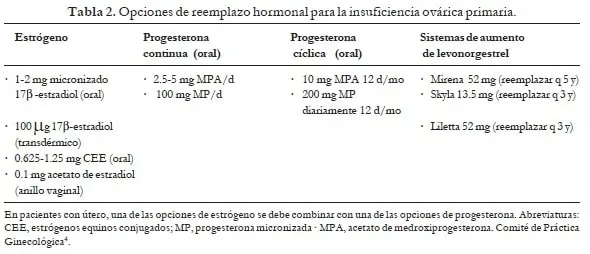
La dosis óptima de suplementos de estrógenos en esta población es desconocida; sin embargo, a menudo se necesitan dosis más altas para mejorar los síntomas y lograr concentraciones de estradiol en sangre similares a las de las mujeres que menstrúan. ACOG recomienda 100 μ g de estradiol al día, que puede administrarse por vía oral, transdérmica o vaginal (tabla 2)4.
 El riesgo de tromboembolismo venoso (TEV) aumenta cuando se toman estrógenos por vía oral, en lugar de modalidades transdérmicas o vaginales. El estudio multicéntrico de Estrógeno y Riesgo de Tromboembolismo (ESTHER) evaluó el peligro de estrógeno oral versus estrógeno transdérmico en mujeres posmenopáusicas.
El riesgo de tromboembolismo venoso (TEV) aumenta cuando se toman estrógenos por vía oral, en lugar de modalidades transdérmicas o vaginales. El estudio multicéntrico de Estrógeno y Riesgo de Tromboembolismo (ESTHER) evaluó el peligro de estrógeno oral versus estrógeno transdérmico en mujeres posmenopáusicas.
Descubrieron que el riesgo de TEV para el estrógeno oral era de 4,2 (intervalo de confianza [IC] del 95%, 1,5-11,6) en comparación con 0,9 (IC del 95%, 0,4-2,1) en los usuarios transdérmicos5. Esto debe tenerse en cuenta al seleccionar un régimen de tratamiento.
Hiperplasia Endometrial y el Cáncer
En mujeres con útero intacto, la administración de suplementos con progesterona cíclica o continua está indicada para prevenir la hiperplasia endometrial y el cáncer. También se puede considerar la colocación de un dispositivo intrauterino de levonorgestrel; especialmente en mujeres que desean anticoncepción.
Sin embargo, es importante señalar que el dispositivo intrauterino de levonorgestrel solo se ha estudiado en mujeres posmenopáusicas de más edad que usan dosis bajas de estradiol y no en mujeres con IOP.
La TH compuesta a medida que contiene estradiol y progesterona entre otras hormonas ha ganado atención popular; sin embargo, estas formulaciones no están reguladas por la FDA y, por lo tanto, no son recomendadas por ninguna sociedad médica importante.
Con poca frecuencia, la fertilidad puede persistir en las mujeres con IOP:
A pesar de la escasez de folículos ováricos funcionales, y aproximadamente del 5% al 10% de estas mujeres pueden experimentar un embarazo espontáneo. La efectividad de los anticonceptivos orales (AO) en esta población no está clara.
Se hipotetiza que la concepción mientras está en AOs puede ocurrir porque estos no pueden suprimir los altos niveles de hormona estimulante de folículos. Por lo tanto, se deben fomentar los métodos de barrera o un dispositivo intrauterino.
Además, algunas mujeres con IOP pueden experimentar una mayor incidencia de manchado en TH debido a la persistencia de actividad ovárica residual. Estas mujeres pueden beneficiarse de las dosis anticonceptivas para el control hormonal.
Sin embargo, debido a que la dosis de estrógeno y progesterona es mucho más alta en los anticonceptivos hormonales combinados que en la TH de reemplazo, puede aumentar el riesgo de tromboembolia, accidente cerebrovascular, aumento de la presión arterial e hiperlipidemia. El beneficio de iniciar una dosis más alta de hormona debe sopesarse contra los riesgos.
Otra desventaja de la anticoncepción hormonal es la «semana libre de píldoras». Aunque es temporal, se produce un estado deficiente en estrógenos, que puede provocar el regreso de los síntomas de la menopausia no deseados durante ese intervalo. (Lea También: Uso de Testosterona)
Deficiencia de Testosterona
Las mujeres con IOP también experimentan síntomas relacionados con la deficiencia de testosterona. La producción de testosterona endógena es normalmente de aproximadamente 300 μg al día; mitad producida por las glándulas suprarrenales y el resto por los ovarios. Actualmente, la literatura no respalda el tratamiento de la deficiencia de testosterona en mujeres con IOP. Se necesitan más estudios a largo plazo para evaluar la seguridad y eficacia del uso; sin embargo, estudios limitados muestran una función sexual mejorada con suplementos de testosterona.
La dehidroepiandrosterona (DHEAS) es otro andrógeno producido por la suprarrenal y el ovario. Hay evidencia que apoya que 6 semanas de suplemento con DHEAS mejora la respuesta ovárica en mujeres con insuficiencia ovárica que se someten a tratamiento de fertilidad. Sin embargo, la evidencia actual no respalda el reemplazo rutinario de DHEA para mujeres con IOP.6
La insuficiencia ovárica primaria y la menopausia precoz están asociadas con numerosas implicaciones para la salud a largo plazo y una disminución de la calidad de vida. En ausencia de contraindicaciones fuertes, se recomienda TH para prevenir riesgos de salud a largo plazo y tratar los síntomas causados por el hipoestrogenismo. El tratamiento temprano es esencial para mejorar los resultados.
Referencias
- Sullivan SD, Sarrel PM, Nelson LM. Hormone replacement therapy in young women with primary ovarian insufficiency and early menopause. Fertil Steril. 2016;106(7):1588-1599.
- Swerdlow AJ, Cooke R, Bates A, et al; England and Wales Hodgkin Lymphoma follow-up Group. Risk of premature menopause after treatment for Hodgkin’s lymphoma. J Natl Cancer Inst. 2014;106(9). pii: dju207. Doi 10.1093/dju207.
- Faubion SS, Kuhle CL, Shuster LT, Rocca WA. Long-term health consequences of premature or early menopause and considerations for management. Climacteric. 2015;18(4): 483-491.
- Committee on Gynecologic Practice. Committee opinion no. 698: hormone therapy in primary ovarian insufficiency. Obstet Gynecol. 2017;129(5):e134-e141.
- Canonico M, Oger E, Plu-Bureau G, et al; Estrogen and Thromboembolism Risk (ESTHER) Study Group. Hormone therapy and venous thromboembolism among postmenopausal women: impact of the route of estrogen administration and progestogens: the ESTHER study. Circulation. 2007;115(7): 840-845.
- Luisi S, Orlandini C, Regini C, Pizzo A, Vellucci F, Petraglia F. Premature ovarian insufficiency: from pathogenesis to clinical management. J Endocinol Invest. 2015;38(6):597-603.
Monica M Christmas, MD,
FACOG, NCMP
Assistant Professor
Section of Minimally Invasive
Gynecologic Surgery
The University of Chicago Medicine
Chicago, Illinois
Conflicto de intereses
No reporta conflictos de intereses financieros relevantes.



