Explicando a las mujeres que los SVM están asociados con un pequeño aumento de la temperatura corporal se puede ayudar a que ellas los entiendan y los manejen.
Enfoques simples, no médicos, pueden ser suficientes en mujeres que prefieren no usar la TH. Algunos ejemplos pueden ser:
– Identificar y evitar los factores desencadenantes de sofocos.
– Vestirse en varias capas removibles.
– Llevar un ventilador eléctrico portátil o de accionamiento manual.
– Aplicación de hielo o un producto de la evaporación en la muñeca o en la espalda o el cuello al inicio de los sofocos.
– Dormir en una habitación fresca con una bolsa de hielo debajo de la almohada o usar la ropa de cama y la ropa para dormir de lino.
Los datos existentes sobre la efectividad de las intervenciones de estilo de vida están en conflicto. Estudios de ejercicio (por ejemplo, yoga) y las intervenciones dietéticas (por ejemplo, la soja) muestran resultados mixtos. Respiración regular-establecido 1 paso y otros esfuerzos de cuerpo y mente han demostrado ser algo útil para los SVM, pero la formación y la práctica en curso requeridas son a menudo poco prácticas.9
Está disponible una variedad de más productos de venta libre que dicen que son curativos para los fogajes; sin embargo, según los estudios científicos de apoyo, su seguridad y eficacia son escasos, y algunos de los mejores ensayos clínicos no muestran efecto.10 Los clínicos deben advertir a las mujeres que estos productos no están regulados por el gobierno, ni están obligados a cumplir con las normas rigurosas de fabricación. Curiosamente, pequeños estudios han demostrado que el ácido fólico (5 mg/d)11, y más recientemente, el óxido de magnesio (400 mg/d),12 alivian los sofocos. Sin embargo, el primero fue solo un estudio de cohorte, y el segundo fue un estudio piloto. Ensayos controlados aleatorios (ECA) más grandes son necesarios para confirmar estos resultados.
Alternativas con receta
Observaciones al azar han conducido a la identificación de prescripciones alternativas al estrógeno que proporcionan alivio a los fogajes (tabla 1). El número de investigaciones publicadas de posibles opciones se ha incrementado dramáticamente a la luz de la creciente preocupación por los riesgos de las hormonas. Ninguno de estos productos está aprobado por el gobierno para este uso, pero al menos dos agentes neuroactivos (baja dosis de sal mesilato de paroxetine13 y pregabalina [Lyrica])14 se han presentado a la Food and Drug Administration (FDA) de EE.UU. para su revisión.
Tabla 1. Algunos compuestos usados como alternativa para los SVM
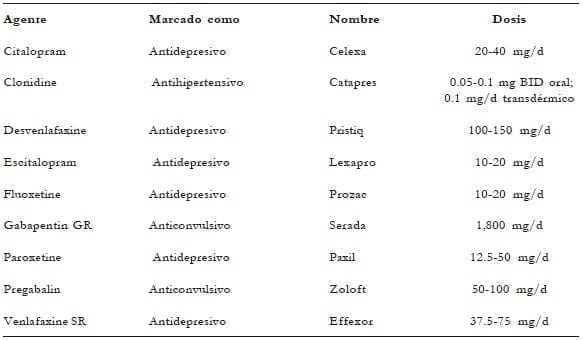
Muchos de los primeros ensayos sobre terapias alternativas se llevaron a cabo en las sobrevivientes de cáncer de mama, cuya renuencia a usar estrógeno ha sido desde hace mucho tiempo. Hasta la fecha, las principales categorías estudiadas incluyen el antihipertensivo clonidina, los antidepresivos inhibidores selectivos de la recaptación de serotonina (ISRS) y los inhibidores de la recaptación de serotoninanorepinefrina (IRSN), y el anticonvulsivante gabapentina y su producto de próxima generación pregabalina. Estas drogas han mostrado ser mejores que el placebo en ensayos a corto plazo, la mayoría de los cuales tenía deficiencias en su tamaño, duración o método de mediciones de los fogajes. Los sofocos no siempre se registraron por la frecuencia, la gravedad y molestias en un diario en tiempo real como es solicitado por la guía de la FDA para la industria.
Una revisión Cochrane identificó16 ECAs que cumplieron con criterios rigurosos y concluyeron que clonidina, SSRIs y SNRIs, la terapia de la gabapentina y la terapia de relajación mostraban una efecto leve a moderado en la reducción de los sofocos en mujeres con antecedentes de cáncer de mama.15
Los médicos se enfrentan a varios retos en la elección entre estas opciones. Los estudios de eficacia utilizaron diferentes medidas. Todos los estudios demostraron efecto placebo significante pero variable.
La mayoría de las dosis son bajas, y los datos sobre el aumento de dosis son limitados. Excepciones son estudios de gabapentina GR (Serada),16,17 dosis bajas de sal mesilato de paroxetina,13 y desvenlafaxina.18 En 2011, la FDA no aprobó el antidepresivo desvenlafaxina para eltratamiento de SVM moderados a severos, indicando que los datos no establecieron un perfil riesgo-beneficio aceptable.18
Los estudios cabeza a cabeza de los tratamientos no hormonales para SVM o, para el caso, entre el estrógeno y las opciones no estrógenos, son muy pocos. Un estudio que comparó la fluoxetina y citalopram no mostró un efecto estadístico de cualquiera de los dos tratamientos para los fogajes, aunque este estudio ha sido criticado por no tener un período de observación antes de iniciar el tratamiento.
19 Un estudio que comparó el estrógeno y la gabapentina mostró una eficacia similar para los dos agentes.
Un ECA reciente de venlafaxina en comparación con la clonidina versus placebo mostró una respuesta más rápida de la venlafaxina, mientras que la clonidina fue estadísticamente diferente del placebo a las 12 semanas solamente.20
Este estudio también muestra las dificultades de los estudios cortos. El acompañamiento editorial pasó a señalar el limitado poder del estudio para distinguir entre las dos drogas.21
Loprinzi y sus colegas de la Clínica Mayo estudiaron tratamientos no estrogénicos de los SVM utilizando datos agrupados para comparar los dos agentes.22 El estudio tenía limitaciones (por ejemplo, solo cuatro semanas de tratamiento), pero en conclusión, este análisis combinado actual no apoya que tanto los antidepresivos más nuevos como la gabapentina sean útiles para el alivio de los fogajes en las mujeres. Se sugiere, sin embargo, que la eficacia de nuevos antidepresivos no es idéntica entre los agentes estudiados; con velafaxina y paroxetina parece que disminuyen losfogajes más que con setralina y fluoxetina.
En una investigación de sertralina para losSVM, los investigadores identificaron algunos resultados dichos.23 Algunas mujeres tenían menos fogajes cuando se trataban, algunas agravaban sus síntomas y otras no mostraban ninguna respuesta a la medicación.
Los efectos adversos de estos medicamentos, que incluyen mareos, náuseas y, por desgracia, la disfunción sexual (para los antidepresivos) son a menudo problemáticos, pero a veces se resuelven con el tiempo. Partir de una dosis baja y luego aumentarla puede ser una buena estrategia para reducir los efectos adversos y maximizar el éxito terapéutico. Una vez más, los médicos tienen limitadas guías de datos para la elección de uno u otro. No hay datos que informen sobre la elección de un fármaco de segunda línea después de que uno ha sido insatisfactorio. La gabapentina es sedante, por lo que a veces es muy eficaz para las mujeres cuyaqueja principal es la interrupción del sueño. El fármaco se puede utilizar a la hora de acostarse, a partir de una dosis tan baja como 100 mg y aumentarla cada tres a cinco días a un máximo de 1.000 mg o más.
Otra área que es una zona libre de datos es cómo el uso de medicamentos no hormonalesrecetados se comporta con el tiempo. ¿Por cuánto tiempo son necesarios? ¿Cuáles son los riesgos a largo plazo? ¿Reaparecen los sofocos cuando estos son descontinuados?
Un interesante estudio recientemente miró la recaída de SVM en mujeres que habían tenido una respuesta a escitalopram.24 Solo un tercio había tenido recurrencia de sus síntomas tres semanas después de que había dejado la medicación. Desafortunadamente, estos resultados no ofrecen mucha orientación sobre meses o incluso años.
Al final de un artículo reciente, Hall y colaboradores concluyeron:
Esta extensa revisión proporciona evidencia de las opciones eficaces para aquellas que no pueden o no quieren usar hormonas.10 La gabapentina es buena para los sudores nocturnos. La paroxetina y la venlafaxina son probablemente las mejores entre los antidepresivos más antiguos y proporcionan alivio a algunas mujeres. Son necesarios más estudios para aclarar las funciones de la desvenlafaxina y la pregabalina.
De hecho, uno puede haber oído hablar de la FDA acerca de esta última en el momento que este artículo se publica. Como ya se ha visto, las elecciones tienen eficacias y efectos adversos variables; la elección de la terapia adecuada para una mujer puede implicar ensayo y error.
Referencias
1. Ockene JK, Barad DH, Cochrane BB, et al. Symptom experience after discontinuing use of estrogen plus progestin. JAMA 2005; 294:183-193.
2. Archer DF, Sturdee DW, Baber R, et al. Menopausal hot flushes and night sweats: where are we now? Climacteric 2011;14:515-528.
3. Mann E, Hunter S. Concordance between selfreported and sternal skin conductance measures of hot flushes in symptomatic perimenopausal and post-menopausal women: a systematic review. Menopause 2011;18:709-722.
4. Thurston RC, Bromberger JT, Joffe H, et al. Beyond frequency: who is most bothered by vasomotor symptoms? Menopause 2008;15: 841-847.
5. Freeman EW, Sammel MD, Lin H, Liu Z, Gracia CR. Duration of menopausal hot flushes and associated risk factors. Obstet Gynecol 2011;117:1095-1104.
6. Rödström K, Bengtsson C, Lissner L, Milsom I, Sundh V, Björkelundi C. A longitudinal study of the treatment of hot flushes: the population study of women in Gothenburg during a quarter of a century. Menopause 2002;9:156-161.
7. Thurston RC, Joffe H. Vasomotor symptoms and menopause: findings from the Study of Women’s Health Across the Nation. Obstet Gynecol Clin North Am 2011;38:489-501.
8. Prior JC, Hitchcock CL. Progesterone for hot flush and night sweat treatmentVeffectiveness for severe vasomotor symptoms and lack of withdrawal rebound. Gynecol Endocrinol 2012;28(suppl 2):7-11.
9. Innes KE, Selfe TK, Vishnu A. Mind-body therapies for menopausal symptoms: a systematic review. Maturitas 2010;66:135-149.
10. Hall E, Frey BN, Soares CN. Non-hormonal treatment strategies for vasomotor symptoms: a critical review. Drugs 2011;71:287-304.
11. Gaweesh SS, Abdel-Gawad MM, Nagaty AM, Ewies AA. Folic acid supplementation may cure hot flushes in postmenopausal women: a prospective cohort study. Gynecol Endocrinol 2010;26:658-662.
12. Park H, Parker GL, Boardman CH, MorrisMM, Smith TJ. A pilot phase II trial of magnesium supplements to reduce menopausal hot flashes in breast cancer patients. Support Care Cancer 2011;19:859-863.
13. Stearns V, Beebe KL, Iyengar M, Dube E.Paroxetine controlled release in the treatment of menopausal hot flashes: a randomized controlled trial JAMA 2003;289:2827-2834.
14. Loprinzi CL, Qin R, Balcueva EP, et al. Phase III, randomized, doubleblind, placebocontrolled evaluation of pregabalin for alleviating hot flashes, N07C1. Clin Oncol 2010;28:641-647.
15. Rada G, Capurro D, Pantoja T, et al. Nonhormonal interventions for hot flushes in women with a history of breast cancer. Cochrane Database Syst Rev 2010;CD004923.
16. Reddy SY, Warner H, Guttuso T Jr, et al. Gabapentin, estrogen, and placebo for treating hot flushes: a randomized controlled trial. Obstet Gynecol 2006;108:41-48.
17. Pandya KJ, Morrow GR, Roscoe JA, et al. Gabapentin for hot flashes in 420 women with breast cancer: a randomised doubleblind placebocontrolled trial. Lancet 2005;366: 818-824.
18. Pinkerton JV, Archer DF, Guico-Pabia CJ, Hwang E, Cheng RJ. Maintenance of the efficacy of desvenlafaxine in menopausal vasomotor symptoms: a 1-year randomized controlled trial. Menopause 2013;20:38-46.
19. Suvanto-Luukkonen E, Koivunen R, Sundström H, et al. Citalopram and fluoxetine in thetreatment of postmenopausal symptoms: a prospective, randomized, 9-month, placebocontrolled, double-blind study. Menopause 2005;12:18-26.
20. Boekhout AH, Vincent AD, Dalesio OB, et al. Management of hot flashes in patients who have breast cancer with venlafaxine and clonidine: a randomized, double-blind, placebo-controlled trial. J Clin Oncol 2011; 29:3862-3868.
21. Loprinzi CL, Barton DL, Qin R. Nonestrogenic management of hot flashes. J Clin Oncol 2011;29:3842-3846.
22. Loprinzi CL, Sloan J, Stearns V, et al. Newer antidepressants and gabapentin for hot flashes: an individual patient pooled analysis. J Clin Oncol 2009;27:2831-2837.
23. Kerwin JP, Gordon PR, Senf JH. The variable response of women with menopausal hot flashes when treated with sertraline. Menopause 2007; 14:841-845.
24. Joffe H, Guthrie KA, Larson J, et al. Relapse of vasomotor symptoms after discontinuation of the selective serotonin reuptake inhibitor escitalopram: results from the Menopause Strategies: Finding Lasting Answers for Symptoms and Health Research Network. Menopause 2013;20:261-268.
