Los datos del WISDOM sugieren que las mujeres que empiezan o reinician terapia combinada de estrógenos y progestágeno, en promedio 14 años luego de la menopausia, tienen mayor riesgo de desarrollar enfermedad cardiovascular y tromboembolismo venoso, por lo menos durante los primeros años de tratamiento. Se encontró una tendencia hacia la reducción del riesgo de una fractura osteoporótica y ninguna diferencia en el riesgo de enfermedad cerebrovascular o cáncer. El pequeño número de eventos y el corto tiempo de seguimiento inevitablemente se traducen en que algunos resultados no pueden ser interpretados con confianza. Sin embargo se puede comentar sobre los resultados de aparición temprana de enfermedad cardiovascular y enfermedad tromboembólica. En una comparación directa con la terapia combinada de estrógenos y progestágeno, la terapia de solo estrógenos puede tener efectos similares, pero menores, a corto plazo. Estos resultados son consistentes con los hallazgos del brazo de terapia combinada de estrógenos y progestágeno del estudio de iniciativa de salud de las mujeres y con los estudios de prevención secundaria y soportan la conclusión de que la terapia combinada de estrógenos y progestágeno no debe utilizarse para prevención de la enfermedad cardiovascular en mujeres posmenopáusicas mayores4,7-9.
Valor del estudio
A pesar del hecho que el WISDOM no corrió hasta completarse, este ensayo hace una contribución importante a la masa de conocimiento sobre terapia de reemplazo hormonal iniciada en mujeres posmenopáusicas mayores con edad promedio de 63 años. La población del WISDOM fue reclutada de mujeres de los registros de la práctica general en países donde el cuidado de la salud es gratis o con costos bajos. Las mujeres aleatorizadas tenían un perfil similar de salud con respecto a los factores de interés del estudio, así como aquellas en el mismo rango de edad que fueron seleccionadas inicialmente. Exceptuando la historia de cáncer de seno, una historia familiar de tromboembolismo venoso y otros factores de exclusión que las hubiera hecho menos aptas a recibir terapia de reemplazo hormonal, las participantes del WISDOM eran similares a la población registrada y a la poblacióndelReino U nido del m ism o rango de edad19.
Tabla 5. Números de eventos adversos serios entre las participantes del WISDOM por grupo de tratamiento.
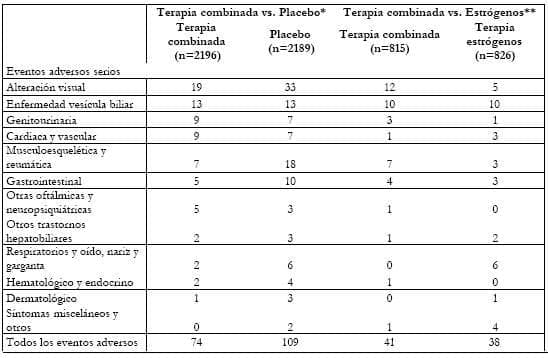
Terapia combinada = estrógenos equinos conjugados 0.625 mg + acetato de medroxiprogesterona 2.5 mg orales diarios.
† Terapia estrogénica = estrógenos equinos conjugados 0.625 mg orales diarios
Una fortaleza del estudio es que las participantes posiblemente son representativas de la población general de esta edad y sus resultados aplicables a este grupo de mayor edad. Comparando la población en el estudio de iniciativa de salud de las mujeres, muchas de ellas en el WISDOM, de manera similar, estaban en sobrepeso o eran obesas y tenían factores de riesgo cardiovascular similares7,12. La edad promedio al ingreso también fue semejante. Sin embargo, el uso previo de terapia de reemplazo hormonal fue mayor en el WISDOM que en el estudio de iniciativa de salud de las mujeres (45% comparado con 26% en mujeres con útero).
Comparación de los resultados
Para la terapia combinada de estrógenos y progestágeno, los resultados del WISDOM son similares a los hallazgos de los primeros años del estudio de iniciativa de salud de las mujeres.
Tromboembolismo venoso. La tasa de eventos en mujeres que recibían terapia combinada de estrógenos y progestágeno en el WISDOM fue superior a aquella reportada en los años iniciales del estudio de iniciativa de salud de las mujeres, a pesar de haber excluido en el WISDOM aquellas con eventos previos.
La razón para esto no es clara, pero en vista del pequeño número de eventos, puede ser un hallazgo al azar. El aumento en la tasa de tromboembolismo venoso con la terapia combinada fue mayor durante el primer año en el estudio de iniciativa de salud de las mujeres7. Es posible que aquellas personas con una predisposición genética a la trombosis tengan una vulnerabilidad temprana a la terapia de reemplazo hormonal20.
Enfermedad cardiovascular. Aunque el número de eventos cardiovasculares observados fue pequeño, todos ocurrieron en los grupos de terapia de reemplazo hormonal, con una tasa de 27 por 10.000 mujeres año en el brazo de terapia combinada del WISDOM. Esta tasa fue más pequeña que la de 51 por 10.000 mujeres al año, observada en el primer año en el brazo de terapia combinada del estudio de iniciativa de salud de las mujeres (WHI). El incremento temprano en el riesgo de eventos cardiovasculares en ambos estudios es compatible con la hipótesis de que la administración de terapia de reemplazo hormonal, particularmente la combinación de estrógenos y progestágeno, a mujeres varios años después de la menopausia, quienes probablemente tengan arteriosclerosis establecida, puede causar disrupción de la superficie de la placa con la consecuente adherencia de plaquetas, coagulación y posterior estrechamiento arterial21. La mayoría de eventos en el WISDOM ocurrieron en mujeres mayores de 64 años, muchas de las cuales tenían factores de riesgo cardiovascular.
Fracturas. La tendencia no significativa hacia el riesgo reducido de fracturas después del periodo de seguimiento promedio de tan solo un año es acorde con la reducción significativa de fracturas vista en el estudio de iniciativa de salud de las mujeres7,12.
Ni el WISDOM ni el estudio de iniciativa de salud de las mujeres requirieron un aumento en el riesgo de fractura dentro de los criterios de inclusión, por lo cual los resultados sugieren un efecto preventivo potente en una población no seleccionada. Así como en el estudio de iniciativa de salud de las mujeres, no se encontró una diferencia aparente entre la terapia combinada y la de solo estrógenos en su efecto sobre prevención de fracturas.
Cáncer. No se encontró ningún efecto sobre las tasas de cáncer, incluyendo el de seno, pero esto debe ser interpretado con cautela ya que el máximo seguimiento fue por tres años (mediana un año). Un descenso en el riesgo anual de cáncer de seno de 7 por 10.000 casos comparado con placebo luego de casi siete años de terapia con estrógenos fue reportado en el estudio de iniciativa de salud de las mujeres, que se aproximó a la significancia estadística, pero la terapia combinada se asoció con un incremento significativo en el riesgo anual de 8 por 10.0000 casos luego de cinco años7,12,22. WISDOM fue incapaz de dar luces sobre la relación entre el progestágeno y el cáncer de seno, aunque los datos de todos los desenlaces sugirieron mayor seguridad de la terapia con solo estrógenos, similar a los resultados del estudio de iniciativa de salud de las mujeres
Muerte. El aparente, pero no significativo, aumento en la mortalidad en usuarias de la terapia combinada frente al placebo no es acorde con un meta-análisis reciente de todos los estudios aleatorios y controlados de terapia de reemplazo hormonal (incluyendo la iniciativa de salud de las mujeres), que no mostró una mortalidad aumentada sobre una reducción global y significativa de la mortalidad de usuarias de hormonas en aquellas menores de 60 años (razón de disparidad 0.67 [intervalo de confianza 95% 0.49-0.92]) 2 3. El corto tiempo de seguimiento y el pequeño número de muertes registrado en el WISDOM no permiten conclusiones robustas.
Limitaciones del estudio
El período de seguimiento en el WISDOM fue corto debido al cierre prematuro y el poder del estudio se vio reducido de manera importante por el reclutamiento acortado, que también condujo a relativamente pocas mujeres en los grupos de menor edad. No se pueden sacar conclusiones sobre los desenlaces en relación con estos grupos de edad.
Implicación de los resultados
En el WISDOM tan solo se estudiaron dos regímenes de terapia de reemplazo hormonal que contenían estrógenos equinos conjugados y cuando eran combinados, contenían acetato de medroxiprogesterona.
La profesión médica y los medios deben interpretar y diseminar los resultados del WISDOM con cautela y responsabilidad. En el 2002 las respuestas desconsideradas, y en ocasiones exageradas, al primer reporte de uno de los brazos del estudio de iniciativa de salud de las mujeres produjeron alarma y ansiedad alrededor del mundo, con muchas mujeres suspendiendo abruptamente la terapia de reemplazo hormonal sin consultar a su médico y en algunos casos con consecuencias adversas24,25.
Los resultados del WISDOM, así como los del estudio de iniciativa de salud de las mujeres, ayudan a probar la hipótesis de que iniciar terapia de reemplazo hormonal a largo plazo en mujeres mayores, frecuentemente asintomáticas y en sus sesentas, puede reducir morbilidades mayores, en particular la enfermedad cardiovascular. Con excepción de las fracturas, esto no parece ser probable. Sin embargo, usualmente dichas mujeres rara vez inician terapia de reemplazo hormonal a esa edad. La mayoría de mujeres que inician terapia de reemplazo hormonal lo hacen cerca a la menopausia, con el ánimo de reducir los síntomas y mejorar la calidad de vida. Los estudios clínicos y animales sugieren que los efectos de los estrógenos sobre el sistema cardiovascular, y probablemente el cerebro, pueden ser muy diferentes y probablemente benéficos cuando estos se usan cerca o en el momento de la menopausia26-28. En particular un meta-análisis reciente de 23 estudios aleatorios y controlados sobre terapia de reemplazo hormonal mostró que reducía de manera significativa la enfermedad coronaria en mujeres que iniciaban la terapia jóvenes, menores de 60 años o dentro de los primeros 10 años desde la menopausia29.
La terminación temprana del WISDOM antes de poder reclutar un gran número de mujeres recientemente menopáusicas significa que la “hipótesis de una ventana crítica” no pudo ser examinada para ver si el estrógeno tiene efectos cardioprotectores y neuroprotectores20,30. La ecuación riesgo/beneficio para una mujer posmenopáusica más joven puede ser diferente de aquella vista en las mujeres predominantemente mayores del WISDOM y el estudio de iniciativa de salud de las mujeres.
La publicidad que rodeó el primer reporte del primer brazo del estudio de iniciativa de salud de las mujeres impuso gran presión sobre los patrocinadores del WISDOM para frenar el estudio15,31. Detalles sobre los resultados más favorables del brazo de solo estrógenos y los reanálisis del estudio de iniciativa de salud de las mujeres por edad y años de la menopausia, que sugerían resultados diferentes cuando la terapia de reemplazo hormonal se inicia en la menopausia temprana, estuvieron disponibles solo varios años después del cierre del WISDOM32. Un estudio a largo plazo, aleatorio, controlado con placebo sobre la terapia de reemplazo hormonal desde la menopausia aún es necesario pero presenta grandes problemas en términos de patrocinio, cumplimiento y continuidad, especialmente en mujeres sintomáticas.
Conclusiones
Las mujeres en el estudio de iniciativa de salud de las mujeres y el WISDOM no han respondido la pregunta respecto a los beneficios y riesgos de la terapia de reemplazo hormonal en la gran mayoría de quienes la empiezan alrededor de la menopausia para el control de síntomas. Sin embargo, han mostrado que no existe un beneficio de prevención global de enfermedades y sí un riesgo potencial, en mujeres con pocos o sin síntomas de deficiencia estrogénica que inician terapia de reemplazo hormonal varios años después de la menopausia. Si existe una ventana de beneficio terapéutico, su límite superior no ha sido establecido y es probable que varíe con la salud arterial y factores de riesgo asociados como obesidad y el síndrome metabólico33.
Tanto las mujeres del estudio de iniciativa de salud de las mujeres como las del WISDOM estaban buscando específicamente prevención de enfermedades crónicas en mujeres posmenopáusicas mayores que no tenían síntomas menopáusicos incapacitantes.
Un aumento en la calidad de vida asociado con la reducción en los síntomas de la menopausia es la motivación usual para tomar terapia de reemplazo hormonal. Datos sobre calidad de vida del WISDOM se publicarán separadamente y esos resultados deben considerarse a la par de los principales desenlaces de morbilidad y mortalidad descritos en esta publicación.
Aquellos que ayudan a las mujeres a tomar decisiones sobre el tratamiento deben considerar tanto los resultados como las limitaciones del estudio de iniciativa de salud de las mujeres y el WISDOM, particularmente aquello que puede verse influenciado por el tiempo de inicio de la terapia de reemplazo hormonal.
Referencias
1. MacLennan AH, Broadbent JL, Lester S, Moore V. Oral oestrogen and combined oestrogen/progestogen therapy versus placebo for hot flushes. Cochrane Database Syst Rev 2004; (4): CD002978.
2. Suckling J, Lethaby A, Kennedy R. Local oestrogen for vaginal atrophy in postmenopausal women. Cochrane Database Syst Rev 2003; (4): CD001500.
3. Moehrer B, Hextall A, Jackson S. Oestrogens for urinary incontinence in women. Cochrane Database Syst Rev 2003; (2): CD001405.
4. Hulley S, Grady D, Bush T, Furberg C, Herrington D, Riggs B, et al. Randomized trial of estrogen plus progestin for secondary prevention of coronary heart disease in postmenopausal women. Heart and Estrogen/ progestin Replacement Study (HERS) Research Group. JAMA 1998; 280: 605-613.
5. Hoibraaten E, Qvigstad E, Arnesen H, Larsen S, Wickstrom E, Sandset PM. Increased risk of recurrent venous thromboembolism during hormone replacement therapy. Results of the randomized, double-blind, placebo-controlled estrogen in venous thromboembolism trial (EVTET). Thromb Haemost 2000; 84: 961-967.
6. Viscoli CM, Brass LM, Kernan WN, Sarrel PM, Suissa S, Horwitz RL. A clinical trial of estrogen—replacement therapy after ischemic stroke. N Engl J Med 2001; 345: 1243-1249.
7. Writing Group for the Women’s Health Initiative Investigators. Risks and benefits of estrogen plus progestin in healthy postmenopausal
women. Principal results from the women’s health initiative randomized controlled trial. JAMA 2002; 288: 321-333.
8. Clarke SC, Kelleher J, Lloyd-JonesH, SlackM, Schofield PM. A study of hormone replacementtherapy in postmenopausal women with ischaemic heart disease: the Papworth HRT atherosclerosis study. BJOG 2002; 109: 1056- 1062.
9. ESPRIT Team. Oestrogen therapy for prevention of re-infarction in postmenopausal women: a randomised controlled trial. Lancet 2002; 359: 2001-2008.
10. Waters DD, Alderman EL, Hsia J, Howard BV, Cobb FR, Rogers WJ, et al. Effects of hormone replacement therapy and antioxidant vitamin in postmenopausal supplements on coronary atherosclerosis in postmenopausal women: a randomized controlled trial. JAMA 2002; 288: 2432-2440.
11. Holmberg L, Anderson H, for the HABITS steering and data monitoring committees. HABITS (hormonal replacement therapy after breast cancer—is it safe?), a randomised comparison: trial stopped. Lancet 2004; 363: 453-455.
12. Women’s Health Initiative Steering Committee. Effects of conjugated equine estrogen in postmenopausal women with hysterectomy. The women’s health initiative randomised controlled trial. JAMA 2004; 291: 1701-1712.
13. Veerus P, Hovi S, Fischer K, RahuM, HakamaM, Hemminki E. Results from the Estonian postmenopausal hormone therapy trial. Maturitas 2006; 55: 162-173.
14. Manson JE, Hsia J, Johnson KC, Rossouw JE, Assaf AR, Lasser NL, et al. Estrogen plus progestin and the risk of coronary heart disease. N Engl J Med 2003; 349: 523-534.
15. Vickers M. The MRC long-term randomised controlled trial of hormone replacement therapy: background, design and objectives. J Br Menopause Soc 1996; 1: 9-13.
16. Vickers M, Meade T, Darbyshire J. WISDOM: history and early demise —was it inevitable? Climacteric 2002; 5: 317-325.
17. Vickers MR, Martin J, Meade TW and the WISDOM Study Team. The women’s international study of long duration oestrogen after menopause (WISDOM): a randomised controlled trial. BMCWomen’s Health 2007; 7: 2. www.biomedcentral.com/1472-6874/7/2.
18. Collett D. Modelling survival data in medical research. London: Chapman and Hall, 1994.
19. Bajekal M. Use of health services and prescribed medicines. In: Department of Health. Health survey for England 1998 . www.archive.official-documents.co.uk/ document/doh/survey98/hse-07.
20. Cushman M, Kuller LH, Prentice R, Rodabough RJ, Psaty BM, Stafford RS, et al. Oestrogen plus progestin and risk of venous thrombosis. JAMA 2004; 292: 1573-1580.
21. Phillips LS, Langer RD. Postmenopausal hormone therapy: critical reappraisal and a unified hypothesis. Fertil Steril 2005; 83: 558-566.
22. Stefanick ML, Anderson GL, Margolis KL, Hendrix SL, Rodabough RJ, Paskett ED, et al. Effects of conjugated equine estrogens on breast cancer and mammography screening in postmenopausal women with hysterectomy. JAMA 2006; 295: 1647-1657.
23. Salpeter S. Mortality associated with hormone replacement therapy in younger and older women. J Gen InternMed 2004; 19: 791-804.
24. Lawton B, Rose S, McLeod D, Dowell AC. Changes in use of hormone replacement therapy after the report from the women’s health initiative: cross sectional survey of users. BMJ 2003; 327: 845-846.
25. MacLennan AH, Taylor AW, Wilson DH. Hormone therapy use after the women’s health initiative. Climacteric 2004; 7: 138-142.
26. MacLennan AH, Henderson VW, Paine BJ, Mathias J, Ramsay EN, Ryan P, et al. Hormone therapy, timing of initiation, and cognition in women older than 60 years: the REMEMBER pilot study. Menopause 2006; 13: 28-36.
27. Clarkson TB, Appt SE. Controversies about HRT—lessons from monkey models. Maturitas 2005; 51: 64-74.
28. Grodstein F, Manson JE, Stampher MJ. Hormone therapy and coronary heart disease: the role of time since menopause and age at hormone initiation. J Women’s Health 2006; 15: 35-44.
29. Salpeter SR, Walsh JME, Greyber E, Salpeter EE. Coronary heart disease events associated with hormone therapy in younger and older women. J Gen Intern Med 2006; 21: 363-366.
30. Salpeter S. Hormone therapy for younger postmenopausal women: how can we make sense out of the evidence? Climacteric 2005; 8: 307-310.
31. MacLennan AH, Sturdee D. The end of WISDOM. Climacteric 2002; 5: 313-316.
32. Manson JE, Allison MA, Rossouw JE, Carr JJ, Langer RD, Hsia J, et al. Estrogen therapy and coronary-artery calcification. N Engl J Med 2007; 356: 2591-602.
33. Tankó LB, Christiansen C. Adipose tissue, insulin resistance, and low-grade infla – mmation: implications for atherogenesis and the cardiovascular harm of estrogen plus progestogen therapy. Climacteric 2006; 9: 169-180.
