Para el mantenimiento de la secreción y biosíntesis de gonadotropinas es necesaria la liberación pulsátil de LHRH hipotalámica. La exposición sostenida del gonadotropo a altas concentraciones constantes de LHRH reduce la respuesta celular frente a estímulos subsiguientes con LHRH. Esto se conoce como desensibilización homóloga y es el principal mecanismo de acción de los análogos de la LHRH. El mecanismo exacto de la desensibilización homóloga es desconocido pero comprende: 1- Desacoplamiento del receptor de su proteína G reguladora; 2- Pérdida de receptores; 3- desensibilización de la vía de la proteinkinasa C; 4- Depleción del pool de gonadotropinas; 5- Inactivación de canales de calcio; y 6- Reducción en la eficiencia para la movilización del calcio por los fosfatos de inositol17-19.
El LHRH se une a dos tipos de receptores de membrana en las células de la hipófisis, unas de baja y otras de alta afinidad. El LHRH es desplazado por el Cetrorelix de ambos receptores que tiene una afinidad constante 5 veces mas para el receptor de baja y 1,4 veces mas para el segundo.
En resumen el mecanismo de acción de los antagonistas es dependiente de un equilibrio entre el nivel endógeno de GnRH y el agonista que se aplica, lo cual lo hace dosis dependiente, a diferencia de los agonistas.
Farmacocinética
Por medio de análisis farmacocinético del Cetrorelix se halló una vida media terminal luego de la inyección única subcutánea que tiene un rango de 5 a 10 horas26. Con la administración de dosis mayores el Cetrorelix puede alcanzar niveles detectables en sangre por periodos más prolongados. Posterior a la administración múltiple la vida media terminal calculada fue mucho mayor, de 20 a 80 horas. Basados en la vida media calculada de 80 horas, se pudo predecir que el punto de estabilidad era alcanzado después de 240-400 hrs. de administración, es decir, de 3 a 5 vidas medias27.
En los estudios con Ganirelix, se demostró una vida media de eliminación de 13.7 a 16.2 horas luego de tratamiento subcutáneo por 7 días con 0.125 mg y 0.25 mg respectivamente.
Seguridad
Durante la evaluación preclínica del Cetrorelix se encontró que la dosis necesaria para producir liberación de histamina era mucho mayor que la concentración farmacológica plasmática efectiva. La inyección de Cetrorelix en ratas a dosis de 1.5 mg /Kg no mostró reacción edematosa. Además el examen de los efectos sistémicos reveló que con inyecciones i.v. en dosis de 1 a 4 mg/Kg no provocaron cambios en las funciones cardiorrespiratoria y vascular.
Tampoco se observaron otros efectos colaterales en los estudios toxicológicos a largo plazo. Una variedad de cambios orgánicos relacionados con los efectos farmacodinámicos no demostraron ser progresivos o fueron morfológicamente y funcionalmente reversibles al terminar el tratamiento. No se encontró tampoco toxicidad directa sobre el órgano blanco en experimentos de toxicidad con dosis subagudas, agudas o crónicas, ni potencial teratogénico o influencia en el desarrollo embrionario temprano, ni efectos sobre la implantación.
Los tests de mutagenicidad fueron inequívocamente negativos para mutaciones genéticas o aberraciones cromosómicas27.
Lo estudios en los cuales se han utilizado diferentes dosis de Cetrorelix y Ganirelix han demostrado una buena tolerancia. Los eventos adversos reportados han sido leves, entre los que se incluyen cefalea, reacción local (eritema, prurito y ocasionalmente hematoma o dolor), fatiga, oleadas de calor. Las reacciones locales por la aplicación del medicamento en ocasiones llegaron a ser moderada y desaparecieron pocos minutos u horas luego de la aplicación. Ninguno de estos síntomas ha sido atribuible a la liberación sistémica de histamina12-13, 28-29.
Indicaciones
Hiperestimulación ovárica controlada en reproducción asistida
La utilización de gonadotropinas menopaúsicas(hMG) y más recientemente la FSH recombinante seguidas de la gonadotropina coriónica humana cuando hay un adecuado número de folículos ováricos maduros han sido considerados de primera línea para las pacientes que necesitan técnicas de reproducción asistida.
Tienen la desventaja de no poderse predecir la respuesta ovárica y la aparición de picos prematuros de LH que producen una mala calidad ovocitaria y aparición de niveles de progesterona que tienen un efecto negativo en el endometrio, lo cual reduce las tasas de embarazo y la cancelación de los ciclos30.
Por lo anterior se adicionaron los análogos de LHRH existiendo tres tipos de esquemas: el protocolo largo o fase lútea, el protocolo corto que se inicia el primer día del ciclo menstrual y el ultracorto por solo pocos días en las fase folicular temprana para pacientes con pobre respuesta a la inducción de ovulación.
El empleo de los antagonistas luego de los estudios iniciales fase II en los cuales luego de evaluar la seguridad y eficacia, se lograron establecer dos regímenes de administración: a) múltiples dosis de 0,25 mgrs s.c. las que se inician en el día 5 del ciclo menstrual y se suspenden el día de la administración de la hCG y b) dosis única de 3 mgrs s.c. que se aplica en el día 7 del ciclo menstrual. En las pacientes con respuesta lenta a la inducción de ovulación, puede ser necesaria la aplicación de una dosis adicional antes de la administración de la hCG (31-33) (fig. 2).
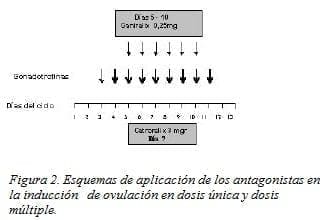
La inhibición por parte del antagonista, de la liberación prematura de LH brinda la opción de la utilización de LHRH o de LH recombinante para la maduración final de los ovocitos y la ovulación ya que se encuentra preservada la respuesta hipofisiaria a la LHRH.
Lo anterior es benéfico en aquellas pacientes que tienen alto riesgo de hiperestimulación ovárica o las que tienen síndrome de ovarios poliquísticos33-34.
La tendencia actual a realizar estimulación ovárica mínima para los ciclos de reproducción asistida se ha visto beneficiada con la administración de los antagonistas, los cuales se aplican en una sola dosis de 0,5 a 1 mgr. s.c. en la fase folicular tardía cuando los niveles de estradiol se encuentran en promedio en 150 pgrs/ml y se ha logrado disminuir el número de ampollas de hMG a un promedio de 4,7, con una tasa de embarazo del 32% por transferencia35.
En los estudios comparativos entre los agonistas de LHRH en presentación de depósito y los antagonistas, los resultados han sido similares en cuanto al número de folículos en crecimiento, ovocitos en metafase II, tasa de fertilización y número de embriones de buena calidad36-38 observando una mejoria en las tasas de embarazos en los estudios más recientes38. Con base en los datos actuales se ha demostrado que la utilización de los antagonistas de LHRH en las pacientes que son sometidas a técnicas de reproducción asistida, es segura, corta y bien tolerada.
Recientemente se han utilizado los antagonistas en las pacientes con antecedentes de pobre respuesta a la inducción de ovulación pero los resultados son similares a los del grupo control sin agonista39-40.
Miomatosis uterina
Entre las patologías más frecuentes en ginecología están la endometriosis y los leiomiomas uterinos caracterizadas por ser enfermedades dependientes de estrógeno en las que el uso terapéutico de agonistas de LHRH está bien establecido, estando en su contra el estímulo o flare-up inicial y la necesidad de inducir un estado de hipoestrogenismo total con concentraciones mínimas o nulas de estradiol.
De ahí que la ventaja potencial del antagonista de la LHRH es obvia: produce una disminución más rápida de los niveles de FSH y LH. En cuanto a los resultados de los estudios piloto con Cetrorelix muestran una reducción efectiva en el tamaño de los miomas, en un período de tratamiento más corto en comparación con el agonista LHRH y no fue necesaria la supresión total de los niveles de estradiol para lograr la disminución de tamaño de los miomas.
Al igual que con los agonistas hay una disminución en el tamaño y en la vascularización del mioma lo cual hace más fácil su extirpación.
Su aplicación se puede hacer en dosis de Depósito41-43.
Cáncer ovárico
Los estudios en tejido ovárico de pacientes con cáncer han demostrado que existen receptores para la LHRH y que son expresados en aproximadamente el 80% de los cánceres de ovario, asimismo existe evidencia que el crecimiento de las células receptoras positivas puede ser inhibido por análogos de la LHRH43.
A raíz de haberse demostrado que el Cetrorelix era más activo que los compuestos agonistas en algunos modelos de cáncer de ovario, estudios en pacientes con enfermedad avanzada se iniciaron después del primer ciclo de quimioterapia, administrando dosis de 10 mg s.c. al día, dando como resultado en la gran mayoría remisión parcial o estabilización de la enfermedad. Dichos estudios se hallan en fase I-II en este momento44.
Conclusiones
La aparición de los antagonistas de la LHRH (Cetrorelix y Ganirelix) y los estudios realizados en sus diferentes fases han demostrado unos efectos supresores de la LHRH los cuales son dependientes de la dosis y pueden ser inducidos inmediatamente luego de su administración, evitando el efecto de “flare-up”que se ve cuando se utilizan los agonistas. Sus efectos son reversibles y no teratogénicos, ni mutagénicos o que produzcan efectos de sensibilización.
Su empleo como coadyuvante en la inducción de ovulación hasta el momento ha demostrado ser seguro y eficaz, produciendo una adecuada inhibición de los picos endógenos de LH, lo cual posibilita su uso en el desarrollo folicular y permite la inducción de la maduración ovocitaria administrando el agonista.
Entre las ventajas observadas está la simplificación del procedimiento, la reducción del riesgo y tiempo de administración de los inductores, sobre todo en las pacientes con síndrome de ovarios poliquísticos o las pacientes con riesgo de presentar un cuadro de hiperestimulación ovárica. Así mismo han demostrado buenos resultados en las pacientes con antecedentes de mala respuesta a la inducción de ovulación en ciclos previos.
Sin embargo estos medicamentos y los protocolos en los cuales se utilizan, deben ser evaluados cuidadosamente para determinar cuál es el más adecuado en la estimulación ovárica para los casos de reproducción asistida.
Los estudios preliminares en los casos de miomatosis uterina han mostrado una excelente respuesta con disminución del volumen, y vascularización dentro de las primeras cuatro semanas del tratamiento.
La posibilidad de nuevos esquemas de tratamiento nos permitirá su empleo en una sola dosis semanal de 3 mgrs s.c. (Depot) lo cual facilitaría su administración por varias semanas.
Bibliografía
- 1. Matsuo H., Baba Y., Nair R., et al. Structure of the porcine LH- and FSH-releasing hormone. Biochem Biophys Res Comm. 1971; 43: 1344-1339.
- 2. Burgus R., et al. Primary structure of the ovine hypothalamic luteinizing hormone-releasing factor (LFR). Proc. Natl. Acad. Sci. USA. 1972; 69: 278.
- 3. Arimura A. The backstage story of the discovery of LHRH. Endocrinology 1991; 129: 1687-1689.
- 4. Shally A. Use of GnRH in preference to LH-RH terminology in scientific papers. Hum. Reprod. 2000; 15: 2059-2061.
- 5. Conn PM., Crowley WF. Jr. Gonadotrophin-releasing hormone and its analogues. N Engl J Med. 1991; 324: 93-103.
- 6. Loumaye E. The control of the endogenous secretion of luteinizing hormone by gonadotroping releasing agonist during ovaria hyperestimulation for in-vitro fertilization and embryo transfer. Hum Reprod 1990; 5: 357-376.
- 7. Macnamee MC., Howles CM., Edwards RG. Short term luteinizing hormone-releasing hormone agonist treatment: prospective trial of a novel ovarian stimulation regimen for in vitro fertilization. Fertil Steril 1989; 52: 264-269.
- 8. Smitz J., Ron-El R., Tarlatzis BC. The use of gonadotrophin-releasing hormone agonist for in vitro fertilization and other assisted procreation techniques: experience from three centres. Hum Reprod 1992; 7(suppl 1): 49-66.
- 9. Loumaye E., Porchet HC., Beltrami V et al. Ovulation induction with recombinant human follicle-stimulating hormone and luteinizing hormone. En Filicori Marco y Flamigni Carlo (eds), Ovulation Induction. Basic Science and Clinical Advances. Elsevier Science, The Netherlands, pp. 227-236.
- 10. Edwards RG., Lobo R. and Bouchard P. Time to revolutionize ovarianj stimulation. Hum Reprod. 1996; 11: 917-919.
- 11. Bajusz S., Kovacs M., Gazdag M., et al. Higly potent antagonist of LH-RH free of edematogenic effects. Proc. Natl Acad. Sci. USA, 1988; 85: 1637-1641.
Referencias
- 12. The Ganirelix Dose-finding Study Group. A double-blind, randomizdes, dose-finding study to assess the efficacy of the gonadotrophin-releasing hormone anataginist ganirelix (Org 37462) to prevent premature luteinizing hormones surges in women undergoing ovarian stimulation with recombinant follicle stimulating hormones (Puregon). Hum Reprod 1998; 13: 3023-31.
- 13. Oberyé JJL., Mannaerts BMJL., Huisman JAM., Timmer CJ. Pharmacokinetic and pharmacodynamic characteristics of ganirelix (Antagon/Orgalutran). Part II. Dose- porportionality and gonadotropin suppression after multiple doses of ganirelix in healthy female volunteers. Fertil Steril 1999; 72: 1006-1012.
- 14. Reissmann TH., Felberbaum R., Diedrich K., Engel J., Comaru-Schally AM., and Schally A.V. Development and applications of luteinizing hormone-releasing hormone antagonists in the treatment of infertility: an overview. Hum Reprod 1995; 10: 1974-1981.
- 15. Reissmann T., Engel J., Kutscher B., et al. The LHRH antagonist Cetrorelix. Drugs Future 1994; 19: 228-237.
- 16. Pinski J., Yano T., Reissmann T., et al. Evaluation of the in vitro and in vivo activity of the L-,D,L- and D-Cit6 forms of the LHRH antagonist Cetrorelix(SB-75). Int. J. Peptide Protein Res. 1995; 45: 410-417.
- 17. Conn PM and Crowley WF. Gonadotropin releasing hormone and its analogs. N. Engl. J. Med. 1991; 324: 93-103.
- 18. Stojilkovic SS., Reinhart J. and Catt KJ. Gonadotropin-releasing hormone receptors: structure and signal transduction pathways. Endocr. Rev. 1994; 15: 462-499.
- 19. Kaiser UB., Conn PM., and Chin WW. Studies of gonadotropin-releasing hormone(GnRH) action using GnRH receptor-expressing pituitary cells line. Endocr. Rev. 1997; 18: 46-70.
- 20. Horn F., Bilezikjian LM., Perrin MH., et al. Intracellular responses to gonadotropin-releasing hormone in a clonal cell line of gonadotrope lineage. Mol. Endocrinol. 1991; 5: 347.
Fuentes
- 21. Stojilkovic SS. and Katt KJ. Expression and signal transduction pathway of gonadotropin releasing hormone receptors. Recent. Prog. Horm. Res. 1995; 50:161-205.
- 22. Ortmann O., Ansari-Pirsarai B., Bloh P., et al. Modulatory actions of progesterone on gonadotropin releasing hormone induced arachidonic acid liberation from perifused rat pituitary cells. Eur. J. Endocrinol. 1996; 135: 626-630.
- 23. Ortmann O., Felberbaum R., Eick F., et al. The GnRH antagonist Cetrorelix does not affect steroidogenesis of human granulosa lutein cells. Exp. Clin. Endocrinol. (Suppl.), 1998.
- 24. Naor Z. Signal transduction mechanisms of calcium mobilizing hormones: the case of gonadotropin releasing hormone. Endocr. Rev., 1990; 11: 326-353.
- 25. Ortmann O., Tilse B. and Emons G. Modulatory actions of estradiol and progesterone on phorbol esther-estimulated LH secretion from cultured rat pituitary cells. J. Steroid Biochem. Mol. Biol. 1992; 43: 619-627.
- 26. Behre HM, Kliesch S., Puhse G., et al. High loading and low maintenance doses of a gonadotropin-releasing hormone antagonist effectively supressmserum luteinizing hormone, follicle-stimulating hormone, and testosterone in normal men. J. Clin. Endocrinol. Metab. 1997; 82: 1403-1408.
- 27. Reissmann T., Schally AV., Bouchard P., Riethmuller H., Engel J. The LHRH antagonist Cetrorelix: a review. Hum Reprod Update 2000; 6: 322-331.
- 28. Duijkers I. J. M., Kippling C., et al. Single and multiple dose pharmacokinetics and pharmacodynamics of the gonadotropin releasing hormone antagonist Cetrorelix in healthy female volunteers, Human Reproduction, 1998; 13: 2392-2398.
- 29. Oberyé JL., Mannaerts BMJL., Kleijn HJ., Timmer CJ. Pharmakinetic and pharmacodynamic charaacteristics of Ganirelix (Orgalutran). Part I. Absolut bioavailability of 0.25 mg of Ganirelix after a single subcutaneous injection in healthy female volunteers. Fertil. Steril. 1999; 72: 1001-1005.
- 30. Schmutlzer RK., Diedrich K. Basic and Clinical aspects of GnRH-agonist in reproduction. Int. J. Gynecol. Obstet. 1990; 32: 311-324.
Referencias Bibliográficas
- 31. Olivennes F., Álvarez S., Bouchard P., et al. The use of a GnRH antagonist(Cetrorelix(r)) in a single dose protocol in IVF-embryo transfer: a dose finding study of 3 versus 2 mgr. Hum.Reprod. 1998; 13: 2411-2414.
- 32. Olivennes F., Fanchin R., Bouchard P., et al. Scheduled administration of a gonadotrophin-releasing hormone antagonist (Cetrorelix) on day 8 of in vitro fertilization cycles: A pilot study. Hum Reprod. 1995; 10: 1382-1386.
- 33. Felberbaum R., Diedrich K. Ovarian stimulation for in vitro fertilization/intracitoplasmic sperm injection with gonadotrophins and gonadotrophin-releasing hormone analogues: agonist and antagonist. Hum. Reprod. 1999; 14: 207-221.
- 34. Sills Es., Levy DP., Moomjy M., et al. A prospective, randomized comparison of ovulation induction using higly purified follicle-stimulating hormone alone and with recombinant human luteinizing hormone in in-vitro fertilization. Hum.Reprod. 1999; 14: 2230-2235.
- 35. Rongiéres-Bertrand C., Olivennes F., Righini C., et al. Revival of the natural cycles in in-vitro fertilization with the use of a new gonadotrophin- releasing hormone antagonist (Cetrorelix): a pilot study with minimal stimulation. Hum. Reprod. 1999; 14: 683-688.
- 36. Olivennes F., Belaisch-Allart J., Emperaire JC., et al. Prospective randomized controlled study of in vitro fertilization-embryo transfer with a single dose of a luteinizing hormone-releasing hormone (LH-RH) antagonist (cetrorelix) or a depot formula of an LH-RH agonist (triptorelin). Fertil Steril 2000; 73: 314-320.
- 37. Felberbaum RE., Albano C., Ludig M., et al and on behalf of the European Cetrorelix Study Group. Hum Reprod. 2000; 15: 1015-1020.
Fuentes Bibliográficas
- 38. The European and Middle East Orgalutran Study Group. Comparable clinical outcome using the GnRH antagonist ganirelix or a long protocol of the GnRH agonist triptorelin for the prevention of premature LH surges in women undergoing ovarian stimulation. Hum.Rep. 2001; 16: 644-651.
- 39. Akman MA., Ereden HF., Tosun S., Bayazit N., Aksoy E., Bahceci M. Addition of GnRH antagonist in cycles of poor responders undergoing IVF. Hum. Reprod. 2000; 15: 2145-2147.
- 40. Akman MA., Erden HF., Tosum SB., Bayasit N., Aksoy E., Bahceci M. Comparison of agonistic flare-up protocol and antagonistic multiple dose protocol in oarian stimulation of poor responders: results of a prospective randomized trial. Hum. Reprod. 2001; 16: 868-870.
- 41. González-Barcena D., Banuelos Álvarez R., Pérez Ochoa E., et al. Treatment of uterine Leiomyomas with LHRH antagonist Cetrorelix. Hum. Reprod. 1997; 12: 2028-2035.
- 42. Felberbaum R., Germer U., Ludwid M., et al. Treatment of uterine fibroids with a slow-release formulation of the gonadotropin releasing hormone antagonist Cetrorelix. Hum.Reprod. 1998; 13: 1660-1668.
- 43. Schally AV. LHRH Analogues: I. Their impact on the control of tumorigenesis. Peptides. 1999; 20: 1247-1262.
- 44. Emons G., and Schally AV. The use of luteinizing releasing hormone agonists and antagonist in gynaecologycal cancers. Hum. Reprod. Update. 1994; 9: 1364-1379.