Resultados
Estandarización del cultivo
El Agar HPM suplementado soportó mejor el crecimiento de Helicobacter, con y sin suplemento antibiótico; además, la incubación prolongada en este medio no mostró un aumento considerable de las formas cocoides. El crecimiento de la bacteria fue mejor en caldo Brucella, pues después de la incubación, el crecimiento bacteriano fue abundante y las formas cocoides se presentaron en cantidades mínimas. En ensayos previos, se demostró que un suplemento de 3% de suero equino era el porcentaje mínimo necesario para el crecimiento de Helicobacter en medio líquido, y que una incubación mayor a 48 horas (sin cambiar medio de cultivo) lleva a la aparición de formas cocoides.
Características de los pacientes
Se enrolaron 144 pacientes, 74 hombres y 70 mujeres, con edad promedio de 56 años. Se diagnosticó gastritis crónica antral en 14 pacientes (9,8%), con edad promedio de 48 años; úlcera péptica en 54 casos (37,5%), edad promedio de 48 años de los cuales 7 (13%) correspondían a úlceras gástricas y 47 (87%) a úlceras duodenales. Se determinó adenocarcinoma gástrico en 76 pacientes (52,7%) con edad promedio de 61 años. Según el análisis histopatológico, 27 (35,5%) correspondían a adenocarcinoma gástrico de tipo difuso y 49 (64,5%) a tipo intestinal. En diez de estos casos, las biopsias tomadas para el análisis histológico contenían un alto porcentaje de células tumorales y se consideraron como inadecuadas para el diagnóstico de H. pylori.
Detección de H. pylori
La presencia de H. pylori se determinó empleando las pruebas de ureasa rápida, histología y cultivo. Un paciente se consideró positivo o negativo cuando dos de las tres pruebas resultaron positivas o negativas, respectivamente (tabla 1). Setenta y siete pacientes fueron positivos y 54 negativos. H. pylori fue detectado en 29,4% de casos de cáncer gástrico, 90% de los casos de enfermedad ulceropéptica y 93% de pacientes con gastritis crónica.
Tabla 1. Detección de Helicobacter pylori en cáncer gástrico, úlcera péptica y gastritis en una población colombiana, según varios métodos diagnósticos
| Infección | Cultivo (+) | PUR (+) | Histología(+) | Estado de infección por H.pylori (+)* |
|
| Patología | Cáncer gástrico | 21/76 (28%) | 19/76 (25%) | 28/66 (42%) | 20/68 (29.4%) |
| Ulcera péptica | 30/54 (56%) | 49/54 (91%) | 44/47 (93.6%) | 44/49 (90%) | |
| Gastritis | 13/14 (93%) | 12/14 (86%) | 7/8 (87%) | 13/14 (93%) | |
| Tipo de úlcera péptica | Difuso | 3/27 (11%) | 8/27 (29%) | 8/24 (33%) | 16/44 (36.4%) |
| Intestinal | 18/49 (37%) | 11/49 (22%) | 20/44 (48%) | 4/24 (16.6%) | |
| Significancia | *P = 0.016 | -P = 0.335 | *P = 0.258 | -P = 0.08 | |
| Tipo de cáncer gástrico | Duodenal | 26/47 (55%) | 44/47 (94%) | 40/47 (85%) | 40/43 (93%) |
| Gástrica | 4/7 (57%) | 5/7 (71%) | 4/7 (67%) | 4/6 (67%) | |
| Significancia | *P = 0.636 | -P = 0.313 | *P = 0.039 | -P = 0.106 |
* Número y porcentaje de casos con al menos dos de tres pruebas positivas.
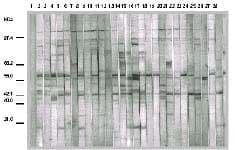
El análisis serológico demostró anticuerpos en el 100% de la población estudiada, indicando infección previa aun cuando la bacteria no fue detectada en todos los casos (figura 1). No se presentaron diferencias significativas entre la prevalencia de infección por H. pylori en casos de cáncer gástrico de tipo intestinal y difuso, excepto en los resultados del cultivo. De la misma manera, no se presentaron diferencias significativas entre los porcentajes de infección entre los pacientes con úlceras gástricas y duodenales.
Los cálculos de especificidad, sensibilidad, valor predictivo positivo y negativo fueron determinados de acuerdo con el estado de infección (tabla 2). Los métodos más sensibles para detectar H. pylori en pacientes con úlcera péptica fueron la prueba de ureasa rápida (100%) y el análisis histológico (100%), siendo el cultivo el menos sensible (60%). El valor predictivo positivo del estado de infección establecido en pacientes con úlcera péptica fue alto con los tres métodos evaluados (100% en cultivo, 95% para la prueba de ureasa y la histología).
De igual forma, estas pruebas mostraron altos porcentajes de sensibilidad y especificidad para detectar la bacteria en pacientes con gastritis. En pacientes con adenocarcinoma gástrico, el cultivo fue la prueba más sensible (85%) y específica (96%) para detectar la infección por Helicobacter; con valores predictivos positivos y negativos de 89,4 y 93,8%, respectivamente. En estos pacientes, la prueba de ureasa rápida y el examen histológico presentaron baja especificidad (9,6 y 68,7%, respectivamente) y sensibilidades (65 y 72%, respectivamente).
Tabla 2. Especificidad y sensibilidad de los métodos diagnósticos.
|
Cultivo |
PUR |
Histología |
|
|
Especificidad |
97% Publicidad |
87% |
69% |
VPP: valor predictivo positivo
VPN: valor predictivo negativo
Discusión
Los resultados obtenidos, demostraron que el Helicobacter crece muy bien en el medio HPM, el cual tiene de particular la presencia de carbón activado. Como se ha informado previamente (9), su importancia puede radicar en su capacidad de absorber o inactivar factores tóxicos que resultan del metabolismo bacteriano.
El uso de antibióticos es necesario para impedir la proliferación de contaminantes exógenos y, con más frecuencia, de contaminantes endógenos presentes en las biopsias (9-11), principalmente en los pacientes con cáncer gástrico (12-13).
El crecimiento del Helicobacter en medio líquido es difícil, debido en parte a que la bacteria requiere una excelente dispersión de gases a través del medio, de un suplemento nutritivo adecuado y de un inóculo inicial denso (8).

FIGURA 1. Detección de anticuerpos anti H.pylori por inmunotransferencia.
Se cree que las formas cocoides del Helicobacter son producto del estrés bacteriano y que estos organismos no son viables y de difícil cultivo (9, 14). En este estudio, se observaron no sólo como resultado del cultivo prolongado sino como formas viables y cultivables a partir de biopsias gástricas de pacientes con cáncer.
Además, las formas cocoides obtenidas por cultivo prolongado regresaron a la forma espiralada característica después de un período de almacenamiento a _70°C.
El significado biológico de esta observación no es claro y se requieren más estudios para determinar su importancia.
En este trabajo, se evaluaron tres métodos diagnósticos para la detección del H. pylori a partir de biopsias gástricas.
Varios factores pueden haber contribuido a los resultados obtenidos al comparar los métodos invasores con la prueba no invasora (serológica), debido a que la infección se distribuye a parches en el estómago, es lógico pensar que el ensayo serológico puede detectar la bacteria en casos negativos según las pruebas invasoras (15-16). Aunque el examen histológico y el cultivo siguen siendo los mejores estándares disponibles, estas técnicas tienen algunas limitaciones.
En el cultivo, se puede asegurar la presencia de la bacteria, pero no puede asegurarse que un cultivo negativo refleje la ausencia de infección (15). Estos casos, la bacteria no puede aislarse debido a las exigencias del organismo o al crecimiento de flora competente que oculta o limita el crecimiento de Helicobacter, especialmente en pacientes con cáncer gástrico (17). En cuanto al examen histológico con hematoxilina-eosina, se pueden observar falsos negativos pues ésta no es la tinción más adecuada para la identificación del H. pylori. Actualmente se cuenta con técnicas de coloración más sensibles (18).
En todos los pacientes con cáncer gástrico:
Se encontraron anticuerpos anti-H. pylori, mientras que la bacteria fue detectada sólo en 29,4%. Este resultado indica que aunque la bacteria no sea detectada, existió al menos una infección previa. En varios trabajos se ha demostrado que la bacteria puede desaparecer en los casos de atrofia gástrica o puede ser desplazada por otros microorganismos que colonizan el estómago (19-20).
Estos resultados indicarían que el dato serológico global sería de poca utilidad en el estudio de estas patologías gástricas; no obstante, es importante determinar si los perfiles de respuesta obtenidos reflejan formas de interacción cuyo análisis sería de valor tanto para el diagnóstico como para el manejo y el seguimiento.
En este estudio, se corroboró la asociación entre infección por H. pylori, gastritis y úlcera péptica:
Con prevalencias de 93 y 90%, respectivamente. Previamente se ha observado que la infección por H. pylori está asociada con un mayor riesgo de desarrollar cáncer gástrico (21-24). Esta neoplasia puede dividirse en dos tipos histológicos, el intestinal y el difuso, que difieren tanto en sus características morfológicas como biológicas (25-26).
Recientemente, Parsonnet y colaboradores demostraron que existe una tasa de infección más alta en pacientes con cáncer gástrico de tipo intestinal que en el de tipo difuso (27).
En este estudio se encontró una prevalencia de infección similar en los dos tipos histológicos, al igual que lo reportado por Loffeld y colaboradores. Clarkson (1992) sugiere que la asociación entre la presencia de H. pylori y los dos tipos de adenocarcinoma gástrico es una evidencia de que la infección es un factor de riesgo en ambos tipos histológicos.
Este autor propone varios mecanismos que pueden actuar cuando no se presenta atrofia gástrica ni metaplasia, los cuales incluyen daños al ADN y una reducción en la secreción de antioxidantes debidos a la infección por Helicobacter (20).
En conclusión, los resultados sugieren que en la población colombiana no hay diferencias en la prevalencia de la infección por H. pylori en los dos tipos de adenocarcinoma gástrico, indicando que la bacteria puede estar implicada en un evento común a ambos tipos histológicos. La mayoría de los métodos diagnósticos tienen sensibilidad limitada para detectar la infección en pacientes con cáncer gástrico. En estos casos, el análisis serológico puede ser eficaz para estudiar la historia de la infección, lo cual es una herramienta importante para conocer las bases de la interacción hospedero-parásito.
Agradecimientos
Queremos agradecer al personal médico, paramédico y técnico de las unidades de Gastroenterología y Patología del Instituto Nacional de Cancerología y del Hospital Universitario de La Samaritana.
Este trabajo fue financiado por el Instituto Nacional de Cancerología y el Hospital Universitario de la Samaritana.
Diana Marcela Cittelly Piñeros
Bióloga, Laboratorio de Inmunología, Instituto Nacional de Cancerología.
Sandra Consuelo Henao Riveros
Bacterióloga, M.Sc., Laboratorio de Inmunología, Hospital Universitario de La Samaritana.
Oscar Orozco DIaz
Médico, Coordinador, Grupo de Inmunología, Instituto Nacional de Cancerología.
JuliAn David MartInez
Médico, Jefe, Unidad de Gastroenterología, Hospital Universitario de La Samaritana.
Bibliografía
- 1. Macdonald S, Hill M, Roberts I. Gastric cáncer: epidemiology, pathology, detection and staging. 1993; 12: 151-158.
- 2. INC. Registro Institucional de Cáncer. 1996. República de Colombia, Min. Salud.
- 3. INC. Protocolo de tratamiento y seguimiento de cáncer gástrico. 1993. República de Colombia, Min. Salud.
- 4. Forman D. The prevalence of Helicobacter pylori infection in gastric cancer. Aliment. Pharmacol Ther 1996; 9(Suppl. 2): 71-6.
- 5. Rugeles G, Vargas L, Posso H. Prevalencia del Helicobacter pylori en personas sintomáticas y asintomáticas en San Gil, Santander. En: Avances en el diagnóstico y tratamiento de la patología gastroduodenal por Helicobacter pylori. Primera Edición. Italmex. 1993.
- 6. García FT, Lima E, Cuello C, et al. Correlación clínica, endoscópica y patológica en 107 pacientes con gastritis asociada a Helicobacter pylori. En: Avances en el diagnóstico y tratamiento de la patolo
- 7. García Del Risco F, Caraballo JM, Urbina D. Helicobacter pylori en sujetos asintomáticos, con úlcera duodenal, úlcera gástrica y dispepsia no ulcerosa en Cartagena. Rev Colomb Gastroenterol 1994; 9(4): 188_93.
- 8. Morgan DR, Freedman R, Depew CE, et al. Growth of Campylobacter pylori in liquid media. J Clin Microbiol 1987; 25(11): 2123-5.
- 9. Ansorg R, Recklinghausen GV, Pomarius R, et al. Evaluation of techniques for isolation, subcultivation, and preservation of Helicobacter pylori. J Clin Microbiol 1991; 29(1): 51-3.
- 10. Hachem CY, et al. Comparison of agar based media for primary isolation of Helicobacter pylori. J Clin Pathol 1995; 48: 714-6.
- 11. Buck GE, Smith JS. Medium supplementation for growth of Campylobacter pyloridis. J Clin Microbiol 1987; 25(4): 597-9.
- 12. Krajden S, Bohnen J, Anderson J, et al. Comparison of selective and nonselective media for recovery of Campylobacter pylori from antral biopsies. J Clin Microbiol 1987; 25(6): 1117-8.
- 13. Moshkowitz M, Gorea A, Arber N, et al. Morphological transformation of Helicobacter pylori during prolongated incubation: association with decreased acid resistance. J Clin Pathol 1994; 47: 172-4.
- 14. Talley NJ, et al. Serodiagnosis of Helicobacter pylori: comparison of enzime linked immunosorbent assays. J Clin Microbiol 1991; 29(8): 1635-9.
- 15. Vijayakumari S, et al. The pathogenic role of the cocoid form of Helicobacter pylori. Cytobios 1995; 82(331): 251-60.
- 16. Cutler AF. Accuracy of invasive and noninvasive test to diagnose Helicobacter pylori infection. Gastroenterol 1995; 109: 136-41.
- 17. Peterson WL. Helicobacter pylori and peptic ulcer disease. N Engl J Med 1991; 324(15): 1043-8.
- 18. Rodríguez A, Márquez A, Dennis R. Asociación entre Campylobacter pylori y dispepsia ulcerosa y no ulcerosa. Universitas Médicas 1989; 3(30): 7-11.
- 19. Sivaprakash R, et al. Investigation for the prevalence of Helicobacter pylori infection in patients with gastric carcinoma in Madras, India. Jpn J Med Sci Biol 1996; 49: 49-56.
- 20. Clarkson KS, West KP. Gastric cancer and Helicobacter pylori infection. J Clin Pathol 1993; 46: 997-9.
- 21. Buruk F, Berberoglu U, Pak I, et al. Gastric cancer and Helicobacter pylori infection. Br J Surg 1993; 80: 378-9.
- 22. Siponenn P, Kosunen TU, Valle J, et al. Helicobacter pylori infection and chronic gastritis in gastric cancer. J Clin Pathol 1992; 45: 319-23.
- 23. Hu PJ, Mitchell HM, LI YY, et al. Association of Helicobacter pylori with gastric cancer and observations on the detection of this bacterium in gastric cancer cases. Am J Gastroenterol 1994; 89(10): 1806-10.
- 24. McFarlane GA, Munro A. Helicobacter pylori and cancer gastric. Br J Surg 1997; 84: 1190-9.
- 25. Kuipers EJ, Meuwissen GM. Helicobacter pylori and gastric carcinogenesis. Scand J Gastroenterol 1996; 31(Suppl 218): 103-5.
- 26. Nakamura K. Histogénesis del cáncer gástrico. Las etapas iniciales de su desarrollo. Gastr Latinoam 1990; 1(1): 71-90.
- 27. Parsonnet J. Helicobacter pylori and gastric cancer. Gastroenterol Clin North Am 1993; 22(1): 89-101.