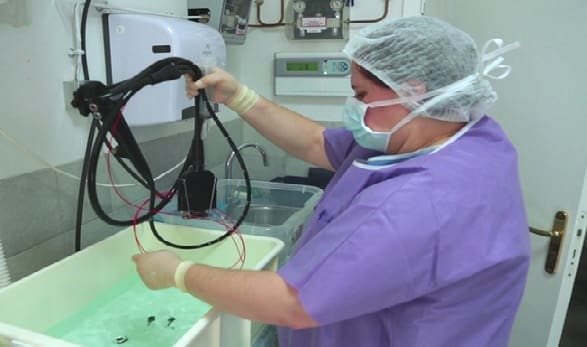
Pasos Generales para la Limpieza y Desinfección de los Equipos y Accesorios Endoscópicos
1. Protección para el personal médico:
durante el proceso, se deben utilizar guantes, cubrebocas, gafas, gorro, bata, delantal y polainas.
2. Endoscopios:
-
lnmediatamente el endoscopio es removido del paciente, se debe pasar aire durante 10 a 15 segundos por el canal aire/agua para expulsar cualquier resto de moco o sangre que haya refluido y aspirar detergente por el canal de succión durante 10 a 15 segundos.
-
Limpieza: Sumergir el endoscopio en un recipiente con detergente enzimático durante 3 minutos y lavar la superficie externa con una gasa suave. Limpiar la punta del endoscopio con un cepillo de dientes de cerdas suaves, con especial atención al extremo del canal aire/agua y, en los duodenoscopios, al elevador del catéter. Remover todas las válvulas e irrigar todos los canales con cantidades suficientes de detergente enzimático, utilizando para ello una jeringa plástica de 3 cc, incluyendo el canal del elevador en el caso de duodenoscopios para ERCP.
-
Cepillado del canal de biopsia: Introducir el cepillo de limpieza a través de la entrada del canal de biopsia hasta que el cepillo emerja por la punta distal por 3 ocasiones. Introducir el cepillo de limpieza por la entrada de la válvula de succión hasta que emerja por la punta distal por 3 ocasiones. Introducir el cepillo de limpieza por la entrada de la válvula de succión a través del cordón que conecta a la fuente de luz hasta que el cepillo emerja por el extremo que se conecta al succionador por 3 ocasiones.
-
d. Enjuagar el equipo con agua tibia, externa e internamente.
-
Levantar el equipo para que escurra el agua y secar con un paño limpio.
-
Pasar aire comprimido por los canales para secarlos y expulsar restos de material orgánico que haya quedado. NOTA: si existe máquina automática de desinfección, colocar el equipo en ella. Si no, continuar con el siguiente paso.
-
Desinfección, Sumergir el endoscopio en una solución alcalina de glutaraldehido al 2%. Llenar todos los canales del equipo con la solución de glutaraldehido al 2%, utilizando una jeringa plástica de 3 cc, incluyendo en el caso de duodenoscopios, el canal del elevador. Tiempo de inmersión: entre paciente y paciente, son suficientes 4 minutos de acuerdo con algunos autores (20). En este punto, sin embargo, la Asociación Americana de Endoscopia Gastrointestinal (ASGE) recomienda mantener la inmersión de los equipos durante 20 minutos (22) y la Asociación Europea de Endoscopia Gastrointestinal (ESGE) recomienda al menos 10 minutos de inmersión (23). Esta guía, a la fecha, recomienda una inmersión de 10 minutos entre paciente y paciente. Después del último paciente, se requieren 20 minutos para reducir el riesgo de colonización durante la noche (20).
-
Enjuage: Levantar el endoscopio para que el glutaraldehído escurra. Sumergir el equipo en agua destilada. lrrigar todos los canales con agua destilada en suficiente cantidad para eliminar el glutaraldehído, utilizando una jeringa plástica. Secar los canales con aire comprimido. Pasar una gasa impregnada de alcohol al 70% por toda la superficie externa del endoscopio. Secar la superficie con una compresa estéril .
-
Endoscopios no sumergibles: Limpiar las partes no sumergibles (los controles y el cordón que se conecta a la fuente de luz) con agua y detergente. Pasar por toda la superficie una gasa empapada en alcohol al 70%. Secar con una compresa estéril.
-
Final de la sesión: Al final de la sesión diaria, luego de la desinfección durante 20 minutos y después del enjuague de los equipos, instilar alcohol al 70% en todos los canales y, luego, secarlos con aire comprimido (23).
-
Máquina de desinfección: Tienen la ventaja de que el médico no está en contacto con los líquidos de desinfección como en el procedimiento manual. Se debe poner mucha atención a la temperatura, a la irrigación, limpieza y secado de los canales. lgualmente, debe haber control microbiológico regular ya que microorganismos oportunistas pueden colonizar los reservorios y los conductos internos (23).
-
Almacenamiento: Guardar el equipo completamente seco, en posición vertical en un mueble seco, ventilado y fresco, cuyas superficies se puedan lavar y limpiar adecuadamente. Proteger los lentes con las cubiertas plásticas adecuadas.
3. Accesorios
Excepto si se usan accesorios desechables, todos deben ser sometidos, entre paciente y paciente, a desinfección de alto nivel si son elementos semicríticos (válvulas, dilatadores) o a esterilización si son elementos críticos (pinzas de biopsias, papilótomos, agujas de esclerosis, asas de polipectomía, etc.).
- Lavar inmediatamente después de usar, en una solución de detergente enzimático.
- Desarmar el accesorio si es posible.
- Cepillar con un cepillo blando los restos orgánicos adheridos.
- Lavar con detergente todos los orificios utilizando una jeringa plástica.
- Enjuagar con agua destilada y secar con aire.
- Desinfectar con solución de glutaraldehido, con óxido de etileno o con autoclave, si es posible.
- Almacenar adecuadamente.
NOTA: la botella de agua para irrigación del endoscopio debe llenarse siempre con agua estéril. Tanto la botella como su tubo conector deben ser sometidos a desinfección de alto nivel, por lo menos, una vez al día
Programa de Desinfección en la Práctica Clínica
Es fundamental para todas las unidades de endoscopia digestiva del país que exista un adecuado programa de manejo de los equipos endoscópicos.
El conocer los riesgos de transmisión de enfermedades infecciosas por vía endoscópica y la manera de prevenir esta transmisión, obligan a la adopción de un proceso sistemático de desinfección de equipos y accesorios que conviertan los estudios endoscópicos, en procedimientos médicos seguros, lo cual es en últimas, el objetivo principal de esta guía.
Referencias Bibliográficas
- 1. Silvis SE, et al. Endoscopic complications: results of the 1974 American Society for Gastrointestinal Endoscopy Survey. JAMA 1976; 235: 928-930.
- 2. Colin-Jones DE, et al. Current endoscopic practice in the United Kingdom. Clin Gastroenterol 1978; 7: 775-786.
- 3. Doherty DE, et al. Pseudomonas aeruginosa sepsis following retrograde cholangio pancreatography Dig Dis Sci 1982; 27: 169-170.
- 4. American Society for Gastrointestinal Endoscopy. lnfection control during gastrointestinal endoscopy: guidelines for clinical application. Gastroint Endosc 1988; 34: 375-405.
- 5. Weller lV D, et al. Cleaning and disinfection of equipment for gastrointestinal flexible endoscopy: interim recomendations of a Working Party of the British Society of Gastroenterology. Gut 1988; 29: 1134-51.
- 6. Bond WW. Disinfection and endoscopy: microbial considerations. J Gastroenterol Hepatol 1991; 6: 31-36.
- 7. Kaczmarek RG, et al. Multi-state investigation of the actual desinfection/sterilization of gastrointestinal endoscopes in health care facilities. Am J Med 1992; 92: 257-261.
- 8. Jefferies DJ. Zidovudine after occupational exposure to HIV. Br Med J 1991; 302: 1349-1350.
- 9. Langenberg W, et al. Patient to patient transmission of Campylobacter pylori infection by fiberoptic gastroduodenoscopy and biopsy. J Infect Dis 1990; 161: 507-511.
- 10. McAdam JG, Leicester RJ. lnfection in endoscopy. Protection in staff. Gastroint Endosc Clin N Am 1993; 3: 447-457.
Fuentes Bibliográficas
- 11. O’connor HJ, Axon ATR. Disinfecting endoscopes used on hepatitis B carriers. Lancet 1984; 1: 631.
- 12. Cowen A. Infection and endoscopy. Patient to patient transmission. Gastroint Endosc Cl N Am 1993; 3: 483-496.
- 13. Durack DT. Profilaxis of infectious endocarditis. ln: Mandell GL, Bennett JE, Douglas RE, editors. Principles and Practice of Infectious Disease. Second Edition. 1984.
- 14. Martin MA, Reicheldelfer M. APIC guideline for infection prevention and control in flexible endoscopy. Am J Infect Control 1994; 22: 19-38.
- 15. Norfleet RG, et al. Does bacteremia follow colonoscopy? Gastroenterology 1976; 70: 20-21.
- 16. Norfleet RG, et al. Does bacteremia follow upper gastrointestinal endoscopy? Am J Gastroenterol 1981; 76: 420-422.
- 17. Roberts W, et al. Prevalence of Cryptosporidium in patients undergoing endoscopy. Evidence for asymptomatic carrier state. Gastroenterology 1987; 92: 1597.
- 18. Birnie GG, et al. Endoscopic transmission of hepatitis B virus. Gut 1983; 24: 171-174.
- 19. Bronowicki JP, et al. Patient to atient transmission of hepatitis C virus during colonoscopy. N Engl J Med 1997; 337: 237-240.
- 20. Cotton PB, Williams CB. Cleaning and disinfection. ln: Practical gastrointestinal Endoscopy. 3r ed. Blackwell Sci Publications. 1990.
- 21. Zeroske J. Practical disinfection tecnique. Gastroint Endosc Cl N Am 1993; 3: 469-481.
- 22. DiMariano AJ, et al. Reprocessing of flexible gastrointestinal endoscopes. Gastroint Endosc 1996; 43: 540-546.
- 23. Axon A, Kruse A, et al. ESGE guidelines on cleaning and disinfection. Endoscopy 1995; 27: 199-202.
- 24. Axon A, et al. ESGE guidelines for the reprocessing of accesories in digestive endoscopy. Endoscopy 1996; 28: 534-535.