En el Hospital Universitario Fundación Santa Fe de Bogotá
An Exploratory Study Of Phlebitis Induced By Intravenous Clarithromycin At The Hospital Universitario Fundación Santa Fe De Bogotá (FSFB)
Ángela María Vargas*, Ana María Garzón Porras**, Ángela Caro Rojas***
Hospital Universitario Fundación Santa Fe de Bogotá; Universidad Nacional de Colombia
Resumen
Objetivo:
Determinar la frecuencia de flebitis en pacientes del Hospital Universitario Fundación Santa Fe de Bogotá (HUFSFB) a quienes se les administró claritromicina intravenosa (IV), y analizar las posibles variables que pueden afectar su aparición.
Metodología:
Estudio retrospectivo y observacional de utilización de medicamentos en pacientes del HUFSFB que recibieron al menos una dosis de claritromicina IV durante el mes de febrero de 2011. La información se tomó de las historias clínicas de los pacientes incluidos en el estudio.
Resultados y discusión:
La incidencia de flebitis fue de 35%, todos los casos (7 de 20) se presentaron en pacientes mayores de 58 años, con sitios de punción en venas de pequeño calibre (tres en el pliegue braquial y cuatro en el dorso de la mano).
A seis de los siete pacientes que presentaron flebitis se les pasó a claritromicina vía oral sin antes cambiar el sitio de punción a una vena de mayor calibre, como lo indica el protocolo. El grado de flebitis, y en general la incidencia de la misma, fue menor cuando la claritromicina se diluyó en lactato de Ringer.
Conclusiones:
La dilución de claritromicina en lactato de Ringer disminuyó la incidencia y el grado de flebitis química. La edad avanzada del paciente y la administración del antibiótico en venas de menor calibre favoreció la aparición de flebitis.
Palabras clave: claritromicina vía intravenosa, flebitis, sitio de venopunción, días de tratamiento
Abstract
Objective:
This study’s objective was to how often phlebitis occurred among patients at the FSFB who had had intravenous administration of clarithromycin in February 2011. The study analyzes variables that may affect occurrence.
Methods:
This is a retrospective and observational drug utilization study using information gathered from patients’ medical records of patients at the FSFB who had received at least one IV dose of clarithromycin in February 2011.
Results:
The incidence of phlebitis was 35%. All cases (7 of 20) occurred in patients who were older than 58 years of age. The venipuncture sites of all seven were located in small caliber veins (3 in the brachial fold and 4 on the back of the hand). Oral administration of medication was substituted for intravenous administration in six out of the seven patients who had phlebitis without attempting a change of venipuncture site to a larger caliber vein as called for in the protocol. Overall incidence and degree of phlebitis were less when clarithromycin was diluted in Ringer’s lactate.
Conclusions:
The dilution of clarithromycin in Ringer’s lactate decreased the incidence and degree of chemical phlebitis. Older patient age and administration of the antibiotic in smaller caliber veins were associated with the development of phlebitis.
Key words:
Intravenous Clarithromycin; phlebitis; venipuncture site; days of treatment.
Introducción
La claritromicina es un antibiótico macrólido, bacteriostático, y bactericida a altas concentraciones. Su estructura química consta de un anillo lactónico de 14 átomos con dos desoxiazúcares; es una base débil de carácter lipofílico y alto peso molecular. Como mecanismo de acción, se une a la subunidad 50S ribosomal de organismos susceptibles, y de esta forma impide la síntesis bacteriana de proteínas RNA- dependientes.
Sus indicaciones de acuerdo con la FDA son: exacerbación de infección aguda de enfermedad pulmonar obstructiva crónica, otitis media aguda, neumonía adquirida en la comunidad, infección diseminada debido al grupo Mycobacterium avium – intracellulare, profilaxis infección por VIH, infección del tracto gastrointestinal por Helicobacter pylori, infección de la piel y tejidos subcutáneos sin complicaciones, sinusitis maxilar aguda, enfermedad pulmonar por infección compleja por Mycobacterium avium y faringitis por Streptococcus.(1)
De otro lado, la flebitis se define como una inflamación de los vasos venosos resultado de una lesión de la pared vascular, la cual puede ser provocada por medios mecánicos, químicos o infecciosos. La flebitis química se presenta con la administración de medicamentos o soluciones irritantes, muy ácidos o demasiado alcalinos (pH menor de 5 o mayor de 9), y de osmolaridad elevada (superior a 500 mOsm/l).
La flebitis puede progresar a otras complicaciones más serias, como la formación de trombos que puede llevar a una tromboflebitis, una trombosis venosa profunda o aún a embolismo pulmonar.
Prevenir la flebitis
Para prevenir la flebitis se debe hacer seguimiento desde el momento de la inserción en búsqueda de signos tempranos como dolor, rubor y calor en el sitio de la venopunción; si la flebitis avanza, se presenta edema en la extremidad involucrada y un cordón palpable a lo largo de la ruta venosa.
Para tratar la flebitis se debe retirar lo antes posible el catéter y aplicar compresas húmedas y calientes en la zona afectada, y antiinflamatorios si es necesario. La administración de soluciones irritantes por una vía central o de mayor flujo es otra forma de prevenir la aparición de la flebitis.(2)
El riesgo de flebitis secundaria a la administración de claritromicina ha sido reportado en varios estudios, complicación considerada de alta incidencia.( 3-5) En los dos últimos años (2009 y 2010) en el HUFSFB se ha hecho un seguimiento estricto a los casos de flebitis inducidos por Claritromicina.
Como respuesta a la problemática, desde la oficina de Seguridad del paciente se desarrolló el Estándar Operacional para la Administración de Claritromicina Intravenoso,avalado y socializado en el mes de diciembre de 2010. Dicho estándar indica, entre otras, que la dilución se debe hacer en lactato de Ringer y la infusión durante una hora, así como las actividades a realizar antes, durante y después de la administración de claritromicina IV, con el fin de evitar al máximo la aparición de flebitis en el paciente.
Clasificación de la Flebitis
Adicionalmente, en el estándar se define la clasificación de la Flebitis:(6)
- Primero, Grado 0: Sin signos ni síntomas de flebitis.
- Segundo, Grado I: Dolor en el sitio de punción.
- Tercero, Grado II: Dolor, eritema y/o edema.
- Cuarto, Grado III: Dolor, eritema y/o edema, endurecimiento en trayecto menor a 5 cm.
- Quinto, Grado IV: Dolor, eritema y/o edema, endurecimiento en trayecto mayor a 5 cm.
- Sexto, Grado V: Franca trombosis venosa/salida de material purulento en el sitio de inserción.
Objetivos
- Determinar la frecuencia de flebitis en un grupo de pacientes del HUFSFB a los cuales se les administró claritromicina vial x 500 mg/10 mL intravenosa (IV) en febrero de 2011.
- Determinar el grado de adherencia al estándar establecido para la administración del medicamento Claritromicina IV.
- Describir las posibles variables que pueden afectar la aparición y el manejo de la flebitis.
Más información de Flebitis:
- Estudio Exploratorio sobre Flebitis Inducida, Resultados y Discusión
- Limitaciones del Estudio Exploratorio sobre Flebitis Inducida
Metodología
Estudio observacional descriptivo de corte transversal con recolección prospectiva de la información. Corresponde a un estudio de utilización de medicamentos (EUM) sobre uso administración
Población: pacientes hospitalizados en el HUFSFB que en el mes de febrero recibieron al menos una dosis de Claritromicina vial x 500 mg /10 mL.
- Criterios de inclusión: haber recibido Claritromicina vía IV en febrero de 2011.
- Criterios de exclusión: haber recibido la Claritromicina IV por un acceso central.
Periodo de toma de datos: 1˚ de febrero de 2011 al 28 de febrero de 2011. Fuente de obtención de la información: registro de los medicamentos dispensados desde farmacia en el mes de febrero de 2011. Historias clínicas de los pacientes del HUFSFB.
Variables
Para cumplir los objetivos del estudio se analizaron las siguientes variables (tabla 1):
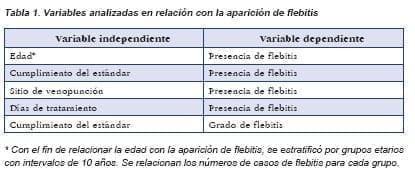
- Presencia de flebitis: cualitativa dicotómica (Si/No). Se expresó en términos de porcentaje de ocurrencia del evento.
- Grado de flebitis: cualitativa ordinal. Basada en la escala definida por la institución en el Estándar Operacional para la Administración de Claritromicina Intravenoso.
- Edad: cuantitativa discreta. Se describió en términos del promedio y rango.
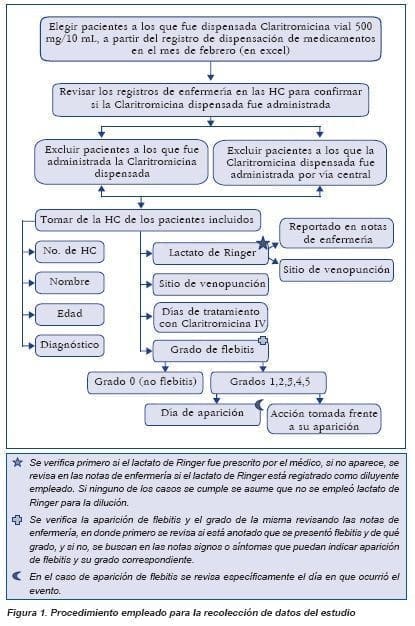
- Cumplimiento del estándar institucional. Cualitativa dicotómica (Si/No). Evaluado como cumplido si se evidencia la dilución en lactato de Ringer en los registros de la Historia Clinica, en términos de porcentaje de cumplimiento.
- Sitio de venopunción. Cualitativa nominal. Se expresa en términos del número de pacientes con venopunción en cada sitio definido.
- Días de tratamiento. Cuantitativa discreta.
- Acción tomada frente a la flebitis. Cualitativa nominal. Expresada en términos de proporción de las acciones tomadas en cada caso.
- Adicionalmente se exploró la relación entre las siguientes parejas de variables, informadas en término de proporción.
Autores:
* Ángela María Vargas. Estudiante X semestre de Química Farmacéutica, Universidad Nacional de Colombia.
Correspondencia: angmvargasr@gmail.com.
** Ana María Garzón Porras. Estudiante IX semestre de Química Farmacéutica Universidad Nacional de Colombia
Correspondencia: conenis@gmail.com.
***Ángela Caro Rojas. Química Farmacéutica. Especialista en Epidemiología General, Magíster en Atención Farmacéutica. Coordinadora de Farmacovigilancia del Hospital Universitario Fundación Santa Fe de Bogotá.
Correspondencia: angela.caro@fsfb.org.co.
Recibido: julio de 2011
Aceptado para publicación: Julio de 2011