Origen
Las glándulas suprarrenales o adrenales, son un par de estructuras localizadas en cada lado del cuerpo, en la parte superior de los riñones. Cada una pesa 5 g, aproximadamente. Existen tres arterias adrenales predominantes. La superior es una rama de la arteria frénica inferior; la media se origina directamente de la aorta, mientras que la infe rior procede de la arteria renal. El drenaje venoso se hace fundamentalmente a través de una simple y bien definida vena central, la cual en el lado derecho se evacua en la cava, y la del lado izquierdo lo hace en la vena renal.
Diagrama secuencial N° 1. Definiciones y secuencias de las neoplasias adrenocorticales.
| Histología | Estado endocrino | Diagnóstico | Presentación clínica |
| Benigna | Funcional | Adenoma Aldosteronoma |
Sínd. Cushing Sínd. Conn |
| No Funcional | Adenoma Quiste Mielolipoma |
“Incidentaloma” | |
| Maligno Primario | Funcional | Carcinoma Adrenal | Sínd. Cushing Virilización Feminización Sínd. Conn |
| No Funcional | Carcinoma Adrenal | pérdida de peso, fiebre, dolor, anemia, masa en CT y MRI |
|
| Maligno Secundario | No funcional | Primario conocido | Insuficiencia adrenal, Masa CT y MRI |
| No Funcional | Primario desconocido | Insuficiencia adrenal “Incidentaloma” |
La glándula adrenal está compuesta de dos regiones distintas, la más extensa, amarillo brillante llamada corteza, cargada de lípidos, da a la glándula la apariencia externa característica. Cubierta por las capas de la corteza, está la otra región de color gris oscuro, la médula adrenal.
La corteza es de origen mesodérmico. Su desarrollo comienza en un grupo de células conocidas como primordio cortical. Estas células están localizadas cerca de las gonadas sobre la cresta adrenogenital en la quinta semana de la gestación. Esta localización explica porqué algunos fragmentos de tejido cortical (restos adrenales) se encuentran en sitios como los ovarios, cordón espermático y testículos. Las células crecen rápidamente y penetran al mesénquima retroperitoneal, superior al mesonefros para formar la corteza primitiva o fetal.
Durante la séptima semana del embarazo, un grupo de células migran del primordio cortical y se organizan en una corteza permanente. En esta misma época, la corteza es invadida por células que han migrado de la cresta neural y forman la médula adrenal. La asociación íntima entre la corteza y la médula adrenal, se ve sólo en los mamíferos (17).
La corteza fetal crece rápidamente y en la cuarta semana, las glándulas adrenales son más grandes que los riñones. El crecimiento de la corteza es altamente dependiente de la hormona adrenocorticotrópica. La corteza se atrofia inmediatamente después del parto. Poco después, la corteza permanente comienza su diferenciación en zona glomerulosa, fascicular y reticular, lo cual se completa al tercer año de vida.
La zona glomerulosa, la más extensa, se encuentra justamente debajo de la cápsula fibrosa de la glándula. Es muy delgada y es el sitio de producción de los mineralocorticoides (aldosterona). La zona media, llamada fascicular, elabora glucocorticoides, cortisol y esteroides sexuales adrenales. La capa o zona más interna, la reticular, es adyacente a la médula, y secreta cortisol, andrógenos y estrógenos.
Un resumen de las neoplasias adrenocorticales, su estado funcional y su presentación clínica, se muestra en el Diagrama Secuencial N° 1.
Como se puede observar en el Diagrama, se ha introducido el término “Incidentaloma” que es un nuevo hecho que ha sirgido con el advenimiento de la CT y la resonancia magnética (MRI) y que es el ocasional descubrimiento de una masa adrenal, asintomática e incidental durante uno de estos procedimientos de imágenes diagnósticas. En forma más rara, tales masas son descubiertas en el curso de una pielografía intravenosa, ultrasonografía, arteriografía, en una radiografía simple o en una intervención quirúrgica (18). Sin embargo, como el uso de la CT está cada vez más extendido, un mayor número de estas masas serán descubiertas, y el clínico tendrá que determinar el significado clinicopatológico de cada una de ellas.
Secreción y Síntesis de las Hormonas Adrenocorticotrópicas
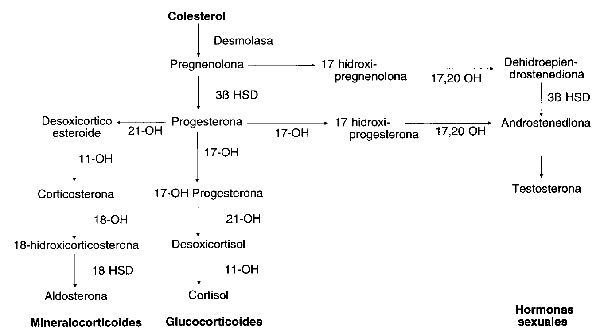
Aunque el control de la secreción de los productos corticoides de mayor categoría difiere algo entre sí, la vía primaria de la esteroidogénesis es común para todos los esteroides. La sustancia fundamental es el colesterol, (Diagrama de flujo N° 1). El colesterol es convertido en pregnenolona, progesterona, 17-0H progesterona, y de aquí a andrógenos adrenales o a cortisol. La progesterona es convertida a aldosterona por una vía diferente (21-hidroxilasa). Los 17-cetosteroides (andrógenos adrenales) son producidos en cantidades de 25 a 30 mg/día, los 17-hidroxiesteroides (cortisol) de 15 a 20 mg/día, y la aldosterona de 75 a 125 mcg/día. Como ya se mencionó, la aldosterona es producida en la zona glomerulosa, mientras que los 17-cetosteroides y los 17-hidroxicorticosteroides son producidos en las zonas fasciculada y reticular. La zona más externa y las dos internas, están bajo mecanismos reguladores separados.
Diagrama de flujo N° 1. Vías de la esteroidogénesis de la corteza adrenal.
Hormonas sexuales, mineralocorticoides y glucocorticoides, las mismas
etapas iniciales de síntesis.
Control de la Secreción del Cortisol
El estimulador próximo de la producción de cortisol, es el péptido, hormona adrenocorticotrópica (ACTH), que se origina en el lóbulo anterior de la hipófisis y es regulada
por la hormona liberada de corticotropina (CRH); ésta es almacenada en el hipotálamo anterior y al ser estimulada, se libera en el sistema portal hipofisario donde alcanza la hipófisis anterior para liberar ACTH. La estimulación de la CRH es controlada por varias influencias neurales. Es probable que el sistema nervioso central esté implicado en las variaciones de la secreción diurna. La producción incrementada del cortisol durante el miedo u otras emociones productoras de estrés, es otro indicador de la regulación del sistema nervioso central. Por otro lado, el notorio incremento de la secreción de cortisol durante el dolor y el trauma físico, atestiguan la importancia de las 17,20 OH Testosterona vías sensoriales periféricas en la estimulación de la producción de cortisol.
La liberación de CRH está sometida a la influencia inhibitoria de la retroalimentación negativa del cortisol. Aunque existen evidencias de un asa corta de retroalimentación de ACTH sobre CRH, son clínicamente notables tanto la retroalimentación lenta como la rápida del cortisol sobre los mecanismos de liberación de la hipófisis. En circunstancias normales, el punto para la retroalimentación negativa inhibitoria de la secreción de ACTH, está en la extensión de las concentraciones fisiológicas del cortisol en el plasma; esto es, una concentración plasmática del cortisol en el límite superior normal de 15 a 20 mcg/dL de plasma, resulta en supresión de la secreción de ACTH y una consecuente baja de la secreción de cortisol por la corteza adrenal.
Hay pruebas que sugieren que la elevación aguda de las concentraciones de cortisol en el plasma, puede suprimir tanto la liberación de CRH como la respuesta de la ACTH, en el estímulo de la CRH.
La secreción de andrógenos adrenales, los cuales son convertidos periféricamente a estrógenos, es básicamente controlada por los mismos mecanismos de la secreción del cortisol. Esto es diferente a los estrógenos y andrógenos secretados por las gonadas, los cuales son regulados por un conjunto completamente distinto de péptidos hipofisanos.
