Supervivencia a dos Años en Pacientes con Cáncer Gástrico localmente Avanzado en una institución de Popayán entre 2018 y 2020
Two-year survival in patients with locally advanced gastric cancer at an institution in Popayán between 2018 and 2020
Resumen
Introducción. El tratamiento oncológico perioperatorio en pacientes con cáncer gástrico localmente avanzado está indicado; aun así, no siempre es posible. El objetivo de este estudio fue evaluar la supervivencia de los pacientes según la administración de quimioterapia perioperatoria.
Métodos. Estudio observacional, tipo cohorte ambispectivo, incluyendo pacientes con cáncer gástrico localmente avanzado quienes recibieron o no quimioterapia perioperatoria.
Resultados. Se incluyeron 33 pacientes, 90,9 % pertenecían al régimen subsidiado de salud y el 78,8 % en estadio T4. El grupo que recibió quimioterapia perioperatoria, que solo tuvo 5 pacientes (15,1 %), presentó mayor supervivencia global a 2 años (100 %), seguido del grupo de quimioterapia postoperatoria (58,8 %) y del grupo sin quimioterapia, que alcanzó una supervivencia global a 2 años de 54,5 %.
Discusión. La supervivencia global fue mayor en el grupo de quimioterapia perioperatoria, consonante a lo descrito a nivel internacional, aunque los pacientes se encontraban en un estadío localmente más avanzado, la mayoría con T4 y N+ según AJCC VIII edición.
Conclusiones. El estadío clínico es un factor pronóstico importante y, en nuestro medio, la mayoría de los pacientes consultan en estadíos localmente más avanzados. A eso se suman las dificultades en el acceso a la atención en salud. Aun así, la quimioterapia perioperatoria mostró una supervivencia mayor en pacientes con cáncer gástrico localmente avanzado.
Palabras clave: neoplasias gástricas; quimioterapia adyuvante; mortalidad; pronóstico; análisis de supervivencia.
Abstract
Introduction. Perioperative cancer treatment in patients with locally advanced gastric cancer is indicated; even so, it is not always possible. The objective was to evaluate survival according to time and receipt of perioperative chemotherapy.
Methods. Observational study, ambispective cohort type, including patients with locally advanced gastric cancer who received or did not receive perioperative chemotherapy. Results. Thirty-three patients were included, 90.9% belonged to the subsidized regimen and 78.8% with TNM T4. The perioperative chemotherapy group, which only had five patients (15.1%), had a higher overall survival at 2 years (100%), followed by the postoperative chemotherapy group and by the group without chemotherapy, with an overall survival at 2 years of 58.8% and 54.5%, respectively.
Discussion. Overall survival was higher in the perioperative chemotherapy group, consistent with what has been described internationally, although the patients were in a more advanced stage, most being with T4 and N+ according to the AJCC VIII edition.
Conclusions. The clinical stage is an important prognostic factor and in our environment, most patients consult in more advanced stages, coupled with difficulties in accessing health care. Even so, perioperative chemotherapy showed a longer survival in patients with locally advanced gastric cancer, the data should not be extrapolated since the number of patients in each group is significantly different.
Keywords: stomach neoplasms; adjuvant chemotherapy; mortality; prognosis; survival analysis.
Introducción – Supervivencia a dos Años en Pacientes con Cáncer Gástrico localmente Avanzado
El cáncer gástrico se encuentra entre las 5 primeras causas de mortalidad por cáncer en el mundo según Globocan 2018, presentando 1.033.701 casos nuevos en 2018 y 782.685 muertes anuales 1. En Colombia es la primera causa de muerte por cáncer; según el Instituto Nacional de Cancerología (INC), entre 2007 y 2013 hubo 234.763 muertes por neoplasia gástrica, 115.708 en hombres y 119.055 en mujeres, siendo la causa del 13,7 % de todas las muertes 2.
Aunque ha disminuido la mortalidad por este evento de manera importante durante las últimas décadas 3,4, persiste como la primera causa de muerte por cáncer en hombres en Colombia, y entre las mujeres es la tercera causa después de la neoplasia maligna de mama y cuello uterino 2.
Aunque la adyuvancia mejora la supervivencia de los pacientes, se han descrito mayores ventajas con la terapia neoadyuvante, entre las que se destacan una mayor tasa de resección R0 y regresión tumoral, representando buena respuesta clínica y patológica de los individuos al tratamiento 5-7.
Las guías NCCN 2019 8 y ESMO 2016 9:
Recomiendan el manejo con terapia perioperatoria en pacientes con enfermedad avanzada locorregional y potencialmente resecables, con un mayor nivel de evidencia a favor de la quimioterapia perioperatoria. En Colombia, un estudio multicéntrico realizado en la ciudad de Bogotá, D.C., mostró, entre otras ventajas, mayor supervivencia en pacientes que se trataron con neoadyuvancia y gastrectomía con respecto a los pacientes que se trataron con cirugía y adyuvancia 5.
Debido a que el Departamento del Cauca, en Colombia, presenta una de las tasas de prevalencia más altas en el país 4, se decidió realizar este estudio con el objetivo de determinar la supervivencia global y libre de enfermedad a dos años en pacientes con cáncer gástrico localmente avanzado que recibieron o no tratamiento con quimioterapia perioperatoria.
Métodos – Supervivencia a dos Años en Pacientes con Cáncer Gástrico localmente Avanzado
Estudio observacional, tipo cohorte ambispectivo, en el que se incluyeron de manera consecutiva los pacientes con cáncer gástrico en estadio clínico II a III, que aceptaron participar mediante la firma del consentimiento informado, fueron llevados a gastrectomía en Clínica La Estancia de Popayán, departamento de Cauca, entre julio de 2018 y junio de 2020, y se hizo seguimiento a dos años. Se excluyeron pacientes con estadios tempranos, estadio IV e información incompleta.
Se recolectaron datos de quimioterapia perioperatoria, estadificación clínica, grado de respuesta tumoral, extensión de resección, supervivencia global, supervivencia libre de enfermedad y mortalidad. Los datos fueron extraídos de las historias clínicas y reportes de histopatología.
Quienes no habían asistido a los últimos controles a dos años se les contactó por llamada telefónica para verificar su estado de salud y supervivencia.
La información se recogió en una base de datos diseñada por los investigadores en Excel y se llevó a cabo un análisis descriptivo y exploratorio en el programa IBM® SPSS® V.25, empleando para las variables cualitativas, frecuencias y proporciones, así como medidas de tendencia central y de dispersión para las variables cuantitativas.
Resultados – Supervivencia a dos Años en Pacientes con Cáncer Gástrico localmente Avanzado
Se incluyeron 33 pacientes, con predominio de género masculino (n=19; 57,6 %) y promedio de edad de 62,4 años (rango de 42 a 80 años) (Tabla 1).
Tabla 1. Características de los pacientes con cáncer gástrico llevados a gastrectomía (n=33).
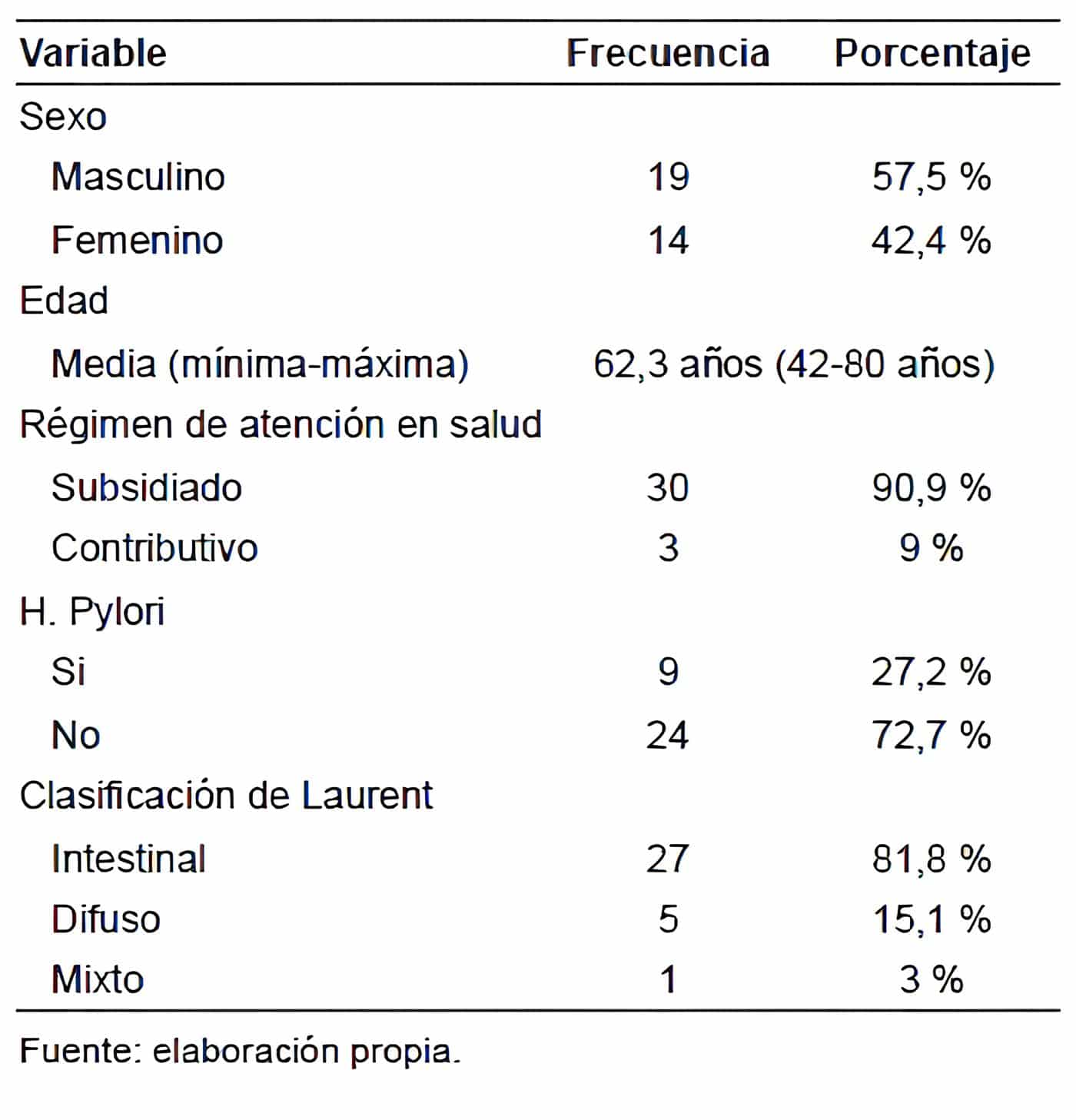
El 90,9 % (n=30) de los pacientes pertenecían al régimen subsidiado de salud. El tipo histológico más frecuente según la clasificación de Lauren fue el intestinal (n=27; 81,8 %) y solo en el 27,2 % de los pacientes se identificó la presencia de Helicobacter pylori.
Basados en la AJCC UICC VIII edición 10, 26 pacientes (78,8 %) presentaban tumor T4 y 5 (15,2 %) T3; 30 pacientes (90,9 %) tenían compromiso ganglionar (N+), por lo que la estadificación clínica más frecuente correspondió al estadio III, en el 90,9 % (n=30) de los pacientes.
Entre los pacientes evaluados, se realizó neoadyuvancia con el esquema FLOT en 5 (15,2 %) pacientes; de estos, el grado de respuesta tumoral fue completa en un paciente (20 %), parcial en 2 (40 %) y nula o mala en 2 (40 %).
Se realizó adyuvancia en 17 (51,5 %) pacientes y 11 (33,3 %) no recibieron neoadyuvancia ni adyuvancia. En cuanto a la extensión de resección, correspondió a R0 en 31 (93,9 %) pacientes y R1 en 2 (6,1 %).
De los 5 pacientes que recibieron neoadyuvancia, ninguno murió durante los dos años de seguimiento; por el contrario, en los pacientes que no recibieron neoadyuvancia se presentó una mortalidad del 42,8 % (12/28), con una supervivencia global a dos años del 57,3 %. Entre los 17 pacientes que recibieron quimioterapia postoperatoria, se presentó una mortalidad del 41,7 % (n=7), con una supervivencia global a dos años de 58,8 % y libre de enfermedad en 41,2 %.
De los 11 pacientes que no recibieron quimioterapia antes o después de la cirugía, la mortalidad fue del 45,5 % (n=5), con una supervivencia global a 2 años del 54,5 % (Figura 1). Los pacientes que murieron durante el seguimiento pertenecían en su mayoría al grupo de estadificación patológica IIIA y IIIB (33 % cada una), seguida de IIIC (25 %).
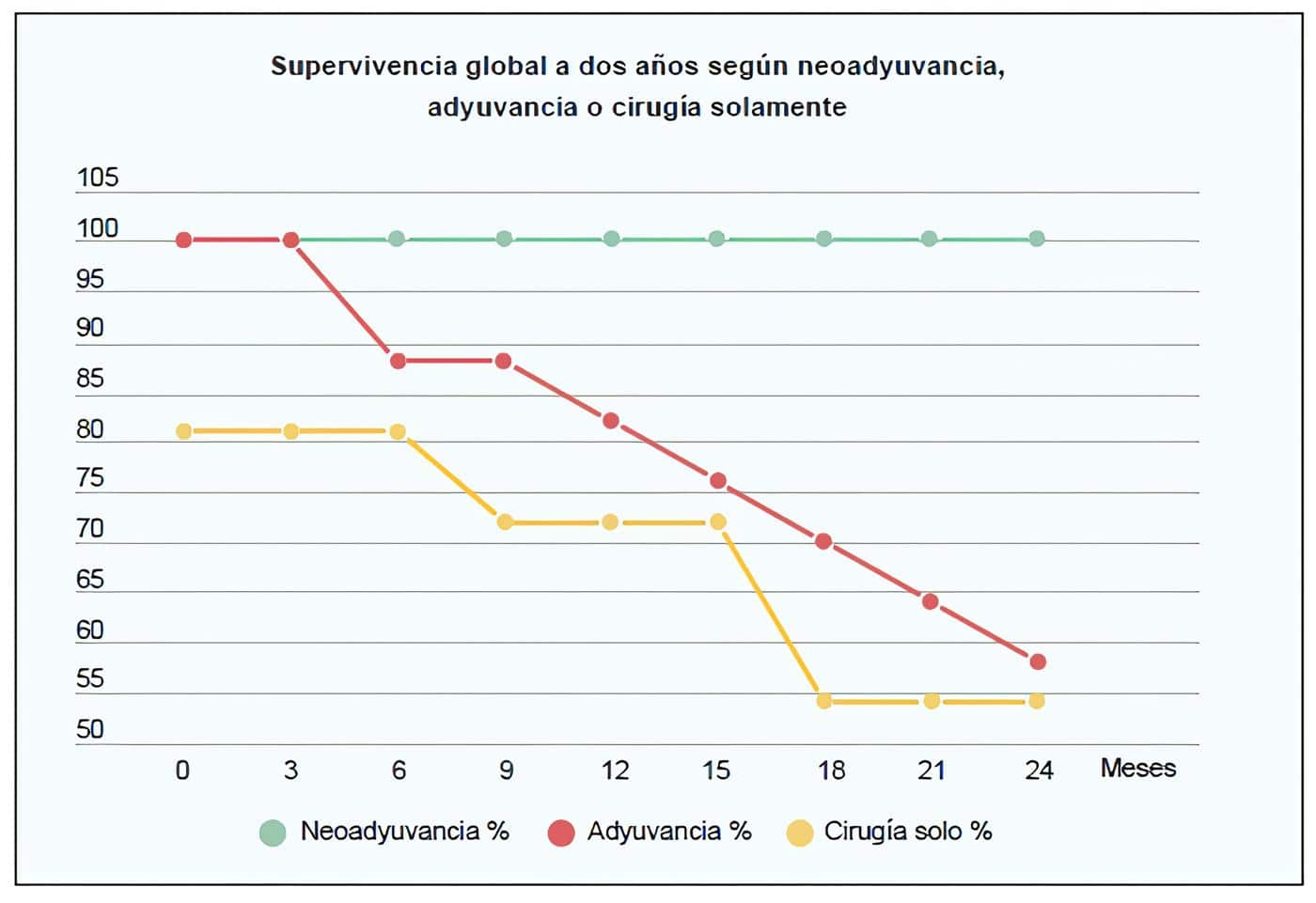
Figura 1. Supervivencia global a dos años en los pacientes sometidos a gastrectomía, según
administración de quimioterapia peri versus postoperatoria. Fuente: elaboración propia.
Discusión – Supervivencia a dos Años en Pacientes con Cáncer Gástrico localmente Avanzado
El 90,9 % de nuestros pacientes estaban afiliados al régimen subsidiado de salud, pertenecientes a los estratos socioeconómicos más bajos y residentes en viviendas rurales distantes.
Los pacientes y sus familiares relataron las dificultades para obtener atención en salud, relacionadas con su vivienda en zona rural dispersa, los costos para el desplazamiento, así como demoras en la autorización para los controles y la cirugía por parte de la entidades promotoras de salud (EPS).
Estas barreras para el acceso a la atención en salud durante el seguimiento fueron agravadas por la pandemia por COVID.
Al respecto, un estudio realizado en Bucaramanga en 2009 11, denotó cambios en el pronóstico de sobrevida según el estrato y régimen de salud, con disminución en la supervivencia en los pacientes quienes se encontraban afiliados al régimen subsidiado o que pertenecían a estratos más bajos; por tanto, se debe trabajar en las barreras de acceso a la atención en salud para mejorar el pronóstico de los pacientes con cáncer.
Según la clasificación de Lauren, en su mayoría los tumores correspondieron al tipo intestinal, los cuales presentan un mejor pronóstico, hallazgo que concuerda con el comportamiento a nivel nacional demostrado en Bogotá 5 y a nivel internacional, en Alemania 12.
Basados en la clasificación AJCDC UICC VIII edición 10, nuestros pacientes tuvieron tumores localmente avanzados, con un diagnóstico más tardío que lo descrito a nivel internacional:
Encontrándose tan solo el 6,1 % entre T1 y T2, a diferencia de lo reportado en el estudio FLOT 12, que presentaban un 17 % entre T1 y T2 y solo un 9 % en T4. El compromiso ganglionar también fue mayor en nuestro estudio (N+ en 90,9 %) con respecto al FLOT (N+ en 81 %).
Entre nuestros pacientes fue inferior el porcentaje que recibió neoadyuvancia y adyuvancia en comparación con el mismo estudio colombiano presentado en 2018 5, donde se realizó neoadyuvancia en el 56 % y adyuvancia en 43 %.
La tasa de supervivencia global a 2 años en pacientes que recibieron neoadyuvancia fue mayor (100 %) con respecto a la de los pacientes llevados a cirugía sin recibir quimioterapia antes o después (54,5 %); sin embargo, este resultado debe interpretarse con cautela teniendo en cuenta el pequeño número de pacientes que recibieron neoadyuvancia.
En consonancia, el estudio MAGIC 13, que reportó la supervivencia a 5 años en 503 pacientes con neoadyuvancia versus cirugía sola, encontró diferencias significativas entre los grupos a favor de la neoadyuvancia (36 % vs 23 %).
Al analizar los pacientes llevados a cirugía con y sin adyuvancia, encontramos mayor supervivencia a 2 años entre quienes recibieron adyuvancia (58,8 % vs 54,5 %).
Esto se corresponde con lo descrito en el estudio CLASSIC 14, con seguimiento a 5 años, pero estadificación menor a la de este trabajo, donde los pacientes que recibieron adyuvancia tuvieron supervivencia de 78 % vs un 69 % en los pacientes que observaron clínicamente.
El 60 % de los pacientes con neoadyuvancia presentaron respuesta completa o parcial, semejante a lo publicado en AIO FLOT 15, donde se presentó respuesta completa en el 10 % y parcial en el 50 %.
La extensión de resección R0 se reportó en 93,9 % similar a lo reportado en otros estudios nacionales 5 e internacionales 15.
Al comparar la supervivencia global de nuestros pacientes que recibieron quimioterapia perioperatoria con respecto a aquellos pacientes llevados a cirugía y adyuvancia, se encontró mejores resultados en el primer grupo, similar a los resultados de un estudio realizado en Bogotá en 2018 5, el cual presentó supervivencia global a 2 y 5 años mayor en los pacientes con quimioterapia perioperatoria (80,1 %) respecto a pacientes llevados a cirugía y adyuvancia (61,2 %), con una diferencia estadísticamente significativa.
Conclusiones – Supervivencia a dos Años en Pacientes con Cáncer Gástrico localmente Avanzado
La supervivencia global y libre de enfermedad a dos años en pacientes con cáncer gástrico localmente avanzado se comportó similar a lo descrito a nivel mundial, con un aumento de la supervivencia en los pacientes que recibieron neoadyuvancia comparado con los pacientes que recibieron manejo adyuvante o no recibieron quimioterapia.
El estadio clínico es un factor pronóstico importante y, en nuestro medio, la mayoría de los pacientes consultan con estadios localmente más avanzados debido a factores demográficos y del mismo sistema de salud, lo que conlleva a una disminución en las oportunidades de acceder a un tratamiento a tiempo.
Cumplimiento de normas éticas
Consentimiento informado: Se obtuvo el consentimiento informado de los pacientes participantes.
El comité de ética de Clínica La Estancia de Popayán – Cauca, en cabeza del subdirector científico aprobaron el diseño y metodología del estudio, teniendo en cuenta el artículo 11 de la Resolución 008430 de 1993 del Ministerio de Salud de Colombia, que consideró el estudio como una investigación sin riesgo; fue registrado en el sistema de información de investigaciones bajo el ID 5623.
Conflicto de interés: Ninguno declarado por los autores.
Fuentes de financiación: Ninguna fuente externa.
Contribución de los autores
– Concepción y diseño del estudio: Henry Muñoz-Orozco, Julián A. Meza, Angela Merchán-Galvis. – Recolección de datos: Henry Muñoz-Orozco.
– Análisis e interpretación de datos: Henry Muñoz-Orozco, Julián A. Meza, Angela Merchán-Galvis. – Redacción del manuscrito: Henry Muñoz-Orozco, Angela Merchán-Galvis.
– Revisión y aprobación final del manuscrito: Julián A. Meza, Angela Merchán-Galvis.
Referencias – Supervivencia a dos Años en Pacientes con Cáncer Gástrico localmente Avanzado
1 Bray F, Ferlay J, Soerjomataram I, Siegel RL, Torre LA, Jemal A. Global cancer statistics 2018: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J Clin. 2018;68:394- 424. https://doi.org/10.3322/caac.21492
2 Pardo C, de Vries E, Buitrago L, Gamboa O. Atlas de mortalidad por cáncer en Colombia. Cuarta edición. Bogotá D.C.: Instituto Nacional de Cancerología; 2017. p. 124.
3 Bray F, Piñeros M. Cancer patterns, trends and projections in Latin America and the Caribbean: a global context. Salud Publica Mex. 2016:58:104-17. https://doi.org/10.21149/spm.v58i2.7779
4 Sierra MS, Soerjomataram I, Antoni S, Laversanne M, Piñeros M, de Vries E, Forman D. Cancer patterns and trends in Central and South America. Cancer Epidemiol. 2016;44 Suppl 1:S23-S42. https://doi.org/10.1016/j.canep.2016.07.013
5 Campillo J, Suárez L, Guevara R, Burgos R, Villegas C, Cendales M, Henao F, Rosero G. Supervivencia y complicaciones en pacientes con cáncer gástrico y de la unión gastroesofágica tratados con quimioterapia perioperatoria más cirugía comparada con cirugía más terapia adyuvante: estudio multicéntrico, Bogotá D.C., 2010-2017. Rev Colomb Cir. 2018;33:353-61. https://doi.org/10.30944/20117582.82
6 Hu Y, Hu D, Li W, Yu X. Neoadjuvant chemotherapy brings more survival benefits than postoperative chemotherapy for resectable gastric cancer: a Meta- analysis of randomized controlled trials. J BUON. 2019;24:201-14.
7 Xu AM, Huang L, Liu W, Gao S, Han WX, Wei ZJ. Neoadjuvant chemotherapy followed by surgery versus surgery alone for gastric carcinoma: systematic review and meta- analysis of randomized controlled trials. PLoS One. 2014;9:e86941. https://doi.org/10.1371/journal.pone.0086941
8 Ajani JA, D’Amico TA, Bentrem DJ, Chao J, Cooke D, Corvera C, et al. Gastric Cancer, Version 2.2022, NCCN Clinical Practice Guidelines in Oncology. J Natl Compr Canc Netw. 2022;20:167-192. https://doi.org/10.6004/jnccn.2022.0008
Bibliografías – Supervivencia a dos Años en Pacientes con Cáncer Gástrico localmente Avanzado
9 Smyth EC, Verheij M, Allum W, Cunningham D, Cervantes A, Arnold D, ESMO Guidelines Committee. Gastric cancer: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol. 2016;27(suppl_5):38-49. https://doi.org/10.1093/annonc/mdw350
10 Amin MB, Greene FL, Edge SB, Compton CC, Gershenwald JE, Brookland RK, et al. The Eighth Edition AJCC Cancer Staging Manual: Continuing to build a bridge from a population-based to a more “personalized” approach to cancer staging. CA Cancer J Clin. 2017;67:93-9. https://doi.org/10.3322/caac.21388
11 de Vries E, Uribe C, Pardo C, Lemmens V, Van de Poel E, Forman D. Gastric cancer survival and affiliation to health insurance in a middle-income setting. Cancer Epidemiol. 2015;39:91-6. https://doi.org/10.1016/j.canep.2014.10.012
12 Al-Batran SE, Homann N, Pauligk C, Goetze TO, Meiler J, Kasperet S, et al. Perioperative chemotherapy with fluorouracil plus leucovorin, oxaliplatin, and docetaxel versus fluorouracil or capecitabine plus cisplatin and epirubicin for locally advanced, resectable gastric or gastro-oesophageal junction adenocarcinoma (FLOT4): a randomised, phase 2/3 trial. Lancet. 2019;393:1948- 57. https://doi.org/10.1016/S0140-6736(18)32557-1
13 Cunningham D, Allum WH, Stenning SP, Thompson JN, Van de Velde CJH, Nicolson M, et al. Perioperative chemotherapy versus surgery alone for resectable gastroesophageal cancer. N Engl J Med. 2006;355:11-20. https://doi.org/10.1056/NEJMoa055531
14 Noh SH, Park SR, Yang HK, Chung HC, Chung IJ, Kim SW, et al. Adjuvant capecitabine plus oxaliplatin for gastric cancer after D2 gastrectomy (CLASSIC): 5-year follow-up of an open-label, randomised phase 3 trial. Lancet Oncol. 2014;15:1389-96. https://doi.org/10.1016/S1470-2045(14)70473-5
15 Al-Batran SE, Homann N, Pauligk C, Illerhaus G, Martens UM, Stoehlmacher J, et al. Effect of neoadjuvant chemotherapy followed by surgical resection on survival in patients with limited metastatic gastric or gastroesophageal junction cancer: The AIO-FLOT3 Trial. JAMA Oncol. 2017;3:1237-44. https://doi.org/10.1001/jamaoncol.2017.0515
Autores – Supervivencia a dos Años en Pacientes con Cáncer Gástrico localmente Avanzado
1 Henry Muñoz-Orozco, Médico, residente de Cirugía General, Universidad del Cauca, Popayán, Colombia.
2 Julián A. Meza, Médico, especialista en Cirugía general y Cirugía oncológica, Servicio de Cirugía Oncológica, Clínica La Estancia; docente,
Departamento de Ciencias Quirúrgicas, Universidad del Cauca, Popayán, Colombia.
3 Ángela Merchán-Galvis, Médica, magíster en Epidemiología Clínica, docente, Departamento de Medicina Social y Salud Familiar, Universidad del Cauca,
Popayán, Colombia.
Fecha de recibido: 22/10/2022 – Fecha de aceptación: 5/11/2022 – Publicación en línea: 06/03/2023
Correspondencia: Henry Muñoz-Orozco, Portales del Norte Carrera 8ª # 26 AN – 04, Popayán, Colombia. Teléfono: +57 3147398183. Dirección electrónica: henryo@unicauca.edu.co
Citar como: Muñoz-Orozco H, Meza JA, Merchán-Galvis A. Supervivencia a dos años en pacientes con cáncer gástrico localmente avanzado en una institución de Popayán entre 2018 y 2020. Rev Colomb Cir. 2023;38:468-73. https://doi.org/10.30944/20117582.2282
Este es un artículo de acceso abierto bajo una Licencia Creative Commons – BY-NC-ND https://creativecommons.org/licenses/by-nc-nd/4.0/deed.es