Diagnosis and Current Management of Achalasia
Resumen
Introducción. La acalasia es un trastorno motor del esófago poco común, de etiología no clara, caracterizado por la pérdida de relajación del esfínter esofágico inferior, pérdida del peristaltismo normal, regurgitación y disfagia.
Métodos. Se realizó una revisión narrativa de la literatura en revistas científicas y bases de datos en español e inglés, con el fin de presentar información actualizada en lo referente al diagnóstico y tratamiento de esta patología.
Resultado. Se presenta la actualización de los criterios de los trastornos motores esofágicos según la clasificación de Chicago (CCv4.0) para el diagnóstico de acalasia y sus subtipos de acuerdo con los nuevos criterios, así como los tratamientos actuales.
Conclusión. La acalasia es un trastorno esofágico multimodal, con manifestaciones de predominio gastrointestinal, por lo que su diagnóstico y abordaje terapéutico oportuno es esencial para mejorar la calidad de vida de los pacientes.
Palabras clave: trastornos de deglución; acalasia del esófago; manometría; clasificación; miotomía de Heller.
Abstract
Introduction. Achalasia is a rare motor disorder of the esophagus of unclear etiology, characterized by loss of lower esophageal sphincter relaxation, loss of normal peristalsis, regurgitation, and dysphagia.
Methods. A narrative review of the literature in scientific journals and databases in Spanish and English was carried out, in order to present updated information regarding the diagnosis and treatment of this pathology.
Result. The update of the Chicago esophageal motor disorders criteria (CCv4.0) is presented for the diagnosis of achalasia and its subtypes according to the new criteria, as well as current treatments.
Conclusion. Achalasia is a multimodal esophageal disorder, with predominantly gastrointestinal manifestations, so its timely diagnosis and therapeutic approach is essential to improve the quality of life of patients.
Keywords: swallowing disorders; achalasia of the esophagus; manometry; classification; Heller’s myotomy.
Introducción – Acalasia del Esófago
La acalasia es un trastorno motor esofágico de etiología desconocida y baja prevalencia, que afecta por igual a hombres y mujeres. El grupo etario más afectado está entre 30 y 60 años, con una incidencia global de 0,03 a 1,63 casos por cada 100.000 personas por año y una prevalencia de 10 por cada 100.000 personas 1-3.
Inicialmente ocurre la degeneración del plexo mioentérico, después hay alteración en la relajación gastroesofágica y en el peristaltismo del cuerpo esofágico, lo que conduce a regurgitación y disfagia 1.
Se desconoce la causa de la inhibición neuronal, pero se ha encontrado asociación con procesos autoinmunes desencadenados por infecciones virales como herpes o sarampión. El proceso inflamatorio se asocia con un infiltrado de linfocitos T que causan la destrucción ganglionar, como ocurre en la enfermedad de Chagas 3-5.
La inflamación del plexo mioentérico produce una disfunción de las neuronas posganglionares inhibidoras en el esófago distal, las cuales liberan óxido nítrico y péptido intestinal vasoactivo como neurotransmisores, por lo que su disfunción lleva a un desequilibrio en el control de excitación e inhibición del esfínter esofágico 4-6.
La acalasia se clasifica en tres subtipos de acuerdo con los hallazgos manométricos: el tipo 1 se caracteriza por ausencia de peristalsis y presurización, el tipo 2 por compresión esofágica, ausencia de peristalsis y presurización panesofágica mayor del 30 % y el tipo 3 por presentar contracciones espásticas con periodos de presurización.
Los tres tipos presentan presión integrada de la relajación (IRP, por sus siglas en inglés) elevada 5,6.
Diagnóstico – Acalasia del Esófago
El cuadro clínico se caracteriza por la disfagia progresiva a los alimentos líquidos y sólidos y por el reflujo gastroesofágico; puede haber síntomas adicionales como el dolor retroesternal o la pérdida de peso 3,4.
La mayoría de los pacientes pueden presentar desnutrición por la rápida pérdida de peso, asociada no solo con el trastorno motor esofágico sino con los cambios en la alimentación debido a la disfagia 7,8.
El abordaje diagnóstico de un paciente con disfagia debe iniciar con una endoscopia digestiva alta para descartar obstrucción, neoplasia, reflujo gastroesofágico o procesos inflamatorios crónicos. Después de descartar estas posibles etiologías, se deben realizar estudios para evaluar la motilidad esofágica 3, 4.
La disfunción del esfínter esofágico inferior (EEI) en pacientes con acalasia representa una barrera protectora contra el reflujo, pero en algunos casos ocurre relajación del EEI, lo que permite el ingreso del contenido gástrico al esófago y genera la sintomatología característica de la enfermedad por reflujo gastroesofágico (ERGE), con disfagia, pirosis, dolor retroesternal o regurgitación.
En etapas iniciales estos pacientes pueden compartir síntomas entre un 13,2 – 68 %, por lo que se pueden confundir 9,10.
Los pacientes con acalasia son diagnosticados tardíamente, con un promedio de demora de cinco años; hasta el 36,8 – 50 % son manejados inicialmente como una ERGE, por lo que ante un paciente diagnosticado con enfermedad por reflujo que no responda al tratamiento o presente sintomatología adicional, se deben realizar los estudios imagenológicos y manométricos pertinentes para descartar un trastorno de la motilidad esofágica, entre ellos la acalasia 11,12.
Radiografía de vías digestivas altas
Por su disponibilidad y bajo costo es considerado un estudio adecuado, donde se puede observar el signo clásico de “pico de pájaro”, por la dilatación esofágica con abertura mínima del EEI.
Además de orientar el diagnóstico, muestra la anatomía del esófago, lo que permite establecer un plan quirúrgico adecuado.
Es útil en el diagnóstico oportuno de esófago corto, presbiesófago, cambios peristálticos del esófago asociados al envejecimiento (disminución o ausencia de peristalsis y aumento de contracciones), hernia hiatal o alguna otra al-teración anatómica 13-15.
Manometría esofágica de alta resolución
Se considera el “patrón de oro” para el diagnóstico de la acalasia. Se basa principalmente en el análisis de tres parámetros: la presión integrada de relajación (IRP), la presión integral contráctil (DCI, por sus siglas en inglés) y la latencia distal (DL, por sus siglas en inglés).
La IRP es la presión promedio más baja en el EEI durante la deglución y se toma por cuatro segundos. La DCI es el índice de intensidad contráctil de la presión esofágica, calculado a través de la amplitud, la duración y extensión de la contracción esofágica distal.
La DL es la medida de tiempo desde la apertura del esfínter esofágico superior (EES) inducida por la deglución, hasta la llegada de la contracción esofágica. Estas medidas permiten determinar alteraciones en la motilidad esofágica mediante una serie de valores de referencia 3,16-20.
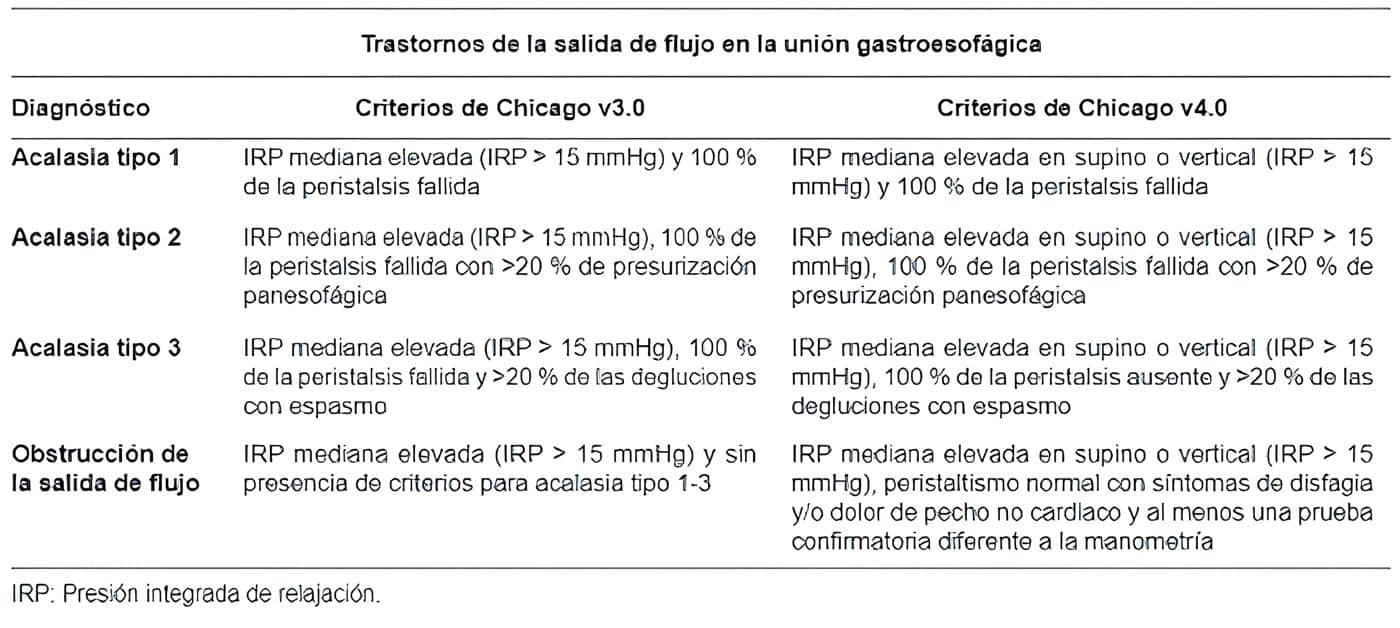
Sobre los resultados obtenidos en esta prueba se desarrolló la clasificación de Chicago para trastornos motores esofágicos, que actualmente se encuentra en su cuarta versión (CCv4.0), en la que se realizaron modificaciones que incluyen la realización de degluciones con el paciente en decúbito, en sedestación y el uso de maniobras para mejorar la sensibilidad y especificidad en los hallazgos, también se modificaron los criterios de hipomotilidad y obstrucción de salida en la unión gastroesofágica (tabla 1) 20-22.
Tabla 1. Criterios diagnósticos de la manometría esofágica de alta resolución según la Clasificación de Chicago 17,18
Tomografía computarizada de tórax y de abdomen superior contrastada
Permiten hacer el diagnóstico diferencial entre la acalasia primaria y la pseudoacalasia; en esta última se observa engrosamiento de la pared esofágica distal de forma nodular, lobulado y asimétrico, una masa de partes blandas en la unión gastroesofágica, adenopatías mediastínicas y metástasis pulmonares, hepáticas u óseas 22,23.
Es importante tener en cuenta el diagnóstico diferencial de pseudo-acalasia, la cual se caracteriza por presentar síntomas similares a la acalasia, provocados por etiologías secundarias, que en la mayoría de los casos son malignas, como los tumores primarios de esófago o de la unión gastroesofágica, tumores secundarios.
También hay causas benignas como tumores mesenquimales benignos, amiloidosis secundaria, neuropatía periférica, pseudoquiste pancreático, sarcoidosis, neurofibromatosis y leiomiomatosis esofágica 23-25.
Tratamiento – Acalasia del Esófago
La acalasia es una patología esofágica crónica sin tratamiento curativo definitivo. El objetivo es disminuir la presión del EEI mediante tratamientos farmacológicos, endoscópicos o quirúrgicos, con el fin de aliviar síntomas, evitar complicaciones y recidivas a largo plazo 3-5,26,27.
Tratamiento farmacológico
Se basa en el uso de relajantes musculares que pueden actuar a nivel del EEI. Los más usados son los nitratos, los bloqueadores de los canales de calcio y, más recientemente, los inhibidores de la fosfodiesterasa 5, logrando reducir la presión del EEI en un 30-60 % 26,28,29.
El efecto de estos medicamentos proporciona un beneficio sintomático, pero no son tratamientos a largo plazo ya que no evitan la progresión de la dilatación esofágica, ni mejoran el paso de los alimentos; además generan síntomas como cefalea, mareo y edema en miembros inferiores, por lo que no son muy empleados 3,29.
Tratamiento endoscópico – Acalasia del Esófago
Consiste en la aplicación de toxina botulínica mediante inyección o la dilatación neumática 27,28.
La toxina botulínica A es una neurotoxina que reduce la acetilcolina de las terminaciones nerviosas; se inyecta en el EEI bajo visión endoscópica directa, causando la relajación del esfínter 28,30.
El procedimiento tiene bajo riesgo y su respuesta es rápida, con tasas de éxito superiores al 90 %, sin embargo, su eficacia disminuye a largo plazo, por lo que se prefiere reservar este tipo de tratamientos para los adultos mayores o pacientes en quienes el tratamiento quirúrgico o endoscópico invasivo está contraindicado, ya que en algunos casos en necesario repetir el procedimiento 5,28.
La dilatación neumática se realiza con un balón dilatador cilíndrico, de 30-40 mm, guiado por endoscopia o fluoroscopia, que se ubica en el EEI generando una ruptura progresiva de las fibras musculares a este nivel 3,31.
Con esta técnica se ha logrado una disminución de la disfagia del 60 % a tres años, pero su eficacia decae con el paso del tiempo, por lo que se recomienda especialmente en pacientes mayores de 40 años.
El uso de una segunda o tercera dilatación no ha demostrado mejoría a largo plazo, con recaídas a cinco años del 35 % 27.
Tratamiento quirúrgico – Acalasia del Esófago
Antes de cualquier cirugía se debe aplicar el índice Eckardt, que evalúa la severidad de síntomas como disfagia, regurgitación, dolor torácico y pérdida de peso, y permite predecir la eficacia y respuesta del paciente al tratamiento quirúrgico, especialmente en pacientes con un puntaje menor o igual a 3, con una eficacia del 70,8 % 24,25.
Existen dos alternativas, la miotomía de Heller y la miotomía endoscópica peroral (POEM), que fue descrita en el año 2007 por Pasricha como tratamiento experimental para acalasia.
La POEM consiste en un procedimiento endoscópico donde se inyecta solución salina y epinefrina en la capa submucosa, 12-13 cm proximales a la unión gastroesofágica en la posición de las dos en punto del reloj, luego se realiza un túnel en el espacio submucoso en la pared anterior del esófago hasta los primeros tres cm del estómago y después de completar el túnel se seccionan las fibras musculares circulares 27,32,33.
Algunos estudios han demostrado una alta eficacia de la POEM a corto plazo, con mejoría sintomática en el 90 % de los pacientes, incluyendo la reducción del dolor torácico, pero otros han reportado una alta incidencia de ERGE, es-tenosis, esofagitis erosiva y esófago de Barret a largo plazo en los pacientes sometidos a este tratamiento; se ha observado solo un leve aumento de los síntomas después de 36 meses de seguimiento, por lo que se requieren estudios más prolongados que establezcan el papel de la POEM en la acalasia 32-36.
La miotomía de Heller suele hacerse por vía laparoscópica y consiste en una sección longitudinal anterior del EEI en una extensión de 2-3 cm en el cardias y de 5-6 cm en el esófago distal.
Este procedimiento debe ir acompañado de una cirugía antirreflujo; las más utilizadas son la funduplicatura de Dor (90 grados) y de Toupet (270 grados) 27-28,37, que consisten en envolver la porción inferior del esófago con el fondo gástrico, fijado con suturas para mantener una presión elevada en el esófago y evitar que haya reflujo de ácido gástrico posteriormente 38.
Antes se realizaba la funduplicatura total de Nissen, que era eficaz para controlar los síntomas de reflujo gastroesofágico, pero causaba efectos secundarios como disfagia y distensión abdominal, por lo que actualmente está contraindicada en la mayoría de los casos 39.
Las funduplicaturas parciales han mostrado mejores resultados a largo plazo y menor incidencia de efectos adversos con respecto a la funduplicatura total 39,40.
Algunos autores han mencionado desventajas en la funduplicatura posterior (Toupet) debido a que la angulación de la unión gastroesofágica puede causar obstrucción del bolo y ruptura del ligamento periesofágico llevando a reflujo, a diferencia del abordaje anterior (Dor) en el que se conserva el ligamento periesofágico, lo que disminuye el riesgo de reflujo.
Una ventaja del abordaje posterior es que permite mantener los puntos de la miotomía separada, evitando la estenosis de la cicatriz de la miotomía y proporcionando mayor control antirreflujo 41,42.
Diversos estudios que comparan las funduplicaturas parciales no han encontrado diferencias significativas en el uso de ambas técnicas.
En una revisión sistemática y metaanálisis se concluyó que estas dos funduplicaturas fueron equivalentes en términos de reflujo postoperatorio, disfagia, tasa de complicaciones y fracaso del tratamiento, aunque hubo una diferencia significativa en la calidad de vida, donde la funduplicatura tipo Toupet fue superior 43.
De acuerdo a la clasificación de Chicago, se ha encontrado que la acalasia tipo 1 tiene tasas de mejoría del 56-85 %, mientras que la tipo 2 tiene las tasas más altas (85-95 %) y la tipo 3 tiene las tasas de mejoría más bajas (29-69 %) 3,44.
La miotomía de Heller se puede realizar por vía robótica, con resultados comparables a los obtenidos con laparoscopia convencional, en términos de tiempo de cirugía, hospitalización y recidiva, pero con incremento de costos por el uso del robot 45.
También se puede realizar por vía abierta mediante un abordaje transtorácico izquierdo o transabdominal46-47; inicialmente esta técnica presentaba una alta incidencia de reflujo gastroesofágico patológico postoperatorio (19-22 %) que mejoró con el abordaje transto-rácico 47-48.
Tratamiento según subtipos de acalasia
No todas estas opciones terapéuticas logran una adecuada respuesta en cada subtipo de acalasia con respecto a la disminución de síntomas, eficacia a corto y largo plazo, presencia de complicaciones y recidiva. La dilatación neumática con balón presenta un adecuado efecto terapéutico en acalasia tipo I y un mejor resultado en la de tipo II, mientras que a 6 y 12 meses la de tipo III no mantiene un adecuado efecto terapéutico 49.
La miotomía de Heller logra una gran efectividad terapéutica en acalasia tipo II, sin embargo, en comparación con la acalasia tipo I, transcurridos 12 y 24 meses de la intervención, no tiene diferencias estadísticamente significativas en la tasa de éxito, por lo cual se encuentra indicado su uso terapéutico en ambos escenarios; en acalasia tipo III no se mantiene una tasa de éxito y pronóstico satisfactorio a los 12 y 24 meses 49,50.
La POEM en acalasia tipo III tiene una tasa de éxito clínico del 94,3 % a los 12 meses, con sintomatología postoperatoria que no representa gravedad.
Este tratamiento logra la mayor tasa de efectividad con respecto a los demás, posiblemente porque permite una miotomía más extensa que la miotomía de Heller 51,52. En la figura 1 se resume el tratamiento según el subtipo de acalasia.
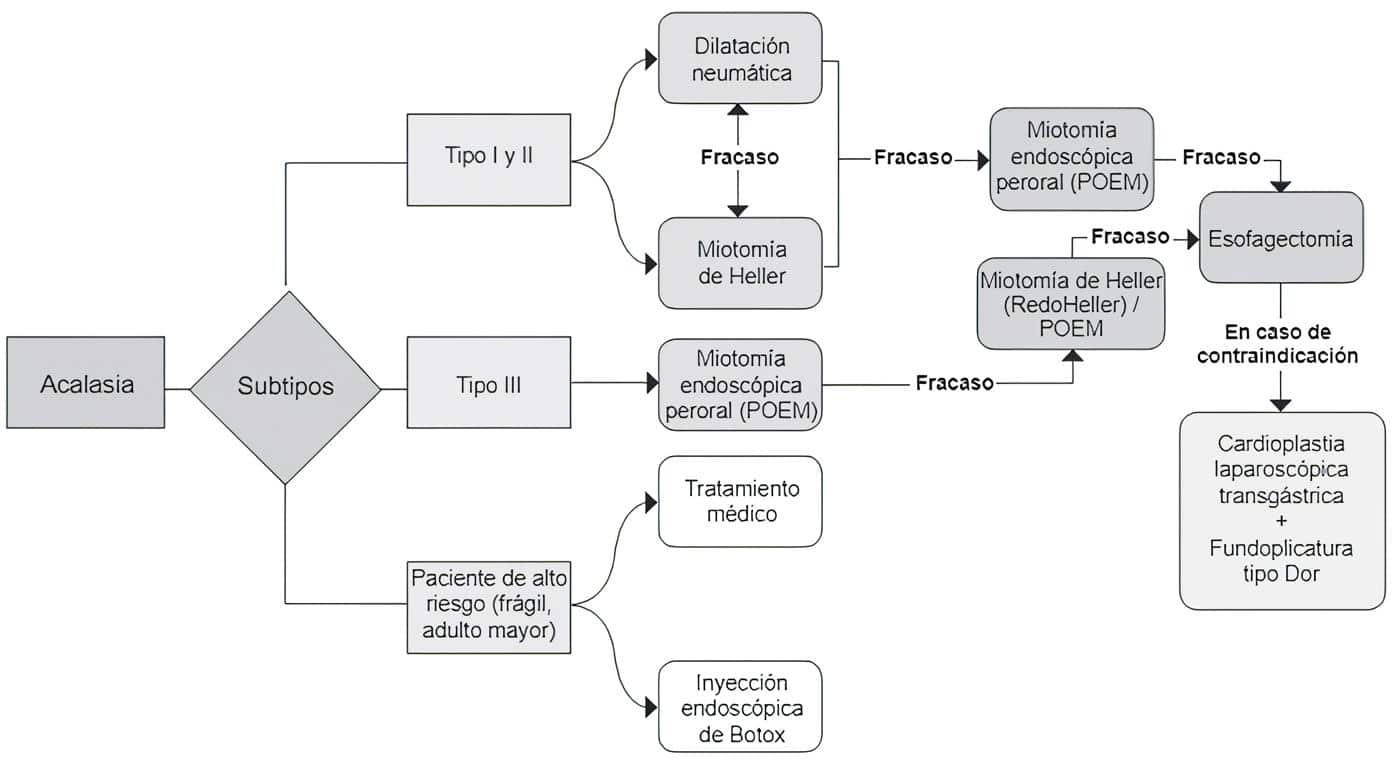
Figura 1. Algoritmo de tratamiento de la acalasia según los subtipos 49-55
Recidivas
Las intervenciones propuestas para cada subtipo de acalasia tienen un amplio efecto terapéutico, sin embargo, los síntomas pueden persistir o reaparecer, indicando una falla terapéutica.
En estos casos, la reintervención con miotomía de Héller y POEM han demostrado una eficacia del 45 % y 63 %, respectivamente. La dilatación neumática no logra una eficacia significativa 53-58.
Pacientes con acalasia que se considere terminal o hayan tenido múltiples intervenciones y en donde la miotomía de Heller se considere inútil, una opción adecuada es la esofagectomía con abordaje híbrido de Ivor-Lewis o mínimamente invasiva.
En casos donde esta se encuentre contraindicada, se puede considerar una cardioplastia laparoscópica transgástrica con grapas, combinada con fundoplicatura tipo Dor 59.
En la tabla 2 se muestra la frecuencia de recidiva en los pacientes con acalasia posterior al manejo por miotomía de Heller, POEM o dilatación neumática a 5 y 10 años 23,60-65.
Tabla 2. Recidiva a 5 y 10 años según el tratamiento de la acalasia 23,60-65

Conclusiones – Acalasia del Esófago
La acalasia tiene una etiología multimodal relacionada con la pérdida de la motilidad esofágica, la cual se manifiesta con disfagia, regurgitación y desnutrición.
Existen valiosas herramientas diagnósticas, como la endoscopia digestiva alta, la radiografía de vías digestivas altas y la manometría esofágica de alta resolución que permite estadificar de acuerdo con la clasificación de Chicago 4.0.
El enfoque terapéutico se debe realizar según el subtipo de acalasia y existen varias opciones que permiten mejorar la calidad de vida de los pacientes y evitar recidivas a largo plazo.
Cumplimiento de normas éticas
Consentimiento informado: Por tratarse de una revisión de la literatura, no se requiere diligenciamiento de consentimiento informado.
Conflictos de interés: los autores declararon no tener ningún conflicto de interés.
Fuentes de financiación: recursos propios de los autores.
Contribución de los autores
Concepción y diseño del estudio: Bryan Nicolás Forero-Vásquez, Jeisón Javier Yopasa-Romero
Adquisición de datos: Bryan Nicolás Forero-Vásquez, Jeisón Javier Yopasa-Romero
Análisis e interpretación de datos: Bryan Nicolás Forero-Vásquez, Jeisón Javier Yopasa-Romero
Redacción del manuscrito: Bryan Nicolás Forero-Vásquez, Jeisón Javier Yopasa-Romero
Revisión crítica: Bryan Nicolás Forero-Vásquez, Jeisón Javier Yopasa-Romero
Referencias – Acalasia del Esófago
1. Khashab MA, Vela MF, Thosani N, Agrawal D, Buxbaum JL, Abbas-Fehmi SM, et al. ASGE guideline on the mana-gement of achalasia. Gastrointest Endosc. 2020;91:213-227.e6. https://doi.org/10.1016/j.gie.2019.04.231
2. Samo S, Carlson DA, Gregory DL, Gawel SH, Pandolfino JE, Kahrilas PJ. Incidence and prevalence of achalasia in central Chicago, 2004–2014, since the widespread use of high-resolution manometry. Clin Gastroenterol Hepatol. 2017;15:366-73. http://dx.doi.org/10.1016/j.cgh.2016.08.030
3. Prieto RG, Prieto JE, Casas F, Ballén H. Acalasia, una visión actual. Rev Colomb Cir. 2019;34:171-8. https://doi.org/10.30944/20117582.111
4. Pandolfino JE, Gawron AJ. Achalasia: A systematic re-view. JAMA. 2015;313:1841-52. http://dx.doi.org/10.1001/jama.2015.2996
5. Furuzawa-Carballeda J, Torres-Landa S, Valdovinos MÁ, Coss-Adame E, Del Campo LAM, Torres-Villalobos G. New insights into the pathophysiology of achalasia and implications for future treatment. World J Gastroen-terol. 2016;22:7892-907. http://dx.doi.org/10.3748/wjg.v22.i35.7892
6. Torresan F, Ioannou A, Azzaroli F, Bazzoli F. Treatment of achalasia in the era of high-resolution manometry. Ann Gastroenterol. 2015;28: 301-8.
7. Newberry C, Vajravelu RK, Pickett-Blakely O, Falk G, Yang YX, Lynch KL. Achalasia patients are at nutritional risk regardless of presenting weight category. Dig Dis Scien. 2018;63:1243-9. https://doi.org/10.1007/s10620-018-4985-8
8. Milito P, Aquilino K, Lazzari V, Boveri S, Munizio N, Ogliari C, et al. The malnutrition universal screening tool can predict malnutrition in patients with esophageal achalasia. Eur J Gastroenterol Hepatol. 2020;32:1135-40. https://doi.org/10.1097/MEG.0000000000001798
Otras Referencias – Acalasia del Esófago
9. Jung DH, Park H. Is gastroesophageal reflux disease and achalasia coincident or not? J Neurogastroenterolog Motil. 2017;23:5-8. https://doi.org/10.5056/jnm16121
10. Pohl D, Tutuian R. Achalasia: an overview of diagnosis and treatment. J Gastrointestin Liver Dis. 2007;16:297-303.
11. Kessing BF, Bredenoord AJ, Smout AJPM. Erroneous diagnosis of gastroesophageal reflux disease in acha-lasia. Clin Gastroenterol Hepatol. 2011;9:1020-4. http://dx.doi.org/10.1016/j.cgh.2011.04.022
12. Khan A, Yadlapati R, Gonlachanvit S, Katzka DA, Park MI, Vaezi M, et al. Chicago Classification update (ver-sion 4.0): Technical review on diagnostic criteria for achalasia. Neurogastroenterolog Motil. 2021;33:1-9. https://doi.org/10.1111/nmo.14182
13. Castillo-León J, Pacheco-Barzallo F, Arias-Garzón W. Tratamiento actual de la acalasia, reporte de un caso y revisión de la literatura. Revista Metro Ciencia. 2016;24:25-30.
14. Kaths JM, Foltys DB, Scheuermann U, Strempel M, Nie-bisch S, Ebert M, et al. Achalasia with megaesophagus and tracheal compression in a young patient: A case report. Int J Surg Case Rep. 2015;14:16-8. http://dx.doi.org/10.1016/j.ijscr.2015.06.020
15. Borráez-Segura BA, Gómez DF, Meza JA, Oliveros R, Pi-nilla RE, Prieto RG, et al. Esofagograma: Imágenes que valen más que mil palabras. Rev Colomb Gastroenterol. 2017;32:258-68. https://doi.org/10.22516/25007440.157
16. Córdoba C, Rodil A, Cisternas D. Novedades acerca de los trastornos motores del esófago tras la reciente cla-sificación de chicago 4.0. Acta Gastroenterol Latinoam. 2021;51:131-42. https://doi.org/10.52787/hoho3531
Bibliografías – Acalasia del Esófago
17. Yadlapati R, Pandolfino JE, Fox MR, Bredenoord AJ, Kahrilas PJ. What is new in Chicago Classification ver-sion 4.0? Neurogastroenterol Motil. 2021;33:e14053. https://doi.org/10.1111/nmo.14053
18. Yadlapati R, Kahrilas PJ, Fox MR, Bredenoord AJ, Gyawa-li PC, Roman S, et al. Esophageal motility disorders on high-resolution manometry: Chicago classification version 4.0. Neurogastroenterol Motil. 2020;33:e14058. https://doi.org/10.1111/nmo.14058
19. Abubakar U, Bashir MB, Kesieme EB. Pseudoachalasia: A review. Niger J Clin Pract. 2016;19:303-7. https://doi.org/10.4103/1119-3077.179275
20. Ponds FA, van Raath MI, Mohamed SMM, Smout AJPM, Bredenoord AJ. Diagnostic features of malignancy-associated pseudoachalasia. Aliment Pharmacol Ther. 2017;45:1449-58. https://doi.org/10.1111/apt.14057
21. Schizas D, Theochari NA, Katsaros I, Mylonas KS, Triantafyllou T, Michalinos A, et al. Pseudoachala-sia: a systematic review of the literature. Esophagus. 2020;17:216-22. https://doi.org/10.1007/s10388-020-00720-1
22. Jovanovic S, Djuric-Stefanovic A, Simić A, Skrobic O, Pes-ko P. Value of multidetector computed tomography in the assessment of achalasia subtypes and detection of pulmonary and thoracic complications. Med Princ Pract. 2019;28:539-46. https://doi.org/10.1159/000501057
23. Licurse MY, Levine MS, Torigian DA, Barbosa EM. Utility of chest CT for differentiating primary and secondary achalasia. Clin Radiol. 2014;69:1019-26. http://dx.doi.org/10.1016/j.crad.2014.05.005
24. Nurczyk K, Patti MG. Surgical management of achalasia. Ann Gastroenterolog Surg. 2020;4:343-51. https://doi.org/10.1002/ags3.12344
Otras Bibliografías – Acalasia del Esófago
25. Paula DMP, Barbosa JP, Barbosa E, Barbosa J. Surgery outcomes and quality of life in achalasia’s treatment. J Laparoendosc Adv Surg Tech. 2020;30:1308-13. https://doi.org/10.1089/lap.2020.0186
26. Crespin OM, Tatum RP, Xiao K, Martin AV, Khandelwal S, Pellegrini CA, et al. The relationship between manometric subtype and outcomes of surgical treatment for patients with achalasia: Achalasia: manometric subtypes. Surg Endosc. 2017;31:5066-75. https://doi.org/10.1007/s00464-017-5570-5
27. Allaix ME, Patti MG. Endoscopic dilatation, Heller myotomy, and peroral endoscopic myotomy: treat-ment modalities for achalasia. Surg Clin North Am. 2015;95:567-78. http://dx.doi.org/10.1016/j.suc.2015.02.009
28. Gunasingam N, Perczuk A, Talbot M, Kaffes A, Saxe-na P. Update on therapeutic interventions for the management of achalasia. J Gastroenterol Hepatol. 2016;31:1422-8. https://doi.org/10.1111/jgh.13408
29. Kahrilas PJ, Pandolfino JE. Treatments for achalasia in 2017: How to choose among them. Curr Opin Gas-troenterolog. 2017;33:270-6. https://doi.org/10.1097/MOG.0000000000000365
30. Nassri A, Ramzan Z. Pharmacotherapy for the management of achalasia: Current status, challenges and future directions. World J Gastrointest Pharmacol Ther. 2015;6:145-55. https://doi.org/10.4292/wjgpt.v6.i4.145
31. Kappelle WFW, Bogte A, Siersema PD. Hydraulic dilation with a shape-measuring balloon in idiopathic achalasia: A feasibility study. Endoscopy. 2015;47:1028-34. http://dx.doi.org/%0A10.1055/s-0034-1392481
32. Estremera-Arévalo F, Albéniz E, Rullán M, Areste I, Iglesias R, Vila JJ. Efficacy of peroral endoscopic myotomy compared with other invasive treatment options for the different esophageal motor disorders. Rev Esp Enf Dig. 2017;109:578-86. https://dx.doi.org/10.17235/reed.2017.4773/2016
Lecturas Recomendadas – Acalasia del Esófago
33. Pasricha PJ, Hawari R, Ahmed I, Chen J, Cotton PB, Hawes HR, et al. Submucosal endoscopic esophageal myotomy: a novel experimental approach for the treat-ment of achalasia. Endoscopy. 2007;39:761-4. https://doi.org/10.1055/s-2007-966764
34. Hungness ES, Jorge JM. Per-Oral Esophageal Myotomy: Is it a safe and durable procedure for achalasia? Adv Surg. 2017;51:193-205. http://dx.doi.org/10.1016/j.yasu.2017.03.015
35. Schlottmann F, Luckett DJ, Fine J, Shaheen NJ, Patti MG. Laparoscopic Heller myotomy versus peroral en-doscopic myotomy (POEM) for achalasia: a systematic review and meta-analysis. Ann Surg. 2018;267:451-60. https://doi.org/10.1097/SLA.0000000000002311
36. Cappell MS, Stavropoulos SN, Friedel D. Updated syste-matic review of achalasia, with a focus on POEM thera-py. Dig Dis Sci. 2020;65:38-65. https://doi.org/10.1007/s10620-019-05784-3
37. Kahrilas PJ. Treating achalasia; more than just flipping a coin. Gut. 2016;65:726-7. https://doi.org/10.1136/gutjnl-2015-311016
38. Inoue H, Ueno A, Shimamura Y, Manolakis A, Sharma A, Kono S, et al. Peroral endoscopic myotomy and fundoplication: A novel NOTES procedure. Endoscopy. 2019;51:161-4. https://doi.org/10.1055/a-0820-2731
39. Hopkins RJ, Irvine T, Jamieson GG, Devitt PG, Watson DI. Long-term follow-up of two randomized trials compa-ring laparoscopic Nissen 360° with anterior 90° partial fundoplication. Br J Surg. 2020;107:56-63. https://doi.org/10.1002/bjs.11327
40. Gotley DC, Frankel AJ. Partial fundoplications (270° Toupet, 90° Dor). Foregut. 2021;1:182-4. https://doi.org/10.1177/26345161211021767
Otras Lecturas Recomendadas – Acalasia del Esófago
41. Håkanson BS, Lundell L, Bylund A, Thorell A. Compa-rison of laparoscopic 270° posterior partial fundo-plication vs total fundoplication for the treatment of gastroesophageal reflux disease: a randomized clinical trial. JAMA Surg. 2019;154:479-86. https://doi.org/10.1001/jamasurg.2019.0047
42. Alimi YR, Esquivel MM, Hawn MT. Laparoscopic Heller myotomy and Toupet fundoplication. World J Surg. 2022;46:1535-41. https://doi.org/10.1007/s00268-022-06471-7
43. Siddaiah-Subramanya M, Yunus RM, Khan S, Memon B, Memon MA. Anterior Dor or posterior Toupet with Heller myotomy for achalasia cardia: A systematic review and meta-analysis. World J Surg. 2019;43:1563-70. https://doi.org/10.1007/s00268-019-04945-9
44. Roque-González R, Martínez-Alfonso MÁ, Jiménez-Ramos R, Anido-Escobar V, Morera-Pérez M. Calidad de vida y evolución clínica después de miotomía de Heller con fundoplicatura de Dor. Rev Cuba Cir. 2019;58:e784.
45. Sollie ZW, Jiwani AZ, Wei B. Robotic Heller myotomy. Mini-invasive Surg. 2020;4:80. https://doi.org/10.20517/2574-1225.2020.81
46. Allaix ME, Patti MG. Heller myotomy for achalasia. From the open to the laparoscopic approach. World J Surg. 2015;39:1603-7. https://doi.org/10.1007/s00268-014-2914-3
47. Vaezi MF, Pandolfino JE, Vela MF. ACG clinical guideline: Diagnosis and management of achalasia. Am J Gastroenterolog. 2013;108:1238-49. https://doi.org/10.1038/ajg.2013.196
48. Fontan AJA, Batista-Neto J, Pontes ACP, Nepomuceno M da C, Muritiba TG, Furtado R da S. Minimally inva-sive laparoscopic esophagectomy vs. transhiatal open esophagectomy in achalasia: A randomized study. Arq Bras Cir Dig. 2018;31:e1382. https://doi.org/10.1590/0102-672020180001e1382
Fuentes Bibliográficas – Acalasia del Esófago
49. Ou YH, Nie XM, Li LF, Wei ZJ, Jiang B. High-resolution manometric subtypes as a predictive factor for the treatment of achalasia: A meta-analysis and systematic review. J Dig Dis. 2016;17:222-35. https://doi.org/10.1111/1751-2980.12327
50. Kroch DA, Grimm IS. POEM for achalasia. Am Surg. 2018;84:489-95. https://doi.org/10.1177/000313481808400419
51. Dreifuss NH, Schlottmann F, Di Corpo M, Patti MG. Com-parison of different treatment modalities and treat-ment algorithm for esophageal achalasia. In: Patti MG, Di Corpo M, Schlottmann F, editors. Foregut surgery. Copenhagen: Springer Cham; 2020. p. 91-102. https://doi.org/10.1007/978-3-030-27592-1_11
52. Schlottmann F, Patti MG. Esophageal achalasia: current diagnosis and treatment. Expert Rev Gastroenterolog Hepatol. 2018;12:711-21. https://doi.org/10.1080/17474124.2018.1481748
53. Patti MG, Fisichella PM. Controversies in management of achalasia. J Gastrointest Surg. 2014;18:1705-9. https://doi.org/10.1007/s11605-014-2556-7
54. Zaninotto G, Bennett C, Boeckxstaens G, Costantini M, Ferguson MK, Pandolfino JE, et al. The 2018 ISDE acha-lasia guidelines. Dis Esophagus. 2018;31 (9). https://doi.org/10.1093/dote/doy071
55. Sanagapalli S, McGuire J, Leong RW, Patel K, Raeburn A, Abdul-Razakq H, et al. The clinical relevance of mano-metric esophagogastric junction outflow obstruction can be determined using rapid drink challenge and solid swallows. Am J Gastronterol. 2021;116:280-8. https://doi.org/10.14309/ajg.0000000000000988
56. Van Hoeij FB, Ponds FA, Werner Y, Sternbach JM, Fockens P, Bastiaansen BA, et al. Management of recurrent symptoms after per-oral endoscopic myotomy in achalasia. Gastrointest Endosc. 2018;87:95-101. http://dx.doi.org/10.1016/j.gie.2017.04.036
Otras Fuentes Bibliográficas – Acalasia del Esófago
57. Patti MG, Allaix ME. Recurrent symptoms after Heller myotomy for achalasia: Evaluation and treatment. World J Surg. 2015;39:1625-30. https://doi.org/10.1007/s00268-014-2901-8
58. Schlottmann F, Andolfi C, Kavitt RT, Konda VJA, Patti MG. Multidisciplinary approach to esophageal achalasia: A single center experience. J Laparoendoscop Adv Sur Tech. 2017;27:358-62. https://doi.org/10.1089/lap.2016.0594
59. Milito P, Siboni S, Lovece A, Andreatta E, Asti E, Bo-navina L. Revisional therapy for recurrent symptoms after Heller myotomy for achalasia. J Gastrointest Surg. 2022;26:64-9. https://doi.org/10.1007/s11605-021-05098-8
60. Kilic A, Schuchert MJ, Pennathur A, Gilbert S, Lan-dreneau RJ, Luketich JD. Long-term outcomes of la-paroscopic Heller myotomy for achalasia. Surgery. 2009;146:826-33. http://dx.doi.org/10.1016/j.surg.2009.06.049
61. Perry KA, Kanji A, Drosdeck JM, Linn JG, Chan A, Mus-carella P, et al. Efficacy and durability of robotic He-ller myotomy for achalasia: patient symptoms and satisfaction at long-term follow-up. Surg Endoscop. 2014;28:3162-7. https://doi.org/10.1007/s00464-014-3576-9
62. Jeansonne LO, White BC, Pilger KE, Shane MD, Zagorski S, Davis SS, et al. Ten-year follow-up of laparoscopic Heller myotomy for achalasia shows durability. Surg Endosc. 2007;21:1498-502. https://doi.org/10.1007/s00464-007-9500-9
63. Zhang WG, Chai NL, Zhai YQ, Linghu EQ, Li HK. Long-term outcomes of peroral endoscopic myotomy in acha-lasia patients with a minimum follow-up of 7 years. Chin Med J. 2020;133:996-8. https://doi.org/10.1097/CM9.0000000000000735
64. Ramchandani M, Nageshwar Reddy D, Nabi Z, Chavan R, Bapaye A, Bhatia S, et al. Management of achalasia cardia: Expert consensus statements. J Gastroenterol Hepatol. 2018;33:1436-44. https://doi.org/10.1111/jgh.14097
65. Hulselmans M, Vanuytsel T, Degreef T, Sifrim D, Coose-mans W, Lerut T, et al. Long-term outcome of pneumatic dilation in the treatment of achalasia. Clin Gastroente-rol Hepatol. 2010;8:30-5. http://dx.doi.org/10.1016/j.cgh.2009.09.020
Autores – Acalasia del Esófago
1 Bryan Nicolás Forero-Vásquez, Jeisón Javier Yopasa-Romero, Estudiante de medicina, Universidad de Ciencias Aplicadas y Ambientales U.D.C.A, Bogotá, D.C., Colombia.
Fecha de recibido: 07/04/2022 – Fecha de aceptación: 16/06/2022 – Publicación en línea: 09/12/2022
Correspondencia: Jeisón Javier Yopasa-Romero, Carrera 156 A # 135-24, Bogotá, D.C., Colombia, Teléfono: +57 3507024054,
Dirección electrónica: yopasa99@gmail.com
Citar como: Forero-Vásquez BN, Yopasa-Romero JJ . Diagnóstico y manejo actual de la acalasia. Rev Colomb Cir. 2023;38:330-8. https://doi.org/10.30944/20117582.2187
Este es un artículo de acceso abierto bajo una Licencia Creative Commons – BY-NC-ND https://creativecommons.org/licenses/by-nc-nd/4.0/deed.es