Las fugas de la anastomosis esofagogástrica representan una complicación determinante en este procedimiento reportada entre el 3,8 y 11,7 % de los pacientes. En nuestro medio se pueden presentar hasta en un 30 % de los pacientes y comúnmente se asocian a mala perfusión del tubo gástrico. La perfusión del conducto generalmente se evalúa de manera subjetiva por el cirujano, basándose en la presencia de sangrado en el muñón gástrico, la vitalidad del tejido y, por supuesto, la palpación del pulso de la arcada proveniente de la arteria gastroepiploica derecha17,18.
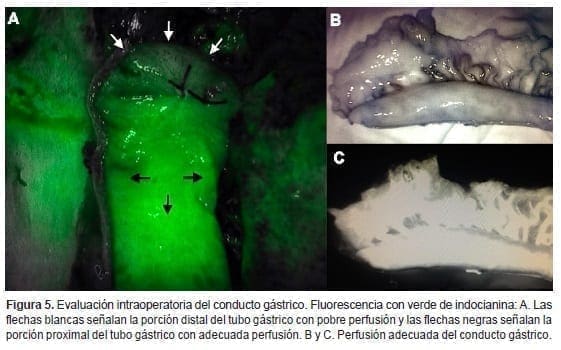
Cuando la tecnología está al alcance de la mano se pueden utilizar herramientas como la fluorescencia con verde de indocianina, que consiste en la administración endovenosa de este colorante y la evaluación del conducto, mediante la aplicación de una luz infrarroja que induce a la fluorescencia de los tejidos. Aunque este tipo de tecnología aún se encuentra a prueba, estudios iniciales reportados por Zehetner et al. han demostrado que podrían disminuir la tasa de fugas anastomóticas después de esofagectomía cuando la anastomosis se realiza en un lugar con mejor perfusión (2 vs. 45%)17,18 (figura 5).
Bordes de sección (margen de resección)
Múltiples factores se asocian a los resultados oncológicos entre ellos los márgenes de sección. En general se prefieren márgenes de sección proximales alrededor de los 10 cm y distales 5 cm19,20.
La distancia puede depender de la técnica utilizada pero los bordes libres de tumor deben ser una prioridad en la cirugía. Por su parte, Barbour et al. definen como adecuado un borde proximal in situ de aproximadamente 5 cm, Marriette et al. no encontraron infiltración tumoral cuando el borde proximal excedía los 7 cm, mientras que Miller et al. consideran un margen seguro de 12 cm. Adicionalmente, Tam et al. reportan una tasa de 20 % de recurrencia con márgenes menores de 5 cm, de 8 % con márgenes de entre 5 y 10 cm y de 0 % con márgenes mayores de 10 cm19,20.
Por otro lado, el margen distal representa menores dificultades. Di Musto y Orringer mostraron que con márgenes de 4 a 6 cm se consigue una tasa de márgenes microscópicamente negativos en un 98 % de los casos. Así mismo, el margen circunferencial puede afectar la sobrevida de los pacientes indicando un promedio de 12 meses en grupos con margen circunferencial comprometido19,20.
Piloroplastia
El uso o no de piloroplastia continúa siendo otro de los temas en discusión. La esofagectomía resulta en una inevitable lesión vagal con dismotilidad y denervación pilórica que genera alteraciones en el vaciamiento gástrico y se asocia a síntomas como plenitud, náuseas y vómito con posible riesgo de aspiración. En contraparte, la piloroplastia es un área potencial de fugas, con incremento del tiempo operatorio y predisposición al reflujo biliar. A pesar de los pro y los contra, aún no existe una diferencia significativa clara, pero se reportan menos fugas anastomóticas, complicaciones pulmonares y reducción de la estasis gástrica cuando se emplea drenaje pilórico después de la esofagectomía21, 22.
Cuidados posoperatorios
Al finalizar el procedimiento, el paciente es llevado a la unidad de cuidados intensivos para monitorización; se procura la extubación posoperatoria inmediata temprana; el catéter peridural desempeña un papel importante dado que permite el control acertado del dolor. Se promueve la movilización temprana y el retiro de sondas, así como el inicio de la nutrición enteral y la ingesta rápida (previa realización de estudios contrastados –opcional-). Los tubos de tórax son una queja frecuente de los pacientes debido al dolor que producen y la limitación de la movilidad. Estos pueden ser removidos si no se sospechan fugas con drenajes de hasta 200 ml23,24.
En caso de sospechar fugas anastomóticas, se practican estudios radiológicos con contraste y tomografía axial computarizada, para evaluar su tamaño, así como pruebas de laboratorio que alerten sobre la presencia de signos de reacción inflamatoria sistémica23,24.
Los programas ERAS (Enhanced Recovery After Surgery), ampliamente descritos en múltiples procedimientos, son actividades encaminadas a disminuir la estancia hospitalaria así como la morbimortalidad. Inician en el preoperatorio (consejería, carga de carbohidratos, ayuno mínimo, nutrición preoperatoria, entrenamiento de músculos inspiratorios y optimización de hemoglobina), intraoperatoria (analgesia preventiva, cirugía de mínima invasión y fluido-terapia adecuada) y postoperatoria (nutrición temprana, retiro rápido de sondas y tubos, analgesia, profilaxis antitrombótica y movilización), actividades que buscan mejorar la evolución de pacientes y obtener resultados tempranos prometedores aun en espera de resultados conclusivos23,24.
Conclusiones
La esofagectomía mínimamente invasiva es un procedimiento técnicamente difícil, que requiere entrenamiento, habilidad y experiencia, asociado a un cuidado pre- y posoperatorio preciso. Las múltiples variaciones en el procedimiento así como la mezcla de procedimientos abiertos con procedimientos vídeo-asistidos hacen de esta una técnica con mayor aceptación, factible y segura, con resultados oncológicos adecuados si se implementa de manera correcta.
La técnica quirúrgica debe elegirse con base en la preferencia del cirujano, sus fortalezas y habilidades.
Referencias
1. Wullstein C, Ro-Papanikolaou HY, Klingebiel C, Ers¬ahin K, Carolus R. Minimally Invasive Techniques and Hybrid Operations for Esophageal Cancer. Viszeral¬medizin. 2015;31:331-6. doi: 10.1159/000438661.
2. Bonavina L, Asti E, Sironi A, Bernardi D, Aiolfi A. Hybrid and total minimally invasive esophagectomy: how I do it. J Thorac Dis. 2017;9(Suppl.8):S761-S72. doi: 10.21037/jtd.2017.06.55.
3. Putora PM, Bedenne L, Budach W, Eisterer W, Van Der Gaast A, Jäger R, et al. Oesophageal cancer: Exploring controversies overview of experts’ opinions of Austria, Germany, France, Netherlands and Switzerland. Radiat Oncol. 2015;10:116. doi: 10.1186/s13014-015-0418-4.
4. Hagens ER, Van Berge Henegouwen MI, Cuesta MA, Gisbertz SS. The extent of lymphadenectomy in esoph¬ageal resection for cancer should be standardized. J Thorac Dis 2017;9(Suppl.8):S713-S23. doi: 10.21037/ jtd.2017.07.42
5. Fujita H, Sueyoshi S, Tanaka T, Fujii T, Toh U, Mine T, et al. Optimal lymphadenectomy for squamous cell carcinoma in the thoracic esophagus: comparing the short- and long-term outcome among the four types of lymphadenectomy. World J Surg. 2003;27:571-9.
6. Cuesta MA, van der Wielen N, Weijs TJ, Bleys RL, Gis¬bertz SS, van Duijvendijk P, et al. Surgical anatomy of the supracarinal esophagus based on a minimally invasive approach: vascular and nervous anatomy and technical steps to resection and lymphadenectomy. Surg Endosc. 2017;31:1863-70. doi: 10.1007/s00464-016- 5186-1.
7. Rizk NP, Ishwaran H, Rice TW, Chen LQ, Schipper PH, Kesler KA, et al. Optimum lymphadenectomy for esophageal cancer. Ann Surg. 2010;251:46-50. doi: 10.1097/SLA.0b013e3181b2f6ee.
8. Talsma AK, Ong CA, Liu X, van Hagen P, Van Lanschot JJ, Tilanus HW, et al. Location of lymph node involve-ment in patients with esophageal adenocarcinoma pre¬dicts survival. World J Surg. 2014;38:106-13. doi: 10.1007/ s00268-013-2236-x.
9. Osugi H, Takemura M, Higashino M, Takada N, Lee S, Ueno M, et al. Learning curve of video-assisted thoraco-scopic esophagectomy and extensive lymphadenecto¬my for squamous cell cancer of the thoracic esophagus and results. Surg Endosc. 2003;17:515-9.
10. Guo W, Zou YB, Ma Z, Niu HJ, Jiang YG, Zhao YP, et al. One surgeon’s learning curve for video-assisted thoracoscopic esophagectomy for esophageal can¬cer with the patient in lateral position: how many cases are needed to reach competence? Surg Endosc. 2013;27:1346-52. doi: 10.1007/s00464-012-2614-8.
11. Ramage L, Deguara J, Davies A, Hamouda A, Tsigritis K, Forshaw M, et al. Gastric tube necrosis following minimally invasive oesophagectomy is a learning curve issue. Ann R Coll Surg Engl. 2013;95:329-34. doi: 10.130 8/003588413X13629960045751.
12. Borráez AM, Páez J, Borráez OA, Borráez BA. Esofagec¬tomía híbrida: esofagectomía transtorácica con ascenso gástrico laparoscópico, cómo lo hacemos. Rev Colomb Cir. 2016;31:91-7.
13. Allaix ME, Long JM, Patti MG. Hybrid Ivor Lewis Esophagectomy for esophageal cancer. J Laparoendosc Adv Surg Tech A. 2016;26:763-7.
14. Law Simon YK. Esophagogastrectomy for carcinoma of the esophagus. In: Mastery of surgery. Sixth edition. Philadelphia: Lippincott Williams Wilkins; 2012. p. 886- 902.
15. Law S. Minimally invasive techniques for oesopha¬geal cancer surgery. Best Pract Res Clin Gastroenterol. 2006;20:925–40.
16. Straatman J, van der Wielen N, Nieuwenhuijzen GA, Rosman C, Roig J, Scheepers JJ, et al. Techniques and short-term outcomes for total minimally invasive Ivor Lewis esophageal resection in distal esophageal and gastroesophageal junction cancers: Pooled data from six European centers. Surg Endosc. 2017;31:119-126. doi: 10.1007/s00464-016-4938-2.
17. Schlottmann F, Patti MG. Evaluation of gastric conduit perfusion during esophagectomy with indocyanine green fluorescence imaging. J Laparoendosc Adv Surg Tech A. 2017;27:1305-08. doi: 10.1089/lap.2017.0359.
18. Zehetner J, DeMeester SR, Alicuben ET, Oh DS, Lip¬ham JC, Hagen JA, et al. Intraoperative assessment of perfusion of the gastric graft and correlation with anastomotic leaks after esophagectomy. Ann Surg. 2015;262:74-8. doi: 10.1097/SLA.0000000000000811.
19. Migliore M, Rassl D, Criscione A. Longitudinal and cir¬cumferential resection margin in adenocarcinoma of distal esophagus and cardia. Future Oncol. 2014;10:891- 901. doi: 10.2217/fon.13.241.
20. Allum WH, Bonavina L, Cassivi SD, Cuesta MA, Dong ZM, Felix VN, et al. Surgical treatments for esophageal cancers. Ann N Y Acad Sci. 2014;1325:242-68. doi: 10.1111/ nyas.12533.
21. Arya S, Markar SR, Karthikesalingam A, Hanna GB. The impact of pyloric drainage on clinical outcome following esophagectomy: a systematic review. Dis Esophagus. 2015;28:326-35. doi: 10.1111/dote.12191 .
22. Gaur P, Swanson SJ. Should we continue to drain the pylorus in patients undergoing an esophagectomy? Dis Esophagus. 2014;27:568-73. doi: 10.1111/dote.12035.
23. Findlay JM, Gillies RS, Millo J, Sgromo B, Marshall RE, Maynard ND. Enhanced recovery for esophagec¬tomy: a systematic review and evidence-based guidelines. Ann Surg. 2014;259:413-31. doi: 10.1097/ SLA.0000000000000349.
24. Findlay JM, Tustian E, Millo J, Klucniks A, Sgromo B, Marshall RE, et al. The effect of formalizing enhanced recovery after esophagectomy with a protocol. Dis Esophagus. 2015;28:567-73. doi: 10.1111/dote.12234.
