En este momento se investigan varios frentes de desarrollo para el sistema; se busca hacer que su utilización sea aun más intuitiva, más sencilla y dotada de herramientas que garanticen una mayor precisión con la mayor seguridad para el paciente. Estos frentes son:
· Proveer realidad aumentada (RA) para CMI robótica: RA es la mezcla o superposición de objetos sintéticos o artificiales con situaciones reales, en tiempo real. Este proyecto busca dotar al sistema con un programa que permita integrar una imagen reconstruida en 3D de TAC o resonancia magnética preoperatoria con el campo operatorio, representado por la imagen en 3D producida por el videoendoscopio del robot. En otras palabras, el cirujano podrá ver la lesión y los puntos de referencia anatómicos superpuestos al campo operatorio y decidir con más precisión, por ejemplo, márgenes de resección.
Tres propiedades de tal superposición deben ser perfeccionadas para hacer posible la inclusión de la RA: calibración, registro y seguimiento (Tracking). La calibración determina las propiedades de la cámara empleada para ver el campo operatorio, propiedades que deben conocerse para crear la escena simulada sin distorsionar la imagen.
El siguiente paso es alinear con absoluta precisión los objetos virtuales con su contraparte real en las imágenes de vídeo. Este emparejamiento de elementos reales y virtuales se llama registro.
Una vez lograda esta mezcla, se debe tener en cuenta la dinámica del procedimiento quirúrgico.
Cualquier deformación de los tejidos, especialmente por contacto con los instrumentos, debe ser rastreada. De esta forma las imágenes virtuales pueden ser actualizadas según la evolución de la operación y retransmitidas al visor del cirujano con la imagen real del campo quirúrgico.
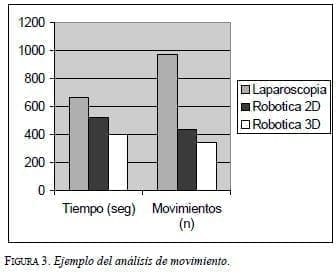
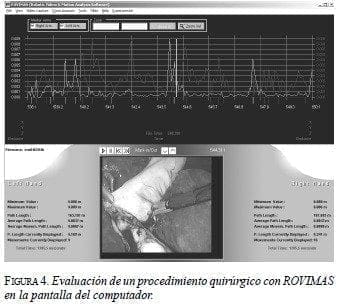
· Debido a la exitosa aplicación del análisis de movimiento con el ICSAD (11, 16), se decidió aplicar el mismo concepto para la evaluación de destrezas quirúrgicas en el sistema da Vinci. Para ello fue necesario crear un programa de computador completamente nuevo, ROVIMAS (12). Éste pue puede calcular y presentar datos de los movimientos de las manos, incluyendo tiempo, la distancia total recorrida, el número de movimientos hechos, la dirección de las manos, la velocidad y otros más. Un desarrollo adicional reciente es que al filmar en cinta electrónica de vídeo el procedimiento, el análisis de movimientos se puede sincronizar con la imagen, y en consecuencia, datos de un momento específico de la cirugía o tarea que se esté realizando pueden ser analizados (figura 3). Esto facilita una evaluación subjetiva y objetiva muy completa, permitiendo analizar errores o movimientos de experto con mediciones de destreza (17) (figura 4).
Actualmente se realiza una investigación más profunda del análisis de movimiento para mejorar su sensibilidad, mediante el uso de modelos estocásticos tratando de discriminar el nivel de experiencia y destreza en procedimientos reales y complejos. Los casos de cirugía cardiovascular que hoy se practican son los más firmes candidatos. Se emplean los Modelos Ocultos de Markov usados ampliamente en áreas de reconocimiento de patrones como en la voz o la escritura. En el caso del sistema da Vinci se utilizan para reconocer diferentes pasos de un procedimiento, distintos niveles de pericia y para modelar movimientos quirúrgicos.
· Desde el punto de vista de retroalimentación táctil del robot al cirujano se trabajan dos aspectos:
háptica y restricción activa.
Háptica se denomina desde el punto de vista técnico al estudio de cómo combinar el sentido del tacto con un mundo generado por computador.
Para nuestros propósitos, se trata de la información que el cirujano obtendría en su interacción con los controles del robot, información a su vez generada originalmente en el campo operatorio.
En la actualidad, el excelente desempeño del sistema depende principalmente de la información obtenida por su visión en 3D, su manejo intuitivo y el entrenamiento del cirujano. Existe aún un vacío de datos que puede ser llenado con la retroalimentación háptica. Esto permitiría al cirujano “sentir” cuando toca un tejido o graduar la presión con que sujeta o retrae una estructura.
Como hoy no es posible poner sensores en la punta de los instrumentos, esto se hace con métodos indirectos, tomando mediciones de expertos en diferentes tejidos para establecer parámetros que permitan graduar las sensaciones que se transmiten al cirujano.
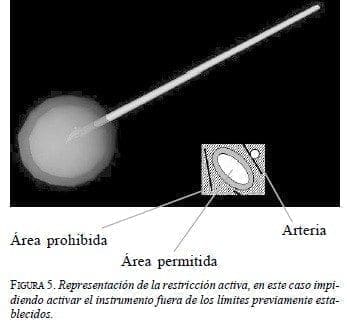
La restricción activa, desarrollada por B. Davies en el Imperial College (18, 19), consiste en establecer límites a los movimientos de los instrumentos, creando áreas prohibidas (figura 5). En un caso, la restricción impide al instrumento salirse de un área demarcada; por ejemplo, el electrocauterio no podría cortar sobre una región donde de antemano se sabe que hay una arteria mayor. Lo opuesto también es posible, el instrumento puede funcionar solamente por fuera de un área establecida, como cuando se reseca un tumor tratando de mantener márgenes adecuadas.
La transición de una región a otra, es decir, permitir el paso del instrumento cerca del área prohibida cuando no se está utilizando, para entrar o salir, se hace con mecanismos especiales que evitan inestabilidad en el sistema (20).
Discusión
La CR, en la cual el cirujano controla un sistema telemanipulador que amplifica las destrezas del cirujano para permitir la práctica de un procedimiento de alta complejidad con gran precisión, es una realidad.
Así lo evidencian las cifras de la experiencia clínica de St Mary’s (tabla 1) y de otros centros donde inclusive se han creado programas de entrenamiento (21). Estas experiencias muestran que el da Vinci permite un aprendizaje rápido de técnicas complejas, los cirujanos se adaptan fácilmente al sistema y su desempeño es mejor que con la CMI convencional en procedimientos complejos y en el laboratorio. De hecho, estas afirmaciones son a la inversa en la CMI.
La CMI ha demostrado ampliamente sus beneficios para el paciente. Menor invasión, menor riesgo de infección, recuperación y retorno a las activida- des normales más rápido (22, 23). Todo ello a un costo igual o menor a la cirugía abierta. Ha sido tal su éxito, que inclusive ha modificado la actitud de los clínicos hacia los tratamientos quirúrgicos de patologías como el reflujo gastroesofágico (24, 25). Sin embargo, el cirujano tiene que adaptarse a perder su visión estereoscópica, confiar lo que sus ojos ven a un ayudante y emplear instrumentos con un diseño ergonómico inapropiado, colocados en puntos fijos y con un movimiento paradójico por el efecto de fulcro (26). Como consecuencia, el cirujano pierde su destreza habitual y su habilidad para resolver situaciones difíciles o inesperadas (27), lo cual puede ir en detrimento del paciente. Tal vez es por eso que, a pesar de que casi todos los hospitales de alto nivel de complejidad poseen una torre de laparoscopia, a nivel mundial son relativamente pocos los cirujanos dedicados a la CMI avanzada.
Los sistemas telemanipuladores tienen con características que superan estas desventajas; tres aspectos se destacan sobre los demás. El primero es el uso de instrumentos articulados. La punta o parte funcional del instrumento cuenta con “carpo”. De esta forma, todos los movimientos efectuados por el cirujano en la consola son reproducidos por el brazo robótico y el instrumento en su extremo. Esto es particularmente útil en maniobras complejas como la sutura intracorpórea, y absolutamente indispensable, por ejemplo, en un puente coronario, que era imposible realizar en forma endoscópica antes de la aparición del da Vinci. Dos ventajas adicionales son la abolición del temblor, es decir, que los movimientos no intencionales son filtrados y, por otro lado, los movimientos se producen a una escala de 10 a 1: si el cirujano mueve su mano 5 cm, la punta del instrumento se mueve 0,5 cm. Todo esto hace que los movimientos sean más precisos, se pierda menos tiempo y haya menos riesgos de complicaciones.
Esto quedó demostrado en el experimento que comparó la CMI con la CR, donde se vio que el número de errores y el desempeño en el análisis de movimiento mejoraron sensiblemente aun con visión 2D, lo que da valor por sí mismo al diseño de los instrumentos.
El segundo aspecto es la visión en 3D, que a diferencia de los incómodos y costosos aparatos que se fijaban a la cabeza del cirujano y producían una imagen de poca calidad (28), el instrumento binocular del da Vinci crea dos imágenes independientes, una para cada ojo. Esto es posible porque el endoscopio tiene dos lentes en su interior, cada uno con fuente de luz y cámara propias. Cada imagen es proyectada en el visor por un monitor para cada ojo, creando así una visión realmente estereoscópica. Este es un elemento indispensable del robot, ya que la única fuente de información para el cirujano en CR son sus ojos (3, 29). El tacto, tan útil en cirugía abierta, no existe debido a la separación entre el cirujano y el campo operatorio. El segundo estudio (comparación 2D/3D) y marginalmente el aluaron la importancia de la visión en 3D. Todas las pruebas realizadas demuestran su superioridad sobre la 2D, controlando todas las variables, ya que para todo el experimento se utilizó el propio da Vinci cambiando el tipo de visión (5). La destreza mejoró hasta 25% como lo muestra la reducción en el tiempo y los movimientos realizados, y la precisión aumentó de tal forma que llevó casi a cero el número de errores.
Varios estudios han demostrado que los cirujanos expertos en CMI se benefician poco o nada de la visión en 3D, porque aprenden a compensar la falta de ésta con otras claves y signos en el campo operatorio. El trabajo de Mueller y colaboradores sugiere que ni siquiera los novicios se benefician de la 3D (30). Sin embargo, las pruebas que emplearon no parecen ser apropiadas para evaluar objetivamente este asunto.
En los experimentos expuestos en este escrito hubo una ventaja significativa de la visión en 3D sobre la 2D en cirujanos con y sin experiencia.
El tercer aspecto combina los dos anteriores y es el manejo intuitivo del robot. Al sentarse frente a la consola, tomar los controles y mirar por el visor, la persona tiene al frente los instrumentos, en una posición similar a la que encontraría en cirugía abierta (eje ojos-mano-instrumento). Al mover sus manos, parece que los instrumentos fueran una extensión de éstas, ya que duplican los movimientos con gran precisión. El visor tiene una almohadilla sobre la cual descansa la frente y de esta forma el cirujano se siente inmerso en el campo quirúrgico. Con un pedal controla la cámara (movimientos, foco, profundidad), de manera que recupera la independencia en cuanto a lo que sus ojos ven, ya no depende de un ayudante.
Esto tiene el beneficio de hacer la CMI accesible a los cirujanos en entrenamiento, disminuye el tiempo de aprendizaje de la técnica laparoscópica y presumiblemente la duración de la curva de aprendizaje.
La ventaja para los cirujanos expertos en CMI es que el aumento de la precisión les permite realizar procedimientos muy difíciles o imposibles para la CMI, como los puentes coronarios.
El primer estudio mencionado mostró como después de sólo cinco sesiones con el robot realizando una prueba muy compleja (anastomosis intestinal), todos los cirujanos, tanto experimentados como no experimentados, mejoraron la calidad de su desempeño (OSATS), disminuyeron el tiempo requerido en más de la tercera parte y necesitaron casi 40% menos movimientos. En una encuesta cuyos datos no han sido publicados, todos los participantes se adaptaron rápidamente al sistema, lo encontraron cómodo (considerando que algunos tardaron más de una hora en las primeras pruebas) y no experimentaron molestias. Además, fue posible construir una curva de aprendizaje con todos los parámetros, que se considera inconclusa por el número de mediciones realizadas.
Una etapa fascinante es la del desarrollo de nuevas propiedades para el sistema. La disponibilidad de la RA permitiría realizar CR guiada por imágenes diagnósticas en tiempo real, haciendo que ciertos procedimientos sean más precisos, ya que se conocería la posición exacta de la lesión que se va a tratar y de estructuras adyacentes que deban preservarse.
Esto también facilitará la preparación de cirujanos en entrenamiento, permitiéndoles efectuar procedimientos simulados sobre estas imágenes. El ROVIMAS permitirá analizar y guardar la información del desempeño de expertos en diferentes procedimientos no sólo para evaluar a otros cirujanos, sino para que cirujanos en entrenamiento puedan aprender de expertos duplicando sus patrones de movimientos. La seguridad en el empleo del sistema se verá incrementada con el uso de la háptica. El cirujano tendrá conciencia de la presión o tracción que ejerce sobre un tejido y podrá regularla para evitar el trauma de éste. En conclusión, la CR tiene, con los modelos existentes y la tecnología disponible, su campo principalmente en los casos complejos que requieren gran habilidad y mucha precisión, o que se practican en campos quirúrgicos limitados. Ejemplos pueden ser los puentes coronarios, remplazo de válvulas cardiacas, prostatectomía radical, adrenalectomía. Sin embargo, se ha visto cómo casi cualquier procedimiento de CMI puede ser realizado con CR con buenos resultados y sin compromiso del paciente.
Abstract
Hypothesis: The da Vinci™ Surgical System allows surgeons to overcome the limitations imposed by minimally invasive surgery (MIS) in terms of dexterity, operative field control and ergonomy. The studies included evaluate the learning curve, 3-D vision and motion analysis to reveal the system’s advantages over MIS and to establish performance assessment methods.
Methods: system employed: da Vinci™ Surgical System. Three comparative experiments with 11 to 13 surgeons performing different tasks looking at: learning curve comparing experienced and non-experienced surgeons, advantages of 3D over 2D vision, and advantages of robotic surgery over Minimally Invasive Surgery (MIS). Assessment: measurement of surgeon’s performance by means of a global scale for skills (OSATS) and errors count, with blind scoring by experts. Additionally, motion analysis software for MIS (ICSAD) and robotic surgery (ROVIMAS), both developed by the Department and previously validated in other studies. Statistic calculations: SPSS 10,0™ software. P<0,05.
Results: The learning curve rendered an OSATS score of 18 for the first attempt and 26 for the fifth (p=0,02, Cronbah alpha: 0.894). Motion analysis showed reduction in number of movements and path length (p=0,01). Comparing robotic surgery with 3-D vision vs. MIS rendered a 40% reduction in time taken (p=0,001) and 70% reduction in path length (0,008), with 93% less skill-related errors. 3-D vision was proved to be superior to 2-D in several trials.
Conclusion: “Endowrist” instruments, tremor abolition, motion scaling and 3-D vision of the da Vinci™ Surgical System enhance the surgeon’s dexterity and performance in robotic assisted MIS. Key words: Robotics, video-assisted surgery, learning, task performance and analysis.
Referencias
1. MUNZ Y, MOORTHY K, KUNDCHADKAR R, HERNÁNDEZ JD, MARTIN S, DARZI A, ROCKALL T. Robotic assisted rectopexy. Am J Surg 2003; 187: 88-92.
2. HERNÁNDEZ J, BANN SD, MUNZ Y, MOORTHY K, MARTIN S, DOSIS A, BELLO F, et al. Qualitative and quantitative analysis of the learning curve of a simulated surgical task on the da Vinci system. Surg Endosc 2004; 18 (3): 372-378.
3. MUNZ Y, HERNÁNDEZ J, BANN SD, BELLO F, DOSIS A, MARTIN S, MOORTHY K, et al. The use of motion analysis in determining the advantages of 3D vision in surgical performance with the da Vinci telemanipulation robotic system. Surg Endosc 2003; 17:S59.
4. MOORTHY K, MUNZ Y, DOSIS A, HERNÁNDEZ J, BANN SD, MARTIN S, BELLO F, et al. Dexterity enhancement with robotic surgery. Surg Endosc 2004; 18: 790-795.
5. MUNZ Y, HERNÁNDEZ J, BANN SD, BELLO F, DOSIS A, MARTIN S, MOORTHY K, et al. The advantages of 3D visualization in surgical performance with the da Vinci telemanipulation robotic system. J Soc Laparoendoscopic Surg 2002; 6: 264.
6. HERNÁNDEZ J, BANN SD, MUNZ Y, MOORTHY K, MARTIN S, DOSIS A, BELLO F, et al. The learning curve of a simulated surgical task using the da Vinci telemanipulator system. Br J Surg 2002; 89 (Suppl 1): 17-18.
7. FALK V, AUTSCHBACH R, KRAKOR R, WALTHER T, DIEGELER A, ONNASCH JF, CHITWOOD WR, et al. Computer-enhanced mitral valve surgery: Toward a total endoscopic procedure. Semin Thorac Cardiovasc Surg 1999; 11: 244-249.
8. WATSON DI, BAIGRIE RJ, JAMIESON GG. A learning curve for laparoscopic fundoplication: definable, avoidable, or a waste of time? Ann Surg 1996; 224: 198-203.
9. PATKIN M, ISABEL L. Ergonomics, engineering and surgery of endosurgical dissection. J Royal Coll Surg Edinburgh 1995; 40: 120-132.
10. TAFFINDER N, SMITH S, MAIR J, et al. Can a computer measure surgical precision? Reliability, validity and feasibility of the ICSAD. Surg Endosc 1999; 13: 81.
11. DATTA V, MACKAY S, MANDALIA M, DARZI A. The use of electromagnetic motion tracking analysis to objectively measure open surgical skill in the laboratory-based model. J Am Coll Surg 2001; 193: 479-485.
12. DOSIS A, BELLO F, ROCKALL T, MUNZ Y, MOORTHY K, MARTIN S, DARZI A, “ROVIMAS: A software package for assessing surgical skills using the da Vinci telemanipulator system”, Itab 2003: 4Th International Ieee Embs Special Topic Conference on Information Technology Applications in Biomedicine, Conference Proceedings – New Solutions for New Challenges, 2003; 326-329.
13. FAULKNER H, REGEHR G, MARTÍN J, REZNICK R. Validation of an objective structured assessment of technical skill for surgical residents. Acad Med 1996; 71: 785-790.
14. MARTIN JA, REGEHR G, REZNICK R, MACRAE H, MUMAGHAN J, HUTCHINSON C, BROWN M. Objective structured assessment of technical skills (OSATS) for surgical residents. Br J Surg 1997; 84: 273-278.
15. MACRAE H, REGEHR G, LEADBETTER W, REZNICK RK. A comprehensive examination for senior surgical residents. Am J Surg 2000; 179: 190-193.
16. DATTA VK, MACKAY SM, CHANG AA, DARZI AW. Electromagnetic motion analysis in the assessment of surgical technical skill. British J Surg 2001; 88: 79.
17. DOSIS A, BELLO F, MOORTHY K, MUNZ Y, GILLIES D, DARZI A. Real-time synchronization of kinematic and video data for the comprehensive assessment of surgical skills. 98, 82-88. 2004. Newport Beach, Los Ángeles, California, Stud Health tech Inform. Medicine Meets Virtual Reality 12 (MMVR). Westwood JD, et al. 14-1-2004. Conference Proceedings.
18. DAVIES BL, HARRIS SJ, LIN SL, HIBBERD RD, MIDDLETON R, COBB JC. Active compliance in robotic surgery- the use of force control as dynamic constraint. Proc Instn Mech Eng 1997; 214 (H): 285- 292.
19. DAVIES B. Robotic devices in surgery. Min Invas Ther & Allied Technology 2003; 12: 5-13.
20. BORELLI J, BELLO F, RODRÍGUEZ Y, BENA F, DAVIES B, An active constraint environment for minimally invasive heart surgery: early experience of a cutting operation. Medicine Meets Virtual Reality 12 CA, USA, IOS Press, ISSN: 0926-9630, 2003.
21. CHITWOOD RW, NIFONG LW, CHAPMAN WHH, FELGER JE, BAILEY BM, BALLINT T, MENDLESON KG, et al. Robotic surgical training in an academic institution. Ann Surg 2001; 234: 475-486.
22. WILLIAMS LF, CHAPMAN WC, BONAU RA, MCGEE EC, BOYD RW, JACOBS JK. Comparison of laparoscopic cholecystectomy with open cholecystectomy in a single center. Am J Surg 1993; 165: 459-465.
23. ZUNDEL N, HERNÁNDEZ J. Profilaxis antibiótica en cirugía laparoscópica. Rev Colomb Cir 1998; 13: 159-162.
24. HINDER RA, PERDIKIS G, KLINGER PJ, DE VAULT KR. The surgical option for gastroesophageal reflux disease. Am J Med 1997; 103: 144S-148S.
25. WATSON DI, BAIGRIE RJ, JAMIESON GG. A learning curve for laparoscopic fundoplication: definable, avoidable, or a waste of time? Ann Surg 1996; 224: 198-203.
26. SMITH CD, FARRELL TM, MCNATT SS, METREVEL RM. Assessing laparoscopic manipulative skills. Am J Surg 2001; 181:547-550.
27. CADIERE GB, HIMPENS J, GERMAY O, IZIZAW R, DEGUELDRE M, VANDROMME J, CAPELLUTO E, et al. Feasibility of robotic laparoscopic surgery: 146 cases. World J Surg 2001; 25: 1467- 1477.
28. CHEAH WK, LENZI JE, SO J, DONG F, KUM CK, GOH P. Evaluation of a head-mounted display (HMD) in the performance of a simulated laparoscopic task. Surg Endosc 2001;15: 990-991.
29. SCHURR MO, KUNERT W, AREZZO A, BUESS G. The role and future of endoscopic imaging systems. Endoscopy 1999; 31: 557-562.
30. MUELLER MD, CAMARTIN C, DREHER E, HANGGI W. Three-dimensional laparoscopy. Gadget or progress? A randomized trial on the efficacy of three-dimensional laparoscopy. Surg Endosc 1999; 13: 469-472.
Correspondencia:
JUAN DAVID HERNÁNDEZ RESTREPO, MD.
juandah@uniandes.edu.co
Bogotá, D.C., Colombia
