La definición de la edad en la cual se debe iniciar el tamizaje para la detección temprana del cáncer de seno debe basarse en parte en la incidencia del cáncer según la edad. En los Estados Unidos las probabilidades de desarrollar cáncer invasivo según los intervalos de edad son: 20-29, 30-39, 40-49, 50-59, 60-69 y 70-79 años, 0,04, 0,04, 1,49, 2,54, 3,43 y 4,31 por 100 mujeres, respectivamente, y son equivalentes a un 13% de riesgo en el curso de la vida, o sea, aproximadamente, una de cada ocho mujeres (26). Nótese el importante incremento del riesgo relativo al pasar de llos 30 a los 40 años.
En Latinoamérica, varios países, siguiendo las recomendaciones americanas para el tamizaje de seno, han demostrado la utilidad de la mamografía en mujeres mayores de 40 años en estudios con seguimiento postquirúrgico hasta por cinco años (27), a través de correlación patológica mamográfica (28,29), análisis costo-beneficio (30) o con estudios randomizados; algunos incluyen 1.700 mujeres con más de 2.500 mamografías donde se muestra detección de lesiones no palpables hasta en un 1.4% con detección de cáncer en estadios tempranos (31). Aunque no hay cifras definitivas, un estudio chileno con 15.864 mujeres ha calculado que la mamografía tiene una sensibilidad de 79%, especificidad de 90% y eficacia de 84% (32).
Casi 34% de todos los años de expectativa de vida perdidos por cáncer de seno se deben a la aparición de cáncer entre los 40-49 años (33). Es por ello que podría ser razonable, para muchas mujeres sin factores de riesgo, comenzar el tamizaje mamográfico a los 40 años.
Aunque se han identificado numerosos factores de riesgo para cáncer de seno, cerca del 75% de todas la mujeres que lo padecen no tienen un factor de riesgo mayor identificable (34). Razón por la cual, el grupo de edad de 40 años o más no debe ser excluido del tamizaje anual. Algunos autores recomiendan que aquellas mujeres con riesgo alto (antecedente de cáncer familiar de presentación premenopáusica) deberían comenzar el tamizaje anual antes de los 40 años (35,36), pero falta evidencia médica que respalde esta práctica.
Otros Aspectos
Es prudente insistir en el auto-examen de seno mensual y en el examen físico anual, puesto que algunos tumores pueden ser hallados sólo por estos métodos, especialmente en regiones donde se carece de facilidades de mamografía de tamizaje; por lo tanto acudir a un examen médico y mamográfico tiene mejores posibilidades ante el desarrollo de un cáncer mamario, no sólo desde el punto de vista estético, sino por la supervivencia más prolongada del cáncer temprano no palpable(37).
La variabilidad en la calidad técnica y la interpretación de la mamografía están en constante cambio. La ACR continúa el desarrollo de métodos para mejorar y monitorear la calidad técnica de la mamografía de tamizaje y la exactitud de la interpretación; además, elaboró el manual de garantía de calidad en los servicios de mamografía (38). Actualmente la Asociación Colombiana de Radiología en colaboración con el Ministerio de Salud diseñan las guías de calidad para su implementación en el territorio nacional y para el Sistema General de Seguridad Social en Salud. Sin embargo, existen centros radiológicos como el de la Fundación Santa Fe de Bogotá, que ya instauró el programa que cumple con los criterios de calidad recomendados por la ACR.
Tamizaje en Mujeres Mayores
No hay evidencia suficiente para recomendar la mamografía de tamizaje en mujeres mayores de 69 años. Las mejores candidatas para detener el tamizaje son mujeres mayores con co-morbilidades significativas, estado funcional pobre, densidad ósea baja, poco interés en el cuidado preventivo o aversión a aceptar el potencial daño del tamizaje (grado de recomendación C, basado en estudios retrospectivos de cohortes) (39).
Es ampliamente recomendado el tamizaje mamográfico para mujeres hasta los 70 años. Sin embargo, su papel en mujeres mayores aún no es claro, a pesar de que la expectativa de vida sea larga. Pacientes con tres o más co-morbilidades (hipertensión, diabetes, artritis, infartos del miocardio, accidentes cerebro-vasculares, enfermedad respiratoria u otros cánceres) tienen una probabilidad 20 veces mayor de morir por una causa diferente del cáncer de seno dentro de tres años (40). Aunque la mitad de todos los cánceres son diagnosticados en mujeres mayores de 65 años, el tamizaje en estas posee algún riesgo. Por cada 1000 mujeres en tamizaje mayores de 70 años, 81 mamografías van a mostrar anormalidad, requiriendo 79 pruebas de seguimiento y 26 biopsias para detectar once carcinomas (41). El cuadro se puede complicar por la posibilidad de que estos carcinomas suelen ser menos agresivos. Los carcinomas pueden crecer más lentamente en esta edad, y el 25% de todos los tumores en mujeres mayores son carcinomas ductales in-situ, los cuales es improbable que causen morbilidad o muerte dentro del lapso de vida restante (42).
Desafortunadamente, los estudios aleatorizados de tamizaje mamográfico han involucrado pocas mujeres entre los 70 y 74 años y ninguna mayor de 74.
Tamizaje en Mujeres Menores de 40 Años de Alto Riesgo
La tendencia actual en cuanto a la evaluación de pacientes muy jóvenes de alto riesgo (historia familiar de cáncer o mutaciones en los genes BRCA1 y BRCA 2 o con enfermedad de Hodgkin) está cambiando.
Los antecedentes familiares de cáncer mamario conllevan aproximadamente el doble de riesgo que en una mujer normal; por lo general el cáncer se presenta mucho antes de lo esperado en pacientes jóvenes que tienen familiares con historia de cáncer mamario, así como en el grupo de mujeres con cambios genéticos en el BRCA. Estos cambios aumentan el riesgo de cáncer mamario hasta un 54% en mujeres de 60 años y en 85% en mujeres de 70 años.
Aunque no hay estudios definitivos de la eficacia del tamizaje en estas pacientes, muchos expertos creen necesaria una mamografía además del examen físico en mujeres en el rango de 25 a 35 años, según el Cancer Genetics Studies Consortium (43).
Un caso excepcional son las pacientes con enfermedad de Hodgking, cuyo el riesgo de cáncer de seno en el rango de 10 a 30 años, es casi de 360 veces con respecto a mujeres sanas y la mamografía es útil para detectar lesiones no palpables, con una sensibilidad hasta del 90%. La recomendación actual es empezar tamizaje ocho a diez años después de iniciada la radioterapia (44).
Proyecciones Estándar para el Tamizaje
Las proyecciones estándar para el tamizaje son la mediolateral oblicua (MLO) y la craneocaudal (CC) (45).
La proyección MLO ofrece la mejor oportunidad para mostrar todo el tejido mamario en una única proyección. Puesto que el seno se ubica sobre el músculo pectoral mayor, la imagen debe incluir una gran cantidad de tejido. Se puede incorporar una mayor cantidad de músculo si el brazo en C de la unidad de mamografía es rotado en forma tal que el “bucky” sea paralelo al plano del músculo pectoral.
Los criterios de una buena proyección MLO incluyen la visualización de una gran cantidad de músculo, el cual debe mostrar una convexidad anterior. Siempre que sea posible, el músculo visualizado debe extenderse hasta o por debajo de la línea posterior del pezón en el plano oblicuo (figura 1). Este criterio se puede lograr en más del 80% de las proyecciones. En la proyección MLO, la línea posterior del pezón se traza en un ángulo aproximadamente perpendicular al músculo, extendiéndose desde el pezón hasta el músculo pectoral o el borde de la placa, cualquiera que sea primero.
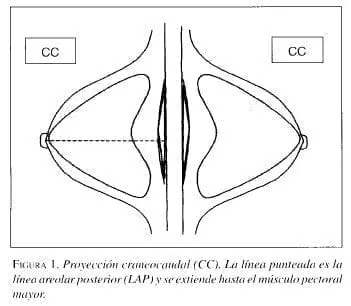
También es deseable visualizar grasa por detrás de todo el tejido fibroglandular; si este tejido se extiende hasta el borde de la placa, debe asumirse que se está excluyendo algo del mismo.
Ocasionalmente se pueden ver pliegues de la piel en la axila y no causa problemas en la interpretación, pero si esto ocurre sobre el tejido mamario, puede ocultar lesiones o simular anormalidades.
La proyección CC puede considerarse un complemento de la MLO. Un objetivo importante de la proyección CC es incluir en la imagen todo el tejido posteromedial, el cual es visualizado de forma incompleta en la MLO. Otra ventaja de la proyección CC, es que el seno puede ser comprimido en forma más efectiva, lo que resulta en una mejor visualización de las estructuras y lesiones de éste.
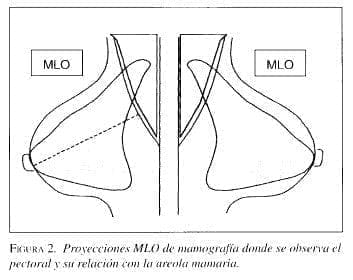
La medida más adecuada para saber si la proyección CC incluye suficiente cantidad de tejido posterior es la longitud de la línea posterior del pezón en esta proyección (figura 2), comparada con la medida en la proyección MLO. Una buena regla general es que la longitud de la línea posterior del pezón en la proyección CC debe estar a menos de 1 cm de diferencia con la medida realizada en la MLO. En la proyección CC la línea posterior del pezón se traza directamente desde la región posterior del pezón hasta el borde de la placa o el músculo pectoral, si éste se logra ver. La visualización del músculo pectoral en la proyección CC se considera generalmente deseable, pero sólo se logra en un 30% de las proyecciones adecuadamente realizadas; sin embargo, la no-visualización del músculo no indica una proyección insuficiente.
La Controversia
Con casi un total de medio millón de mujeres incluidas en diez estudios randomizados y cerca de otro medio millón de mujeres tamizadas desde 1960, el beneficio de la mamografía en la detección del cáncer de seno parecía bien documentado (46). Sin embargo, con la aparición de una conclusión de un artículo de salud pública del Nordic Cochrane Centre en Lancet: “El tamizaje de cáncer de seno con mamografía es injustificado” (47), se inició el controvertido análisis de la mamografía bajo la perspectiva de la medicina basada en la evidencia.
Las dudas iniciales sobre el tamizaje aparecieron en Suecia en 1999, donde cinco estudios en un meta-análisis habían demostrado una disminución en la mortalidad esperada para el cáncer del 29% en mujeres entre 50 y 69 años; sin embargo, los resultados epidemiológicos reunidos desde 1985 sólo mostraron una disminución de 0,8%. Basados en este hecho, Peter Gozsche y Ole Olsen (48), con unos criterios discutibles de inclusión, analizaron cinco estudios, encontrando que sólo dos de ellos no presentaban sesgos y fueron utilizados para el análisis (Tabla 1).
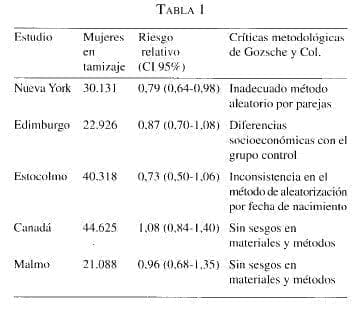
En el mencionado estudio, de manera errónea y utilizando sólo dos meta-análisis, calcularon el riesgo relativo para cáncer de seno en 1,0 (0,84-1,27 CI 95%), y concluyeron que la mamografía no es útil como método de tamizaje y aumenta el número de procedimientos innecesariamente (riesgo relativo de 1,23 para mastec-tomía radical).
Las Consecuencias y el Estado Actual
Numerosas fallas han sido encontradas en el artículo de Gozsche y cols, desde su aparición, como lo argumenta la Cochrane Collaboration Library and Cochrane Breast Cancer Group publicadas en la misma revista (49).
Dentro de esta polémica, tal vez lo más importante fue la injustificada exclusión de más de 94.000 mujeres por razones de poca descripción en las publicaciones o fallas en la recolección de datos, lo que constituye el mayor sesgo estadístico del estudio.
Un segundo argumento en contra de los autores suecos fue la no-medición de la tasa caso-fatalidad en pacientes con intervención temprana, cálculo que constituye la base fundamental de un estudio de tamizaje, puesto que son las pacientes con detección temprana del cáncer las que pueden tener mejor pronóstico a largo plazo. Aunque el análisis inicial no mostró cambios en la mortalidad a cinco años, cohortes calculados estudios recientes después de seis a siete años sí muestran una reducción significativa de la tasa de mortalidad por neoplasia de seno en mujeres de 55 años (50).
También es importante destacar que según el protocolo descrito en el Cochrane Review –número 3 de 2001–, la calidad de los estudios se ha estandarizado en cuatro categorías: alto, medio, pobre y defectuoso. Ninguno de los estudios de tamizaje para detección del cáncer de seno tuvieron la más alta calificación(calidad media: Malmo y Canadá; calidad pobre: Estocolmo; calidad defectuosa: Nueva York y Edimburgo). Es obvio que en estas condiciones no se puede llegar a conclusiones definitivas.
Uno de los factores que tampoco permite una conclusión categórica del valor de la mamografía es la heterogeneidad del comportamiento del carcinoma de seno, que es independiente para cada población. En el polémico articulo la razón para excluir estudios significativos fue la aparente falla en la recolección de los datos de las pacientes, por lo cual fue necesario promediar valores de riesgo relativo de estudios no comparables, ya que tenían diferentes intervalos y duración en la frecuencia de tamizaje y en el seguimiento Canadá, seguimiento por once años y Malmo por tres (51).
Por otra parte, a pesar de los numerosos estudios randomizados ya mencionados, ha sido particularmente difícil establecer con claridad cuándo iniciar y terminar el tamizaje para la detección de cáncer de seno con respecto a la edad. Aunque algunos estudios han mostrado un incremento en el crecimiento del carcinoma en pacientes entre 40-49 años que en mujeres entre 50-59, han existido dos criterios en contra del tamizaje en el grupo de pacientes de 40 años, como son: la mayor densidad del parénquima fibroglandular, que podría oscurecer una lesión sospechosa, y que la mortalidad de una lesión tumoral es independiente de su detección temprana debido a que en la mayoría de los casos, según algunos autores, ya existe diseminación en el momento del hallazgo (52). En la actualidad, se han aceptado dos criterios con mayor fuerza que los mencionados anteriormente en favor de la mamografía en mujeres menores de 40 años, los cuales hacen referencia a los estudios de costo-efectividad aceptados como una fuente significativa de ahorro en intervenciones complejas (53) y a la detección temprana de pequeñas lesiones con carcinoma ductal in-situ (CDIS), lesión que se presenta con una incidencia hasta de 15% en el cáncer de seno (54).
Conclusión
En las ultimas décadas no ha existido una técnica por imágenes diferente a la mamografía que hubiese sido evaluada con tanto rigor. La mayoría de los experimentos clínicos ha demostrado el beneficio de la mamografía en el diagnóstico temprano del carcinoma de seno (especialmente en mujeres mayores de 50 años); además, existen otros beneficios del diagnóstico temprano que no han sido estudiados y evaluados en forma amplia (cirugía conservadora, quimioterapia menos agresiva, ganglio centinela) que tendrían un valor importante en el desenlace y calidad de vida de las pacientes.
A pesar de nuevos y controvertidos estudios que cuestionan la utilidad de la mamografía como técnica de tamizaje, ésta continúa siendo el método por excelencia en la detección temprana del carcinoma de seno
Abstract
Mammography in breast cancer screening seeks to diminish mortality by this malignant disease. However, there is controversy regarding its real impact on mortality, age at which screening should be initiated, an intervals at which mammography should be performed in asymptomatic women. In depth analysis of published information must be undertaken for the benefit of physicians, especially those that take care of female patients. This revision pretends to summarize the principal recommendations for the use of mammography in breast screening according to the best medical evidence. We also discuss the direct and indirect benefits of mammographic screening, as well as its potential risks and disadvantages.
Referencias
1. Patiño JF, Espinosa H. Mamografía en la práctica clínica. Trib Médica (Colombia) 1990; 81: 206.
2. Patiño JF, La mamografía en la práctica quirúrgica. En: Lecciones de Cirugía. Editorial Médica Panamericana, Buenos Aires, Bogotá, 2001.
3. Feig SA, D’Orsi CJ, Hendrick RE, et al. American Collage of Radiology Guidelines for Breast Cancer Screening. AJR 1998; 171: 29-33.
4. The ACR and screening mamography: consensus and continued commitment. ARC Bull June 1997; 53: 4-9.
5. Shapiro S. Screening: assessment of current studies. Cancer 1994; 74: 231-238.
6. Hendrick RE, Smith RA, Rutledge JH III, Smart CR. Benefit of screening mammography in women age 40-49: a new meta-analysis of randomized controlled trials. Monogr Natl Cancer Inst 1997; 22: 87-92.
7. Smart CR, Hendrick RE, Rutledge JH III, Smith RA. Benefit of mammography screening in women ages 40-49: current evidence from randomized controlled trials. Cancer 1995; 75: 1619-1626.
8. Smith RA. The epidemiology of breast cancer. RSNA Categorical Course in breast imaging syllabus 1995, pp 7-20.
9. Page DL, Dupont WD. Premalignat conditions and markers of elevated risk in the breast and their management. Surg Clin North Am 1990; 70: 831-851.
10. Larsson LG, Andersson I, Bjurstam N, et al. Updated overview of the Swedish randomized trials on breast cancer screening with mammography: age groups 40-90 at randomization. Monogr Natl Cancer Inst 1997; 22: 57-62.
11. Anderson I, Janzon L. Reduced breast cancer mortality in women under 50: update results from the Malmo mammographic screening program. Monogr Natl Cancer Inst 1997; 22: 63-68.
12. Bjurstam N, Bjorneld L, Duffy SW, et al. The Gothenburg breast screening trial: first results on mortality, incidence, and mode of detection for women ages 39-49 years at randomization. Cancer 1997; 80: 2091-2099.
13. Sickles EA, Ominsky SH, Sollitto RA, Galvin HB, Monticciolo DL. Medical audit of a rapid through put mammography screening practice: methodology and results of 27,114 examinations. Radiology 1990; 175: 323-327.
14. Linver MN, Paster SB. Mammography outcomes in a practice setting by age: prognostic factors, sensitivity, and positive biopsy rate. Monogr Natl Cancer Inst 1997; 22: 113-118.
15. Kopans DB, Moore RH, McCarty KA, et al. Positive predictive value of breast biopsy performed as result of mammography: there is no abrupt change at age 50 years. Radiology 1996; 200: 357-360.
16. Joensu H, Klemi PJ, Tuominen J, Rasomen O, Parvinen I. Breast cancer found at screening and previous detection by women themselves (Letter). Lancet 1992; 339: 315.
17. Feig SA, Hendrick RE. Radiation risk from screening mammography of women aged 40-49 years. Monogr Natl Cancer Inst 1997; 22: 119-24.
18. Feig SA, Estimation of currently attainable benefit from mammographic screening of women aged 40-49 years. Cancer 1995; 75: 2412-2419.
19. Duffy SW, Day NE, Tabar L, Chen H-H, Smith TC. Markov models of breast tumor progression: some age-specific results. Monogr Natl Cancer Inst 1997; 22: 93-98.
20. Tabar L, Fagerberg G, Chen H-H, et al. Efficacy of breast cancer screening by age: new results from the Swedish two-county trial. Cancer 1995; 75: 2507-2517.
21. Gardenosa G, Eklung GW. Screening mammography in women 40-49 years old. AJR 1995;164: 1104-1106
22. Moskowitz M. Breast cancer: age-specific growth rates and screening strategies. Radiology 1986; 161: 37-41.
23. Tabar L, Fagerberg G, Day NE, Holmberg L. What is the optimum interval between screening examinations? An analysis based on the latest results of the Swedish two-county breast cancer screening trial. Br J Cancer 1987; 55: 547-551.
24. Screening for breast cancer. Recommendations and rationale. Rockville, MD: Agency for Healthcare Research and Quality; February, 2002.
25. Peto R, Boreman J, Clarke M, Davies C, Beral V. UK and USA breast cancer deaths down 25% in year 2000 at ages 20-69. Lancet 2000; 355: 1822.
26. Ries LAG, Kosary CL, Hankey BF, et al. SEER cancer statistics review, 1973-1994. Bethesda, MD: National Cancer Institute, 1997:124. NIH publication 97-2789.
27. Montesinos, Manuel R; Falco, Jorge E; Mezzadri, et al Valor de los métodos de seguimiento en el postoperatorio del cáncer de mama. Rev. Argent. Cir; 61(1/2): 30-6, jul.-ago. 1991.
28. Souza, Aurélio Zecchi de; Hegg, Roberto; Shu, Siok Bwee T. Correlaçäo entre diagnóstico clínico, mamográfico e anatomo patológico em patologia mamária: análise de 1251 casos J. bras. ginecol; 95(10): 459-61, out. 1985.
29. Martínez Corta, Virginia. Rol de la anatomía patológica en el estudio del cáncer mamario.Rev. sanid. def. ac. (Santiago de Chile); 6(1): 17-25, ene.-mar. 1989.
30. Montesinos, Manuel R; Falco, Jorge E; Curuchet, H. et al. Análisis costo/beneficio de la mamografía en el postoperatorio del cáncer de mama. Rev. Argent. Cir; 60(3/4): 116-8, mar.-abr. 1991.
31. Solé, Claudio; Fernández, Consuelo; Acevedo, Juan Carlos; et al. Programa de screening y tratamiento de cáncer de mama. Rev. chil. obstet. ginecol; 55(2): 92-6, 1990.
32. Pierart Pacheco, Jorge. Eficacia de los métodos de diagnóstico en patología mamaria. Rev. chil. cir; 45(3): 282-7, jun. 1993.
33. Shapiro S, Venet W, Strax, Venet L. Periodic screening for breast cancer: the health insurance plan project and its sequelae. Baltimore: Johns Hopkins Univ Press, 1988:13.
34. Seidman H, Stellman S, Mushinski MH. A different perspective on breast cancer risk factors: some implications of the nonattributable risk. CA Cancer J Clin 1982; 32: 301-313.
35. Vogel VG, Yeomans A, Higginbotham E. Clinical management of women at increased risk for breast cancer. Breast Cancer Res Treat 1993; 28: 195-210.
36. Burke W, Daly M, Garber J, et al. For the Cancer Genetics Studies Consortium. Recommendations for follow-up care of individuals with an inherited predisposition to cancer: II. BRCA 1 and BRCA 2. JAMA 1997; 277: 997-1003.
37. Robinson, David S; Love, Neil; Schwade, James G. Pruebas de tamizaje en el diagnostico precoz del cancer mamario.Trib. méd. (Bogotá); 81(4): 187-90, abr. 1990.
38. Standars 2000-2001, Reston, VA: American College of Radiology; 2000.
39. Kopans D future directions for breast imaging. Course No. 625. Uptade Course in Diagnostic Radiology Physics: Physical aspects of breast imaging-Current and future Considerations. RSNA Supplement of Radiology 221; 86 Nov 2001.
40. Zhang Y, Kiel DP, Kreger BE et al. Bone mass and the risk of breast cancer among postmenopausal women. N Engl J Med 1997; 336:611-7.
41. Satariano WA, Ragland DR. The effect of comorbidity on 3 year survival of women with primary breast cancer. Ann Intern Med 1994; 120: 104-10.
42. Welch HG. Diagnostic testing following screening mammography in the elderly. JNCI 1998; 90: 1389-92.
43. Kerlikowske KM, Grady D, Barclay J, et al. Positive predictive value of screening mammography by age and family history of breast cancer. JAMA 1993; 270: 2444-50.
44. Dersaw DD, Yahalom J, Petrek JA. Breast carcinoma in women previously treated for Hodgkin disease: radiologic evaluation. Radiology 1992; 184-421-3.
45. Bassett LW. Quality determinants of mammography: clinical image evaluation RSNA Categorical Course in Breast Imaging, 1995; 57-67.
46. SHAPIROS, VENET, STRAXP et al. lOto 14 years effect of screeningin hreast cancel’ mortality. J Nat Cancel’ lnst 1982; 69: 349-55.
47. GOTZSCIIE P, OLSEN O. Is screening for hreast cancel’ with mammography justifiable? Lancet 2000: 355; 129-133.
48. GOTZSCHE P, OLSEN O. Cochrane review on screening breast cancel’ with mammography. Lancet 2001; 358: 1340-41.
49. HORTON R. Screening mammography-an overview revisited. Lancet 2001; 358: 1284-1285.
50. WELCH HG, SCHWARTZLM, WOLOSIIIN S. Are increasing 5-year survival rates evidence of success against cancer’) JAMA 2000; 283: 2975-8.
51. MOSKOWITZ M. Breast cancer: age-specific growth rates and screening strategies. Radiology 1986; 18: 1137-41.
52. HUYNH PT. JAROLlMEK AM, DAYE S. The false-negative mammogram. Radiographics 1998; 18: 1137-54.
53. TENGS TO, ADAMs M, PUSKIN JS et al. Five-hundred life-saving interventions and their cost-ffectiveness. Risk Anal 1995; 15: 369-90.
54. SAKORAFASGH, TSIOTOU AG. Ductal carcinoma in situ (DCIS) of the breast: evolving perspectives. Cancel’ Treat Rev 2000;
26: 103-25.
Correspondencia:
MIGUEL ANGARITA, MD
Correo electrónico: migueangarita@hotmaiLcom
Bogotá, Colombia
El tiempo de latencia es el tiempo máximo entre la posible detección temprana en el tamizaje y el hallazgo clínico en ausencia de tamizaje. El “lead time” es el tiempo promedio entre la detección real en el tamizaje y el momento en que una lesión detectada tenga una alta probabilidad de curación, mayor del 90%.
