M.A. López y colaboradores de la Pontificia Uni-versidad Javeriana, Bogotá, realizaron mediciones de la longitud del esófago en 60 hombres y 60 mujeres colombianos, con los siguientes resultados de longitud:
- 1: desde la arcada dental hasta la estrechez cricofaríngea, 14-19 (17) cm en hombres y 12-18 (15) en mujeres.
- 2: desde la arcada dental hasta la unión gastroesofágica, 35-46 (39,7) cm en hombres y 29-42 (36,7) cm en mujeres.
- 3: desde la estrechez cricofaríngea hasta la línea Z, 19-29 (23) cm en hombres y 14-25 (21) cm en mujeres.
El esófago normal está recubierto de epitelio escamoso estratificado, el cual se extiende hasta la unión gastroesofágica, que es una línea imaginaria donde hace contacto con el epitelio columnar gástrico en la interfaz que se denomina línea Z. O sea, que la línea Z es la unión escamo-columnar.
Streets y Crookes (2001) relatan cómo, hasta hace relativamente poco tiempo se pensó que la “mucosa cardial”, de glándulas mucosas, era un hallazgo normal en la región anatómica denominada cardias.
Esto se originó en el trabajo de J. Hayward (1961), en el cual describió un segmento de 1-2 cm del esófago distal normal recubierto de epitelio columnar. Hoy muchos consideran, no sin controversia, que el epitelio columnar o sea, la “mucosa cardial”, es un fenómeno adquirido, producido por RGE (Chandrasoma et al 2000). El asunto se discute más adelante.
Con anterioridad a 1976 se denominó esófago de Barrett a cualquier segmento de mucosa columnar visible a la endoscopia, sin tener en cuenta el tipo histológico.
Actualmente se denomina esófago de Barrett aquel que presenta las células caliciformes que caracterizan la metaplasia intestinal. La ausencia de células caliciformes descarta el Barrett (Streets et al 2001. Winstein & Ippoliti 1996).
Paull y colaboradores, del Peter Bent Brigham Hospital de Boston, en su artículo clásico publicado en 1976 en el New England Journal of Medicine, describen tres tipos histológicos de epitelio columnar:
1) el tipo gástrico fúndico, de glándulas con células mucosas, parietales y células principales;
2) el tipo de epitelio de unión (junctional type), de glándulas mucosas, con ausencia de células principales y parietales;
3) un tipo de epitelio especializado de superficie vellosa, con células mucosas y células caliciformes que tiñen con alcian blue y ausencia de células principales y parietales.
En el cuadro siguiente los autores de Boston resumen sus hallazgos (Panel et al 1976):
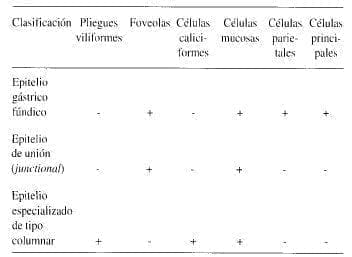
El tipo del epitelio de unión (junctional) es el que con frecuencia se denomina mucosa cardial en la literatura.
Pera y Pera (2002), de Barcelona, España, resumen así los tres tipos de epitelio que recubren un esófago de Barrett con base en el trabajo de Antonioli y Wang (1997):
• Epitelio gástrico-fúndico, el cual semeja el epitelio el epitelio atrófico del fundus; contiene células mucosas en la superficie y células principales y parietales en las partes más profundas de las glándulas.
• Epitelio de unión (junctional, transicional), que es histológicamente similar al del cardias normal. Las foveolas están recubiertas por epitelio columnar mucosecretor.
• Epitelio especializado, el fenotipo histológico histológico más común, virtualmente patognomónico del esófago de Barrett. Es idéntico a la mucosa intestinal y su superficie vellosa se encuentra cubierta por células columnares y caliciformes (goblet cells). Comúnmente se lo conoce como metaplasia intestinal incompleta y es propenso a la transfor-mación maligna.
Hoy se considera la presencia de las células caliciformes (goblet cells) por lo menos en una de las biopsias del esófago distal como un requerimiento para el diagnóstico de esófago de Barrett (Weintein & Ippoliti 1996). Estas células e colorean azul con hematoxilina-eosina-alcian blue.
Pera y Pera (2002) revisan el origen, la patogénesis, del epitelio de Barrett y relatan que estudios recientes sugieren que las poblaciones celulares progenitoras, que se presume residen en la capa basal del epitelio escamoso y en el epitelio de los ductos de las glándulas esofágicas, pueden diferenciarse hacia un fenotipo glandular que conduce a la aparición del epitelio columnar en el esófago distal.
Otros estudios también dan soporte a la hipótesis que el epitelio del cardias puede preceder a la aparición de la metaplasia intestinal especializada.
“No queda claro si el epitelio de tipo cardial del esófago de Barrett se origina en epitelio escamoso o a partir de la migración de epitelio cardial nativo de la unión gastroesofágica hacia el esófago distal”.
Tytgat y Hameeteman (1992) señalan que el esófago de Barrett, o sea, el epitelio columnar que aparece en el esófago distal, debe ser considerado como un mosaico de células, glándulas y tipos arquitectónicos, que exhiben grados variables de maduración hacia el epitelio de tipo gástrico e intestinal.
El término displasia se refiere a una inequívoca alteración neoplásica del epitelio. La displasia puede variar desde un grado leve hasta un alto grado. La displasia de alto grado consiste en cambios neoplásicos celulares y/o de la arquitectura, pero dentro del epitelio columnar, sin invadir la membrana basal.
Aunque la displasia ha sido identificada en todos los tipos de epitelio, en la vasta mayoría se encuentra en el epitelio intestinal especializado (Thompson et al 1983).
Actualmente, como se describe enseguida, se define el esófago de Barrett como la presencia de metaplasia intestinal especializada, que es la alteración verdaderamente premaligna.
Los términos cardias, cardias gástrico y mucosa cardial han dado lugar a confusión, que viene desde la aseveración de J. Hayward de que el esófago distal estaba recubierto por un epitelio de glándulas mucosas.
En un estudio de la histología normal de la región cardial, o sea, de la unión gastroesofágica, realizado en autopsias, Chandrasoma et al (2000) de la University of Southern California, Los Angeles.
Clasificaron los tipos de epitelio que ocurren en la región así.
1. Epitelio escamoso estratificado.
2. Mucosa oxíntica pura, caracterizada por glándulas compuestas por células parietales y principales.
3. Mucosa cardial pura caracterizada por glándulas compuestas sólo por células mucosas.
4. Mucosa oxínticocardial caracterizada por glándulas que contiene una mezcla de células mucosas y parietales.
5. Mucosa intestinal caracterizada por células calici-formes.
El estudio de Chandrasoma et al (2000) vino a contradecir la creencia, planteada por J. Hayward en 1961, sobre el epitelio columnar “normal” en la porción más distal del esófago: mucosa cardial pura estuvo ausente en 56% de los casos, y todos los pacientes exhibieron mucosa oxínticomucosa con glándulas que contienen una mezcla de células mucosas y parietales.
Mucosa cardial y oxinticocardial se halló apenas en parte de la circunferencia de la unión gastroesofágica en 50% de los casos.
La máxima longitud de la mucosa cardial más la mucosa oxinticocardial fue 0,5 cm en el 76% de los pacientes.
Los hallazgos anteriores plantean serias dudas sobre la creencia de que la mucosa cardial y la mucosa oxinticocardial sean componentes normales de la región de la unión gastroesofágica.
O sea, la evidencia indica que la mucosa cardial es una condición adquirida, lo cual se apoya en el hecho de que cuando está presente, siempre se asocia con signos histológicos de infla-mación.
Hoy se plantean dos posibles agentes causales de la “carditis”: el Helicobacter pylori (Goldblum et al 2002) y el reflujo gastroesofágico (Streets & Crookes 2001).
En una segunda publicación de 2001, Chandrasoma & Wickramasinghe revisan en forma comprensiva la patología de la ERGE y del esófago de Barrett e insisten en la comprensión del proceso.
“El primer paso en la comprensión es fundamental:
En el año 2001, la enfermedad por reflujo no es puramente una enfermedad del epitelio escamoso inducida por ácido. Más bien debe reconocérsela como una enfermedad inducida por algún elemento carcinogénico presente en el material gástrico que refluye, el cual actúa sobre un epitelio glandular en el esófago”.
En esta segunda publicación de Chandrasoma & Wickramasinghe (2001) se resume bien su clasificación del epitelio de la ERGE y del Barrett en cuatro tipos:
1) mucosa cardial, que se define por la presencia de glándulas que contienen células mucosas sin células parietales;
2) mucosa oxíntica, que se define por la presencia de glándulas que contienen células parietales y principales, con ausencia de células mucosas;
3) mucosa oxíntico-cardial, que se define por glándulas que contienen una mezcla de células mucosas y células parietales;
4) mucosa de metaplasia intestinal (intestinal metaplásica), que se define por la presencia de células caliciformes.
Las anteriores definiciones son idénticas a las de Paull et al en su clásico estudio de la histología del esófago recubierto de epitelio columnar, excepto por el uso de los términos cardial e intestinal. en vez de epitelio de unión (junctional) y especializado que usan Paull et al.
J.J. Thompson y asociados, de la Universidad de Pensilvania, Filadelfia, realizaron un estudio en especímenes de esofagogastrectomía utilizando microscopía electrónica y otras técnicas.
Los autores concluyen que la metaplasia de Barrett es una mezcla compleja y aleatoria de diferentes tipos celulares, que exhibe variables grados de maduración, cuya presencia, caracterizada por una arquitectura vellosa de células caliciformes, establece el diagnóstico de esófago de Barrett.
Csendes y asociados (1993), de Santiago de Chile. también han aportado evidencia, al demostrar que con creciente severidad del reflujo gastroesofágico, la unión escamo-columnar migra en el sentido proximal y crea una interposición de mucosa columnar entre el epitelio escamosos y la mucosa oxíntica.
Streets y Crookes (2001), de la University of Southern California, Los Angeles, dicen: “Creemos que la mucosa cardial es un epitelio adquirido.
En el estado normal, la mucosa escamosa esofágica llega directa-mente a la mucosa gástrica oxíntica, o puede existir un corto segmento (1-2 mm) intermedio de mucosa oxintico-cardial o de mucosa cardial, según la persona.
En algunas personas una distensión gástrica recurrente causa episodios repetidos de incompetencia del esfínter. Permitiendo que el jugo gástrico lesione la mucosa escamosa esofágica. La consecuencia es la aparición de mucosa cardial.
Inicialmente tales cambios se limitan al esfínter, pero con una injuria progresiva, el esfínter pierde su competencia y la enfermedad se extiende al esófago.
En esta etapa, la biopsia muestra mucosa cardial en el esófago distal, cerca de la unión gastroesofágica.
En la medida que empeora el reflujo y se deteriora más la barrera gastroesofágica, avanza la mucosa cardial hacia arriba en el esófago, dando así lugar a un esófago recubierto de mucosa columnar”.
T.R. DeMester (2001) publicó una revisión del proceso de intestinalización, el cual se describe en párrafos ulteriores.
Lo anterior puede dar lugar a confusión en cuanto a qué son realmente el cardias y la unión gastroesofágica en términos tanto histológicos como anatómicos, lo cual es importante para la inspección endoscópica. Por ello es pertinente revisar los trabajos de S.J. Spechler, de la Universidad de Texas, Dallas, al respecto.
Spechler (2002) describe e ilustra bien la distinción entre la unión escamocelular y la unión gastroesofágica: la interfaz entre el pálido epitelio escamoso y el rojizo epitelio columnar marca una línea visible, la llamada línea Z, que es la unión escamo-columnar.
La unión gastroesofágica (UGE), el punto imaginario donde termina el esófago y comienza el estómago, se identifica a la endoscopia por la parte más proximal de los pliegues gástricos.
En el esófago normal, la línea Z y la unión gastroesofágica frecuentemente coinciden, y no existe epitelio columnar entre las dos.
Cuando la línea Z está ubicada por encima de la unión gastroesofágica, se encuentra un segmento de esófago recubierto de epitelio columnar.
Por todo lo anterior, se ha planteado el interrogante: ¿realmente existe la mucosa cardial? Es un interrogante surgido desde la descripción en 1961 por Hayward de su presencia (mucosa de unión, junctional) como un hecho normal (DeMeester et al 2001).
Los estudios de Chandrasoma et al (2000) muestran que en 9 de 11 personas menores de 20 años, el epitelio escamoso hace transición a la mucosa oxíntica gástrica en forma directa, sin ningún tipo de mucosa interpuesta, o sea que carecen de mucosa cardial. Aunque la prevalencia de mucosa cardial aumenta con la edad, su ausencia se observó en individuos de todas las edades: en autopsias en personas sin historia de reflujo, el 56% (10 de 18 casos) no presentó mucosa cardial.
Hallazgos similares de ausencia de mucosa cardial en niños normales han sido informados por otros autores, pero Kilgore et al (2000), que plantean en el título de su artículo si el cardias es real o es ficción, encontraron mucosa cardial en la autopsia de 30 niños libres de historia de reflujo, en un segmento con longitud promedio de 1,8 mm (rango 1,0-4,0 mm) sobre la vertiente gástrica de la UGE.
Estos autores, de la Clínica Cleveland, concluyen que el cardias gástrico está presente desde el nacimiento como una estructura normal.
DeMeester et al (2001) transcriben un párrafo de un artículo por Goldman y Beckman publicado en 1960:
“Entre el epitelio escamoso del esófago y las glándulas gástricas del estómago existe una estrecha zona, usualmente de unos pocos milímetros de ancho, que contiene glándulas cardiales. Están compuestas por células epiteliales cilíndricas y por células mucosas en las criptas gástricas, pero no contienen células parietales ni pépticas”.
Pero DeMeester, Peters y DeMeester (2001), de la University of Southern California, Los Angeles, y otros autores, sostienen que la mucosa cardial es un fenómeno secundario al RGE y no un hecho anatómico normal.
Si existe mucosa cardial, ella no sobrepasa 1 a 4 mm, ubicada entre la mucosa estratificada del esófago y la mucosa oxíntica del estómago. En contraste, estos autores han encontrado que en la mayor parte de los pacientes con reflujo se encuentra mucosa cardial al tomar biopsias de la UGE y que la longitud de la mucosa cardial aumenta con el aumento de la exposición del esófago al ácido del reflujo. Los pacientes con más de 2 cm de mucosa cardial + oxinticocardial tenían una mucho más alta exposición al ácido que los pacientes con menos de 2 cm.
O sea, que la presencia de mucosa cardial u oxinticocardial en la región de la UGE es indicativa de exposición ácida anormal y que su hallazgo histológico es un criterio válido para establecer RGE, más que un hallazgo normal. Sin embargo, P.T. Chandrasoma, del Departamento de Patología Quirúrgica de la misma University of Southern California, Los Angeles, dicen en un artículo en que unos de los coautores es T.R. DeMeester, que “… se considera que la presencia de mucosa glandular en el esófago distal es anormal cuando excede 2 cm de longitud…
El hallazgo de mucosa glandular sin metaplasia intestinal en los 2 cm distales del esófago tubular es considerado actualmente como normal.
” Pero en el texto concluyen que el hallazgo de mucosa cardial o de mucosa oxinticocolumnar en la región de la UGE representa la primera evidencia morfológica de exposición anormal al ácido.
Su presencia es un marcador de lesión epitelial altamente significante de lesión epitelial por reflujo, y por lo tanto puede ser interpretada como la definición histológica de exposición anormal a ácido.
En el ICD-O, el cardias es también denominado unión gastroesofágica, y en realidad se ha considerado que la “unión GE” comprende parte del tercio distal del esófago y el cardias gástrico.
Como lo anotan Lembert y Viscaïne (1999), tal ambigüedad explica los errores relativos a clasificación y a distribución de los lugares de ubicación tumoral: el mismo tumor puede ser clasificado como de origen esofágico (tercio inferior) o gástrico (cardias). “El esófago se une al estómago por debajo del diafragma luego de un corto segmento intraabdominal. Sin embargo, la unión escamocolumnar (EC) está ubicada proximalmente (2 cm), en la parte tubular del esófago.
Es por ello que en la endoscopia la unión EC (o línea Z) se ve en el tórax, o inmediatamente por encima de la zona estrecha que marca el paso a través del diafragma. Biopsias de la mucosa inmediatamente distal a la unión EC muestran una mucosa de transición, con células de tipo antral.
Este corto segmento de la llamada mucosa cardial es generalmente de menos de 0,5 cm de longitud y separa el epitelio escamoso de la mucosa francamente gástrica. Este segmento de transición, que está presente desde antes del nacimiento. No es una metaplasia adquirida… La inflamación crónica de la mucosa al nivel de la unión GE causada por reflujo puede alterar la morfología, con un ascenso de la unión EC al tercio distal del esófago.
Esta alteración de carácter adquirido, por reflujo
Consiste en una metaplasia columnar (esófago con epitelio columnar). La metaplasia ocurre como respuesta de células multipotenciales al insulto de del ácido y los metabolitos tóxicos de las sales biliares (Nehra et al 1999). La infección por H. pylori no está involucrada en el proceso.
Cuando aparece metaplasia intestinal en la metaplasia columnar. El fenómeno se denomina esófago de Barrett.
La metaplasia intestinal del esófago de Barrett. Denominada epitelio especializado, es diferente de la metaplasia de la unión EC: es menos diferenciada y pertenece a los tipos II o III. La distribución de las citoqueratinas 7 y 20 es diferente; y hay correlación con el sexo masculino y con la raza caucásica. El mayor riesgo de adenocarcinoma en el esófago de Barrett es proporcional a la longitud del segmento de metaplasia y a la extensión del área de epitelio especializado.
Los bien definidos factores de inflamación a nivel del cardias y del esófago distal y los bien definidos tipos de metaplasia intestinal sugieren que dos tipos de cáncer ocurren en la unión GE”.
Evidentemente continúa el debate sobre la existencia normal de mucosa cardial. La cual se encuentra en personas con historia de reflujo. Pero también en individuos sin tal antecedente. Así como en niños normales.
Es tal vez algo así como la discusión sobre el término “enfermedad fibroquística” del seno, entidad que por encontrarse en un número significante de mujeres normales ha sido denominada una “no enfermedad” (Love et al 1982; Patiño 2001d).
En todo caso. Hoy es generalmente aceptado que la intestinalización de la mucosa cardial y la proliferación del esófago de Barrett son el resultado de la exposición de la mucosa esofágica al pH del reflujo, que se mezcla con la saliva y que estimula una creciente diferenciación celular. Con menor proliferación. Creando así las condiciones para el desarrollo de la metaplasia (DeMeester et al 2001).
La metaplasia intestinal se encuentra regularmente en la parte más proximal de la mucosa cardial, o sea por encima de la UGE. En ocasiones hay un área de mucosa cardial sin metaplasia, distal a la metaplasia, o sea, interpuesta entre la metaplasia y la UGE.
La ubicación de la metaplasia intestinal en la porción más alta, más proximal, de la mucosa cardial es una característica bastante constante.
Se ha discutido mucho si la metaplasia del cardias ocurre también como resultado de reflujo. Por el mismo mecanismo que el esófago de Barrett. Recientemente se ha planteado la etiología infecciosa por Helicobacter pylori (Goldblum et al 1998). El tema de la metaplasia del cardias se discute más adelante.
Entre 5% y 10% de los pacientes con esófago de Barrett presentan displasia (Stein & DeMeester 1992). Y la detección del carcinoma en estudios prospectivos de seguimiento endoscópico usualmente se ve precedida de acentuación en la severidad de la displasia (Tytgat & Hameeteman 1992).
Se define la displasia como una proliferación neoplásica esencialmente equivalente a un adenoma.
La displasia es un marcador o precursor de carcinoma. Pero de por sí puede ser maligna y asociada con invasión de los tejidos subyacentes (Guindi & Riddell 2002; Ridell et al 1983).
La clasificación de la displasia del esófago de Barrett es derivada de la clasificación de la displasia en la enfermedad inflamatoria intestinal establecida en 1983 (Ridell et al 1983).
La displasia se clasifica en displasia de bajo grado y displasia de alto grado, y cada una tiene indicaciones específicas de manejo. La displasia de alto grado incluye los casos de cambios severos y también el carcinoma in situ.
No es práctico separar la displasia de alto grado del carcinoma in situ. Por cuanto sus implicaciones clínicas son idénticas (Guindi & Riddell 2002).
La displasia puede ser identificada y clasificada con base en la biología molecular. Según las alteraciones fenotípicas nucleares consecuentes a anormalidades en el contenido de ADN (Casson 2002; Guindi & Riddell 2002).
Esto es importante, por cuanto el diagnóstico histológico de displasia es preponderantemente subjetivo. Por lo cual se registra considerable variación en la interpretación de los cortes según el observador.
Y es que el diagnóstico de displasia de alto grado quiere decir esofagectomía, como se discute más adelante.
* Profesor Honorario de Cirugía. Universidad Nacional de Colombia. Jefe Honorario, Departamento de Cirugía, Fundación Santa Fe de Bogotá.