ROOSEVELT FAJARDO G.*, GUSTAVO QUINTERO H.**
Resumen
Los tumores papilares mucinosos intraductales del páncreas son una identidad rara que comprenden cerca del 1% de las neoplasias malignas del páncreas.
El espectro radiológico que presenta esta enfermedad puede ser bastante amplio. El tratamiento ideal en este tipo de patología sigue siendo la resección quirúrgica con biopsia por congelación intraoperatoria para asegurar márgenes de sección libres de tumor. El pronóstico de este tumor es bastante favorable comparado con cualquier otro tipo de neoplasia pancreática.
Introducción
Los tumores papilares mucinosos intraductales del páncreas son una entidad rara1 que comprenden cerca del 1% de las neoplasias malignas del páncreas. Según Holguín y colaboradores2 en 1959 Frantz reportó tres casos de tumores papilares del páncreas.
Compagno y Oertel en 19783 fueron los primeros en hacer una descripción histopatológica de las neoplasias quísticas del páncreas, que incluyó dos tipos diferentes de tumor según el comportamiento biológico: el cistadenoma seroso, que se clasificaba como de comportamiento benigno, y el cistadenoma mucinoso (también llamado adenoma macroquístico o neoplasia quística mucinosa), que se creía podía progresar a cistadenocarcinoma invasivo.
Originalmente por Ohhashi en 19824, su clasificación permaneció confusa hasta 1996, cuando la Organización Mundial de la Salud (OMS) estableció la nueva clasificación que actualmente está en boga.
Sólo en 1982 Ohhashi describió esta entidad como una entidad aparte, y fue hasta 1996 cuando la clasificación de los tumores pancreáticos fue remplazada por la nueva nomenclatura de la Organización Mundial de la Salud, separando las ectasias ductales mucinosas de los cistadenomas mucinosos y dejándolos con el término de tumores quísticos papilares mucinosos intraduc-tales del páncreas.
La patogénesis de las neoplasias quísticas mucinosas del páncreas es incierta; sin embargo, este tipo de lesión comparte características clínicas y
patológicas con los tumores mucinosos biliares y ováricos. Inclusive, se ha especulado que el origen embriológico de estas lesiones puede estar relacionado con la migración de células germinales hacia la octava semana de gestación, muy temprano en la vida fetal.
Las neoplasias quísticas del páncreas se encuentran casi exclusivamente en mujeres (más de 95% de los casos), con mayor frecuencia en la cuarta a sexta década de la vida, aunque se ha informado en mujeres desde los 20 hasta los 95 años de edad.
Sus manifestaciones clínicas son básicamente el dolor abdominal difuso o la sensación de masa acompañada de anorexia y, en algunos casos, se detectan como hallazgo incidental imagenológico. Los síntomas generalmente son consecuencia de compresión de estructuras adyacentes, como el estómago o los intestinos, que puede dar la sensación de plenitud5.
Es raro que este tipo de tumor desarrolle metástasis abdominales, o que se ubique en la cabeza del páncreas y se manifiesten con ictericia por obstrucción de la vía biliar.
Las neoplasias quísticas del páncreas usualmente son grandes, con tamaños que oscilan entre 2 y 36 cm, con un tamaño promedio de 10 cm; 90% de estas neoplasias se encuentran en la cabeza y la cola del páncreas6.
Los cortes histopatológicos de este tipo de tumores revelan una lesión multilocular quística con septos llenos de mucina, estas lesiones raramente se comunican con el conducto pancreático.
Histológicamente el epitelio que recubre estas lesiones es de tipo columnar y productor de moco, el cual abruptamente se transforma en epitelio papilar estratificado con atipia celular; el potencial de transformación de este tipo de epitelio a maligno es incierta, por lo cual el Instituto de Patología de las Fuerzas Armadas de Estados Unidos considera que todas las neoplasias quísticas del páncreas son malignas de bajo grado.
Los estudios radiológicos de mayor utilidad en este tipo de patología varían desde el ultrasonido hasta la angiografía. En general, la correlación entre el ultrasonido, o tomografía axial computarizada (TAC) y la resonancia magnética es bastante alta.
En el ultrasonido se pueden apreciar lesiones multiloculadas con septos internos, y se logra demostrar las proyecciones papilares en el interior del quiste. Los estudios imagenológicos complementarios incluyen la TAC, que puede ser con o sin contraste. En la TAC sin contraste se puede apreciar la lesión como una masa lobulada bien encapsulada, pueden verse en algunos casos septos internos7. La resonancia magnética ayuda al diagnóstico, y su aspecto depende directamente de la cantidad de líquido presente en el interior de la lesión. El diagnóstico diferencial es con numerosas entidades, que incluyen los pseudoquistes y todas las neoplasias quísticas8.
El tratamiento de esta entidad es la resección quirúrgica completa, y el pronóstico depende de si la extracción es total. En series en las cuales se logró la extracción completa de la masa, la sobrevida, sin recurrencia tumoral es mayor de 90%; en cambio, si el tumor no es extraído en su totalidad, la tasa de sobrevida puede disminuir a 68%9.
Caso Clínico
Hombre de 54 años de edad con historia de 3 meses de evolución de distensión abdominal posprandial acompañada de dolor epigástrico que posteriormente se irradiaba a la espalda.
Antecedentes de enfermedad ácido péptica, hipertrofia prostática benigna, poliposis colónica, fumador y bebedor en la juventud.
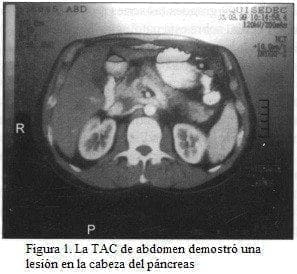
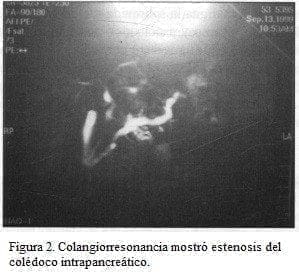
El paciente aparecía en buena condición general; el abdomen era blando depresible, con leve dolor a la palpación en el epigastrio; no se palpan masas ni había visceromegalia. La TAC de abdomen (figura 1) demostró una lesión en la cabeza del páncreas, que fue confirmada en la colangiorresonancia (figura 2) y que además mostró estenosis del colédoco intrapancreático.
 |
 |
Con impresión diagnóstica de cáncer de la cabeza del páncreas y fue llevado a pancreatoduodenectomía sin preservación de píloro. La patología reporta un tumor papilar mucinoso intraductal del páncreas, hipersecretor con un ducto pancreático estático.
Discusión
Presentamos un caso poco frecuente en la práctica quirúrgica9 con una revisión de la literatura mundial sobre el tema. El tratamiento ideal en este tipo de patología sigue siendo la resección quirúrgica con biopsia por congelación intraoperatoria para asegurar márgenes de sección libres de tumor. Según cita de Gigot10, el pronóstico de este tumor es bastante favorable comparado con cualquier otro tipo de neoplasia pancreática.
Es frecuente encontrar múltiples focos de tumor papilar intraductal mucinoso en el mismo páncreas; es por esto que Izawa y col.11 analizaron 37 pacientes sometidos a resección pancreática buscando mutaciones en el codón 12. Estos autores pudieron establecer que de las 37 piezas quirúrgicas, todas tenían dos lesiones de hiperplasia ductal y 23 (67%) tenían mutaciones del codón 12; de éstos, 23 (50%) tenían diferentes mutaciones k ras del codón 12. A su vez Z’graggen et al.12 analizaron especímenes de 16 pacientes, e igualmente encontraron mutaciones k ras del codón 12 en 13 (81.2%) de especímenes.
Otra forma de determinar este tipo de mutaciones y de poder aproximar un diagnóstico lo reportaron Kondo et al.13 quienes analizaron el jugo pancreático de 13 pacientes con tumor papilar intraductal mucinoso del páncreas y encontraron mutaciones del k ras codón 12 en 12 de los 13 pacientes. Sin embargo, estos mismos autores habían encontrado la misma mutación en el jugo pancreático de pacientes con pancreatitis, e incluso con cáncer de páncreas, lo que lo hizo concluir que sólo sirve este análisis para determinar que existe patología pancreática sin que se pueda determinar ni siquiera si es de carácter benigno o maligno. Niall y asociados14 a su vez encontraron la mutación k ras del codón 12 en el 71% de pacientes con tumor papilar intraductal mucinoso del páncreas, lo que corresponde al resto de los reportes de autores sobre esta mutación.
A la vez que el diagnóstico de este tipo de tumor incluye varios tipos de estudios de imágenes diagnósticas, la ultrasonografía endoscópica constituye una herramienta diagnóstica de la mayor utilidad, la cual incluso puede ayudar a determinar características que sugieran malignidad. Kubo y colaboradores15 reportaron un interesante estudio en el cual analizan 51 pacientes con tumor papilar intraductal mucinoso del páncreas, en quienes se hizo ultrasonografía endoscópica preoperatoria; comparando luego con los estudios histopatológicos de los especímenes, se pudo determinar que ductos principales de más de 10 mm y ductos secundarios con septos de más de 40 mm sugieren malignidad, y que la ultrasonografia endoscópica fue capaz de diferenciar benignidad de malignidad en 86% de los casos.
El espectro radiológico que puede presentar el tumor papilar intraductal mucinoso del páncreas puede ser amplio y entre los principales hallazgos imagenológicos según describen Lim y colaboradores16, se puede describir la dilatación multiquística de los conductos pancreáticos secundarios, dilatación difusa del conducto pancreático principal, tumor papilar intraductal, tapones de mucina dentro de los conductos y, aunque la presencia de esta entidad se puede sospechar con la ultrasonografía tradicional además de la tomografía axial computarizada o la resonancia nuclear magnética, el examen ideal es la colangiografía endoscópica retrógrada.
Sin embargo, este examen tiene algunas complicaciones, por lo cual Albert et al.17 proponen la colangiopancreatografía por resonancia magnética, argumentando excelente visualización de los conductos pancreáticos sin las complicaciones de la CPRE. Otros hallazgos imagenológicos característicos de esta entidad y que son citados por Sugiyama y Atomi18 son la apariencia de “racimo de uvas” que pueden adoptar los conductos pancreáticos dilatados y la atrofia del parénquima pancreático. También son de gran utilidad las imágenes diagnósticas para predecir la resecabilidad del tumor. Fuhrman et al.19 pudieron determinar que de 145 pacientes estudiados con tomografía axial computarizada con cortes delgados (intervalos de 10 mm) preoperatoriamente, en 88% de los casos la tomografía pudo predecir la resecabilidad de la lesión. Taouli y asociados20 también determinaron la importancia de la tomografía preoperatoria para definir la resecabilidad de la lesión, e incluso pudieron establecer en los 36 pacientes que estudiaron, que la presencia de diabetes, más los hallazgos imagenológicos característicos de tumor papilar intraductal mucinoso eran altamente sugestivos de malignidad. Silas y asociados21 refieren la importancia de establecer el diagnóstico diferencial con todas las neoplasias quísticas del páncreas, bien sea con o sin dilatación del conducto pancreá-tico principal, como también con las pancreatitis crónicas.
Ya en el campo quirúrgico, es difícil determinar intraoperatoriamente la extensión de la lesión y, por lo tanto, son los márgenes de resección los que van a determinar el pronóstico de la lesión. Kaneko et al.22 estudiaron 27 pacientes en quienes realizó ultrasonografía intraoperatoria de alta resolución, mediante esta técnica se pudieron detectar 5 casos de tumor papilar intraductal que no se detectaron por ultrasonografía endoscópica. La sensibilidad y la especificidad para detectar lesiones en el conducto pancreático principal con esta técnica fueron 86% y 100%, respectivamente, comparado con la colangiopancreatografía endoscópica retrógrada, la cual mostró una sensibilidad y especificidad de 50% y 100%, respectivamente.
No son muy grandes las series reportadas en la literatura mundial sobre esta patología. Warshaw et al.23 en 1990 fueron los primeros en publicar en Estados Unidos el reporte de 2 casos de pacientes en quienes se realizó resección pancreática cuya patología reportó tumor papilar intraductal mucinoso del páncreas. Traverso y asociados24 reportaron su experiencia de 8 años, durante los cuales pudieron recolectar 33 pacientes con tumor papilar mucinoso del páncreas que fueron llevados a cirugía. Del total de los 33 pacientes, en 15 se practicó lo que llaman pancreatoduodenectomía cefálica, en 5 pancreatoduodenectomía total y en el resto pancreatectomías parciales. De los pacientes que tuvieron patología benigna, todos estaban vivos al final del seguimiento, mientras que los que tuvieron reporte de patología maligna la sobrevida fue de 38 meses en promedio. Traverso y asociados24 plantean el interrogante de cuál de los tipos de tumores intraductales puede estar más asociados con transformación a malignidad, y concluyen que cuando existe historia de abuso de alcohol o de ictericia se debe ser más agresivo en el tratamiento quirúrgico.
También existen aquellos que, como Nakagorhi y asociados25, pregonan la resección de la parte inferior de la cabeza del páncreas en los casos en que la enfermedad se encuentra confinada a esa zona. Estos autores reportan su experiencia con 38 pacientes llevados a cirugía, de los cuales 7 (18%) fueron sometidos a este tipo de resección, evaluando primero con ultrasonografía intraoperatoria la extensión de la lesión; de estos 7 pacientes, 5 tenían adenoma papilar, mientras que 2 pacientes tenían adenocarcinoma papilar. La tasa de sobrevida a 5 años para este grupo de pacientes fue 86%. Es mandatoria, como se menciona anteriormente, la biopsia por congelación para determinar los bordes de sección. Paye y colaboradores26 reportan 41 pacientes en que se practicó resección pancreática de algún tipo.
El tipo de resección puede estar determinado por el conducto que esté afectado por el tumor. Kobari et al.27 plantean dos subtipos de tumores de acuerdo con el compromiso ductal: los que comprometen el conducto pancreático principal y los que comprometen las ramificaciones ductales, y plantean la necesidad de ser más agresivo en los casos en los cuales el compromiso sea de las ramificaciones; para esto proponen la pancreatectomía total. Otros, como Nakaghori et al.28 recomiendan la pancreatoduodenectomía tradicional. Estos autores reportan 36 pacientes que fueron sometidos a este procedimiento, con tasas de sobrevida a 5 años entre 90% y 100% según el tipo de tumor.
Kim et al.29 reportan una entidad que, aunque rara, puede semejar un tumor papilar intraductal mucinoso del páncreas; es el tumor de conducto biliar hipersecretor de mucina.
Sho y asociados30 reportan en su estudio de 14 pacientes los patrones de recurrencia que puede tener el tumor papilar intraductal del páncreas; en su serie el sitio más frecuente de recurrencia fue el páncreas remanente, seguido del hígado y del peritoneo. El tratamiento recomendado cuando existe recurrencia en el páncreas remanente es la pancreatectomía total. En los seis casos de recurrencia, el período posoperatorio libre de enfermedad fue de 38 meses; el seguimiento a largo plazo es mandatorio en todos los casos.
Recientemente se ha descrito una entidad nueva que se ha catalogado como neoplasia intraductal papilar “oncocítica” del páncreas. Adsay et al.31 reportan 11 casos de tumores pancreáticos productores de mucina con características que describen como oncocíticas; 10 de sus 11 pacientes mostraron suficiente atipia en su arquitectura para ser catalogados de esta manera. Jyotheeswaran y asociados32 reportan un caso de un hombre de 69 años en quien se le practicó una pancreatoduodenectomía; la patología reportó un tumor papilar intraductal oncocítico del páncreas. Esta entidad es muy nueva y la información en la literatura es todavía muy escasa para poder predecir el comportamiento biológico de este tipo de tumor32.
En conclusión, el tumor papilar intraductal mucinoso del páncreas es una entidad rara sobre la cual cada vez hay más reportes en la literatura mundial; es una lesión de buen pronóstico luego de la resección quirúrgica del tumor.
Abstract
Intraductal papillary mucinous tumors of the pancreas are rare pathological entities, representing about 1% of all pancreatic malignant neoplasms.
Optimal therapy is surgical resection with intraoperative frozen section biopsy for control of surgical margins. Prognosis is favorable, as compared with other pancreatic tumors.
Bibliografía
1. Galindo F, Kogan Z: Tumores quísticos del páncreas. Rev Argent Cir 1998; 75:140-50.
2. Holguín F, Londoño E: Tumor quístico del páncreas. Rev Col Cir 1991; 6: 87-90
3. Compagno J, Oertel JE: Mucinous cystic neoplasms of the pancreas. A clinicopathologic study of the 34 cases. Am J Clin Pathol 1978; 69: 289-98.
4. Edward V, Loftus Jr: Intraductal papillary mucinous tumors of the pancreas: clinicopathologic features, outcome, and nomenclature. Gastroenterology. 1996; 110:1909-18.
5. Tibayan F, Vierra M: Clinical presentation of mucin-secreting tumors of the pancreas. Am J Surg. 2000; 179: 349-51.
6. Gramática L, Teyssedou C: Tumores quísticos del páncreas: realidad actual.
7. FlIKlIKlIRA Y, FlIJlYOSlI1F: lntraductal papillary mucinous tumor of the pancreas: thin section helical CT findings. AJR Am J Roentgenol2000; 174: 441-7.
8. PROCACCIC, MECIBOW A, CARBOGNING, GlIARISE A: lntraductal papillary mucinous tumor of the pancreas: a pictoral essay. Radiographics 1999; 19: 1447-63.
9. HERNÁNDEZR, SILVAJ: Tumores pancreáticos poco frecuentes: experiencia de 10 años. Cirugía & Cirujanos 1993; 60: 11-9.
10. GIGOT J, DEPREZ P, SEMPOllX C, DESCAMPS C: Surgical management of intraductal papillary mucinous tumor of the pancreas. Arch Surgery 200 1; 136: 1256-62.
11. IZAWAT, OBARA T, TANNO S, MIZlIKAMI Y: Clonality and field cancerization in intraductal papillary mucinous tumor of the pancreas. Cancer 200 I 92: 1807-17.
12. ZGRAGGEN K, RIvERA J, COMPTON C, PINS M: Prevalence of activating k-ras mutations in the eyolutionary stages of neoplasia in intraductal papillary mucinous tumor of the pancreas. Ann Surg. 1997; 226: 491-8.
13. KONDOH, SlIGANO K, FlJKAYAMAN, HOSOKAWAK: Detection of kras mutations at codon 12 in the pancreatic juice of patients with intraductal papillary mucinous tumors of the pancreas, Cancer 1994; 73: 1589-94,
14. NIALL J. MULLlGANN, YANG S, ANDRYC: The role of p21ras in pancreatic neoplasia and chronic pancreatitis. Hum Pathol 1999; 30: 602-10.
15. KUBOH, CHIJ11WAY,AKAHOSHIK, HAMADAS: Intraductal papillary mucinous tumor ofthe pancreas. Ditlerential diagnosis between benign and malignant tumors with endoscopic ultrasonography. Am J Gastroenterol 2002; 96: 1429-34.
16. LIMJ, LEEG, LYUNY: Radiologic spectrum of intraductal papillary mucinous tumor ofthe pancreas. Radiographics 2001; 21: 323-37.
17. ALBERT J, SCHILLlNG D, BREER H, JUNGIUS K: Mucinous cystadcnomas and intraductal papillary mucinous tumors of the pan creas in magnetic resonance cholangiopancreatography. Endoscopy 2000; 32: 472-6.
18. SUGIYAMAM, ATOMIY: Intraductal papillary mucinous tumor of the pancreas: imaging studies and treatment strategies. Ann Surg 1998; 228: 658-91.
19. FUHRMANG, CHARNSANGAVEJ C, ABRUZZESEJ, CLEARYK: Thinsection contrast-enhanced computed tomography accurately predicts the respectability of malignant pancreatic neoplsms. Am J Surg. 1994; 167: 104-11.
20. TAOULl B, YILGRAIN Y, YULLlERME M, TERRIS B: Intraductal papillary mucinous tumor of the pancreas: he1ical CT with histopathologic correlation. Radiology 2000; 217: 757-64.
21. SII.ASAM, MORRINM, RAPTOPOULOSY, KEOGANM: Intraductal papillary mucinous tumor of the pancreas Am J Roetngenol. 2001; 176: 179-85.
22. KANEKO T, NAKAO A, INouE S, SUGIMOTO H: Intraoperative ultrasonography by high-resolution annular array transducer for intraductal papillary mucinous tumor of the pancreas. Surgery 2001; 129: 55-65.
23. WARSHAWA, RATTNERD: Middle segment pancreatectomy: a novel technique for conserving pancreatic tissue. Arch Surg 1998; 1133: 327-31.
24. TRAVERSO L, PERALTA E, RYAN J, KOZAREK R: Intraductal neoplasms of the pancreas. Am J Surg 1998; 177: 426-32.
25. NAKAGHORIT, KENMOCHIT, KAINlIMA0, TOKOROY: Inferior head resection of the pancreas for intraductal papillary mucinous tumors. Am J Surg 2000; 179: 482-4.
26. PAYEF, SAlIVANETA, TERRISB, PONSOTP: Intraductal papillary mucinous tumor of the pancrcas: pancrcatic rcscctions guided by preoperative morphological assessment and intraoperative frozen section examination. Surgery 2000; 127: 535-44.
27. KOBARI M, EGAWAS, SHIBL;YAK, SHIMAMURAH: Intraductal papillary mucinous tumor of the pancreas comprise 2 clinical subtypes: differences in clinical characteristics and surgical management. Arch Surg 1999; 134: 1131-6.
28. NAKAGHORIT, KENMOCHIT, KAINUMA0, TOKOROY: Intraductal papillary mucinous tumor of the pancreas. Am J Surg 1999: 178: 344-7.
29. KIM H, KIM M, LEE S, Yoo S: Mucin hypersecreting bile duct tumor characterized by a striking homology with an intraductal papillary mucinous tumor of the pancreas. Endoscopy 200(); 32: 389-93.
30. SHO M, NAKAJlMA Y, KENEHIRO H, HISANAGAM: Pattern of recurrence after resection for intraductal papillary mucinous tumor of the pancreas. World J Surg 1998: 22: 874-8.
31. ADSAYN, ADAIR C: Intraductal oncocytic papillary ncoplasms of the pancreas. Am J Surg Path 1996; 20: 980-94.
32. JYOTHEESWARANS, ZOTALlSG, PENMETSAP, LEvEA M: A newly recognized entity: intraductal oncocytic papillary ncoplasms of the pancreas. Am J Gastroenterol 1998; 93: 2539-43.
* MD. Sección Cirugía General Fundación Santa Fe dc Bogotá.
** MD FACS FRCS. Sección Cirugía Hepatobiliar Fundación Santa Fe dc Bogotá.