Cirugía Endocrina
DE LA HOZ J., MD, SCC (Hon.)
Palabras clave: Diabetes, Insulina, Páncreas, Glucosa, Metabolismo, Cuerpos cetónicos.
La diabetes mellitus es una alteración metabólica cada día más frecuente. Constituye un formidable riesgo para aquellos pacientes que la sufren y son sometidos a una intervención quirúrgica. Se estima que aproximadamente 60% de ellos en el curso de su vida, serán sometidos al estrés quirúrgico y anestésico. Por eso, el cirujano debe tener conocimientos de su fisiopatología, complicaciones agudas y crónicas y, lo que es más importante, cómo tratarlas. Según su comportamiento clínico y fisiopatológico y, sobre todo su etiología, se acepta clasificar la enfermedad en dos grandes tipos, el tipo 1 de reconocida causa autoinmune y, el tipo 2, con múltiples aspectos, pero predominantemente debido a un incremento de la resistencia de los tejidos a la acción de la insulina; con el descubrimiento de esta hormona, se prolongó la sobrevida, pero continúan siendo un desafío médico sus complicaciones crónicas en órganos como riñón, corazón, retina y vasos sanguíneos, que en definitiva determinan la problemática final de la enfermedad. En este artículo se insiste en ella y se subraya la importancia que reviste la constitución de un grupo interdisciplinario para su cabal y efectivo tratamiento durante el período perioperatorio, equipo en el cual el cirujano forma parte importante.
Introducción
La diabetes mellitus (DM) es una enfermedad común y constituye un importante factor de riesgo para el paciente quirúrgico. Antes de que la insulina exógena estuviera disponible, pacientes con DM tipo 1, podían morir en meses o en breves años después de su diagnóstico, debido a sus complicaciones metabólicas. Como consecuencia de su limitada supervivencia, la factibilidad de una intervención quirúrgica era muy incierta, y el papel del cirujano en su cuidado era mínimo. El aislamiento de la hormona en 1921, por Banting y Best, en los laboratorios de Macleod en el Departamento de Fisiología de la Universidad de Toronto, modificó el papel de la cirugía. Este agente parece ser capaz de prolongar la expectativa de vida en el paciente diabético, casi igual a la de la población no diabética. Desafortunadamente, una nueva y no prevista amenaza se cierne para los afectados, en la forma de complicaciones secundarias como neuropatía, retinopatía, nefropatía, micro y macroangiopatías, etc., cuyo control requiere de intervenciones quirúrgicas. Se calcula que aproximadamente 50% de todos los diabéticos serán sometidos a cirugía mayor en algún momento de su existencia.
Inicialmente los portadores de la enfermedad son tratados por internistas, endocrinólogos o diabetólogos. La DM es única por los desórdenes metabólicos que la caracterizan y por la importancia que la cirugía tiene en su evolución. El cirujano continuará tratándolos en número cada vez más grande debido al incremento de su incidencia y al de las complicaciones secundarias, especialmente las relacionadas con las vasculopatías y nefropatías, además de las varias patologías quirúrgicas que suelen ocurrir en ellos. Al cirujano le incumbe tener un gran conocimiento del impacto de la hiperglicemia en la respuesta metabólica a la intervención quirúrgica; no puede ignorar el manejo de la terapia insulínica y debe prever las posibles complicaciones que le son inherentes.
Los pacientes candidatos a cirugía electiva con diagnóstico conocido de diabetes, se benefician de una estrecha interacción entre el cirujano y el diabetólogo. Aquellos que necesitan una intervención de urgencia o en quienes el diagnóstico es desconocido, presentan un desafío único al cirujano en el transcurso perioperatorio. Independientemente del modo de presentación, ellos tienen un mayor riesgo de morbimortalidad cardíaca, deterioro en el proceso de cicatrización de la herida y disturbios hidroelectrolíticos por alteración de la función renal. Otras complicaciones potenciales, únicas en esta patología, incluyen desórdenes neuropáticos, en la función gastrointestinal y genitourinaria, alteraciones en la tensión arterial y función motora. Aunque las complicaciones infecciosas pueden no ser más comunes en los diabéticos, cuando se presentan lo hacen asociadas a resultados muy infortunados, si se les compara con los no diabéticos sometidos a iguales intervenciones.
Existen algunos interrogantes sobre el diabético en el perioperatorio. ¿Debe ser diferente el tratamiento de los de tipo 1 a los de tipo 2?. ¿Es necesario que un enfermo esté en equilibrio total de electrolitos durante toda la intervención quirúrgica o pueden tolerarse pequeñas desviaciones de lo normal sin provocar consecuencias graves?.
Algunas de estas preguntas no pueden ser contestadas de manera definitiva en la actualidad, pero constituyen la base de investigaciones futuras.
Existen muchos regímenes para tratar pacientes diabéticos en el perioperatorio (3, 11, 28). La mayor parte de los estudios divide la diabetes en tres categorías: 1) El diabético tipo 1, perfectamente controlado únicamente con dieta. 2) El tipo 2 que requiere hipoglicemiantes o insulina. 3) Tipo 3. La gran mayoría de las autoridades no administran insulina a los individuos de la primera categoría si el procedimiento es de tipo menor y no hay otro estrés concomitante (3, 28).
No hay acuerdo de criterios acerca de cómo tratar la segunda categoría.
Los del tercer tipo, siempre son tratados con inyecciones intravenosas o subcutáneas de insulina de efecto rápido y prolongado. No está claro qué resultado final debe medirse para juzgar la mejoría. ¿Será acaso el índice de complicaciones quirúrgicas?. ¿La permanencia en la unidad de cuidados intensivos?. Todos los autores concuerdan en que las concentraciones de glucosa sanguínea deben medirse (directa o indirectamente), a fín de regular la dosis de insulina y evitar la hipo o hiperglicemia (3).
Desde el descubrimiento histórico de la insulina por un cirujano, la práctica quirúrgica ha tenido un especial interés en el potencial para curar esta enfermedad por medio del trasplante. Los cirujanos con frecuencia han sido criticados por llevar a cabo esta terapia en ausencia de un ensayo clínico que demuestre su eficacia. Los resultados recientemente inventariados por la Asociación del Control de la Diabetes y sus Complicaciones, han estimulado el trasplante pancreático. Rígidos controles de la glicemia, disminuyeron dramáticamente las complicaciones secundarias de la enfermedad. El trasplante normaliza la homeostasis de la glucosa y puede, por consiguiente, ser recomendado como terapia para complicaciones secundarias en pacientes seleccionados.
Una terapia alternativa es el trasplante de las células de los islotes pancreáticos, porque teóricamente evita el trasplante concurrente del tejido exocrino y los problemas asociados. Actualmente, menos de 1% de los trasplantes de los islotes de Langerhans ha logrado el objetivo de liberar al paciente de la necesidad de la terapia insulínica. Los intentos de encapsular los islotes para protegerlos del rechazo no han sido exitosos. Hoy el trasplante continúa siendo la mejor esperanza para la solución a la insulino dependencia. Más de 3.000 pacientes han recibido uno de estos trasplantes, pero combinado con el trasplante renal. Las tasas de éxitos corrientes de trasplante combinado de riñón y páncreas son tan buenas como las del riñón solo. Cuando la técnica de inmunosupresión venza la necesidad de usarla indefinidamente, el campo puede extenderse para incluir pacientes con diabetes sin falla renal.
Diabetes Mellitus. Clasificación y Criterios Diagnósticos
La Asociación Americana de Diabetes (AAD), teniendo en cuenta los conocimientos más recientes acerca de los mecanismos complicados en el origen de cada tipo de diabetes, así como del hallazgo de marcadores genéticos en pacientes sin enfermedad clínicamente manifiesta y, además, la evidencia de la progresión de sus complicaciones, ha hecho públicos los recientes críterios diagnósticos y la nueva clasificación de la enfermedad que se basa, sustancialmente, en conceptos etiológicos no considerando términos vinculados a la modalidad de tratamiento, lo cual se presta a equívocos y confusión. Esto quiere decir que las denominaciones de “diabetes mellitus insulino dependiente” y “diabetes mellitus no insulino dependiente”, no se deben seguir utilizando. Los motivos para sostener esta tesis son, por ejemplo, que muchos pacientes diabéticos pueden “depender” de la insulina para sobrevivir, y son clasificados como “no insulino dependientes”, que en fases finales están en insulinopenia y deben ser tratados con la hormona, pero no por eso se convierten en diabéticos insulino dependientes, pues esta clase de enfermedad tiene una historia natural completamente diferente. En la misma forma, muchos individuos diabéticos insulino dependientes, pueden no requerir la insulina durante algún momento al comienzo de la enfermedad (período de luna de miel).
Todas estas razones condujeron a un Comité de Expertos (90), profundos conocedores del problema, a denominar diabetes Tipo 1 a la anteriormente llamada “diabetes insulino dependiente”. Con este término, se hace referencia a la enfermedad caracterizada esencialmente por insulinopenia, debido a la destrucción progresiva de las células beta del páncreas. Estos individuos tienen gran tendencia a padecer cetoacidosis, debido a que la carencia de insulina, los hace incapaces de frenar los fenómenos de lipólisis que dan origen a los cuerpos cetónicos, evento crucial en el desarrollo de esta complicación aguda.
Diabetes Tipo 1
Este tipo de diabetes mellitus (DM) está asociada con características genéticas. Su predisposición hereditaria es como un rasgo multigénico, heterogéneo y con tendencia a baja penetrancia y transmisión (92). Ocurre en miembros de familia en 15% de los casos, y es más común entre gemelos idénticos. El individuo que va a desarrollar la enfermedad, nace con una susceptibilidad dada por predominio de los haplotipos tipo II del complejo mayor de histocompatibilidad (HLADR3 y HLADR4) (94). Subsecuentes estudios han observado que DR1, DR16 y DR18, también predisponen a la enfermedad, mientras que DR15 y DR11 confieren protección (62). Debido a su papel en el proceso de presentación antigénica y de reconocimiento de lo propio, la presencia de estos haplotipos establece un lazo claro entre la predisposición genética y la posibilidad de un fenómeno autoinmune.
No se ha podido demostrar una forma de transmisión simple de la enfermedad. El riesgo de sufrir este tipo de diabetes, a diferencia de la diabetes tipo 2 (para la que algunos han sugerido una forma de transmisión a través del ADN mitocondrial), es casi tres veces mayor en los descendientes de padre diabético, que en los hijos de mujeres afectadas. Así mismo, se han identificado genes involucrados en el cromosoma 11, en donde se codifican factores de crecimiento similares a la insulina. También en los comprometidos en el transporte de los péptidos antigénicos que van a ser presentados a los linfocitos T, cuya mutación, explicaría el origen del fenómeno autoinmune.
No se conoce con exactitud cuál es el factor que desencadena la cascada de eventos autoinmunes que terminarían en la destrucción de las células beta. Algún factor ambiental (infección, dietario), debe ejercer su influencia, para que la enfermedad se exprese en un individuo y no en otro. De acuerdo con algunas investigaciones, virus de tipo Coxackie serían los responsables de disparar el fenómeno autoinmune (58). Otros virus como el de la rubéola y el citomegalovirus, podrían tener importancia en algunos casos (76). Otras teorías sostienen que una albúmina sérica bovina, una proteína contenida en la leche de vaca, podría generar una respuesta cruzada contra antígenos presentes en las células beta al estimular mediante este proceso la producción de autoanticuerpos, haciendo que los mecanismos de defensa inmunológica confundan los antígenos propios con los extraños, iniciando así una respuesta autoinmune con destrucción de las células beta.
Está presente una insulitis prodominantemente por infiltración linfocítica del páncreas y células mononucleares, en la mayoría de los pacientes con diabetes tipo I (14). Los análisis inmunocitoquímicos posmortem del páncreas de pacientes recién diagnosticados, revelaron un predominio de las células citotóxicas / supresoras CD8+ T, con células ayudadoras CD4 + T.
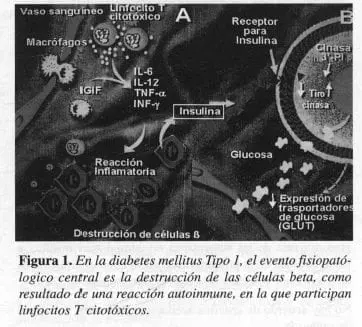
Este proceso inflamatorio es amplificado gracias a la liberación local de diversas citoquinas, en particular el factor inductor de interferón gama (IGIF, por las siglas inglesas Interferón Gamma Inducing Factor), interleucina 2, interleucina 6, interleucina 12 y factor de necrosis tumoral alfa (TNF a, por tumor necrosis factor alfa). Así mismo, ha sido demostrada la expresión del receptor Fas en la membrana de las células beta y, cuando dicha molécula interactúa con su ligando respectivo (Fas I), ubicado en la superficie de los linfocitos T citotóxicos, se desencadenan reacciones intracelulares que llevan a la apoptosis de las células beta (Figura 1).
Para explicar el inicio del fenómeno autoinmune en la diabetes, se han esbozado tres mecanismos básicos. En el primero, la actividad inmunológica sería secundaria a la presencia de virus “escondidos” dentro de las células, que mantendrían activos los mecanismos de defensa, y que conducirían a la destrucción de las células portadoras de los antígenos extraños. En el segundo mecanismo, la infección o la interacción con un factor externo, llevaría a la formación de neoantígenos contra los cuales se montaría la respuesta inmune, mediante un proceso de mímica molecular. En tercer lugar, podría existir un superantígeno como iniciador de la respuesta autoinmune.
El descubrimiento de autoanticuerpos circulantes contra las células de los islotes, primero en diábeticos y después en parientes prediabéticos, han hecho del diagnóstico preclínico de la enfermedad una realidad (59). Las investigaciones van dirigidas a mejorar el poder predictivo de los marcadores serológicos, para determinar la especificidad de los anticuerpos y determinar la historia natural de tal inmunidad. Autoanticuerpos, generalmente de la familia IgG que se unen a las células de los islotes, pueden ser detectados por inmunofluorescencia en el suero de 65% a 85% de los pacientes diabéticos en diagnóstico (59).
Muchos diabéticos, tienen autoanticuerpos no pancreáticos (ej. contra tiroides, adrenales, células parietales), y el riesgo de fallas poliglandulares en tales individuos es significativa (63).
Se han detectado autoanticuerpos contra la insulina en 20 a 60% en pacientes diabéticos tipo 1, antes de la iniciación del reemplazo de la hormona, y son especialmente prevalecientes en aquellos pacientes cuya enfermedad se inicia desde muy jóvenes (10).
Hoy los marcadores humorales de autoinmunidad permiten la identificación de prediabetes. Persistente la incertidumbre de si los autoanticuerpos inician o contribuyen al daño de las células beta. Se piensa que la mayoría de los autoanticuerpos en esta enfermedad, reflejan la respuesta inmune estimulada por los islotes ya dañados o la existencia de un defecto inmunorregularizador generalizado. Se mantiene la esperanza de que la identificación de autoanticuerpos y su especificidad, llevarán a un método más confiable para detectar pacientes prediabéticos y una forma de terapia tolerogenética antígeno específica.
Diabetes Tipo 2
En la diabetes tipo 2, el trastorno central es la resistencia de todos los tejidos periféricos (Nomenclatura 1) a la acción de la insulina, debido a que se produce una hormona defectuosa porque existen trastornos del receptor o, lo que es más importante, a la presencia de alteraciones en los mecanismos intracelulares desencadenados por la unión de la hormona al receptor. Al respecto, se ha demostrado la deficiencia en la actividad, en modelos animales y humanos, de la enzima tirosina cinasa, encargada de la fosforilación de la proteína IRS1 (Insulin Receptor Substrate 1) y la hipoactividad de la enzima cinasa 3 fosfatidil inositol.

La diabetes tipo 2 comprende entre 85 y 90% de los diabéticos. Por lo general se trata de pacientes mayores de 40 años, obesos, en quienes la enfermedad se desarrolla paulatinamente y su expresión clínica puede pasar desapercibida por años. En algunos de estos sujetos, se presenta rápidamente un importante déficit en la producción de insulina, y el paciente debe recibir la hormona para obtener control metabólico. Sin embargo, esta forma de tratamiento no hace al individuo insulino dependiente.
En la mayoría de los estudios (72) la diabetes tipo 2 estadísticamente está relacionada con la obesidad. No obstante, esto no establece una relación causativa. Es la forma más común de diabetes con la que el cirujano tiene que enfrentarse y el hecho de que se presente en personas de edad, es muy probable que requieran de un tratamiento quirúrgico.
En la tercera categoría se encuentra la diabetes asociada con causas específicas: alteraciones genéticas claramente identificadas, como mutaciones en el gen de la glucosinasa, entre otras, que dan origen a la diabetes tipo MODY (Maturity Onset Diabetes of the Young). En esta categoría, también se incluyen defectos genéticos que impiden la acción de la insulina, como las mutaciones en el receptor, características del Leprechaunismo y otros síndromes géneticos raros. En cuanto a las endocrinopatías, quizás las más frecuentes asociadas como causa de diabetes antiguamente llamada “secundaria”, son la acromegalia y el síndrome de Cushing. Hacen parte de este subgrupo los glucocorticoides, tiazidas, diazóxido y ácido nicotínico. Hay infecciones, en las que se cuenta la rubéola congénita o el citomegalovirus, que pueden ser causa de diabetes. La enfermedad, puede ser parte del complejo sintomático de otras enfermedades de origen genético, tal es el caso del síndrome de Down, Klinefelter y Turner.
Existe una cuarta categoría en la que está incluida la diabetes gestacional, o sea, el aumento de la glicemia que se inicia durante el embarazo. No se justifica el uso universal de pruebas de tamizaje, mediante la administración de 50 gm de glucosa hacia la semana 24 a 28 de gestación, pues no todas las mujeres están en riesgo de sufrir la enfermedad.
Doctor Jaime De la Hoz, Profesor Emérito y Honorario de la Fac. de Medicina de la Univ. Na!. de Colombia, Hosp. de San Juan de Dios. Ex Presidente de la Sociedad Colombiana de Cirugía. Santafé de Bogotá, Colombia.
