En el Paciente para Cirugía Torácica
O. JARAMILLO, MD.
Introducción
Este escrito está dirigido, en especial, a la evaluación de aquellos pacientes que serán sometidos a cirugía del tórax con resección pulmonar, pero se extiende a todos los pacientes quirúrgicos.
La correcta evaluación de la función pulmonar en el paciente que será sometido a cirugía del tórax, y a cualquier cirugía en general, hará posible tomar las medidas pre, trans y postoperatorias adecuadas para disminuir las complicaciones pulmonares postoperatorias (CPP), primera causa de morbilidad y mortalidad en los pacientes sometidos a intervención quirúrgica. También determinará si es necesario descartar la cirugía como opción terapéutica en aquellos pacientes de riesgo inadmisible por la imposibilidad de mantener la función respiratoria con el parénquima pulmonar residual o indicará la necesidad de soporte mecánico de la ventilación en el postoperatorio.
Son las pruebas de función pulmonar el método más objetivo y confiable de predecir la función pulmonar en el postoperatorio que, además, permite conocer no sólo la tasa de CPP, sino también la calidad de vida respiratoria que acompañará al paciente durante el resto de su vida.
Efecto de la anestesia sobre la función pulmonar
La anestesia general causa alteración en la respuesta a la hipercarbia (o hipercapnia) y a la hipoxemia, tanto cuando se usan anestésicos inhalados como cuando se utiliza la anestesia intravenosa. Este efecto es más marcado y a la vez más riesgoso en los pacientes con EPOC. La anestesia originauna caída de la Capacidad Residual Funcional mediada por un ascenso del diafragma, una relajación de la pared torácica y, por supuesto, por una disminución de la distensibilidad total.
El desplazamiento del diafragma hacia el tórax originará atelectasias que aparecen tan rápido como 5 minutos después de la inducción de la anestesia. Se presentan en las áreas más dependientes de los pulmones y no están correlacionadas con la edad o con la PlOz, son independientes de si la ventilación es espontánea o mecánica y de si los anestésicos se administran por la vía inhalatoria o por la intravenosa. Estas atelectasias persisten hasta 24 horas después de la cirugía en la mitad de los enfermos.
Los pacientes anestesiados presentan un espacio muerto de hasta el 50% del Volumen Vital (VdJVt: 0.5). Esto se debe al aumento del espacio muerto de los sistemas de tubos para la administración de la anestesia, (aunque el tubo orotraqueal lo disminuye) y la redistribución de la ventilación a las áreas no dependientes de los pulmones. El incremento del shunt (Qs/Qt) es una constante en el paciente sometido a anestesia general y, como se entenderá, es el resultado de las atelectasias y se correlaciona linealmente con ellas. El hecho de que el uso de la Presión Positiva al Final de la Espiración (PEEP, sigla inglesa) no mejore la caída de la PaOz, no desvirtúa la teoría pues la falta de respuesta parece depender de una caída del gasto cardíaco atribuible a la misma PEEP.
Papel tal vez más importante en la caída de la PaO2 es la inhibición del reflejo de vasoconstricción hipóxica, que permite la derivación del flujo vascular pulmonar a áreas pobremente ventiladas. Aún persisten grandes discusiones al respecto.
La mayor tasa de complicaciones cardiopulmonares deben esperarse en los pacientes sometidos a cirugía mayor del abdomen superior o del tórax.
Factores de riesgo de complicaciones pulmonares en el postoperatorio
Hábito de fumar. Se acepta que el fumar aumenta el riego de CPP. La disminución en la frecuencia de estas complicaciones sólo tiene significado estadístico después de transcurridas 8 semanas de la suspensión del hábito de fumar. Sin embargo, el solo hecho de la reducción de los niveles de carboxihemoglobina al abandonar el cigarrillo hacen recomendable dejar de fumar, resultando que cualquier período de tiempo puede ser benéfico.
Enfermedad pulmonar obstructiva crónica (EPOC). Una de las cirugías torácicas que con más frecuencia amerita resección de parénquima pulmonar es la cirugía del cáncer broncogénico. Tanto la EPOC como el cáncer del pulmón tienen directa relación con el uso del tabaco. Más adelante se señalarán las cifras límites en los volúmenes y flujos respiratorios que se constituyen en factor de riesgo. Muchas de estas alteraciones en la función pulmonar son atribuible s a la EPOC, al igual que el incremento de la PaC02. El tratamiento de la infección bronquial, los drenajes posturales, la inspirometría incentiva y la tos asistida, como manejo pre y postoperatorio en este grupo de pacientes, son útiles en mantener la expansión pulmonar, con beneficio adicional si se usan broncodilatadores inhalados. Las complicaciones son más frecuentes si las medidas se inician sólo en el postoperatorio que si se implementan desde antes de la cirugía.
Asma. Lo anotado en paciente con EPOC es válido para el enfermo asmático, pero en este último debe hacerse énfasis en la terapia farmacológica y comprobar el estado de obstrucción de las vías aéreas mediante pruebas de función pulmonar.
Factores de riesgo no pulmonares
Se pueden resumir en la siguiente lista:
– ASA. (Riesgo, de acuerdo con la American Society of Anesthesiology).
– Duración de la cirugía.
– Edad (mayor de 59 años).
– Sitio de la cirugía (mayor para cirugía abdominal alta).
– Obesidad.
– Sexo (masculino).
Efectos Funcionales de la resección pulmonar
Función pulmonar postoracotomía. Los cambios en la función ventilatoria después de una toracotomía medidos por la ventilación voluntaria máxima (VVM), persisten por 3 semanas y mejoran rápidamente entre la cuarta y la sexta semanas.
Los cambios ventilatorios no están completamente relacionados con el dolor incisional o con la magnitud de la resección y se ha comprobado que la limitación funcional de una toracotomía simple es similar a la de una lobectomía.
Los cambios en la distensibilidad propia de la pared torácica juegan un papel primordial, pues llegan hasta caídas de un 75%, consecutivos a toracotomía lateral para resección pulmonar, lo que debe compensarse, para mantener la ventilación con un aumento del trabajo respiratorio.
El paciente presenta hipoventilación alveolar y caída en la saturación de oxígeno que son más marcados entre el segundo y tercer días, pero que pueden persistir hasta por 10 días. El aumento en la producción de CO2 originado en el trauma quirúrgico, agrava la limitación ventilatoria. Por ser el lecho vascular pulmonar un sistema capaz de tolerar grandes aumentos de su volumen sin cambios significativos en la presión son posibles las lobectomías y las neumonectomías. Esto es cierto si el parénquima pulmonar residual es sano. Si existen enfermedades pulmonares difusas, lo cual es frecuente, se producirá, si se ha actuado sin una evaluación previa adecuada, hipertensión pulmonar que eventualmente conducirá a cor pulmonale. Si el parénquima pulmonar residual es normal sólo debe esperarse un aumento de la presión de la arteria pulmonar de un 10% de sus valores preoperatorios.
La estemotomía, con menos dolor postoperatorio y menor disminución en la distensibilidad de la pared torácica, produce pocos cambios en los volúmenes pulmonares a partir del 4° día, pues en los 3 primeros días no se logra demostrar una diferencia significativa en los volúmenes pulmonares de pacientes sometidos a estemotomía comparados con aquellos en quienes se ha practicado toracotomía lateral.
Comportamiento de la cavidad torácica después de resección pulmonar. Después de neumonectomía hay desplazamiento del mediastino lo que permite la sobre distensión del parénquima pulmonar residual, así como el lineamiento de toda la cavidad torácica. Con muy escasas excepciones, los intentos para evitar tal desplazamiento del mediastino y la sobre distensión pulmonar, como la toracoplastia, no se recomiendan desde hace varios años, pues deterioran aún más la función pulmonar.
Otros mecanismos que contribuyen a la resolución del espacio pleural residual postoperatorio son la elevación del hemidiafragma, la escoliosis con acercamiento de las costillas y la producción de tejido fibroso que llena la cavidad pleural vacía.
El espacio pleural residual después de resecciones pulmonares parciales (Iobectomía, segmentectomía o resección en cuña) debe ser evaluado para determinar si se trata de un espacio residual de bueno o de mal pronóstico, de acuerdo con la posibilidad de convertirse en un empiema o de deteriorar la función pulmonar residual. Son espacios pleurales residuales de buen pronóstico los pequeños, los que no crecen, los que tienen paredes delgadas, los que carecen de nivel hidroaéreo y los que no se acompañan de fiebre o leucocitosiso Un espacio que se aleje de estas características debe ser tratado quirúrgicamente.
Evaluación pulmonar preoperatoria
Se sabe que las pruebas de función pulmonar tienen un valor predictivo mayor que la historia clínica y el examen físico para predecir la aparición de CPP. La falta de claridad sobre lo que es realmente una CPP ha producido resultados bien distintos en los estudios prospectivos. Hallazgos postoperatorios esperados y por lo demás sin repercusión sobre los resultados finales, tales como hipoxemia mínima, caídas en los volúmenes pulmonares y la aparición de pequeñas atelectasias laminares, no deben llamarse complicaciones. Son verdaderas complicaciones aquellas que prolongan la estancia hospitalaria, incrementan los costos e incrementan la mortalidad.
Verdaderas complicaciones postoperatorias serían: atelectasias que requieren terapia específica, arritmias que ameriten tratamiento, bronquitis, hipotensión y shock, infarto del miocardio, neumonía, edema pulmonar, embolismo pulmonar y falla respiratoria.
Algunos autores basados en metanálisis parecen demostrar que las pruebas de función pulmonar son un mal predictor para pacientes con cirugía abdominal alta, pero siguen siendo de utilidad en los pacientes para cirugía resectiva del pulmón.
Las pruebas funcionales pulmonares (PFP) deben ser capaces de predecir:
1. Cuál es el riesgo de complicaciones pulmonares.
2. Cuánto parénquima pulmonar es resecable manteniendo una tasa de morbimortalidad postoperatoria tolerable y, por tanto, vislumbrar la calidad de vida respiratoria que tendrá el paciente en el postoperatorio tardío.
De acuerdo con el riesgo del desarrollo de complicaciones pulmonares en el postoperatorio se pueden establecer 5 grupos quirúrgicos con tasas decrecientes:
I. Cirugía torácica con resección pulmonar.
II. Cirugía torácica sin resección pulmonar.
III. Cirugía abdominal alta (Incisiones por encima del ombligo).
IV. Cirugía abdominal baja (Incisiones por debajo del ombligo).
V. Cirugía no torácica, no abdominal.
Aquellas cirugías que comprometerán la conciencia, así estén por fuera del tórax y del abdomen (neurocirugía, por ejemplo) deben clasificarse en los grupos de mayor riesgo.
La imposibilidad técnica de resección (especialmente para tumores) se llamará irresecabilidad. La imposibilidad funcional se denominará inoperabilidad.
Un principio importante debe tenerse siempre presente en la cirugía del cáncer del pulmón: cada paciente debe evaluarse como si fuera a ser sometido a neumonectomía, independiente de la probable resección decidida en el preoperatorio de acuerdo con el estado clínico, pues el hallazgo de lesiones que se extienden más allá de lo previsto y la necesidad latente de una neumbnectomía es un hecho real en todos los pacientes y que sucede con frecuencia en la práctica quirúrgica.
Con muy pocas excepciones, todos los pacientes que serán sometidos a resección parenquimatosa pulmonar deben tener como mínimo una prueba espirométrica, y los estudios más complejos se harán a medida que sean necesarios. Por esta razón se han determinado 3 pasos en la evaluación:
Paso 1: Espirometría
Gases arteriales.
Capacidad de difusión del ca.
Paso 2: Pruebas de función pulmonar unilateral:
Broncoespirometría
Pruebas en decúbito lateral.
Oclusión temporal de la arteria pulmonar.
Gamagrafía cuantitativa de perfusión pulmonar.
Paso 3: Pruebas de ejercicio
La broncoespirometría, las pruebas en decúbito lateral y la oclusión unilateral de la arteria pulmonar deben nombrarse sólo por su interés histórico.
Veamos el desarrollo de los 3 pasos:
PASO 1
Los parámetros absolutos de alto riesgo que se establecían eran:
CVF < 2L, VEFl < 1.5 L, FEF 25%-75% < 0.6 L/SEG, VVM<50%.
Valores expresados como porcentuales de la normalidad, deben reemplazar a estas cifras absolutas, que pueden ser bajos para un paciente de peso y talla altos pero normales para una persona de contextura pequeña. Las cifras porcentuales recomendables para predecir el riesgo se expresan en la Tabla 1.

Los pacientes clasificados funcionalmente como dudosos no deben rechazarse para cirugía sino ser sometidos a evaluaciones complementarias iniciando por una gamagrafía cuantitativa de perfusión pulmonar.
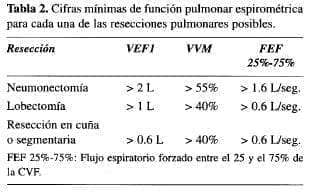
Las cifras mínimas de función pulmonar espirométrica para cada una de las resecciones pulmonares posibles han sido las establecidas en la Tabla 2; sin embargo, deberán sustituirse por los valores porcentuales establecidos para las variables antropométricas del paciente y por las cifras calculadas para el postoperatorio, como se establecerá más adelante.
Algunos estudios como el de Fergunson (1988) parecen demostrar que la DCco es el mejor predictor de complicaciones pulmonares en el postoperatorio. Esta es una prueba que habla del área disponible para intercambio gaseoso, la integridad de la membrana alveolar y el volumen sanguíneo capilar pulmonar.
Evaluar la función residual postoperatoria ha sido el objetivo de muchos trabajos y debe ser paso obligatorio en la evaluación de los pacientes que serán sometidos a resección de parénquima pulmonar. Desde que se llegó a establecer que la hipercapnia aparecía en los pacientes con EPOC que presentaban menos de 0.85 L de VEFl se dejó este parámetro como norma para el mínimo de VEFl postoperatorio calculado. Pero siendo, de nuevo, una cifra absoluta, es preferible declarar la inoperabilidad cuando el VEFl calculado es menor que el 35% de lo predicho para el paciente, pues tiene en cuenta sus variables antropométricas.
El cálculo del VEFl postoperatorio después de resecciones pulmonares, puede hacerse de varias maneras: VEFl postoperatorio= VEFl preoperatorio -% (No. segmentos por resecar/ 19 * Función).
En esta ecuación la función de los segmentos por resecar nace del estudio clínico y radiológico (ver ejemplos).
El total de segmentos de ambos pulmones es de 19.
Debe recordarse el número de segmentos para cada pulmón y para cada lóbulo, así:
Pulmón derecho: 10 segmentos (lóbulo superior 3; lóbulo medio 2; lóbulo inferior 5).
Pulmón izquierdo: 9 segmentos (lóbulo superior 5; lóbulo inferior 4).
Algunos ejemplos tratarán de aclarar este concepto.
Ejemplo 1
Un paciente será sometido a lobectomía superior derecha por un carcinoma broncogénico; su VEFl es de 2 L Yen la radiografía del tórax aparece una atelectasia del lóbulo superior derecho.
Discusión: En este paciente se resecarán 3 segmentos pulmonares correspondientes al lóbulo superior derecho, pero ellos no están aportando nada.a la función pulmonar pues ya aparecen atelectásicos en la radiografía; es decir, el paciente ya tiene una “auto-lobectomía”.
Entonces lps cálculos serían así:
VEFl (postoperatorio)= 2.0L -(3/19*0): 2.0 L-OL: 2.0 L.
La cifra supera los 0.85 litros por lo tanto el paciente es susceptible de cirugía. Será mejor determinar si esta cifra es superior al 35% de lo predicho para su sexo, edad y talla.
Ejemplo 2
Este paciente presenta un tumor del bronquio lobar superior encontrado en un estudio broncoscópico que trataba de aclarar la etiología de una expectoración hemoptoica en un paciente fumador. La radiografía del tórax es normal. En esta nueva situación los 3 segmentos del lóbulo superior derecho que será necesario resecar, sí estarían aportando volúmenes a la función pulmonar. Los resultados de los cálculos variarían de la siguiente manera:
VEFl (postoperatorio)= 2.0 -(3/19*1): 2.0-0.157: 1.843 L.
Estos resultados están por encima de 0.85 como cifra mínima de operabilidad, pero habría que confrontar, mejor aún, si representan más del 35% de lo esperado para las características del paciente en cuanto edad, sexo y talla.
Algunos autores incluyen un factor K, que es una variable de tiempo, dado que en los pacientes neumonectornizados la función predicha tiende a ser estable con el tiempo, pero en aquellos sometidos a lobectomía, la función mejora a medida que transcurre el tiempo postoperatorio.
PASO 2
Gamagrafía cuantitativa de perfusión
Cuando un paciente está clasificado como dudoso en las pruebas espirométricas hay indicación de progresar en su estudio con pruebas de perfusión o con pruebas de ejercicio. Estos exámenes han sustituido a pruebas invasoras como la broncoespirometría para medir consumo de oxígeno que requería la implantación de un tubo de doble luz o las pruebas en decúbito lateral que se usaron durante algún tiempo para tratar de definir la función pulmonar en el postoperatorio.
La gamagrafía de perfusión que establece con mayor certeza la perfusión de cada uno de los lóbulos, mejora la evaluación del VEFl postoperatorio.
La gamagrafía podría decimos que la perfusión de este lóbulo superior derecho representa el 18% del total de la perfusión de ambos pulmones; así el cálculo es más simple, pues el 18% de 2 L son 360 mL; entonces, el VEF1 postoperatorio será: 2.0 L – 0.36 L: 1.64 L. Recordemos que si esa cifra es mayor que el 35% de lo predicho para el paciente, la posibilidad quirúrgica debe mantenerse.
Otra forma de expresarlo es:
VEFl postoperatorio= VEF1 preoperatorio * Total de perfusión del pulmón residual: 2 litros * 82/100: 1.64 L.
La prueba de oclusión de la arteria pulmonar con balón para simular una neumonectomía, midiendo la presión media de la arteria pulmonar o la resistencia vascular pulmonar, son pruebas invasoras que no tienen un índice de predicción tan elevado que las justifique; de aquí que hayan sido suplantadas por las pruebas de ejercicio. Se consideran de riesgo una PAP mayor de 35 mm Hg o una resistencia mayor de 190 dinas/s por Cm-5.
PASO 3
Pruebas de ejercicio
Estas pruebas estarán indicadas si el valor del VEF1 postoperatorio calculado por gamagrafía cuantitativa de perfusión es inferior al 40%.
Eugene en 1982, encontró que aquellos pacientes sometidos a resección pulmonar y con consumos de oxígeno máximo en ejercicio (V02 máx.) menor de I L, presentaban una mortalidad del 75%. Ninguno murió si superaban esa cifra; sin embargo, cuando estos 2 grupos se compararon en sus volúmenes pulmonares no mostraban diferencias significativas.
El V02 máx. es aquel punto en el cual por más que se aumente el ejercicio no se incrementa el consumo de oxígeno, lo que representa la máxima eficiencia del sistema corazón pulmón- vasos-músculos. La cifra límite predictora de mortalidad y complicaciones tales como arritmias, atelectasias y neumonías, es de 15 mL/kg/min. llegando al 66% de complicaciones.
Cuando esta medición supera los 20 mL/kg/min. la tasa de complicaciones es inferior al 10%. Los pacientes con menos de 10 mL/kg/min. deben descartarse para cirugía, así las pruebas espirométricas sean adecuadas.
Mayor complejidad se ha agregado a esta evaluación, pero ensayos tan simples como la prueba de subir 3 pisos (76 escalas) han igualado su capacidad predictiva con exámenes más invasores y costosos, convirtiéndose en pruebas low tech aceptables de evaluación preoperatoria, pero de muy difícil estandarización.
Referencias
1. Bates D, Macklem P, Cristle R: Respiratory Function in Disease. W. Saunders Company, 1971
2. Delguercio L, Savino JP: Valoración Preoperatoria del individuo con alto riesgo quirúrgico. Clín Quirúrg Norteam, Vol 4. 1985
3. Fishman AP: Assessment of Pulmonary Function McGraw-Hill Book Company, 1980, pp. 779-809
4. Jaramillo RO: Pruebas de Función Pulmonar. Med de Caldas 1979; 1(4): 31-37
5. Jaramillo RO: Las bases de la cirugía torácica no cardíaca. Univ. de Caldas, 1995
6. Morice CR: Preoperative evaluation of the palient with lung cancer. In: Jack A. Roth, James D. Cox, Waun Ki H: Lung Cancer Blackwell Scientific publications. Boston, 1993
7. Nadel JA: Pulmonary Function Testing. Boston Univ School Med, 1978
8. Restrepo MJ, Maldonado D: Neumología. Fundamentos de Medicina Interna. 3a. Ed. Corp Investig Biológ, 1986
9. Tisi M: Preoperative Evaluation of Pulmonary Function. Am Rev Resp Dis 1979; 119: 296-306
10. Olsen GN: Pulmonary Phisiologic Assessment of Operative Risk. In: Thomas W. Shields. General Thorac Surg. Tomo 1. pp. 279-87, 1994
11. Olsen GN: Perioperative Respiratory Careo Clin Chest Med, WB. Saunders Comp. 14 (2), 1993
12. Wilson FA: Pulmonary Function Testing. Indications and Interpretations. Grune & Stratton, 1985
13. Wolfe W, Smith P: Preoperative Assessment of Pulmonary Function, In: Surgery of the Chest. Sabiston & Spencer pp. 1-20, 1990.
Correspondencia:
Doctor Osear Jaramillo Robledo. Departamento de Cirugía Pediátrica. Facultad de Medicina, U. de Caldas, Manizales.
COMENTARIO
Señor Editor:
Revisé detenidamente el artículo, “Evaluación Preoperatoria de la Función Pulmonar en el Paciente para Cirugía Torácica”. En este artículo existen conceptos que no comparto; por ejemplo, en la página 2 dice: “El desplazamiento del diafragma hacia el tórax originará atelectasias que aparecen tan rápido como 5 minutos después de la inducción de la anestesia.
Se presentan en las áreas más dependientes de los pulmones, no están correlacionadas con la edad o con la FI02 y son independientes de si la ventilación es espontánea o mecánica”. Yo pienso que es diferente si la respiración es espontánea o mecánica. Si lo primero, el paciente dormido respira con volúmenes corrientes bajos, pueden estar suprimidos los suspiros y esto favorece que se cierren múltiples unidades respiratorias ocasionando microatelectasias que crean un shunt de derecha a izquierda que se refleja en hipoxemia. Si la ventilación es mecánica, se adaptan volúmenes corrientes mayores que mantienen abiertas estas unidades respiratorias evitando las microatelectasias.
En la misma página 2 dice: “El hecho de que el uso de la presión positiva al final de la espiración, PEEP, no mejore la caída de la Pa02”. Yo creo que el PEEP se instala cuando comienza a descender la Pa02′ Y al comienzo sí mejora la saturación y la presión arterial de oxígeno. Si el paciente tiene un daño alveolar extenso probablemente no mejorará.
En la página 4 dice: “Los cambios ventilatorios no están completamente relacionados con el dolor incisional o con la magnitud de la resección”. Yo creo que sí están relacionados con la magnitud de la resección; no es lo mismo una toracotomía simple, que una resección de parénquima pulmonar. Tanto que los parámetros preoperatorios son diferentes si es toracotomía simple o si se hace resección como lobectomía.
Como puede ver, señor Editor, hay conceptos que no comparto, y me hubiera gustado que el autor los hubiera sustentado con citas bibliográficas insertadas en el texto.
Fidel Camacho Durán, MD, FACS, SCC.
Cirujano del tórax.
