Margarita María Velásquez Lopera, MD.
Dermatóloga,
Profesora Sección de Dermatología
Facultad de Medicina – Universidad de Antioquia
Correspondencia:
Dra. Margarita Velásquez, MD, Dermatóloga
Sección de Dermatología
Hospital Universitario San Vicente de Paúl
Medellín
El reconocimiento de la participación de mecanismos inmunológicos en la fisiopatología de muchas enfermedades ha estimulado el desarrollo de nuevas estrategias terapéuticas de inmunointervención como la fotoféresis. La radioféresis y la vacunación con células dendríticas. Las observaciones clínicas han mostrado efectos positivos y resultados alentadores en la utilización de estas terapias.
Palabras claves: Inmunointervención, fotoféresis, radioféresis, vacuna con células dendríticas.
Abstract
Acknowledgement of the participation of immunological mechanisms in the physiopathology of many diseases has promoted the development of strategic immunointervention therapies such as photoferesis, radioferesis and vaccination with dendritic cells. Clinical observations have shown positive and encouraging results in the use of these therapies.
Key Terms: Inmunointervention, photoferesis, radioferesis, vaccination with dendritic cells.
Introducción
El conocimiento de las bases inmunológicas de las diferentes enfermedades ha permitido el desarrollo de nuevas estrategias terapéuticas conocidas como inmunointervención. Éstas se refieren a la fotoféresis, la radioféresis y la vacunación con células dendríticas. Entre otras, utilizadas para el manejo de diversas condiciones no sólo dermatológicas si no sistémicas. Como el linfoma cutáneo de células T, la enfermedad injerto contra huésped y las enfermedades ampollosas autoinmunes.
En Estados Unidos y Europa, la fotoféresis se ha convertido en el tratamiento de primera línea para el manejo del linfoma cutáneo de células T. Especialmente en estadio de eritrodermia y ha despertado gran interés en la prevención y tratamiento del rechazo de trasplantes de órganos sólidos y células hematopoyéticas, por sus excelentes resultados en este grupo de pacientes. En la actualidad, diversos centros de trasplantes en el mundo incluyen la fotoféresis en sus protocolos pre y pos trasplante.
El Grupo de Inmunointervención de la Universidad de Antioquia actualmente realiza estudios clínicos e inmunológicos en una nueva modalidad de inmunointervención denominada radioféresis. La cual se fundamenta en los mismos principios terapéuticos de la fotoféresis. Para el manejo de pacientes con enfermedad injerto contra huésped y linfoma cutáneo de células T, con perspectivas de ampliar su uso a otras enfermedades mediadas inmunológicamente.
La investigación de alternativas terapéuticas para el cáncer, ha llevado a explorar y desarrollar vacunas basadas en la manipulación de las células dendríticas pulsadas con antígenos tumorales. Explotando las enormes capacidades de estas células para la presentación antigénica y estimulación de las respuestas citotóxicas. Esta terapia de inmunointervención plantea múltiples posibilidades y continúa motivando el interés científico para su optimización e implementación. De tal manera que el tratamiento con las vacunas de células dendríticas será una realidad en un futuro próximo.
Fotoféresis
La fotoféresis es una terapia de inmunointervención desarrollada inicialmente por el Doctor Richard Edelson y colaboradores en 1987, para el manejo del linfoma cutáneo de células T (LCCT). Sus aplicaciones clínicas han sido ampliadas a diversas enfermedades mediadas por clones de linfocitos T autorreactivos o malignos, como la enfermedad injerto contra huésped y las enfermedades ampollosas autoinmunes.
Descripción del procedimiento
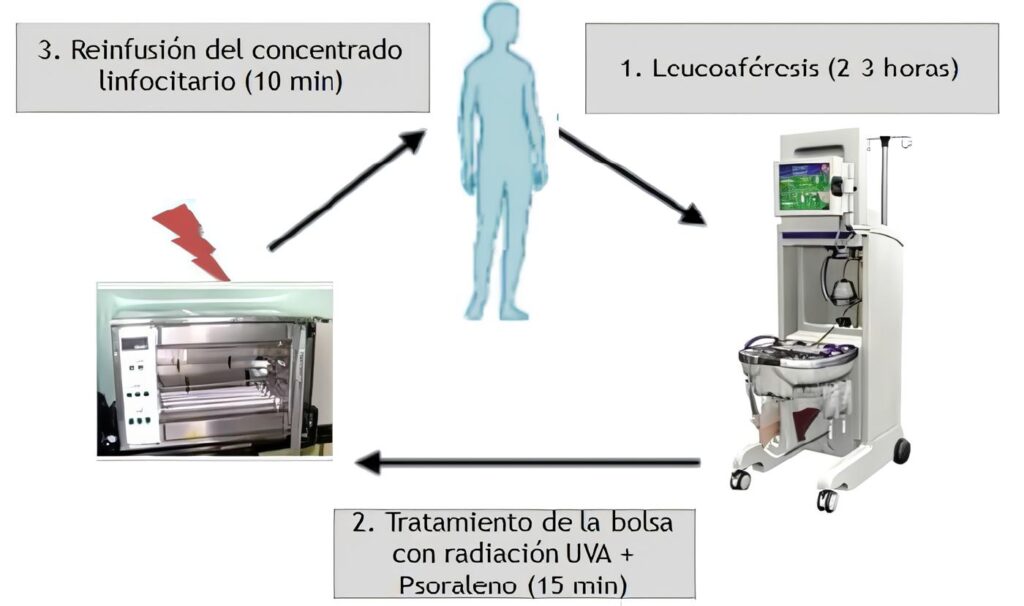
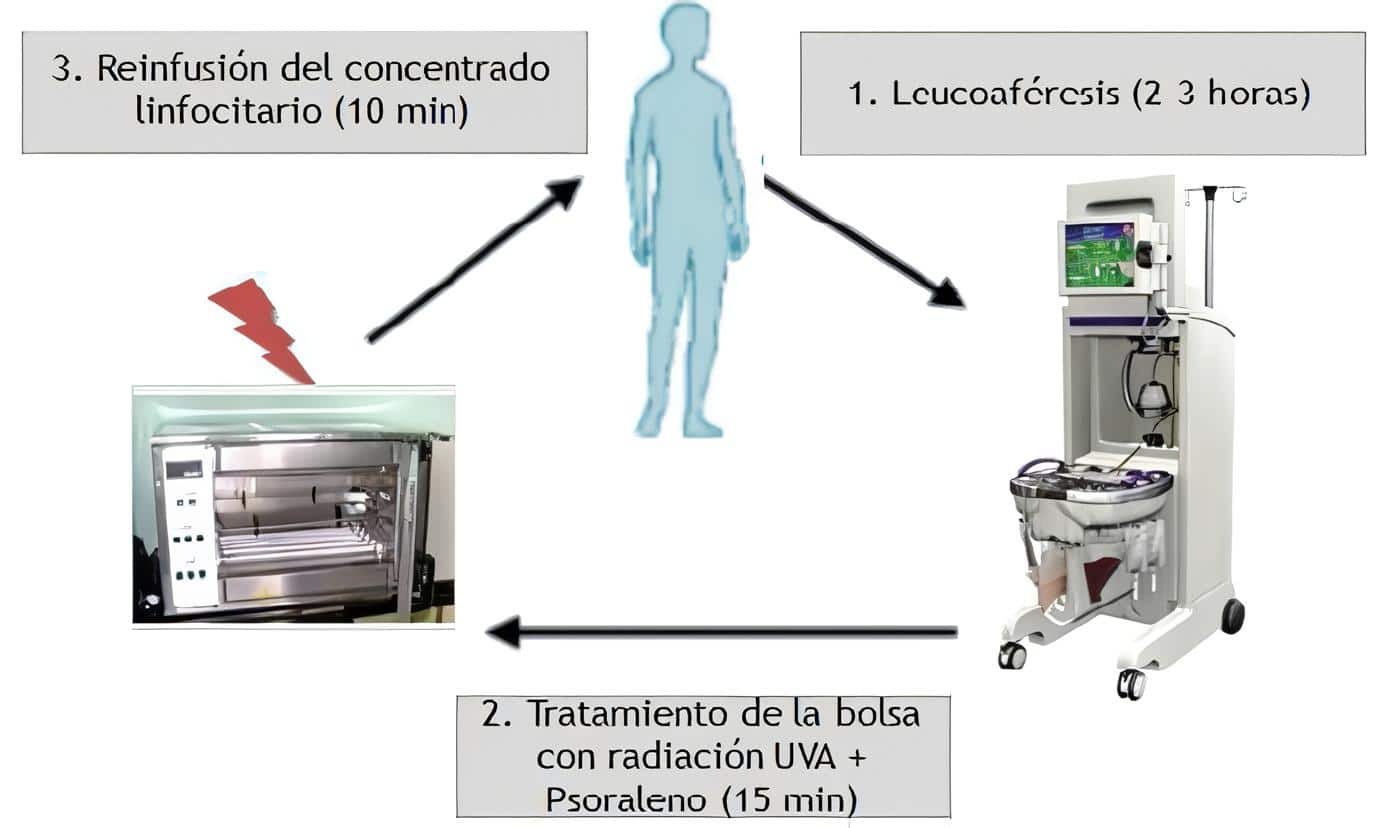
Esta terapia se fundamenta en la manipulación ex vivo de los leucocitos con un psoraleno fotoactivado, por medio de la máquina de fotoféresis. Por un acceso venoso periférico, se realiza una flebotomía de 1.000 a 1.500 cc de sangre, de la cual se separan los leucocitos por centrifugación (leucoféresis). El psoraleno es una sustancia fotosensibilizante que media la acción de esta terapia, puede administrarse en forma oral dos horas antes del procedimiento o en forma líquida directamente en la bolsa de leucocitos, con lo que se optimiza el procedimiento y se disminuyen sus efectos adversos fotosensibilizantes sistémicos.
En el interior de la máquina, los leucocitos pasan a través de una fotocelda donde reciben luz UVA a una intensidad de 2 Jouls/cm2. Al finalizar, las células son nuevamente recolectadas y reinfundidas al paciente. La duración total de una sesión de fotoféresis es de cuatro horas.
Diversos grupos en el mundo investigan acerca de sus mecanismos de acción, aplicaciones clínicas y modificaciones a la técnica, para potenciar su efecto de vacuna, entre ellos, el Doctor Richard Edelson y coinvestigadores, en la Universidad de Yale, quienes han diseñado una modificación en la cual las células no son reinfundidas inmediatamente sino luego de 12 a 18 horas de incubación en una cámara de CO2; esta técnica ha sido denominada transinmunización con fotoféresis.
Mecanismo de acción
Se ha comprobado que la fotoféresis induce inmunidad directa contra clones patógenos de linfocitos T, tanto malignos como autorreactivos, actuando sobre dos poblaciones celulares, los linfocitos T y las células dendríticas. Se considera que sus acciones inmunológicas son más amplias y los mecanismos de acción no están completamente esclarecidos.
-
Células T
En las células T patógenas, el psoraleno fotoactivado se une al DNA e inhibe el ciclo celular, lo que se traduce en muerte celular por apoptosis. Los linfocitos T normales no son modificados.
-
Células dendríticas
La fotoféresis estimula la conversión de monocitos a células dendríticas, aumentando su número en circulación, promoviendo su maduración. Estas células son presentadoras profesionales de antígeno que fagocitan y procesan los linfocitos T apoptóticos y presentan sus antígenos a los linfocitos CD8+ a través del HLA I. Los linfocitos CD8+ son los efectores de la respuesta antitumoral y de la regulación inmunológica, debido a su expansión clonal y a la respuesta citotóxica específica dirigida contra los linfocitos patógenos.
Las células dendríticas maduras están en baja concentración en la circulación (menor del 1%); la fotoféresis incrementa su número, propiedades inmunológicas y maduración por medio de la expresión de marcadores como las moléculas coestimulatorias (B7.1, B7.2 y CD40), moléculas de adhesión (CD11 a, b, c,) y moléculas de presentación antigénica (HLA clase I y clase II). Una molécula de superficie de gran importancia es el CD83, la cual solamente se expresa en las células dendríticas maduras y se considera un marcador específico.
Actualmente se investiga el efecto de la fotoféresis en la producción de citoquinas como la IL-6, IL-12 y TNF-a, y de quimioquinas por las células dendríticas.
-
Vacuna
El mecanismo de acción de vacuna se explica por que con la fotoféresis son directamente modificados menos del 5% de los leucocitos circulantes, de donde las células dendríticas procesan y presentan los antígenos para estimular la respuesta citotóxica específica que destruye a los linfocitos patógenos circulantes (no modificados directamente en el proceso). Atacando sólo a los que exhiban iguales características antigénicas, respetando a los linfocitos normales.
Usos clínicos
La principal indicación es el tratamiento del LCCT, con experiencia mundial desde 1987 en más de 150 unidades de fotoféresis. Las indicaciones clínicas para la terapia con fotoféresis son:
- Linfoma cutáneo de células T.
- Enfermedad injerto contra huésped aguda y crónica.
- Enfermedades ampollosas autoinmunes: pénfigo vulgar y foliáceo, penfigoide ampolloso.
- Escleroderma.
- Prevención del rechazo de trasplantes de órganos sólidos.
- Lupus eritematoso sistémico.
- Artritis reumatoidea.
- Líquen plano.
- Otras: SIDA, hepatitis autoinmune, esclerosis múltiple.
Linfoma cutáneo de células T
En Estados Unidos y Europa, la fotoféresis es el tratamiento de primera línea para la variante eritrodérmica del LCCT, debido a que en ésta se encuentra un alto número de células malignas circulantes que facilitan su acción. En estadios de placas o tumores, puede lograrse una excelente respuesta en los casos asociados a gran cantidad de células malignas en sangre periférica.
La mejoría clínica empieza a ser evidente después del tercer mes de tratamiento, lográndose la remisión total al sexto mes. Se evalúa desde el punto de vista clínico con la desaparición de las lesiones cutáneas, e inmunohistológico al demostrar la ausencia del clon maligno en las biopsias de piel y en los estudios moleculares de rearreglos de receptor del linfocito T (TCR).
Los factores predictores de una buena respuesta en el OCT son:
- Células de Sezary circulantes del 10 al 20%.
- Duración de la enfermedad menor de dos años.
- CD8+ y células NK normales.
- Relación CD4+/CD8+ baja, con alto número de CD8 y bajos CD4.
- Sin historia de quimioterapia intensiva.
- Sin compromiso linfático o visceral maligno.
La experiencia con el uso de esta terapia durante 13 años revela que el 25% de los pacientes obtienen una remisión completa con la fotoféresis como monoterapia, el 50% remisión completa con terapia combinada de fotoféresis y otros tratamientos como PUVA, haz de electrones, retinoides o con bajas dosis de quimioterapia, principalmente metotrexate, y únicamente el 25% de los pacientes no responden, lo cual se relaciona con los factores predictores mencionados. Sorprendentemente, la fotoféresis prolonga la sobrevida después del diagnóstico de OCT, desde 30 a 40 meses cuando se usan otras terapias hasta 100 meses cuando se usa fotoféresis.
Enfermedades ampollosas autoinmunes
La fotoféresis es de gran utilidad en los pacientes con pénfigo foliáceo y pénfigo vulgar, debido a que en estas enfermedades existen clones patógenos de células T autorreactivas contra epítopes de la desmogleína-1 y de la desmogleína-3, respectivamente, que desencadenan autoinmunidad al estimular a los linfocitos B. Con la fotoféresis, por medio del psoraleno fotoactivado, estos linfocitos T sufren apoptosis e inician la respuesta inmunológica ya descrita.
El manejo de las enfermedades ampollosas autoinmunes se ha fundamentado en el uso de medicamentos inmunosupresores a altas dosis. Los cuales no están exentos de severos efectos secundarios, especialmente con el uso de esteroides. Los cuales deben darse en la mayoría de los casos por períodos prolongados. A pesar de las alternativas farmacológicas, incluido el uso de azatioprina, ciclofosfamida y ciclosporina. Entre otros, existe un grupo de pacientes en quienes no se logra el control de la enfermedad y están en riesgo de presentar severos efectos secundarios de la terapia y fallecer a causa de la enfermedad de base y sus complicaciones.
La fotoféresis ha sido utilizada exitosamente para el tratamiento del pénfigo vulgar, pénfigo foliáceo y penfigoide ampolloso refractarios a los tratamientos. Logrando el control de la enfermedad, la disminución de autoanticuerpos y disminuyendo la necesidad de altas dosis de esteroides y de inmunosupresores. En la literatura se han reportado algunas series de pacientes con resultados promisorios, por lo que la investigación se dirige a implementar su uso en estas enfermedades.
Enfermedad injerto contra huésped
La enfermedad injerto contra huésped (EicH) se presenta principalmente después del trasplante de células hematopoyéticas y de órganos sólidos que contengan alto número de células linfoides. Debido a las diferencias de los antígenos de histocompatibilidad entre el donante y el receptor. Y por medio de diversos mecanismos inmunológicos, las células linfoides del injerto montan una respuesta que desencadena fenómenos aloreactivos y autorreactivos mediados por clones de linfocitos T. La fotoféresis es útil al modular estos clones T patógenos.
La EicH es una de las complicaciones más temidas después del trasplante de células hematopoyéticas, y la terapia convencional con inmunosupresores no es suficiente para controlarla en todos los pacientes. Los centros donde se dispone de esta terapia, la fotoféresis es usada exitosamente para el manejo de la EicH aguda y crónica, y como profilaxis en el régimen condicionante pre trasplante. En la EicH aguda es de gran utilidad en los grados II y III. En casos refractarios al tratamiento convencional con altas dosis de esteroides y en aquellos con compromiso de la piel y el hígado.
Con la fotoféresis puede obtenerse el control de la EicH:
Obteniendo la remisión completa y logrando una sobrevida libre de enfermedad. Las curvas de sobrevida de Kapplan y Meier muestran que los pacientes que obtienen remisión completa de la EicH con la fotoféresis tienen una probabilidad de sobrevida cercana al 100%. Luego de 60 meses después de su control y de haber suspendido la terapia con fotoféresis, sin recidiva a largo plazo. Los pacientes que no logran remisión completa de la EicH con la fotoféresis tienen una probabilidad de sobrevida menor del 20%.
La fotoféresis es una terapia con amplias posibilidades terapéuticas en este grupo de pacientes y actualmente se desarrollan estudios multicéntricos para su implementación y optimización. Diversos centros de trasplante en el mundo utilizan la fotoféresis en sus protocolos con excelentes resultados.
Esquema de tratamiento
El esquema utilizado para la mayoría de patologías es un ciclo de dos días consecutivos, cada cuatro semanas. Según el estadio clínico y severidad puede utilizarse cada dos semanas, y en el rechazo de trasplantes de órganos sólidos cada semana.
Efectos adversos
Los efectos adversos son mínimos y se asocian especialmente a la utilización del psoraleno por vía oral. En menos del 10% de los pacientes se presentan febrícula, náuseas, vómito, fotosensibilidad, prurito e hipotensión.
Especificidad
La fotoféresis es altamente específica, sólo destruye el clon patógeno preservando las otras vías del sistema inmunológico. No incrementa las infecciones oportunistas y no desencadena fenómenos de autoinmunidad.