El descubrimiento de la deficiencia de surfactante (que viene del inglés Surface active agent en los pulmones “hepatizados” de los niños que morían por EMH se debió a interacciones con muchos investigadores de diferentes disciplinas (12). En Inglaterra, Richard Pattle había investigado la espuma del edema pulmonar, porque algunos gases usados en la guerra inducían edema pulmonar y se investigaban agentes “anti-espuma” para contrarrestar dicho efecto. La gran estabilidad de las burbujas del pulmón normal, le llevó a concluir que se debían haber originado en el alvéolo el cual debería estar recubierto con una capa de baja tensión superficial. Pattle sugirió que la ausencia de dicha sustancia de recubrimiento alveolar podría ser una de las dificultades que enfrentaba un niño prematuro y que, en algunos casos, causaría atelectasia. Esta predicción fue ignorada durante mucho tiempo por los clínicos.
Posteriormente, Clements estudió los cambios en la tensión superficial dependientes del área, observando que a grandes volúmenes pulmonares, la tensión superficial es alta, mientras que a bajos volúmenes pulmonares la tensión se aproxima a cero. En 1957, Clements denominó “surfactante pulmonar” al material que presumiblemente se localizaba en la interfase alvéolo-aire y lo consideró un factor anti-atelectásico.
En 1958, Pattle informó que las burbujas de los pulmones de conejillos de India eran inestables y al año siguiente, Mary Elen Avery y Jere Mead, describieron la incapacidad de los extractos obtenidos de niños que murieron por EMH para disminuir la tensión superficial (13). La EMH de los niños prematuros se debe a una falla primaria de los neumocitos tipo II para producir los CL que son la forma de almacenamiento y secreción del surfactante pulmonar. Estos niños no alcanzan la maduración suficiente de los neumocitos tipo II y de otras estructuras pulmonares.
Neumocitos y producción de surfactante
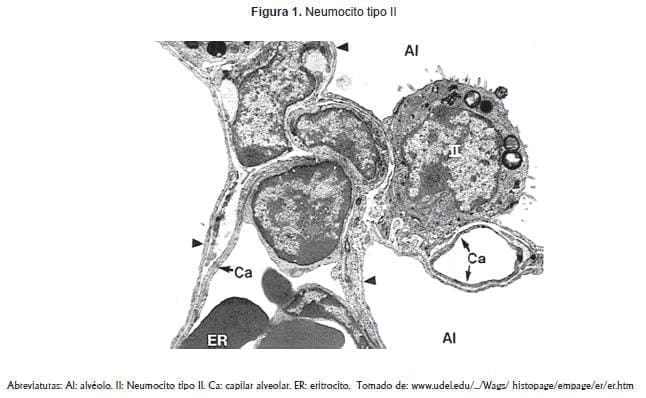
El sistema alveolar tiene dos tipos de células epiteliales, los neumocitos (tipos I y II) y los macrófagos. Los neumocitos tipo I cubren el 95% de la superficie alveolar y son células aplanadas que contienen unas pocas organelas. Los macrófagos están involucrados en la remoción de surfactante, partículas y microorganismos que ingresan con el aire. Los neumocitos tipo II son responsables de la síntesis, empaquetamiento y secreción del surfactante pulmonar; también hacen la re-captación de los componentes del surfactante desde el espacio alveolar y los reutilizan para la secreción (14). Los neumocitos tipo II se caracterizan por la presencia de CL) de 0.2 a 2 μm de diámetro que constituyen un 18 a 24% del citoplasma (https://encolombia.com/medicina/academedicina/Academ320110/Figura 1). Estos CL son la forma de almacenamiento del surfactante pulmonar (15) el cual, además de reducir la tensión superficial para evitar el colapso alveolar, juega un papel muy importante en la protección antioxidante, la inhibición de la exudación de líquido desde el capilar hacia el alvéolo y la defensa contra la infección pulmonar.
El surfactante pulmonar está compuesto por un complejo de fosfolípidos y proteínas. La composición del surfactante pulmonar de numerosas especies de mamíferos es muy similar. Un 80 a 90% del peso del complejo lo constituyen los glicerofosfolípidos, un 10% está dado por el colesterol y el 10% restante por las apoproteínas pulmonares incluyendo SP-A (abreviatura en inglés de proteína surfactante A), SP-B, SP-C y SP-D (16). La principal apolipoproteína es la sialoglicoproteína SP-A (17). EL surfactante también contiene pequeñas cantidades de triglicéridos y ácidos grasos libres. EL https://encolombia.com/medicina/academedicina/Academ320110/Cuadro 1 muestra la composición de fosfolípidos del surfactante pulmonar humano.
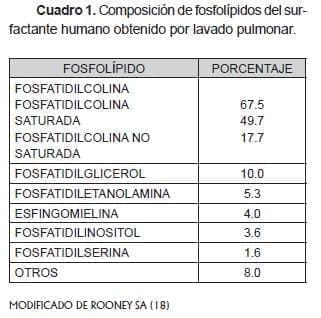
Los fosfolípidos más abundantes en el surfactante pulmonar son la fosfatidilcolina (lecitina o dipalmitoil-lecitina), que constituye el 70 a 80%, y el fosfatidilglicerol, que constituye un 5 a 10%. Cerca del 70% de la fosfatidilcolina es saturada con dos residuos de ácido palmítico (dipalmitoilfosfatidilcolina, denominada también dipalmitoillecitina o simplemente lecitina). Este componente es el principal responsable de disminuir la tensión superficial y dar estabilidad al alvéolo. La dipalmitoil-fosfatidilcolina tiene un extremo polar e hidrofílico, dado por el residuo colina, el cual se orienta hacia el líquido alveolar, y un extremo no polar e hidrofóbico, dado por las cadenas de ácido palmítico, que se orienta hacia el aire.
El 10% del surfactante pulmonar está constituido por las apoproteínas SP-A, SP-B, SP-C y SP-D asociadas a los lípidos. Estas proteínas regulan la estructura, propiedades biofísicas y metabolismo de las lipoproteínas. La proteína SP-A es una proteína multimérica que tiene un peso molecular de 26 a 38 kDa. Esta apoproteína tiene un papel muy importante en el ensamblaje y mantenimiento de la monocapa alveolar ya que controla la secreción y captación del surfactante pulmonar por los neumocitos tipo II. La SP-A también juega un papel en la inmunomodulación, aumentando la migración y capacidad fagocítica de los macrófagos alveolares (19).
La SP-A media la actividad micoplasmicida de los macrófagos alveolares (20) e interviene en la eliminación del Streptococcus del grupo B. El factor de necrosis tumoral alfa inhibe el RNA mensajero y la síntesis de SP-A, por lo que podría ser un factor para el SDR; mientras que, en fetos con corioamnionitis, la elevación de la interleukina-6 promueve la maduración pulmonar fetal induciendo la síntesis de SP-A y disminuyendo el SDR en los neonatos (21).
La SP-A también inhibe la secreción de fosfatidilcolina y facilita la captación de fosfolípidos por los neumocitos tipo II. Los fosfolípidos y la SP-A se secretan coordinadamente al alvéolo (22).
La apoproteína SP-B se secreta en forma independiente de los CL. La forma madura de la proteína tiene un peso molecular de 7 a 8 kDa y tiene una distribución periódica de residuos polares y no polares característicos de proteínas asociadas a superficies de membrana de las interfases aire/ líquido (22).
La secreción del surfactante ocurre mediante exocitosis de los CL. El proceso ocurre por fusión de la membrana limitante que rodea los CL con la membrana plasmática del los neumocitos tipo II. La secreción in vitro del surfactante es estimulada por los agonistas β-adrenérgicos, catecolaminas, adenosina y toxina del cólera, agentes éstos que activan la adenilciclasa e incrementan el AMP cíclico (AMPc). La síntesis de surfactante es estimulada también por glucocorticoides, prolactina, hormonas tiroideas, insulina y estrógenos (22, 23).
La depuración del surfactante de los alvéolos puede ocurrir por varias vías incluyendo ingestión por macrófagos alveolares, ascenso a las vías aéreas, degradación enzimática en la superficie alveolar y re-captación por neumocitos tipo II y otras células. El surfactante puede ser internalizado nuevamente a los CL y secretado; un 25 a 95% del surfactante pulmonar hace reciclaje (24).
