Resumen
La inteligencia artificial (IA) está remodelando rápidamente la investigación en cáncer, al igual que la atención clínica personalizada.
La disponibilidad de conjuntos de datos de alta dimensionalidad junto con los avances en la computación de alto rendimiento y de las arquitecturas innovadoras de aprendizaje profundo ha llevado a una explosión en el uso de la IA en varios aspectos de la práctica e investigación oncológica.
Estas aplicaciones van desde la detección y clasificación de diversas neoplasias, su caracterización molecular incluyendo la evaluación del microambiente tumoral, el descubrimiento y la reutilización de medicamentos, y la predicción de los resultados derivados del tratamiento.
A medida que estos avances penetren en la práctica clínica, se prevé un cambio de paradigma en la atención que se verá fuertemente impulsado por la IA.
Palabras clave: Inteligencia artificial (IA); cáncer; oncología; tratamiento personalizado; terapia; diagnóstico; medicina de precisión.
Systems and Computational Biology in Cancer: From the Basics to the Next Frontier
Abstract
Artificial intelligence (AI) is rapidly reshaping cancer research, as is personalized clinical care.
The availability of high-dimensional data sets coupled with advances in high-performance computing and innovative deep learning architectures has led to an explosion in the use of AI in various aspects of oncology practice and research.
These applications range from detecting and classifying multiple neoplasms, their molecular characterization, including evaluating the tumor microenvironment, the discovery and reuse of drugs, and the prediction of the results derived from the treatment.
As these advances penetrate clinical practice, a paradigm shift in care is anticipated AI will powerfully drive that.
Keywords: Artificial intelligence (AI); Cancer; Oncology; Personalized treatment; Therapy; Diagnostic; Precision medicine.
Introducción – Biología de Sistemas y Computacional en Cáncer
El cáncer es un problema sanitario creciente a nivel global con una importante repercusión en salud pública y sobre la economía de los países con ingresos medios y altos.
De acuerdo con la Organización Mundial de la Salud (OMS), el cáncer es la segunda causa principal de muerte a nivel mundial, y aproximadamente se diagnosticaron 20 millones de nuevos casos y 10 millones de muertes por esta enfermedad en el 2020.
La Agencia Internacional para la Investigación del Cáncer (IARC) estima que una de cada cinco personas desarrollará cáncer a lo largo de su vida. Este flagelo está afectando de manera desproporcionada a los países con ingresos bajos y medios donde la incidencia explica cerca del 70% de las muertes anuales por la enfermedad.
En paralelo, diversas innovaciones en el diagnóstico y tratamiento han mejorado los resultados y la calidad de vida de los pacientes afectos. En concordancia, las tasas globales de mortalidad estandarizadas por la edad han mostrado una disminución del 17% entre 1990 y 2016, hallazgo asociado a la evaluación de la atención que se ha hecho altamente especializada y compleja (1).
Adicionalmente, la enorme afluencia de información derivada de la investigación básica, clínica y de transferencia, se ha traducido en la inclusión de terapias novedosas que usan blancos moleculares específicos, medicamentos biológicos, terapias celulares y génicas, además de la configuración de un sistema avanzado de diagnóstico y apoyo terapéutico que incluye a la patología molecular y la radiómica.
Este modelo requiere de un sistema multidisciplinario integrado para la prestación de la atención, al igual que herramientas que permitan el análisis avanzado de datos (2).
El término inteligencia artificial (IA) se acuñó por primera vez para el Taller de computación de verano de Dartmouth en 1956, donde se designó en remplazo de las “máquinas pensantes”.
En condiciones simples, la IA se puede definir como la capacidad que tiene una máquina para aprender y reconocer patrones y relaciones a partir de ejemplos y hechos representativos con la finalidad de utilizar esta información de manera práctica y eficaz en la toma de decisiones. La AI abarca, y en ocasiones se usa como sinónimo de aprendizaje automatizado (machine learning, ML) y profundo (deep learning, DL). En términos generales, el ML es un subcampo de la IA y el DL es el subconjunto que se centra en las redes neuronales artificiales profundas (es decir, redes neuronales artificiales con múltiples capas ocultas completamente interconectadas – deep artificial neural networks) (Figura 1).

Figura 1. Relación entre la IA, aprendizaje automático y aprendizaje profundo, con algoritmos de uso común (como ejemplos. CART: árboles de clasificación y regresión; CNN: Redes neuronales convolucionales; DNN: redes neuronales profundas; LASSO: Operador de Selección y Contracción Mínima Absoluta; SVM: Máquinas vectoriales de soporte).
En los últimos años, el DL ha ganado un enorme impulso debido al éxito para la gestión de visión automatizada que incluye el reconocimiento facial y la clasificación de imágenes (3).
Esta propiedad del DL ha extendido su aplicabilidad a varios aspectos de la investigación básica, clínica y de transferencia, todos relacionados con la oncología de precisión. Entre otros, cabe mencionar el desarrollo de redes neuronales convolucionales (CNN) para la identificación y clasificación de imágenes, el progreso de la patología digital, y la bioinformática y biología computacional para facilitar el entendimiento de problemas orgánicos complejos propios de la evolución clonal y subclonal de los tumores sólidos y hematológicos (4).
Redes neuronales convolucionales: herramienta primaria para la clasificación de imágenes
Las CNNs han sido la arquitectura de DL más popular y utilizada para la clasificación de imágenes en cáncer (Figura 1).
Las CNNs aplican una serie de transformaciones no lineales a los datos estructurados (como los píxeles sin procesar de una imagen) para aprender características relevantes, a diferencia de los modelos de aprendizaje automatizado convencionales que con frecuencia requieren la curación manual de características.
Por otra parte, aún es difícil saber qué funciones aprenden e integran las CNNs, lo que las convierte en lo que se ha denominado una “caja negra”. Una consecuencia es que las imágenes utilizadas en las CNNs deben procesarse previamente para reducir el riesgo de que el modelo incluya los artefactos de la imagen.
Hay dos enfoques principales para los modelos de las CNNs, uno es el aprendizaje por transferencia que utiliza imágenes obtenidas y promovidas de una gran colección de objetos naturales (como en ImageNet) con el fin de entrenar las capas iniciales (donde el modelo aprende a identificar características generales como formas y bordes), y luego, el sistema usa los datos específicos de la enfermedad para ajustar los parámetros de entrenamiento en las capas finales (5).
La segunda variación de las CNNs se basa en un codificador automático en el que el modelo aprende diversas propiedades de fondo de un subconjunto de imágenes representativas y codifica una figura comprimida de los caracteres básicos que se utilizarán para inicializar el proceso.
En el CAMELYON16 Challenge, se utiliza una función de colaboración colectiva para identificar y clasificar las metástasis en los ganglios de pacientes con cáncer de mama a partir de imágenes de diapositivas completas (WSI) obtenidas a partir de tumores expuestos a hematoxilina y eosina (H&E).
Para este caso, 25 de los 32 algoritmos presentados incluyen CNNs que se basan exclusivamente en el aprendizaje por transferencia, como lo hace GoogLeNet, ResNet, VGG-16 (6).
Khosravi y colaboradores entrenaron y probaron varios modelos de DL de vanguardia para clasificar los WSI provenientes de tejidos tumorales tomados de una de las cohortes provenientes del Atlas Genómico del Cáncer (TCGA, del ingles The Cancer Genome Atlas) (5,6).
Generación de modelos predictivos a partir de grandes conjuntos de datos – Biología de Sistemas y Computacional en Cáncer
En la última década, varias iniciativas internacionales multinstitucionales han dado lugar a la generación de grandes conjuntos de datos sobre la biología molecular del cáncer.
Estos grupos se obtienen de la elaboración de perfiles “ómicos” de muestras biológicas de diversas neoplasias a través de plataformas y tecnologías de alto rendimiento. Los datos se utilizan para diseñar modelos predictivos que maximizan la toma de decisiones clínicas (Figura 2).

Figura 2. Descripción general de los conceptos básicos del aprendizaje automatizado. Conjuntos de datos derivados del paciente que se utilizan para el diseño de los modelos de IA con el objetivo de acelerar la atención del cáncer desde el banco de tejido hasta la cabecera de la cama.
El TCGA es, por mucho, la compilación más completa de acceso libre para el público que permite el análisis de perfiles que incluyen radiómica, genómica, epigenómica, proteómica e histopatología (5,6).
Otros esfuerzos, como PCAWG (del ingles, Pan-Cancer Analysis of Whole Genomes), METABRIC y GENIE, también han recopilado abundante información con disposición abierta.
La tecnología para generar los perfiles ha evolucionado desde el análisis monogénico hasta la valoración exómica (WES, del ingles wide exome sequencing) y genómica completa (WGS, del ingles wide genoma sequencing). En la misma dimensión, la expresión génica se transformó desde el estudio de microarreglos (microarrays) hasta la secuenciación global de ARN (RNAseq) y en una célula única (single cell analysis).
Otras aplicaciones de vanguardia permiten la producción de programas para caracterización de la metilación, perfiles de proteómica, estudios de perturbación que incluyen ensayos de viabilidad celular o citotoxicidad usando terapias blanco dirigidas (moléculas pequeñas), ARN de interferencia (ARNi), pantallas de CRISP y diseños para redes de interacción proteína-proteína (interactoma tumoral).
A partir de la estructuración y organización de esta información se ha logrado el entrenamiento de modelos usando DL que permite la correcta predicción de la supervivencia libre de progresión y global en múltiples tumores sólidos avanzados (7).
Cheerla y colaboradores, desarrollaron el sistema BANDIT siguiendo un enfoque de ML Bayesiano para predecir la utilidad de diversas moléculas farmacológicamente activas sobre oncoproteínas activas (8).
Al integrar el modelo BANDIT con las bases de datos públicas, el modelo logró identificar con una precisión próxima al 90% más de 2.000 medicamentos potenciales.
Posteriormente, la plataforma logró discriminar 14.000 compuestos en estudio con potenciales blancos terapéuticos, a partir de una interacción in silico molécula- objetivo previamente desconocida (8).
A partir de este conjunto, se validaron 14 nuevos inhibidores de microtúbulos, incluidos 3 con actividad sobre células tumorales multirresistentes.
Como prueba de resistencia, el BANDIT logró identificar que el compuesto ONC201 resultó ser un fuerte inhibidor de DDR2, alteración común en los carcinomas de pulmón de células no pequeñas (2,3%), tumores sinunasales (4,6%), adenocarcinoma de la unión gastroesofágica (2,0%), y carcinoma urotelial (4,0%). Este hallazgo, permitió la planeación de un experimento clínico canasta de precisión (8).
En igual dimensión, Madhukar y colaboradores diseñaron un modelo de ML para predecir a partir de datos panómicos el uso de moléculas en estudio. Esta plataforma permitió predecir con exactitud el 78% de la respuesta a potenciales nuevos fármacos (9).
Calidad de los datos y selección del modelo – Biología de Sistemas y Computacional en Cáncer
La estrategia básica para los flujos de trabajo del ML aplicado a la oncología sigue un patrón estándar (Figura 3).

Figura 3. Pasos básicos en los flujos de trabajo del clasificador de aprendizaje automatizado (AUROC: Área bajo la curva de características operativas del receptor; AUPRC: Área bajo la curva de recuperación de precisión; DL: Aprendizaje profundo).
El primer componente del modelo es la recopilación y depuración de la información, seguido de la inspección y corrección de fallos además de los ajustes para disminuir la varianza.
El ajuste excesivo del modelo puede generalizar inadecuadamente la información generando sesgos, por lo que se requieren estrategias de validación cruzada, el aumento del tamaño muestral en el conjunto de entrenamiento, y la selección manual de las características útiles para predecir. Otro de los pasos esenciales dentro de los modelos de ML es su ajuste en función del rendimiento.
La productividad se mide comúnmente utilizando el área bajo la curva del receptor (AUROC o simplemente AUC) que cuantifica el equilibrio entre la sensibilidad y la especificidad. Un buen clasificador dentro del modelo de ML debe lograr un nivel mayor a 0,80, sin embargo, el umbral se considera clínicamente aceptable dependiendo de cada indicación clínica.
Después de entrenar y probar un modelo en una cohorte determinada (generalmente dividido en conjuntos de entrenamiento y prueba) es importante validar el modelo en un conjunto de datos externos e independientes para favorecer la estabilidad y la generalización. Es por esto que el desarrollo de las plataformas de IA aplicables al diagnóstico y tratamiento del cáncer siguen la complejidad de la enfermedad de una forma dinámica.
Los modelos requieren ajustes dinámicos en subconjuntos de datos provenientes de casos o pacientes que expliquen la heterogeneidad y variabilidad de la enfermedad. De igual forma, se requiere el mantenimiento rutinario del modelo con el fin de garantizar su rendimiento evitando la degradación de los conceptos de entrada y salida que con el tiempo sufren cambios imprevistos (10).
La Figura 4 ilustra los modos en que la IA que permiten el desarrollo de la atención clínica en cáncer, así como el impulso de la investigación básica y de transferencia.
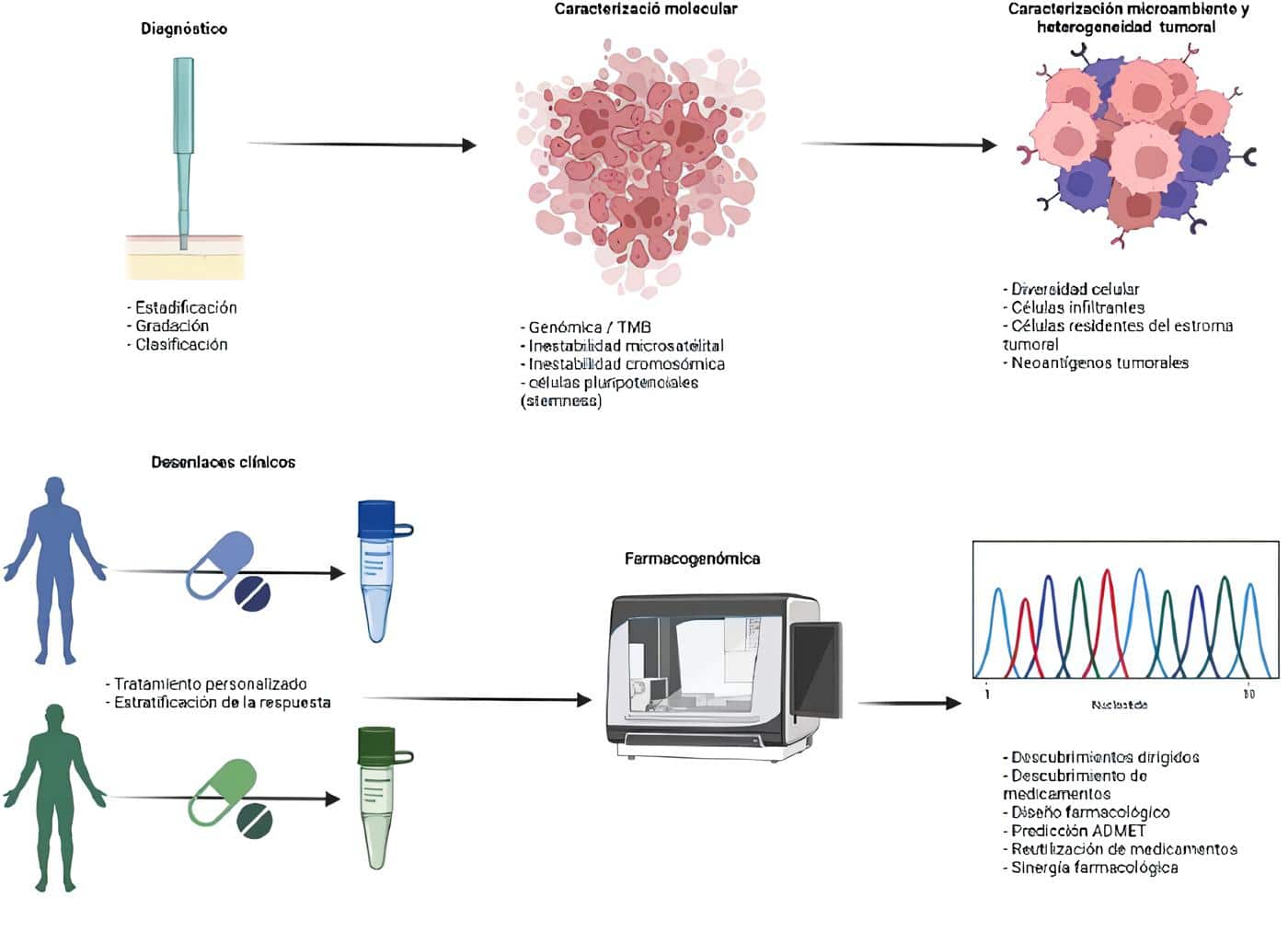
Figura 4. Aplicaciones de la IA en la investigación del cáncer y la medicina de precisión (ADMET: absorción, distribución, metabolismo, excreción y toxicidad).
Detección temprana, diagnóstico y estadificación de la enfermedad – Biología de Sistemas y Computacional en Cáncer
La detección de la enfermedad, la precisión del diagnóstico y la estadificación son determinantes claves para determinar la evolución biológica y la toma de decisiones clínicas y sus resultados. En pocos años, la IA ha realizado contribuciones significativas en esta área crítica para la oncología, algunas veces con un rendimiento comparable al de profesionales expertos, y con una ventaja adicional dada por la escalabilidad y la automatización (11).
Diagnósticos más precisos – Biología de Sistemas y Computacional en Cáncer
Diferentes estudios han demostrado la viabilidad de implementar modelos basados en ML para optimizar el diagnóstico de diversos tumores sólidos y hematológicos a partir de muestras patológicas y de radiología convencional o avanzada.
Las redes neuronales profundas (DNN) representan algoritmos poderosos que permiten aumentar la precisión del diagnóstico y la identificación de subtipos genómicos a partir de análisis moleculares o de patología convencional.
La patología digital permite diferenciar las células normales de las tumorales con una precisión próxima al 99%, especialmente para el segmento de enfermedades con mayor incidencia. De igual forma, las DNN también se utilizan para clasificar el proceso histológico evolutivo de la enfermedad, como ocurre desde las lesiones preinvasivas hasta las infiltrantes en cáncer gástrico y de colón (12,13).
Como ejemplo, Coudray y colaboradores desarrollaron un modelo basado en la arquitectura DeepPATH Inception-v3 (red neuronal convolucional profunda; https://github.com/ncoudray/DeepPATH.) para clasificar simultáneamente los caracteres histológicos y genómicos de una cohorte de muestras de adenocarcinoma de pulmón del TCGA (14).
El rendimiento del método resultó comparable al de los patólogos, con un área media bajo la curva de 0,97. Adicionalmente, el modelo fue capaz de discriminar los caracteres histológicos a partir de tejidos congelados, incluidos en parafina y de biopsias frescas.
La red también fue entrenada para discriminar los patrones patológicos determinantes de las diez mutaciones más frecuentes en el adenocarcinoma, logrando un rendimiento óptimo para seis de ellas (STK11, EGFR, FAT1, SETBP1, KRAS y TP53); para estos casos, el rendimiento del modelo tuvo una AUC de 0,73 a 0,85 (14).
El éxito de las DNN no se limita a la histopatología, sino que se extiende a otras imágenes diagnósticas obtenidas mediante técnicas no invasivas incluyendo fotografías de la piel, tomografías computarizadas, la mamografía y la resonancia magnética.
La clasificación automatizada de las lesiones cutáneas mediante imágenes es una tarea desafiante debido a la variabilidad de grano fino en la apariencia de las mismas.
Las redes neuronales convolucionales (CNN) han demostrado potencial para establecer patrones a partir de lesiones cutáneas con alta variabilidad de presentación clínica, utilizando únicamente píxeles y etiquetas como entradas. Esteva y colaboradores, entrenaron una CNN (arquitectura Inception-V3) a partir de un conjunto de datos de 129.450 imágenes de pacientes.
El estudio probó el desempeño del modelo contra 21 dermatólogos certificados y las biopsias de 2.032 casos encontrando que la clasificación de los carcinomas basocelulares y escamocelulares, además de los melanomas hecha por la CNN superó la precisión media humana (AUC 0,91 a 0,94) (15).
En el ámbito de la radiología, Anthimopoulos y colaboradores demostraron que la información obtenida de las tomografías de pacientes con cáncer se puede utilizar para construir una DNN capaz de clasificar los patrones y texturas de las lesiones pulmonares (opacidades en vidrio esmerilado, micronódulos, y nódulos de patrón sólido) con una precisión media de 0,85 (16).
De forma similar, Jian y su grupo de estudio utilizaron tomografías computarizadas para desarrollar una DNN útil para predecir la presencia de metástasis peritoneales ocultas en pacientes con cáncer gástrico (AUC entre 0,92 y 0,94), incluso mejor que lo obtenido a partir de la integración de las características clínicas y patológicas de la enfermedad (AUC 0,51 a 0,63) (17).
En otro estudio, Wang y colaboradores utilizaron las imágenes de resonancias magnéticas de172 pacientes con cáncer de próstata para entrenar y probar el rendimiento de una DNN (desarrollado utilizando el marco de aprendizaje profundo de Caffe por Berkeley AI Research) capaz de distinguir la presencia de lesiones benignas versus alteraciones nodulares sospechosas, alcanzando una productividad media de 0,84 (18).
Por otra parte, y dada la importancia pública del cribado para cáncer de mama, McKinney y colaboradores desarrollaron un estudio retrospectivo valorando el resultado de las mamografías realizadas a una cohorte de pacientes a quienes se realizó biopsia de seno.
A partir de tres modelos independientes de ML se logró realizar una escala de riesgo para cáncer de seno teniendo en cuenta la información derivada de las imágenes de 29.000 mujeres (AUC 0,75 a 0,88) (19).
El mismo grupo informó una mejora en la sensibilidad y especificidad versus la impresión del radiólogo que oscilo entre el 1,5-5,7% y 2,7-9,4%, respectivamente. La notable acumulación de información sobre la utilidad diagnóstica de la AI en cáncer ha permitido la implementación y puesta a punto de estudios clínicos con asignación aleatoria que permitirán confirmar o desechar estos resultados.
El alcance de esta información podría llegar al análisis automatizado de los datos clínicos a partir de aplicaciones asistidas por IA e instaladas en teléfonos inteligentes, evento que favorecería el diagnóstico temprano, la prevención y la promoción a partir de un dispositivo electrónico colocado en la mano del usuario (20,21).
Por convenientes y prometedoras que parezcan estas impresiones, la precisión diagnóstica de tales aplicaciones localizadas en teléfonos inteligentes aún debe validarse clínicamente. Por el momento parecen especialmente preocupantes los falsos negativos, ya que pueden retrasar al paciente para obtener atención médica oportuna (21).
Estadificación y clasificación del cáncer
La estadificación y correcta clasificación tumoral es uno de los componentes esenciales del proceso diagnóstico del cáncer. De hecho, la estadificación define y modifica dinámicamente las opciones terapéuticas, desde una conducta expectante hasta la cirugía o el uso de la radioterapia, quimioterapia, inmunoterapia o intervenciones blanco dirigidas.
Parte de la estadificación del cáncer de próstata incluye el puntaje de Gleason, una combinación de dos variables que miden la frecuencia de células tumorales en dos ubicaciones diferentes en la misma patología.
Las DNNs ha mostrado resultados prometedores en la predicción de la puntuación del Gleason a partir de patologías convencionales. Nagpal y colaboradores utilizaron un modelo de ML capacitado para valorar secuencias de patologías de cáncer de próstata teñidas con hematoxilina y eosina, seguido de la estructuración de un clasificador soportado por los sistemas de DNN Inception-V3 y k-vecino (22).
Este grupo informó una mejoría consistente en la capacidad diagnóstica del Gleason (0,70) en comparación con las determinaciones hechas por 29 patólogos expertos (0,61).
La confirmación y estadificación tumoral también se puede realizar a partir de imágenes, como es el caso del hepatocarcinoma en hígados cirróticos y de los tumores cerebrales de estirpe glial. Zhou y colaboradores desarrollaron un modelo de ML (basado en SENet y DenseNet) para predecir el grado tumoral derivado de las resonancias hepáticas de pacientes con hepatocarcinoma, plataforma que alcanzó un área bajo la cruva de 0,83 (23).
En general estos estudios demuestran la aplicabilidad plena de la AI para la gradación y estadificación de diferentes tumores sólidos, algunos modelos con un rendimiento superior al logrado por expertos capacitados (24).
Durante la última década la patología convencional ha dado paso a la clasificación tumoral a partir de perfiles genómicos básicos y complejos.
La información derivada de la secuenciación de próxima generación (NGS) ha permitido la perfilación de la enfermedad a partir de la evaluación exómica, del estudio de la transcripción de microarrays, RNA-seq, microARNs y perfiles de metilación.
Debido a que los datos proporcionados por estas plataformas son multidimensionales (evaluando decenas de miles de genes y variantes simultáneamente), el uso de la IA facilita la velocidad y capacidad análisis (25,26).
Recientemente, Capper y colaboradores demostraron que un random forest classifier (RFC) entrenado exclusivamente para definir perfiles de metilación del ADN tumoral pudo mejorar significativamente la precisión de predicción de los subtipos de tumores cerebrales de baja incidencia (AUC 0,99) (27).
Su capacidad de predicción se probó en 139 casos con diagnósticos difíciles no coincidentes entre patólogos; el seguimiento de los pacientes permitió revelar que el 93% de los casos controvertidos por los clínicos fueron catalogados correctamente por el modelo (27).
En paralelo, Sun y colaboradores construyeron y aplicaron un DNN para identificar alteraciones genómicas puntuales que permitieran clasificar 12 tipos diferentes de cáncer seleccionados del TCGA de los tejidos sanos (28).
El clasificador entrenado por múltiples iteraciones logró distinguir entre el tejido sano y el tumoral con alta precisión (AUC 0,94), sin embargo, no fue tan útil para diferenciar las neoplasias entre sí (AUC 0,70). Este trabajo destacó que la precisa clasificación molecular del cáncer tiene limitaciones debido a la evolución dinámica de la enfermedad y la heterogeneidad intratumoral (28).
Detección temprana del cáncer
La IA está permitiendo la rápida migración de las técnicas para detección temprana desde las imágenes secuenciales hasta la introducción de las biopsias líquidas (BL) a partir del análisis de células tumorales circulantes (CTCs), cf/ctADN y microvesículas.
Las BLs obtenidas mediante técnicas mínimamente invasivas permiten la detección precoz de diversas enfermedades tumorales, el seguimiento periódico y la evaluación de resistencia y de la heterogeneidad tumoral.
Chabon y colaboradores desarrollaron un enfoque de análisis basado en ML llamado Lung-CLiP (probabilidad de cáncer en plasma) capaz de predecir la evolución del cáncer de pulmón a partir del análisis de una BL (29).
El método estimó inicialmente la probabilidad de que una mutación encontrada en el cfADN esté asociada con el tumor (usando un modelo de red elástica y las características de la muestra que incluyen el tamaño del fragmento), y posteriormente, integró los resultados junto con las puntuaciones para el número de copias dentro de un clasificador elaborado con cinco algoritmos.
Este modelo demostró un rendimiento predictivo relativamente modesto (AUC 0,69-0,98) dependiente del estado y extensión de la enfermedad.
Por otra parte, Mouliere y colaboradores informaron el uso de un clasificador con patrón aleatorio basado en un RFC capaz de predecir con alta precisión la presencia de cfADN tumoral en sujetos aparentemente sanos (AUC 0,91-0,99) (30).
Como análisis completo (de extremo a extremo) para la determinación temprana del cáncer, Cohen y colaboradores desarrollaron la plataforma CancerSEEK que incluyó 8 variedades de tumores sólidos detectables tempranamente a partir del análisis de cfADN en BL (31).
Inicialmente, las muestras se clasificaron como positivas a partir del análisis de un modelo de regresión que incluyó alteraciones en 16 genes y niveles de expresión de 8 proteínas medidas en cfADN.
A continuación, se predijo el tipo de cáncer usando un RFC que tuvo precisiones que oscilaron entre el 39% y 85% según el tipo de neoplasia (31).
Este trabajo resultó particularmente valioso debido a que 5 de los 8 tipos de cáncer cubiertos tienen pruebas de tamización disponibles y con menor capacidad diagnóstica.
A medida que se expanda y amplifique la adquisición de datos proveniente de BLs se incluirán nuevos modelos, más avanzados y precisos para discriminar la selección manual de las características discriminatorias más relevantes.
Detección de alteraciones genómicas en cáncer utilizando ML
La disponibilidad de la genotipificación vía NGS ha hecho posible la secuenciación masiva del cáncer a nivel poblacional.
La identificación de variantes y mutaciones requiere del apoyo de múltiples herramientas computacionales para el análisis; sin embargo, con frecuencia la observación y descomposición de los datos falla por la baja cobertura sobre regiones génicas complejas, el análisis intrónico o la presencia de grandes deleciones.
Diversos grupos han explorado como optimizar la detección de mutaciones, traslocaciones, amplificaciones o la evaluación del número de copias génicas (CNVs) usando ML (32,33).
DeepVariant, un método de DNN basado en la arquitectura Inception- V2, permitió detectar un mayor número de variantes patogénicas de orden germinal y somático a partir del análisis de imágenes (33).
Este método posibilitó la inclusión de nuevos moldes que optimizaron la detección de SNPs en pacientes con cáncer.
Aprovechamiento de la información genómica en cáncer
Una de las áreas de mayor interés para la IA es la predicción de mutaciones conductoras en tejido tumoral a partir de imágenes de patología, lo que ofrecería una alternativa de cribado óptima, económicamente aceptable y disponible globalmente.
El sistema DeepPATH que permite clasificar diversos subtipos histológicos de cáncer de pulmón, también fue capaz de predecir la presencia de mutaciones en STK11, EGFR, FAT1, SETBP1, KRAS y TP53 (14).
El mismo grupo de investigación también probó su modelo para detectar mutaciones en el EGFR a partir de una cohorte independiente al TCGA alcanzando un rendimiento del 0,68. El AUC más bajo se atribuyó a las diferencias en la preservación del tejido y su manejo preanalítico (14).
En contraposición, un enfoque de DNN basado en ML evaluó la posibilidad de determinar la presencia de mutaciones en el EGFR a partir de los resultados de imágenes provenientes de tomografías preoperatorias en 844 pacientes con adenocarcinoma.
El análisis fue prometedor, documentando un AUC de 0,81 (34), evento homologable a lo obtenido directamente a partir de la exploración de imágenes de 18F-FDG-PET/TAC usando el modelo SResCNN con (AUC >0,81) (35).
Para el caso de los tumores cerebrales de origen glial en los que las imágenes representan el pilar del seguimiento, el uso de la radiómica podría guiar la toma de decisiones.
Las mutaciones en IDH1 (isocitrato deshidrogenasa 1), la acumulación de a-cetoglutarato y el estado de la metilación del promotor de la MGMT (O6-metil-guanin metil-transferasa) podrían perfilarse usando las imágenes de resonancia más el sistema XGBoost (del ingles, eXtreme Gradient Boosting), modelo que alcanzó un rendimiento de 0,70 (36).
En la misma dimensión, Kha y colaboradores usaron el XGBoost para predecir el estado de la codeleción 1p19q en una cohorte de gliomas de bajo grado usando una combinación binaria (37).
A partir del entrenamiento de los datos en la base publica TCIA (del ingles, The Cancer Imaging Archive) el sistema XGBoost combinado con el modelo SHAP (del ingles, SHapley Additive ExPlanations) logró una precisión entre el 82 y 87%.
La radiómica y el análisis integrado para la codeleción 1p19q y las mutaciones en IDH1/2 fue confirmada de forma independiente por varios grupos de investigación adicionales (38-42).
De forma similar, varios modelos basados en DNN (Inception-V3) pueden identificar mutaciones comunes (CTNNB1, FMN2, TP53 y ZFX4) en pacientes con hepatocarcinoma con un rendimiento que oscila entre 0,71 y 0,86 (43,44).
La evaluación de la expresión génica en cáncer se ha extendido a la generación de firmas que permiten la distención patológica por subgrupos o la selección de intervenciones especificas dependiendo de la carga mutacional (del ingles, Tumor Mutational Burden – TMB) o inestabilidad microsatélital (IMS).
Recientemente, la Administración Federal de Medicamentos (del ingles, Federal Drug Administration – FDA) aprobó el uso del pembrolizumab como tratamiento de primera línea para pacientes con tumores que presentan elevada IMS (MSI-H) (45,46).
Como se describió anteriormente, una idea convincente e interesante sería poder predecir el estado de la IMS a partir de las imágenes histopatológicas teñidas con hematoxilina y eosina.
Esto constituiría una alternativa rentable y aditiva a la inmunohistoquímica antes de considerar el uso de la qPCR o de la NGS.
Con este objetivo en mente, Kather y colaboradores aplicaron el sistema ResNet18 CNN para detectar regiones tumorales susceptibles de tener IMS, evento que alcanzó un rendimiento de 0,99. El modelo se aplicó luego a 1.600 muestras de cáncer gástrico, colorrectal y endometrial obtenidas del TCGA; en ellos, el rendimiento del modelo osciló entre 0,75 y 0,84 (47).
La productividad fue superior en la evaluación del tejido embebido en parafina (0,84) versus el congelado (0,77). Lastimosamente, el estudio demostró una enorme variabilidad dependiente de la etnicidad. Recientemente, Yashmita y colaboradores entrenaron y probaron la plataforma MSINet, un modelo de ML centrado en aprendizaje por transferencia usando la arquitectura MobileNetV2 (48).
El MSINet clasificó correctamente 100 tumores colorrectales (AUC 0,93) y luego se comparó con el ResNet18, alcanzando superioridad significativa (AUCs 0,88 y 0,71, respectivamente).
La carga mutacional ha ganado terreno como biomarcador predictivo entre una diversidad de tumores sólidos (49).
Por el momento la TMB solo puede estimarse usando NGS, lo que limita su aplicabilidad clínica, reproducibilidad y harmonización.
El uso de la IA para predecir la TMB a partir de la patología convencional representa un área de interés para iniciar la búsqueda. Jain y colaboradores desarrollaron un modelo de ML basado en la arquitectura Inception-v3/Image2TMB para determinar la TMB a partir de láminas histológicas y catalogarla como positiva o negativa (50).
El estudio valoró 499 muestras de adenocarcinoma de pulmón incluidas en el TCGA usando tres aumentos (5X, 10X y 20X), lo que permitió alcanzar un rendimiento del 0,92. En otro estudio, Wang y colaboradores intentaron clasificar la TMB en 545 muestras de neoplasias gastrointestinales incluidas en el TCGA.
Este grupo basó su modelo a partir de la TMB calculada del recuento de mutaciones no sinónimas a partir de un análisis WES. La plataforma incluyó 8 modelos diferentes usando aprendizaje por transferencia que se informó a GoogLeNet para obtener un AUC de 0,75 para los tumores gástricos y 0,82 para los de colon (51).
La IA también ha permitido predecir la TMB a partir de la patología de carcinomas de pulmón de células no pequeñas con un rendimiento de 0,81 (52), y poco a poco, la investigación se extiende hasta intentar pronosticar la inestabilidad genómica y cromosómica (53).
Determinación del linaje de la célula tumoral – Biología de Sistemas y Computacional en Cáncer
Desde la perspectiva clínica, la determinación del origen tumoral en los primarios no conocidos puede ser útil para dirigir la terapia antineoplásica (54).
Convencionalmente, el tejido de origen tumoral se determina a través de la inmunohistoquímica, proceso que puede amplificarse usando perfiles de expresión génica que tienen una sensibilidad aproximada del 80% (55).
Como alternativa, Jiao y el consorcio PCAWG diseñaron y aplicaron varios modelos de DNN para agrupar y contar las mutaciones encontradas en 6.000 tumores que abarcan 28 tipos de cáncer (56).
La idea básica detrás de este enfoque es que las alteraciones regionales son representativas de la accesibilidad a la cromatina en una región genómica específica, lo que permitiría establecer el estado epigénetico de la célula de origen.
Este modelo permitió discriminar que la distribución regional de las mutaciones somáticas del cáncer está agregada por contenedores de Mb en el genoma, la mayoría siendo alteraciones pasajeras que permiten perfilar el origen de la neoplasia con un rendimiento que oscila entre 0,83 y 0,91.
Curiosamente, este análisis no encontró que la presencia de genes conductores fuera una característica esencial para la clasificación del primario desconocido (56).
En el futuro próximo la IA se podrá utilizar para comprender el impacto funcional de las mutaciones, para predecir el valor de las alteraciones no codificantes en la expresión génica, el valor de múltiples procesos epigenéticos y el riesgo de recaída o progresión de la enfermedad (57,58).
Caracterización del microambiente tumoral – Biología de Sistemas y Computacional en Cáncer
A pesar del rendimiento predictivo consistentemente alto, muchos de los enfoques de IA utilizados en patología digital pueden describirse como una “caja negra”; es decir, sus métodos pueden enseñar a discriminar y aplicar entre diferentes enfermedades, pero a menudo no proporcionan una explicación fácilmente interpretable.
La IA tiene el potencial de ayudar a automatizar los procesos patológicos para simplificar las tareas rutinarias del personal de laboratorio que limitan la estimación de las características de las células tumorales.
Tradicionalmente, los patólogos inspeccionan los portaobjetos con láminas de tejido teñidas para determinar la celularidad, un enfoque que no solo es laborioso, sino también subjetivo debido a la variabilidad intra e interobservador.
La celularidad tumoral también se puede inferir computacionalmente a partir de conjuntos de datos de NGS, pero hay una concordancia limitada entre los métodos de inferencia disponibles y una gran dependencia de la presencia de múltiples alteraciones genómicas (59,60).
Para abordar esta tarea usando IA, Akbar y colaboradores contaron la celularidad tumoral a partir de tejido teñido con hematoxilina y eosina (aumento 20X) de 53 pacientes con cáncer de seno usando un modelo DNN con arquitectura InceptionNet (60).
El grupo entrenó dos modelos, uno para distinguir el tumor del tejido sano, y el otro, para generar puntuaciones entre 0 y 100% respecto de la celularidad. El rendimiento para tal fin fue de 0,82.
Aunque estos hallazgos demuestran la viabilidad de la propuesta, el recurso debe ampliarse en conjuntos de datos más grandes.
La IA también se ha extendido a la evaluación espacial y cuantitativa del microambiente tumoral (del inglés, Tumor Microenviroment – TME) donde las células tumorales interactúan continuamente con otros elementos formes del estroma incluyendo las del sistema inmune (61), comunicación que puede determinar la evolución de la enfermedad y su capacidad para generar metástasis (61).
Saltz y colaboradores demostraron la viabilidad de identificar y cuantificar la infiltración linfocitaria a partir de láminas de patologías teñidas convencionalmente para 13 tipos de cáncer incluidos en el TCGA utilizando una DNN con autoencoder convolucional, en el cual el modelo aprende una representación compacta de las características morfológicas básicas para definir la anormalidad del tumor (62).
En el estudio se entrenaron dos DNN, el primero para clasificar el estado de los linfocitos infiltrantes de tumor (TILs), y el otro, para identificar regiones con necrosis.
Al evaluar un conjunto de adenocarcinomas de pulmón, el rendimiento global del modelo fue de 0,95. Posteriormente, Bejnordi y colaboradores entrenaron y probaron un DNN usando arquitectura VGGNet para estimar las características del estroma de 882 pacientes con cáncer de seno, modelo que logró una precisión del 92% para discriminar entre normalidad y tumor con o sin infiltración linfocitaria.
En adición, Fassler y colaboradores aprovecharon las imágenes de patología obtenidas por inmunohistoquímica multiplex (IHC) en un grupo de muestras de cáncer de páncreas para aplicar un modelo DNN compuesto por un autoencoder (ColorAE) junto con una red neural convolucional U-Net, encontrando un rendimiento para la segmentación y clasificación celular del estroma entre 0,40 y 0,84 (63).
En el futuro próximo, se utilizarán cada vez más las plataformas de imágenes integradas como la Vectra® PerkinElmer o la citometría de masas de imágenes, capaces de valorar una enorme diversidad de aspectos del TME con una resolución creciente y mayor capacidad para el procesamiento gráfico (por su sigla en ingles, GPU).
Estas tecnologías permitirán a investigadores y clínicos estudiar con detalle las complejas interacciones entre las células tumorales y sus acompañantes sanas a nivel del estroma.
Descubrimiento de nuevos objetivos terapéuticos y medicamentos – Biología de Sistemas y Computacional en Cáncer
El descubrimiento y desarrollo de nuevos fármacos y biomarcadores se asocia con costos elevados y largos periodos de tiempo.
El acceso a diversas tecnologías de secuenciación de profundidad e imágenes, junto con una creciente disponibilidad de conjuntos de datos públicos o privados sobre el cáncer, ha generado un interés creciente en aprovechar la inteligencia artificial para hacer este proceso más eficiente.
Lo anterior incluye la generación de modelos que integren diferentes momentos del espectro de gestión de los medicamentos oncológicos (Figura 5).
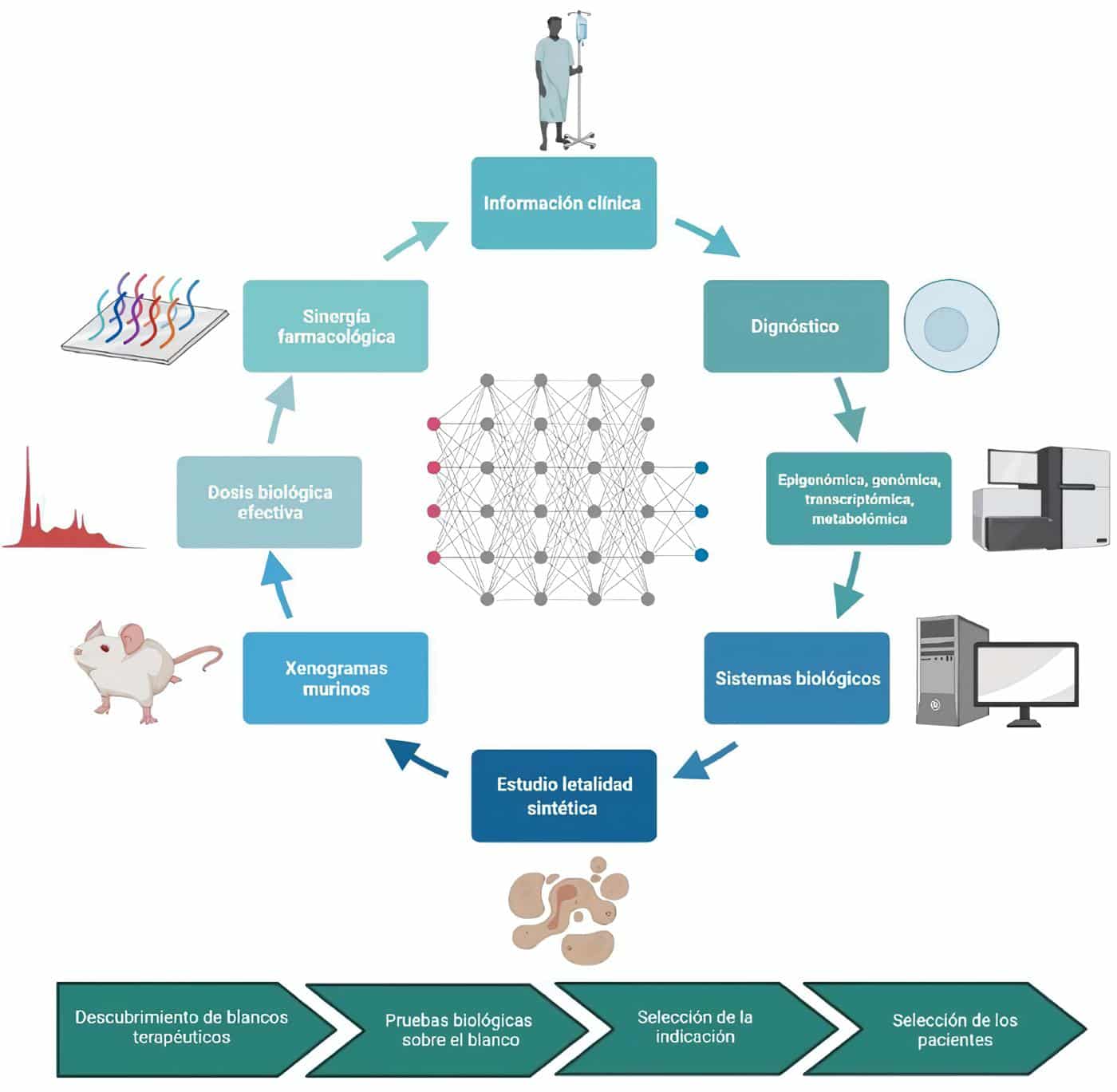
Figura 5. La integración de los conjuntos de datos de múltiples fuentes diversas, que van desde la secuenciación hasta la estructura y la detección de conjuntos de datos, puede aumentar el espacio de características relevantes para los modelos de IA que permiten el descubrimiento de nuevas moléculas de un extremo a otro (ADMET: absorción, distribución, metabolismo, excreción y toxicidad).
Por ejemplo, Tong y colaboradores integraron los datos de perfiles de expresión génica con redes de interacción proteína-proteína para derivar características que podrían predecir posibles blancos terapéuticos en hepatocarcinoma. Usando un diseño de ML con vectores de apoyo se encontró una AUC de 0,88 (64). Otro enfoque basado en DL encontró datos similares para el cáncer de seno (65,66).
El Consorcio DepMap ha puesto a disposición de los investigadores cientos de conjuntos de datos que permiten la implementación de diversas estrategias de IA (67).
Por ejemplo, el enfoque de la plataforma ECLIPSE (ML) es predecir posibles blancos terapéuticos a partir de la información genómica extraída de muestras de pacientes y líneas celulares (68).
Del mismo modo, Chen examinó una amplia gama de características moleculares de DepMap y encontró a partir de la proteómica (específicamente, datos de la matriz de proteínas de fase inversa) que la IA puede predecir la interacción y dependencia celular a diferentes vías de señalización potencialmente modulables (69).
Diseño de medicamentos – Biología de Sistemas y Computacional en Cáncer
La IA también se ha aplicado para diseñar estructuras de fármacos in silico con las propiedades fisicoquímicas deseadas y las especificidades de los objetivos celulares.
Las técnicas tradicionales de IA se han centrado en la clasificación binaria y tienen dificultades para ejecutar y modelar objetivos complicados, como el diseño de nuevas moléculas in silico.
El aprendizaje por refuerzo (reinforcement learning), un subconjunto creciente de la IA suele ser ideal para resolver problemas que presentan objetivos complejos, permitiendo la retroalimentación interactiva (70).
Olivecrona y colaboradores demostraron cómo su enfoque de red neuronal recurrente utilizando el aprendizaje por refuerzo fue capaz de generar análogos del Celecoxib y compuestos sin el azufre (70).
Tú y colaboradores introdujo un modelo de DNN con gráficos para generar moléculas novedosas con alta precisión y sin el requerimiento de conversión computacional a representaciones 2D.
Además, las Redes Generativas Adversarias (GAN), una combinación del generador y el discriminador, también se han aplicado en el proceso de generación de nuevas moléculas (71,72).
El MolGAN, un método para generar moléculas con propiedades específicas, que utiliza tanto GAN como arquitectura de aprendizaje por refuerzo, logró un alto rendimiento para varias propiedades, incluidas la probabilidad, sintetizabilidad y solubilidad del fármaco (62%, 95% y 89%, respectivamente) (72).
Si bien los modelos basados en redes neuronales dominan la generación de moléculas, los modelos no basados en redes neuronales han tenido éxito para predecir las propiedades de los fármacos (73).
Gayvert y colaboradores reportaron un modelo que utilizó distintos tipos de datos preclínicos para predecir la toxicidad de los fármacos oncológicos y sus eventos adversos (74).
En la misma línea, Shen y colaboradores entrenaron un modelo de máquina de vectores de soporte para predecir varias propiedades ADME (absorción, distribución, metabolismo y excreción) de un fármaco y validó su enfoque al predecir con precisión tanto la permeabilidad de la barrera hematoencefálica como la absorción intestinal humana (74).
Pronóstico y respuesta al tratamiento – Biología de Sistemas y Computacional en Cáncer
La capacidad de identificar prospectivamente a los pacientes que mejor se adaptan a una terapia determinada puede ayudar a reducir los riesgos, a mejorar los desenlaces clínicos, y también ayudar a minimizar los altos costos. El uso de la IA en esta área ha sido limitado debido a la disponibilidad de datos insuficientes, pero ahora se está expandiendo gradualmente.
Liu y colaboradores informaron sobre el uso de un clasificador basado en regresión logística entrenado para detectar perfiles genómicos y transcriptómicos en pacientes sin tratamiento previo y adherirlos a múltiples características clínicas para predecir la resistencia a los inhibidores de PD-1 en pacientes con melanoma avanzado.
Globalmente, el rendimiento del modelo osciló entre 0,73 y 0,83 (75). En adición, Litchfield y colaboradores compilaron la mayor cohorte de perfiles genómicos y transcriptómicos pareados para definir la utilidad de la inmunoterapia.
Ellos usaron este conjunto de datos para entrenar y probar un clasificador específico de cáncer basado en XGBoost, elemento que alcanzó una capacidad de predicción entre 0,66 y 0,86 (76). Por otra parte, Johannet y colaboradores informaron el uso de una plataforma de IA más avanzada usando CNN entrenado sobre patologías y sumado a caracteres clínicos para predecir la respuesta a la inmunoterapia en pacientes con melanoma con una precisión cercana a 0,80 (77).
Además de la utilidad de la IA para predecir la respuesta a la inmunoterapia, también se han informado modelos capaces de predecir la respuesta de los pacientes a la terapia blanco dirigida a partir de datos ómicos con o sin imágenes integradas.
Sun y colaboradores aplicaron un modelo DNN a características extraídas de la expresión génica como la alteración en el número de copias más rasgos clínicos en pacientes con cáncer de seno (de METABRIC y TCGA) para predecir el pronóstico después del tratamiento neo y adyuvante obteniendo un rendimiento de 0,80 (78).
Otros enfoques similares basados en DNN han sido capaces de predecir la supervivencia en pacientes con tumores cerebrales, hepatocarcinoma, carcinoma colorrectal y leucemias (79-83).
Sistemas inteligentes como apoyo de la decisión clínica – Biología de Sistemas y Computacional en Cáncer
En los últimos años, el desarrollo de máquinas inteligentes que permitan mejorar la precisión en la toma de decisiones en medicina se ha convertido en la obsesión de diferentes empresas dedicadas a la inteligencia artificial, estos desarrollos han sido analizados en diferentes escenarios incluyendo las decisiones clínicas (84).
IBM Watson for Oncology fue desarrollado y entrenado en conjunto con el Memorial Sloan Kettering Cancer Center (por sus siglas en ingles, WFO y MSKCC), es una herramienta de apoyo a la toma de decisiones clínicas, que aprovecha el poder de la tecnología cognitiva para ayudar a los médicos a elegir terapias para pacientes con cáncer, siendo esta la meta principal de WFO (85).
El sistema fue entrenado por oncólogos del MSKCC para aprender datos clave asociados con el cáncer, incluidos los resultados de análisis de sangre, informes de patología e imágenes que detallan el tipo, tamaño y ubicación del tumor.
Además, la presencia de mutaciones a partir de las cuales revisa diversas bases de datos y gran cantidad de literatura médica, priorizando el tratamiento basado en la mejor evidencia para cada paciente específico. Ahora, diversos estudios muestran que WFO ha logrado un alto grado de concordancia con las recomendaciones médicas.
A la fecha, el sistema de WFO ha sido capacitado para respaldar las decisiones de tratamiento en diversas neoplasias sólidas incluyendo los cánceres de pulmón, seno, colorrectal, vejiga, cuello uterino, endometrio, esófago, gástrico, ovario, próstata, tiroides, y además algunos tipos de linfomas.
Mediante el uso de un software de procesamiento de lenguaje natural para comprender algoritmos probabilísticos, el WFO puede leer y comprender millones de páginas de texto para concentrarse en la información relevante para las consultas de los médicos y generar múltiples posibilidades para su uso en la toma de decisiones terapéuticas.
Inicialmente capacitado en cánceres de pulmón, seno y colorrectal, los primeros estudios demostraron que el WFO tenía más del 90% de correlación con las recomendaciones de tratamiento del MSKCC para pacientes con cáncer de seno en estado I a III, y coincidía con las recomendaciones el 50% de las veces para cáncer de pulmón (86-88).
Desde su introducción en la práctica clínica alrededor de 2015, múltiples trabajos se han realizado para verificar su beneficio en diferentes entornos hospitalarios de los Estados Unidos y en países de Asia.
Aunque WFO todavía se encuentra en la fase de prueba en la mayoría de los centros oncológicos, se está utilizando regularmente en el entorno clínico de hospitales en Tailandia, India, Corea, y Eslovaquia, y se está adoptado progresivamente en los sistemas hospitalarios de China (88).
Somashekhar y colaboradores presentaron sus resultados de 1.000 pacientes que fueron analizados por el sistema y confirmados por una Junta Multidisciplinaria de Tumores. El estudio encontró una concordancia para el tratamiento del 92% (todos los cánceres combinados), y del 93%, 92%, 89% y 81%, para el cáncer de recto, seno, pulmón y de colon, respectivamente.
La Junta cambió su decisión en 136 casos (13,6%), teniendo como razones principales la recomendación de tratamientos recientes no disponibles (55%), la utilización de una alternativa personalizada (30%), y el uso de conocimiento basado en la conjunción de datos genómicos y fenotípicos en el 15% (90).
En adición, Jie y colaboradores presentaron un metaanálisis para evaluar sistemáticamente la coherencia de los esquemas de tratamiento propuestos por el sistema WFO y las Juntas de Tumores. El estudio integrativo incluyó 9 experimentos y 2.463 pacientes, considerando una concordancia global del 81,5%. Entre ellos, el cáncer de seno tuvo el mayor rendimiento (especialmente para los estados I a III) siendo opuesto el resultado para el cáncer de pulmón (91).
Esta y otras herramientas de apoyo en la toma de decisiones mantienen la promesa de valor de la mejor atención en cáncer.
Referencias – Biología de Sistemas y Computacional en Cáncer
1. Torre LA, Siegel RL, Ward EM, Jemal A. Global Cancer Incidence and Mortality Rates and Trends–An Update. Cancer Epidemiol Biomarkers Prev. 2016 Jan;25(1):16- 27. doi: 10.1158/1055-9965.EPI-15-0578. Epub 2015 Dec 14.
2. Tufail AB, Ma YK, Kaabar MKA, Martínez F, Junejo AR, Ullah I, Khan R. Deep Learning in Cancer Diagnosis and Prognosis Prediction: A Minireview on Challenges, Recent Trends, and Future Directions. Comput Math Methods Med. 2021 Oct 31;2021:9025470. doi: 10.1155/2021/9025470.
3. LeCun Y, Bengio Y, Hinton G. Deep learning. Nature. 2015 May 28;521(7553):436-44. doi: 10.1038/nature14539.
4. Pellegrino E, Jacques C, Beaufils N, Nanni I, Carlioz A, Metellus P, Ouafik L. Machine learning random forest for predicting oncosomatic variant NGS analysis. Sci Rep. 2021 Nov 8;11(1):21820. doi: 10.1038/s41598-021- 01253-y.
5. Ding L, Bailey MH, Porta-Pardo E, Thorsson V, Colaprico A, et al.; Cancer Genome Atlas Research Network. Perspective on Oncogenic Processes at the End of the Beginning of Cancer Genomics. Cell. 2018 Apr 5;173(2):305-320.e10. doi: 10.1016/j.cell.2018.03.033.
6. Li F, Wu T, Xu Y, Dong Q, Xiao J, Xu Y, et al. A comprehensive overview of oncogenic pathways in human cancer. Brief Bioinform. 2020 May 21;21(3):957-969. doi: 10.1093/bib/bbz046.
7. Madhukar NS, Khade PK, Huang L, Gayvert K, Galletti G, Stogniew M, et al. A Bayesian machine learning approach for drug target identification using diverse data types. Nat Commun. 2019 Nov 19;10(1):5221. doi: 10.1038/s41467-019-12928-6.
8. Madhukar NS, Khade PK, Huang L, Gayvert K, Galletti G, Stogniew M, et al. A Bayesian machine learning approach for drug target identification using diverse data types. Nat Commun. 2019 Nov 19;10(1):5221. doi: 10.1038/s41467-019-12928-6.
Otras Referencias – Biología de Sistemas y Computacional en Cáncer
9. Cheerla A, Gevaert O. Deep learning with multimodal representation for pancancer prognosis prediction. Bioinformatics. 2019 Jul 15;35(14):i446-i454. doi: 10.1093/ bioinformatics/btz342.
10. Bhinder B, Gilvary C, Madhukar NS, Elemento O. Artificial Intelligence in Cancer Research and Precision Medicine. Cancer Discov. 2021 Apr;11(4):900-915. doi: 10.1158/2159-8290.CD-21-0090.
11. Khosravi P, Kazemi E, Imielinski M, Elemento O, Hajirasouliha I. Deep Convolutional Neural Networks Enable Discrimination of Heterogeneous Digital Pathology Images. EBioMedicine. 2018 Jan;27:317-328. doi: 10.1016/j.ebiom.2017.12.026. Epub 2017 Dec 28.
12. Munir K, Elahi H, Ayub A, Frezza F, Rizzi A. Cancer Diagnosis Using Deep Learning: A Bibliographic Review. Cancers (Basel). 2019 Aug 23;11(9):1235. doi: 10.3390/ cancers11091235.
13. Patil PD, Hobbs B, Pennell NA. The promise and challenges of deep learning models for automated histopathologic classification and mutation prediction in lung cancer. J Thorac Dis. 2019 Feb;11(2):369-372. doi: 10.21037/jtd.2018.12.55.
14. Coudray N, Ocampo PS, Sakellaropoulos T, Narula N, Snuderl M, Fenyö D, et al. Classification and mutation prediction from non-small cell lung cancer histopathology images using deep learning. Nat Med. 2018 Oct;24(10):1559-1567. doi: 10.1038/s41591-018-0177- 5. Epub 2018 Sep 17.
15. Esteva A, Kuprel B, Novoa RA, Ko J, Swetter SM, Blau HM, Thrun S. Dermatologist-level classification of skin cancer with deep neural networks. Nature. 2017 Feb 2;542(7639):115-118. doi: 10.1038/nature21056. Epub 2017 Jan 25. Erratum in: Nature. 2017 Jun 28;546(7660):686.
16. Anthimopoulos M, Christodoulidis S, Ebner L, Christe A, Mougiakakou S. Lung Pattern Classification for Interstitial Lung Diseases Using a Deep Convolutional Neural Network. IEEE Trans Med Imaging. 2016 May;35(5):1207-1216. doi: 10.1109/TMI.2016.2535865. Epub 2016 Feb 29.
Bibliografías – Biología de Sistemas y Computacional en Cáncer
17. Jiang Y, Liang X, Wang W, Chen C, Yuan Q, Zhang X, et al. Noninvasive Prediction of Occult Peritoneal Metastasis in Gastric Cancer Using Deep Learning. JAMA Netw Open. 2021 Jan 4;4(1):e2032269. doi: 10.1001/jamanetworkopen. 2020.32269.
18. Wang X, Yang W, Weinreb J, Han J, Li Q, Kong X, et al. Searching for prostate cancer by fully automated magnetic resonance imaging classification: deep learning versus non-deep learning. Sci Rep. 2017 Nov 13;7(1):15415. doi: 10.1038/s41598-017-15720-y.
19. McKinney SM, Sieniek M, Godbole V, Godwin J, Antropova N, Ashrafian H, et al. International evaluation of an AI system for breast cancer screening. Nature. 2020 Jan;577(7788):89-94. doi: 10.1038/s41586-019- 1799-6. Epub 2020 Jan 1. Erratum in: Nature. 2020 Oct;586(7829):E19.
20. Freeman K, Dinnes J, Chuchu N, Takwoingi Y, Bayliss SE, Matin RN, et al. Algorithm based smartphone apps to assess risk of skin cancer in adults: systematic review of diagnostic accuracy studies. BMJ. 2020 Feb 10;368:m127. doi: 10.1136/bmj.m127. Erratum in: BMJ. 2020 Feb 25;368:m645.
21. Dasgupta S, Vaughan AS, Kramer MR, Sanchez TH, Sullivan PS. Use of a Google Map Tool Embedded in an Internet Survey Instrument: Is it a Valid and Reliable Alternative to Geocoded Address Data? JMIR Res Protoc. 2014 Apr 10;3(2):e24. doi: 10.2196/resprot.2946.
22. Nagpal K, Foote D, Liu Y, Chen PC, Wulczyn E, Tan F, et al. Development and validation of a deep learning algorithm for improving Gleason scoring of prostate cancer. NPJ Digit Med. 2019 Jun 7;2:48. doi: 10.1038/ s41746-019-0112-2. Erratum in: NPJ Digit Med. 2019 Nov 19;2:113.
23. Zhou Q, Zhou Z, Chen C, Fan G, Chen G, Heng H, et al. Grading of hepatocellular carcinoma using 3D SEDenseNet in dynamic enhanced MR images. Comput Biol Med. 2019 Apr;107:47-57. doi: 10.1016/j.compbiomed. 2019.01.026. Epub 2019 Feb 4.
Otras Bibliografías – Biología de Sistemas y Computacional en Cáncer
24. Gong XQ, Tao YY, Wu YK, Liu N, Yu X, Wang R, et al. Progress of MRI Radiomics in Hepatocellular Carcinoma. Front Oncol. 2021 Sep 20;11:698373. doi: 10.3389/ fonc.2021.698373.
25. Grewal JK, Tessier-Cloutier B, Jones M, Gakkhar S, Ma Y, Moore R, et al. Application of a Neural Network Whole Transcriptome-Based Pan-Cancer Method for Diagnosis of Primary and Metastatic Cancers. JAMA Netw Open. 2019 Apr 5;2(4):e192597. doi: 10.1001/jamanetworkopen. 2019.2597.
26. Penson A, Camacho N, Zheng Y, Varghese AM, Al- Ahmadie H, Razavi P, et al. Development of Genome- Derived Tumor Type Prediction to Inform Clinical Cancer Care. JAMA Oncol. 2020 Jan 1;6(1):84-91. doi: 10.1001/ jamaoncol.2019.3985.
27. Capper D, Jones DTW, Sill M, Hovestadt V, Schrimpf D, Sturm D, et al. DNA methylation-based classification of central nervous system tumours. Nature. 2018 Mar 22;555(7697):469-474. doi: 10.1038/nature26000. Epub 2018 Mar 14.
28. Sun Y, Zhu S, Ma K, Liu W, Yue Y, Hu G, et al. Identification of 12 cancer types through genome deep learning. Sci Rep. 2019 Nov 21;9(1):17256. doi: 10.1038/s41598- 019-53989-3.
29. Chabon JJ, Hamilton EG, Kurtz DM, Esfahani MS, Moding EJ, Stehr H, et al. Integrating genomic features for non-invasive early lung cancer detection. Nature. 2020 Apr;580(7802):245-251. doi: 10.1038/s41586-020- 2140-0. Epub 2020 Mar 25.
30. Mouliere F, Chandrananda D, Piskorz AM, Moore EK, Morris J, Ahlborn LB, et al. Enhanced detection of circulating tumor DNA by fragment size analysis. Sci Transl Med. 2018 Nov 7;10(466):eaat4921. doi: 10.1126/scitranslmed. aat4921.
31. Cohen JD, Li L, Wang Y, Thoburn C, Afsari B, Danilova L, et al. Detection and localization of surgically resectable cancers with a multi-analyte blood test. Science. 2018 Feb 23;359(6378):926-930. doi: 10.1126/science. aar3247. Epub 2018 Jan 18.
Lecturas Recomendadas – Biología de Sistemas y Computacional en Cáncer
32. Poplin R, Chang PC, Alexander D, Schwartz S, Colthurst T, Ku A, et al. A universal SNP and small-indel variant caller using deep neural networks. Nat Biotechnol. 2018 Nov;36(10):983-987. doi: 10.1038/nbt.4235. Epub 2018 Sep 24.
33. Park H, Chun SM, Shim J, Oh JH, Cho EJ, Hwang HS, et al. Detection of chromosome structural variation by targeted next-generation sequencing and a deep learning application. Sci Rep. 2019 Mar 6;9(1):3644. doi: 10.1038/s41598-019-40364-5.
34. Yin G, Wang Z, Song Y, Li X, Chen Y, Zhu L, et al. Prediction of EGFR Mutation Status Based on 18F-FDG PET/ CT Imaging Using Deep Learning-Based Model in Lung Adenocarcinoma. Front Oncol. 2021 Jul 22;11:709137. doi: 10.3389/fonc.2021.709137. Erratum in: Front Oncol. 2021 Sep 07;11:747316.
35. Mu W, Jiang L, Zhang J, Shi Y, Gray JE, Tunali I, et al. Non-invasive decision support for NSCLC treatment using PET/CT radiomics. Nat Commun. 2020 Oct 16;11(1):5228. doi: 10.1038/s41467-020-19116-x.
36. Shboul ZA, Chen J, M Iftekharuddin K. Prediction of Molecular Mutations in Diffuse Low-Grade Gliomas using MR Imaging Features. Sci Rep. 2020 Feb 28;10(1):3711. doi: 10.1038/s41598-020-60550-0.
37. Kha QH, Le VH, Hung TNK, Le NQK. Development and Validation of an Efficient MRI Radiomics Signature for Improving the Predictive Performance of 1p/19q Co-Deletion in Lower-Grade Gliomas. Cancers (Basel). 2021 Oct 27;13(21):5398. doi: 10.3390/cancers13215398.
38. Han Y, Xie Z, Zang Y, Zhang S, Gu D, Zhou M, et al. Non-invasive genotype prediction of chromosome 1p/19q co-deletion by development and validation of an MRI-based radiomics signature in lower-grade gliomas. J Neurooncol. 2018 Nov;140(2):297-306. doi: 10.1007/ s11060-018-2953-y. Epub 2018 Aug 10.
Otras Lecturas Recomendadas – Biología de Sistemas y Computacional en Cáncer
39. Zhou H, Chang K, Bai HX, Xiao B, Su C, Bi WL, et al. Machine learning reveals multimodal MRI patterns predictive of isocitrate dehydrogenase and 1p/19q status in diffuse low- and high-grade gliomas. J Neurooncol. 2019 Apr;142(2):299-307. doi: 10.1007/s11060-019-03096-0. Epub 2019 Jan 19.
40. Zhang B, Chang K, Ramkissoon S, Tanguturi S, Bi WL, Reardon DA, et al. Multimodal MRI features predict isocitrate dehydrogenase genotype in high-grade gliomas. Neuro Oncol. 2017 Jan;19(1):109-117. doi: 10.1093/ neuonc/now121. Epub 2016 Jun 26.
41. Kim M, Jung SY, Park JE, Jo Y, Park SY, Nam SJ, et al. Diffusion- and perfusion-weighted MRI radiomics model may predict isocitrate dehydrogenase (IDH) mutation and tumor aggressiveness in diffuse lower grade glioma. Eur Radiol. 2020 Apr;30(4):2142-2151. doi: 10.1007/ s00330-019-06548-3. Epub 2019 Dec 11.
42. Tan Y, Zhang ST, Wei JW, Dong D, Wang XC, Yang GQ, et al. A radiomics nomogram may improve the prediction of IDH genotype for astrocytoma before surgery. Eur Radiol. 2019 Jul;29(7):3325-3337. doi: 10.1007/s00330- 019-06056-4. Epub 2019 Apr 10.
43. Chen M, Zhang B, Topatana W, Cao J, Zhu H, Juengpanich S, et al. Classification and mutation prediction based on histopathology H&E images in liver cancer using deep learning. NPJ Precis Oncol. 2020 Jun 8;4:14. doi: 10.1038/s41698-020-0120-3.
44. Lu L, Daigle BJ Jr. Prognostic analysis of histopathological images using pre-trained convolutional neural networks: application to hepatocellular carcinoma. PeerJ. 2020 Mar 12;8:e8668. doi: 10.7717/peerj.8668.
Fuentes Bibliográficas – Biología de Sistemas y Computacional en Cáncer
45. Sidaway P. MSI-H: a truly agnostic biomarker? Nat Rev Clin Oncol. 2020 Feb;17(2):68. doi: 10.1038/s41571- 019-0310-5.
46. Marabelle A, Le DT, Ascierto PA, Di Giacomo AM, De Jesus-Acosta A, Delord JP, et al. Efficacy of Pembrolizumab in Patients With Noncolorectal High Microsatellite Instability/Mismatch Repair-Deficient Cancer: Results From the Phase II KEYNOTE-158 Study. J Clin Oncol. 2020 Jan 1;38(1):1-10. doi: 10.1200/JCO.19.02105. Epub 2019 Nov 4.
47. Kather JN, Pearson AT, Halama N, Jäger D, Krause J, Loosen SH, et al. Deep learning can predict microsatellite instability directly from histology in gastrointestinal cancer. Nat Med. 2019 Jul;25(7):1054-1056. doi: 10.1038/s41591-019-0462-y. Epub 2019 Jun 3.
48. Yamashita R, Long J, Longacre T, Peng L, Berry G, Martin B, et al. Deep learning model for the prediction of microsatellite instability in colorectal cancer: a diagnostic study. Lancet Oncol. 2021 Jan;22(1):132-141. doi: 10.1016/S1470-2045(20)30535-0.
49. Chan TA, Yarchoan M, Jaffee E, Swanton C, Quezada SA, Stenzinger A, et al. Development of tumor mutation burden as an immunotherapy biomarker: utility for the oncology clinic. Ann Oncol. 2019 Jan 1;30(1):44-56. doi: 10.1093/annonc/mdy495.
50. Jain MS, Massoud TF. Predicting tumour mutational burden from histopathological images using multiscale deep learning. Nat Mach Intell. 2020;2:356-62.
51. Wang L, Jiao Y, Qiao Y, Zeng N, Yu R. A novel approach combined transfer learning and deep learning to predict TMB from histology image. Pattern Recognit. Lett 2020;135:244–48.
52. He B, Dong D, She Y, Zhou C, Fang M, Zhu Y, et al. Predicting response to immunotherapy in advanced non-small-cell lung cancer using tumor mutational burden radiomic biomarker. J Immunother Cancer. 2020 Jul;8(2):e000550. doi: 10.1136/jitc-2020-000550.
53. Xu Z, Verma A, Naveed U, Bakhoum S, Khosravi P, Elemento O. Using Histopathology Images to Predict Chromosomal Instability in Breast Cancer: A Deep Learning Approach. medRxiv 2020.09.23.20200139. 10.1101/2020.09.23.20200139.
Otras Fuentes Bibliográficas – Biología de Sistemas y Computacional en Cáncer
54. Hainsworth JD, Rubin MS, Spigel DR, Boccia RV, Raby S, Quinn R, et al. Molecular gene expression profiling to predict the tissue of origin and direct site-specific therapy in patients with carcinoma of unknown primary site: a prospective trial of the Sarah Cannon research institute. J Clin Oncol. 2013 Jan 10;31(2):217-23. doi: 10.1200/ JCO.2012.43.3755. Epub 2012 Oct 1.
55. Greco FA. Molecular diagnosis of the tissue of origin in cancer of unknown primary site: useful in patient management. Curr Treat Options Oncol. 2013 Dec;14(4):634- 42. doi: 10.1007/s11864-013-0257-1.
56. Jiao W, Atwal G, Polak P, Karlic R, Cuppen E; PCAWG Tumor Subtypes and Clinical Translation Working Group; PCAWG Consortium. A deep learning system accurately classifies primary and metastatic cancers using passenger mutation patterns. Nat Commun. 2020 Feb 5;11(1):728. doi: 10.1038/s41467-019-13825-8.
57. Zhou J, Theesfeld CL, Yao K, Chen KM, Wong AK, Troyanskaya OG. Deep learning sequence-based ab initio prediction of variant effects on expression and disease risk. Nat Genet. 2018 Aug;50(8):1171-1179. doi: 10.1038/s41588-018-0160-6. Epub 2018 Jul 16.
58. Hoffman GE, Bendl J, Girdhar K, Schadt EE, Roussos P. Functional interpretation of genetic variants using deep learning predicts impact on chromatin accessibility and histone modification. Nucleic Acids Res. 2019 Nov 18;47(20):10597-10611. doi: 10.1093/nar/gkz808.
59. Haider S, Tyekucheva S, Prandi D, Fox NS, Ahn J, Xu AW, et al.; Cancer Genome Atlas Research Net work. Systematic Assessment of Tumor Purity and Its Clinical Implications. JCO Precis Oncol. 2020 Sep 4;4:PO.20.00016. doi: 10.1200/PO.20.00016.
60. Akbar S, Peikari M, Salama S, Panah AY, Nofech-Mozes S, Martel AL. Automated and Manual Quantification of Tumour Cellularity in Digital Slides for Tumour Burden Assessment. Sci Rep. 2019 Oct 1;9(1):14099. doi: 10.1038/s41598-019-50568-4.
61. Bhinder B, Elemento O. Computational methods in tumor immunology. Methods Enzymol. 2020;636:209-259. doi: 10.1016/bs.mie.2020.01.001. Epub 2020 Jan 25.
Reseñas Bibliográficas – Biología de Sistemas y Computacional en Cáncer
62. Saltz J, Gupta R, Hou L, Kurc T, Singh P, Nguyen V, et al. Spatial Organization and Molecular Correlation of Tumor-Infiltrating Lymphocytes Using Deep Learning on Pathology Images. Cell Rep. 2018 Apr 3;23(1):181-193. e7. doi: 10.1016/j.celrep.2018.03.086.
63. Fassler DJ, Abousamra S, Gupta R, Chen C, Zhao M, Paredes D, et al. Deep learning-based image analysis methods for brightfield-acquired multiplex immunohistochemistry images. Diagn Pathol. 2020 Jul 28;15(1):100. doi: 10.1186/s13000-020-01003-0. Erratum in: Diagn Pathol. 2020 Sep 24;15(1):116.
64. Tong Z, Zhou Y, Wang J. Identifying potential drug targets in hepatocellular carcinoma based on network analysis and one-class support vector machine. Sci Rep. 2019 Jul 18;9(1):10442. doi: 10.1038/s41598-019-46540-x.
65. López-Cortés A, Paz-Y-Miño C, Cabrera-Andrade A, Barigye SJ, Munteanu CR, González-Díaz H, et al. Gene prioritization, communality analysis, networking and metabolic integrated pathway to better understand breast cancer pathogenesis. Sci Rep. 2018 Nov 12;8(1):16679. doi: 10.1038/s41598-018-35149-1.
66. Tamborero D, Rubio-Perez C, Deu-Pons J, Schroeder MP, Vivancos A, Rovira A, et al. Cancer Genome Interpreter annotates the biological and clinical relevance of tumor alterations. Genome Med. 2018 Mar 28;10(1):25. doi: 10.1186/s13073-018-0531-8.
67. Tsherniak A, Vazquez F, Montgomery PG, Weir BA, Kryukov G, Cowley GS, et al. Defining a Cancer Dependency Map. Cell. 2017 Jul 27;170(3):564-576.e16. doi: 10.1016/j.cell.2017.06.010.
68. Gilvary C, Madhukar NS, Gayvert K, Foronda M, Perez A, Leslie CS, et al. A machine learning approach predicts essential genes and pharmacological targets in cancer. bioRxiv 692277; doi: 10.1101/692277
69. Chen MM, Li J, Mills GB, Liang H. Predicting Cancer Cell Line Dependencies From the Protein Expression Data of Reverse-Phase Protein Arrays. JCO Clin Cancer Inform. 2020 Apr;4:357-366. doi: 10.1200/CCI.19.00144.
70. Olivecrona M, Blaschke T, Engkvist O, Chen H. Molecular de-novo design through deep reinforcement learning. J Cheminform. 2017 Sep 4;9(1):48. doi: 10.1186/ s13321-017-0235-x.
Otras Reseñas Bibliográficas – Biología de Sistemas y Computacional en Cáncer
71. You J, Liu B, Ying R, Pande V, Leskovec J. Graph Convolutional Policy Network for Goal-Directed Molecular Graph Generation. arXiv:1806.02473v3.
72. Maziarka Ł, Pocha A, Kaczmarczyk J, Rataj K, Danel T, Warchoł M. Mol-CycleGAN: a generative model for molecular optimization. J Cheminform. 2020 Jan 8;12(1):2. doi: 10.1186/s13321-019-0404-1.
73. Gayvert KM, Madhukar NS, Elemento O. A Data-Driven Approach to Predicting Successes and Failures of Clinical Trials. Cell Chem Biol. 2016 Oct 20;23(10):1294- 1301. doi: 10.1016/j.chembiol.2016.07.023. Epub 2016 Sep 15.
74. Shen J, Cheng F, Xu Y, Li W, Tang Y. Estimation of ADME properties with substructure pattern recognition. J Chem Inf Model. 2010 Jun 28;50(6):1034-41. doi: 10.1021/ ci100104j.
75. Liu D, Schilling B, Liu D, Sucker A, Livingstone E, Jerby- Arnon L, et al. Integrative molecular and clinical modeling of clinical outcomes to PD1 blockade in patients with metastatic melanoma. Nat Med. 2019 Dec;25(12):1916- 1927. doi: 10.1038/s41591-019-0654-5. Epub 2019 Dec 2. Erratum in: Nat Med. 2020 Jul;26(7):1147.
76. Litchfield K, Reading JL, Puttick C, Thakkar K, Abbosh C, Bentham R, et al. Meta-analysis of tumor- and T cell-intrinsic mechanisms of sensitization to checkpoint inhibition. Cell. 2021 Feb 4;184(3):596-614.e14. doi: 10.1016/j.cell.2021.01.002. Epub 2021 Jan 27.
Referencias Bibliográficas – Biología de Sistemas y Computacional en Cáncer
77. Johannet P, Coudray N, Donnelly DM, Jour G, Illa- Bochaca I, Xia Y, et al. Using Machine Learning Algorithms to Predict Immunotherapy Response in Patients with Advanced Melanoma. Clin Cancer Res. 2021 Jan 1;27(1):131-140. doi: 10.1158/1078-0432.CCR-20- 2415. Epub 2020 Nov 18.
78. Sun D, Wang M, Li A. A multimodal deep neural network for human breast cancer prognosis prediction by integrating multi-dimensional data. IEEE/ACM Trans Comput Biol Bioinform. 2018 Feb 15. doi: 10.1109/ TCBB.2018.2806438. Epub ahead of print.
79. Chaudhary K, Poirion OB, Lu L, Garmire LX. Deep Learning- Based Multi-Omics Integration Robustly Predicts Survival in Liver Cancer. Clin Cancer Res. 2018 Mar 15;24(6):1248-1259. doi: 10.1158/1078-0432.CCR-17- 0853. Epub 2017 Oct 5.
80. Korfiatis P, Kline TL, Lachance DH, Parney IF, Buckner JC, Erickson BJ. Residual Deep Convolutional Neural Network Predicts MGMT Methylation Status. J Digit Imaging. 2017 Oct;30(5):622-628. doi: 10.1007/s10278- 017-0009-z.
81. Mobadersany P, Yousefi S, Amgad M, Gutman DA, Barnholtz-Sloan JS, Velázquez Vega JE, et al. Predicting cancer outcomes from histology and genomics using convolutional networks. Proc Natl Acad Sci U S A. 2018 Mar 27;115(13):E2970-E2979. doi: 10.1073/ pnas.1717139115. Epub 2018 Mar 12.
82. Bychkov D, Linder N, Turkki R, Nordling S, Kovanen PE, Verrill C, et al. Deep learning based tissue analysis predicts outcome in colorectal cancer. Sci Rep. 2018 Feb 21;8(1):3395. doi: 10.1038/s41598-018-21758-3.
83. Skrede OJ, De Raedt S, Kleppe A, Hveem TS, Liestøl K, Maddison J, et al. Deep learning for prediction of colorectal cancer outcome: a discovery and validation study. Lancet. 2020 Feb 1;395(10221):350-360. doi: 10.1016/ S0140-6736(19)32998-8.
84. Bates DW, Auerbach A, Schulam P, Wright A, Saria S. Reporting and Implementing Interventions Involving Machine Learning and Artificial Intelligence. Ann Intern Med. 2020 Jun 2;172(11 Suppl):S137-S144. doi: 10.7326/M19-0872.
Otras Referencias Bibliográficas – Biología de Sistemas y Computacional en Cáncer
85. Cavallo J. How Watson for Oncology is advancing personalized patient care. http://www.ascopost.com/issues/june-25-2017/how-watson-for-oncology-isadvancingpersonalized-patient-care/
86. Zhou N, Zhang CT, Lv HY, Hao CX, Li TJ, Zhu JJ, et al. Concordance Study Between IBM Watson for Oncology and Clinical Practice for Patients with Cancer in China. Oncologist. 2019 Jun;24(6):812-819. doi: 10.1634/ theoncologist.2018-0255. Epub 2018 Sep 4.
87. Seidman AD, Pilewskie ML, Robson ME, et al. Integration of multi-modality treatment planning for early stage breast cancer into Watson for Oncology, a decision support system: Seeing the forest and the trees. 2015 ASCO Annual Meeting. Abstract e12042. Presented May 29, 2015.
88. Kris MG, Gucalp A, Epstein AS, et al. Assessing the performance of Watson for oncology, a decision support system, using actual contemporary clinical cases. 2015 ASCO Annual Meeting. Abstract 8023. Presented May 29, 2015.
89. Cavallo J. Confronting the Criticisms Facing Watson for Oncology https://ascopost.com/issues/september-10-2019/
90. Somashekhar SP, Sepúlveda MJ, Shortliffe, et al. A prospective blinded study of 1,000 cases analyzing the role of artificial intelligence: Watson for Oncology and change in decision-making of a multidisciplinary tumor board from a tertiary care cancer center. 2019 ASCO Annual Meeting. Abstract 6533. Presented June 1, 2019.
91. Jie Z, Zhiying Z, Li L. A meta-analysis of Watson for Oncology in clinical application. Sci Rep. 2021 Mar 11;11(1):5792. doi: 10.1038/s41598-021-84973-5. PMID: 33707577.
Autor – Biología de Sistemas y Computacional en Cáncer
1 Andrés F. Cardona, MD. MSc. PhD. MBA. Dirección de Investigación y Educación, Centro de Tratamiento e Investigación sobre cáncer Luis Carlos Sarmiento Angulo (CTIC), Bogotá, Colombia.
2 Fundación para la Investigación Clínica y Molecular Aplicada del Cáncer – FICMAC, Bogotá, Colombia.
3 Andrés F. Cardona, Grupo de Investigación en Oncología Molecular y Sistemas Biológicos (Fox-G), Universidad El Bosque, Bogotá, Colombia.
4 Luis Eduardo Pino, Erick Cantor, Grupo Oncología Clínica, Instituto de Cáncer Carlos Ardila Lülle, Fundación Santa Fe de Bogotá, Bogotá, Colombia.
Recibido: 12 de noviembre de 2021
Aceptado: 22 de noviembre de 2021
Correspondencia:
Andrés F. Cardona
acardona@fctic.org