Leucemia linfoide aguda y la introducción de la quimioterapia combinada
En la década de1960 se introdujo la quimioterapia con múltiples agentes, lo que permitió vencer la resistencia a agentes únicos y así aumentar drásticamente la supervivencia de pacientes con enfermedades hematológicas. En 1964, E. Frei y E.
Freireich utilizaron un régimen de combinación de múltiples fármacos quimioterapéuticos en niños con leucemia (8). La primera quimioterapia combinada de dosis alta se denominó “VAMP”; comprendía vincristina, ametopterina (metotrexato), mercaptopurina y prednisona.
Sin embargo, este régimen de quimioterapia de combinación de dosis alta tuvo graves efectos adversos, lo que impulsó ensayos clínicos adicionales para alcanzar una combinación de fármacos con mejor perfil toxicológico (9).
En 1965 se introdujo el régimen conocido como POMP (6-mercaptopurine vincristina, metotrexato, y prednisona) que hoy en día continua utilizándose como terapia de mantenimiento en la leucemia linfoblástica aguda (LLA) (10).
No hay duda de que el tratamiento de la (LLA) ha sido un éxito sobresaliente.. La LLA fue el primer cáncer que entró en remisión con quimioterapia.
La euforia inicial que produjeron los resultados esperanzadores en el tratamiento de la LLA se atenuó cuando se evidenciaron las recaídas testiculares y en el sistema nervioso central. Inicialmente se utilizaron la irradiación craneal y el metotrexato intratecal.
Aunque estas modalidades son efectivas para prevenir las recaídas, también se asociaron con toxicidades cognitivas significativas (11).
En la actualidad, en pacientes con enfermedad de bajo riesgo y ausencia de enfermedad residual mínima (definida como <0,01% de células leucemia en la medula ósea) se puede evitar el uso de irradiación craneal sin alterar las tasas de curación (12). Hoy en día, 90% de los niños en países occidentales son sobrevivientes a largo plazo.
La historia de la leucemia promielocítica aguda
La historia de la leucemia promielocítica aguda (LPMA), una variante de la leucemia mieloide aguda (LMA), es otro avance notable en el tratamiento de la leucemia. La LPMA se describió en 1957 por Leif K. Hillested (13).
La inducción con danorubicina no fue exitosa y por el contrario, los pacientes fallecieron a consecuencia de hemorragias y coagulopatías severas. En 1981, Theodore R. Breitman indujo la diferenciación de promielocíticos agudos de leucemia con ácido retinoico (14).
Christine Chomienne, luego demostró los efectos diferenciadores del ácido trans retinoico (ATRA) en células de leucemia promielocítica aguda in vitro y, demostró que el ATRA era diez veces más potente que el ácido 13-cis retinoico.
Posteriormente, en 1988 investigadores en Shanghái, afirmaron que la remisión en la LPMA podría inducirse utilizando el agente diferenciador ATRA (15).
Entre tanto, el arsénico que se utilizó en Manchuria hace más de 2.000 años, solo se reportó en la literatura occidental en 1930 como agente terapéutico. Inicialmente en el tratamiento popular para la leucemia mieloide crónica (LMC).
El compuesto trióxido de arsénico se investigó en China para el tratamiento contra el cáncer desde la década de 1970 y posteriormente se reportaron respuestas exitosas con este compuesto intravenoso en pacientes con LPMA en 1992 (16). Ambos agentes tienen un lugar definido en la medicina occidental en el tratamiento de la LPMA (17, 18).
La introducción de la citogenética y el desarrollo de Imatinib
Durante la década de 1950, los científicos tenían un conocimiento limitado sobre la influencia de las mutaciones genéticas en el desarrollo del cáncer.
A pesar de esto, algunos investigadores centraron sus estudios en la relación de la citogenética y la biología del cáncer. Con el fin de identificar alteraciones cromosómicas especificas con causalidad directa en la oncogénesis.
Durante ese tiempo, Nowell y Hungerford se dedicaron a entender la biología de LMC. En 1960, estos investigadores notaron que uno de los 46 cromosomas era anormalmente corto. Éste se denominó más tarde como “cromosoma Filadelfia” en honor a la ciudad en donde fue descrito (19).
Las investigaciones subsiguientes demostraron que el 95% de los pacientes con LMC tienen el cromosoma Filadelfia.
Gracias al progreso en la citogenética:
Se determinó que este cromosoma era el resultado de una translocación reciproca entre los brazos largos de los cromosomas 9 y 22 t (9, 22) (Figura 3). La translocación produce una proteína de fusión expresada en células malignas conocida como BCR-Abl (breakpoint cluster region–v-Abl Abelson murine leukemia viral oncogene homolog) (20).
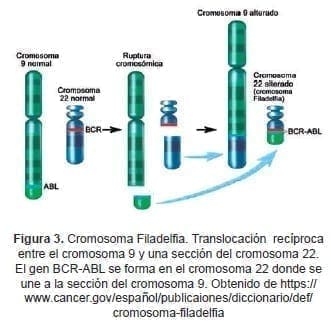
La importancia de la BCR-Abl se demostró a medida que se caracterizaron las proteínas tirosina quinasas, esenciales en el crecimiento y la diferenciación (21).
En consecuencia, el vínculo con la LMC se hizo evidente, al entender que el Abl era una proteína tirosina quinasa. Posteriormente, una serie de estudios confirmaron que la presencia de la BCR-Abl es la causa oncogénica y no el resultado de la LMC (22).
Con esta información, se preparó el escenario para el diseño racional de la terapia dirigida en oncología.
Hasta entonces, la terapia estándar para la LMC era similar al tratamiento de otras neoplasias malignas. Consistente en la administración de esquemas citotóxicos intensos, invasivos y poco efectivos. Sin embargo, la identificación del producto genético causante de la enfermedad alentó a los investigadores a buscar agentes que interfirieran específicamente con la función de la proteína de fusión BCR-Abl.
Esta búsqueda finalmente condujo a la identificación del mesilato de imatinib (Gleevec). Como un inhibidor de BCR-Abl (23) que ha afectado dramáticamente la calidad de vida de los pacientes que padecen LMC.
Así, la historia del cromosoma Filadelfia se estableció como un nuevo paradigma. Donde la observación clínica y la ciencia básica rigurosa resultaron en nuevas hipótesis que pueden traducirse en la práctica clínica.
(Lea También: Linfoma de Hodgkin)
Leucemia mieloide aguda y el esquema “7+3”
Pocos enfoques terapéuticos para las enfermedades malignas se han mantenido esencialmente iguales en los últimos 40 años. Como ocurre con la terapia de inducción para la leucemia mieloide aguda (LMA) consistente en la infusión intravenosa continua de arabinósido de citosina con daunorrubicina (24).
En 1951, el nucleósido natural arabinosa de timina se aisló a partir de la esponja Cryptotethia crypta.
A mediados de la década de 1960, se demostró que el clorhidrato de arabinósido de citosina inhibía el metabolismo in vitro de los ácidos nucleicos en sistemas celulares bacterianos, virales y tumorales (25).
Schabel y Skipper demostraron que el crecimiento de leucemia era sensible al arabinósido de citosina durante la síntesis de ADN. La fase S del ciclo mitótico celular (26).
Posteriormente, Freireich y sus colegas del Instituto Nacional de Cáncer de los Estados Unidos (NCI) trataron a 14 pacientes con LMA con una infusión continua de arabinósido de citosina durante 5 días. Seis pacientes alcanzaron una remisión parcial no duradera.
Ellison, Holland y colegas se centraron en el efecto de la infusión continua de arabinósido de citosina sobre el recuento de células sanguíneas al comprobar que la frecuencia de administración continua del fármaco era esencial para aumentar la efectividad (27).
En cuanto a la daunorrubicina, el otro pilar del esquema 7+3, éste se aisló a principios del siglo XX a partir de antibióticos antimitóticos de bacterias del suelo (actinomycete). En el Hospital General de Massachusetts, distintos colaboradores compararon la terapia combinada con arabinósido de citosina con 5-tioguanina, 6-mercaptopurina o daunorrubicina.
Los investigadores concluyeron que la combinación de arabinósido de citosina con daunorrubicina fueron significativamente superiores para inducir remisión en los pacientes con LMA. Comparado con la administración única de arabinósido de citosina (28).
Con esta experiencia previa, en 1973, Yates y colegas documentaron en un estudio clásico los resultados del programa de tratamiento consistente en 7 días de 100mg /m2 de arabinósido de citosina y 3 días de 45 mg/m2 daunorrubicina en 16 pacientes con LMA. 63% de los pacientes entraron en remisión con este esquema de inducción, que proporcionaba el mejor balance entre la terapia intensiva. La probabilidad de remisión y la toxicidad asociada a la terapia (29).
Si bien la introducción del esquema terapéutico 7+3 mejoró las tasas de remisión y supervivencia, este progreso también surgió gracias a distintos avances en la medicina. Incluyendo el uso de catéteres centrales. La asepsia y disponibilidad de soporte transfusional de plaquetas.
Es evidente, sin embargo, que el desarrollo de terapias alternas de inducción es el centro de investigación para múltiples oncólogos dedicados al tratamiento de la LMA. Que busca mejorar la supervivencia de pacientes adultos mayores quienes con frecuencia no toleran este esquema. Por fortuna en los últimos 5 años hay muchos nuevos tratamientos con resultados esperanzadores (30).