La insulina9-11 está indicada en diabetes tipo 1, en la gestacional y en la diabetes tipo 2, cuando esta última no responde al tratamiento con antidiabéticos orales.
Llamamos insulinas tradicionales a las que tienen una molécula protéica idéntica a la insulina humana, por lo que también se les denomina insulinas humanas. Las insulinas de aparición más reciente son compuestos análogos de insulina humana, es decir, cuya molécula se ha modificado para aumentar la rapidez –y relativa brevedad de acción- o su mayor duración, permitiendo niveles basales prolongados.
Actualmente –entre las insulinas tradicionales- sólo se utilizan insulinas producidas por la tecnología del ADN recombinante, que han reemplazado total mente las insulina bovinas, porcinas y otras. Las usuales son las insulinas cristalinas o R, las NPH o N (Humulín, Novolín, Gansulín) y las combinaciones 70/30 (70 unidades de NPH y 30 de cristalina, por cada mililitro), cuyas marcas son Humulín 70/30 (NPH y R), Humalog mix (75% NPH, 25% lispro) y Novomix 70/30 (70% NPH, y 30% aspártica). En relación a las mezclas, debemos anotar que el Plan Obligatorio de Salud (POS) en Colombia no las cubre, pero se puede hacer una premezcla manual de NPH y cristalina, extrayendo primero la dosis correspondiente insulina R y luego la N, para aplicar en una sola inyección. Aunque hay algunas diferencias en la técnica de manufactura, en la práctica son moléculas idénticas.
Las presentaciones son de cien unidades por ml (U-100), aunque en la China todavía hay presentaciones de Gansulín U-40, que requieren jeringas especiales para esta concentración. En nuestro medio, las jeringas desechables (en las que se puede meter hasta 30, 50 o 100 unidades), están todas hechas para U-100. Es de anotar que estas jeringas pueden utilizarse hasta 10-12 veces, descartándolas una vez la aguja se pone roma. La aplicación subcutánea se hace con la aguja dirigida de frente a la piel, ligeramente inclinada.
Es necesario utilizar sitios nuevos cada vez, pues no deben reutilizarse los sitios al menos en un mes, ya que la generación de aprotininas locales reduce la eficacia hipoglicemiante de la insulina. Los sitios de inyección son el abdomen (alrededor del ombligo, a cierta distancia de este), cintura y glúteos, parte posterior de brazos y anterior de muslos.
Para facilitar el uso de la insulina –particularmente en personas con mala visión- o cuando se quiere tener la jeringa ya preparada para su aplicación, existen las plumas de insulina (Humapen, Novopen). El cartucho recambiable contiene 300 unidades o 3 ml. Estas plumas disminuyen los errores en la dosificación de insulina, sobre todo en pacientes de edad avanzada. Se puede verifi car la exactitud de la dosis, no sólo visualmente (aparece un número con la cantidad de unidades que se inyectan), sino también mediante un control auditivo o “clic”.
Otro sistema de administración de la insulina es por medio de una bomba de infusión continua subcutánea de insulina, de uso en diabetes tipo 1. La temperatura recomendada para la conservación de la insulina, ya en uso diario, en de menos de 30º C y más de 2º C, pues dura un mes sin degradarse. La insulina sin abrir debe mantenerse en el refrigerador en una temperatura de entre 2º y 8º, o –si esto no es posible debe mantenerse en un lugar fresco y oscuro.
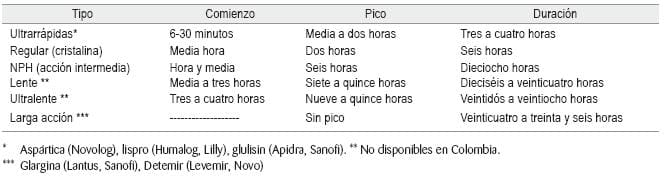
La aplicación convencional de la insulina es cada doce horas, iniciando con 10 unidades antes del desayuno y comida, bien NPH o 70/30. Se puede iniciar administrando 0.3 U/Kg/peso –pasando paulatinamente a una dosis de 0.5/0.6 mg/Kg/peso diarios) y distribuyendo 2/3 de la dosis antes del desayuno, y 1/3 antes de la cena, y una proporción rápida/NPH de 1/3 antes del desayuno y 1/2 antes de la cena. Teniendo en cuenta que para un adulto de 65-70 Kg, la dosis total es usualmente de unas 40 unidades diarias (25 en a.m., 15 en p.m.), de las veinticinco unidades de la mañana podrían ser aproximadamente 20 de NPH y 5 de cristalina, y de las quince de la noche, 10 de NPH y 5 de cristalina. Cuando las glicemias postprandiales están > 180 mg/dL, es conveniente utilizar la mezcla 70/30. Una única dosis de NPH hacia las 10:00 p.m. (entre 6 y 15 unidades) se utiliza en casos en que el control no es bueno con dos hipoglicemiantes orales asociados.
Probablemente el paciente en un plazo no muy distante de tiempo, tendrá que pasar a solo insulinoterapia, con suspención de la terapia oral. Estas dosifi caciones son algo empíricas, pues dependen del grado de absorción y de la sensibilidad de los receptores (que tiene que ver con el peso, con medicamentos, etc). Lo importante es cumplir con la meta de obtener hemoglobinas glicosiladas de < 7%, o glicemia en ayunas normales y postprandiales un poca más altas. La insulinoterapia que se aplica en microgoteo (1-2 UI/hora) se utiliza en casos de cetoacidosis diabética (con la correspondiente hidratación y administración de electrolitos y glucosa), o durante procedimientos quirúrgicos, particularmente en los de una duración mayor a cuatro horas. En la tabla 1 vemos los esquemas de aplicación de la insulina.
Para facilitar el uso de la insulina –particularmente en personas con mala visión- o cuando se quiere tener la jeringa ya preparada para su aplicación, existen las plumas de insulina. El cartucho recambiable contiene 300 unidades o 3 ml. Estas plumas disminuyen los errores en la dosificación de insulina, sobre todo en pacientes de edad avanzada. Se puede verificar la exactitud de la dosis, no sólo visualmente (aparece un número con la cantidad de unidades que se inyectan), sino también mediante un control auditivo o “clic”. Otro sistema de administración de la insulina es por medio de una bomba de infusión continua subcutánea de insulina, de uso en diabetes tipo 1. En la tabla 2 vemos el inicio y duración de acción de las insulinas humanas y de los nuevos análogos.
Las nuevas insulinas
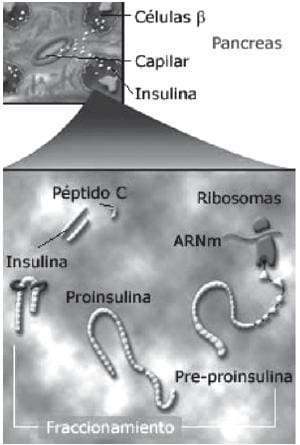
La secreción fisiológica de insulina tiene un componente basal continuo y otro agudo, desencadenado por la hiperglicemia. Este a su vez es bifásico; cuando se logra experimentalmente durante una hora un incremento de dos a tres veces los niveles basales de ayuno en una persona, los niveles de insulina aumentan marcadamente, debido a la liberación de insulina ya formada y almacenada. Después comienza un segundo pico de insulinemia, que corresponde a nueva hormona sintetizada que se va liberando de inmediato, lo que indica que la hiperglicemia postprandial no sólo estimula la liberación de insulina almacenada sino también la trascripción nuclear del gen insulínico y la traducción de su ARN mensajero12. El ARN mensajero infl uye sobre los ribosomas para que se produzca una pre-proinsulina, que luego se trastorna en proinsulina, la que por clivaje da lugar a la insulina y al péptido C (Figura 2). La principal sustancia que estimula la secreción de insulina es la glucosa. Las etapas involucradas en este proceso son las siguientes:
TABLA 1. Esquema simplificado de insulinoterapia

TABLA 2. Tipos de insulinas (Tiempo aproximado de acción)
 ✓ Un transportador de glucosa –por difusión facilitadora- introduce el monosacárido a la beta célula.
✓ Un transportador de glucosa –por difusión facilitadora- introduce el monosacárido a la beta célula.
✓ Al aumentar la concentración de glucosa dentro de la célula beta, la membrana se despolariza e ingresa calcio proveniente del espacio extra-celular, lo que induce la exocitosis de los gránulos de insulina.
✓ El aumento en la glucosa intra-celular activa también mecanismos calcio-independientes de la secreción de insulina.
En no diabéticos, la comida produce un rápido aumento en la concentración de insulina plasmática hacia la media hora, seguida por una disminución a las cifras basales hacia las dos o tres horas. Para lograr replicar este patrón, se han desarrollado análogos como la glargina o el detemir, que dan un nivel basal continuo, y otras rápidas como la lispro o la aspártica, que se administran antes de cada comida. Estos análogos que poseen diferente rapidez de absorción y de duración, se han logrado gracias al cambio en la secuencia de aminoácidos de la insulina humana.
Las rápidas –con menor tendencia a asociarse en complejos hexaméricos- son la lispro o Humalog, que presenta un intercambio entre la prolina de la posición 28 de la cadena B por la lisina de la posición 29 y la aspártica o Apidra, en la que se sustituye la prolina en la posición 28 de la cadena B por ácido aspártico, lo que reduce la tendencia a la agregación de los monómeros.
La insulina glargina (Lantus) es un análogo de insulina de acción larga que se produce al añadir a la insulina humana -por recombinación genética- dos argininas en la región C-terminal de la cadena B, y sustituir la asparagina por glicina en la posición A 21 de la cadena A, lo que da una insulina estable que es soluble en el pH 4 del vial, pero se precipita en microcristales en el pH neutro del lugar de la inyección; al disolverse estos, la insulina pasa a la sangre en forma lenta y sin picos.
La insulina detemir (Levemir) es un análogo soluble que se caracteriza por la unión de la insulina al ácido graso mirístico. El complejo formado se une a receptores de ácidos grasos presentes en la albúmina del paciente, tanto en el tejido celular subcutáneo como en sangre como en líquidos intersticiales, separándose de la proteína para ser luego recaptada. La insulina detemir circulante está unida a la albúmina en más de un 98 % y sólo su fracción libre puede unirse a los receptores de las células blanco.
Una nueva insulina inhalada (Exubera) fue aprobada por la FDA. Sus principales inconvenientes han sido la de necesitar dosis de insulina mayores debido a su penetración limitada al alveólo, lo que la hace menos eficiente que la insulina subcutánea, pues parte se deposita en el dispositivo inhalador, en la boca o en la garganta, y tiene un costo mayor. Después de comercializada, la casa Pfizer resolvió retirarla del mercado, por poca aceptación por parte de médicos y pacientes, ya que no resultó mejor que la subcutánea, y tenía efectos colaterales a nivel pulmonar, algunos preocupantes como la eventual fibrosis pulmonar. En la figura 3, vemos los niveles que dan la combinación de insulinas de acción larga y las de acción corta, que recuerdan el patrón fisiológico de liberación con la insulina en relación con la ingesta.
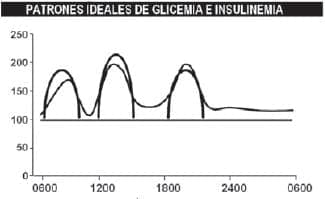
FIGURA 3. La línea recta corresponde a los niveles basales de insulina de larga acción (glargina), los tres picos que se desprenden de la línea basal corresponden a la insulina de acción ultra-rápida, y la línea ondulada a los niveles pre y postprandiales de glicemia. La línea vertical muestra los niveles de glicemia en mg/dL y la línea horizontal, las horas del día.
Incretinomiméticos y otros medicamentos nuevos, de uso en diabetes y en obesidad
Incretinomiméticos
Se calcula que el páncreas produce diariamente unas cincuenta unidades de insulina, cuyo principal estímulo secretor es la glucosa. Existen estímulos secundarios: cuando este carbohidrato se administra endovenosamente, los niveles insulínicos suben rápidamente en sangre pero no llegan a ser tan altos como cuando la glucosa se administra por vía yeyunal a través de un catéter. Esto se debe a la secreción –cuando se comede dos hormonas intestinales insulinotrópicas llamadas incretinas, el péptido tipo glucagón (GLP-1) y el péptido inhibitorio gástrico (GIP), también denominado péptido insulinotrópico dependiente de glucosa (inicialmente llamado enterogastrona); estos secretagogos estimulan la producción de insulina.
Además de su acción insulinotrópica, el GLP-1 inhibe la secreción de glucagón, baja los niveles de glicemia, promueve la diferenciación de las células progenitoras de los islotes y mejora la función y la duración de la beta-célula. El incretinomimético que se administra por vía oral es la sitagliptina (Januvia), un inhibidor de las enzimas DPP-4 o dipeptidil peptidasa 4, que se encarga de la hidrólisis de las incretinas GLP-1 y el péptido insulinotrópico glucosa dependiente (GIP). Puede usarse sola, como monoterapia, o en asociación con la metformina y eventualmente las glitazonas. En investigación está otra molécula de la categoría, la vidagliptina13.
Al mantener estas incretinas por un periodo más largo en el organismo, la sitagliptina –que es neutra en relación con la ganancia o pérdida de peso y no tiene efectos secundarios gastrointestinales, logra mejorar los niveles de hemoglobina glicosilada, gracias a las acciones del péptido tipo glucagón 1 y del GIP. La dosis es de 100 mg diarios, y se espera que prolongue el período que termina cuando el paciente se torna insulinopénico14,15,16.
Otro incretinomimético –este inyectable- es la exenatida o Byetta. Hace una mímica de la secreción insulínica glucosa-dependiente, suprime la secreción elevada del glucagón (poniendo especial acción en la hiperglicemia post-prandial), y retarda el vaciamiento gástrico, lo que facilita la pérdida de peso pero genera intolerancia gástrica, como las náuseas. Este polipéptido de 39 aminoácidos tiene una estructura parecida a la del GLP-1. Se puede utilizar en asociación con la metformina o una sulfodroga, en dosis de 5 a 10 mg subcutáneos cada doce horas, antes de las comidas. Se aplica en las mismas áreas donde se inyecta la insulina.
