La Historia Natural de las metástasis hepáticas por cáncer colo-rectal sin tratamiento, tienen un pronóstico muy malo: es así como los trabajos realizados antes de perfeccionarse el tratamiento quirúrgico, mostraba una supervivencia media de 5 a 10 meses, y la sobre vida a 5 años era de 0.
Los pacientes, una vez diagnosticada la metástasis, fallecen el 30%, y el 70% de las muertes restantes se atribuye a enfermedades concomitantes.
Los trabajos de Foster1 durante los años 70, mostraron que la resección de las metástasis únicas o limitadas a un lóbulo, se podría realizar en un 10 a un 30% de los pacientes sometidos a Laparotomía (Hemicolectomía), por cáncer de colon o recto. (Lea también: Artículo de Revisión, Cirugía de Hígado por Metástasis Secundarias a Cáncer Colo-Rectal)
Con esta cirugía se logró una sobre vida del 20% de los pacientes a 5 años, siendo esto un gran avance al compararlos con los anteriores resultados sin resección (cercana al 0%). Este mismo autor revisó la experiencia en 99 Instituciones de renombre Mundial durante 14 años en las que se practicaron 168 resecciones hepáticas, observando en 5 años una supervivencia del 20%.
Luego de esta experiencia inicial, algunos Centros Quirúrgicos fueron mejorando la técnica y se obtuvieron notables resultados en las resecciones hepáticas, disminuyendo su morbilidad y mortalidad, lo que les permitió ampliar las indicaciones.
Una de las mayores experiencias se obtuvo en el Hospital Universitario de Erlangen (Alemania), donde hubo un total de 1718 pacientes con metástasis a hígado de carcinoma colo-rectal, durante el período de 1960 a 1992 a los que se les practicaron 469 resecciones hepáticas (27,3%).
De estas resecciones 434 (25,3%) fueron realizadas con intento curativo, con seguimiento a largo plazo. La sobre vida a 5 años fue del 39%, a los 10 años del 24%, y a los 20 años fue del 18%.
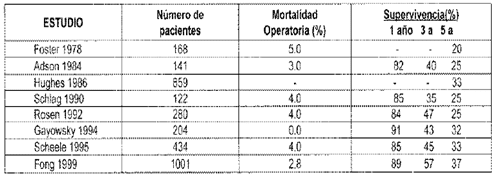
TABLA 1. Resecciones Hepáticas por Metástasis Cáncer Colo-Rectal (2)
Otro aspecto destacado de esta experiencia fue la mortalidad operatoria del 4,4%, esta se redujo al 1,8% durante los últimos 3 años del período estudiado.También se encontró que el número de metástasis no afectaba la sobre vida si todas eran resecables.2
En 1996, se publicó la experiencia en varios centros médicos franceses, reunidos en la Asociación Francesa de Cirugía. Se revisaron 1568 historias clínicas a cuyos pacientes se les practicó resección hepática por metástasis de cáncer colo-rectal, encontrándose como factores pronósticos de supervivencia posterior, las siguientes:
– Edad del paciente.
– La metástasis de mayor tamaño.
– Los niveles de antígeno carcinoembrionario.
– El estado del tumor primario.
– El intervalo libre de enfermedad (2 años).
– El número de nódulos hepáticos.
– El margen de resección.
Así mismo encontraron como factores pronósticos de recurrencia posterior:
– La edad del paciente (mayor de 60 años).
– Extensión a la serosa por el cáncer primario.
– Invasión linfática del cáncer primario.
– Período libre de metástasis (2 años).
– Metástasis mayores a 5 cms.
– Más de cuatro metástasis.
La localización de las metástasis y la extensión de la resección, no fueron significativas. Con base en lo anterior, la misma Asociación Médica propuso un sistema de puntaje para establecer el pronóstico de los pacientes en la resección de cáncer colo-rectal metastásico, así:
– Grupo de bajo riesgo: aquellos pacientes que tienen de 0 a 2 factores pronósticos, teniendo estos una supervivencia del 79% a dos años.
– Grupo de medio riesgo: aquellos pacientes con 3 o 4 factores pronósticos, teniendo estos una supervivencia del 60% a dos años.
– Grupo de alto riesgo: aquellos pacientes con 5 a 7 factores pronósticos, con una supervivencia del 43% a dos años3.
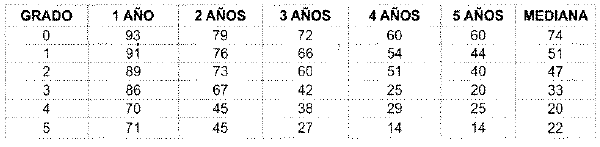
A cada uno de estos factores de riesgo se le otorga un punto, y esto se relaciona con la sobre vida a 5 años (así los pacientes sin ningún factor de riesgo tendrán una sobre vida a 5 años del 60%, con tres factores de riesgo tendrán una sobre vida del 20%). Esto fue sustentado en la revisión de 1001 casos consecutivos de resección hepática por metástasis colo-rectal, en el Memorial Sloan Kettering Cancer Center, New York.
TABLA 2. Grado de Riesgo Clínico de la Recurrencia del Tumor
Para otros investigadores, las recurrencias posteriores a la resección hepática, consecutivas a metástasis colo-rectal están directamente relacionadas con:
– Enfermedad extrahepática.
– Tumor bilateral (metástasis).
– Ganglios positivos en el tumor primario.
– Intervalo libre de enfermedad menor de 12 meses.
– Más de un tumor.
– Tamaño mayor de 5 cms.
– Antígeno carcinoembrionario mayor a 200 ng/ml.
– Inadecuada resección de los márgenes (positivo).
– Invasión microvascular.
Sin embargo, hay mucha controversia respecto a los factores predictores de recurrencia, pues otros autores han encontrado diferentes factores, como se resume en la tabla número 3.
TABLA 3. Predictores de la Recurrencia Posterior a la Resección Hepática por Metástasis de Cáncer Colorectal
2 Schelle J, World J. Surg. 1995; 19: 59-71.
3 Nordlinger B., Association Francaise de Cirurgie. Cancer. 1996; 77: 1254-1262.
En la gráfica número 1, se observa la supervivencia después del tratamiento de la metástasis colo-rectal al hígado. La curva inferior representa el cálculo de supervivencia desde la resección hepática. La curva superior representa la supervivencia calculada desde el tiempo de la resección del cáncer primario colorectal.
En los últimos años, se ha recomendado el uso de la Laparoscopia para descartar enfermedad irresecable, en pacientes con lesiones sospechosas o con tres o más factores de riesgo de residivas
En el Memorial Sloan Kettering Cancer Center de New York, se está utilizando la laparoscopia como método de estadifi cación en tumores hepatobiliares.
En 410 pacientes estudiados, encontraron que 153 tenían enfermedad irresecable, 84 de los cuales fueron identificados laparoscópicamente, aumentando la tasa de resecabilidad del 62% al 78% El Ultrasonido laparoscópico sirve para efectuar una evaluación exacta mediante él se puede observar la capacidad del remanente hepático, así como las metástasis intrahepática.
Es menos sensible para determinar:
– La extensión de la invasión a los órganos adyacentes
– Trombosis vascular en grandes vasos, ocasionados por el tumor Como limitaciones del Ultrasonido laparoscópico podemos mencionar:
– la palpación de la lesión no es posible bajo laparoscopia.
– si se sospecha invasión de órganos adyacentes, no se puede realizar una disección de prueba.
– el ángulo y la dirección del Scan están limitados por el puerto de salida.
– el Ultrasonido laparoscópico es menos exacto en tumores grandes.
Finalmente existe la posibilidad de metástasis en los puertos de laparoscopia cuando se toman biopsias, sin embargo este riesgo parece ser muy bajo. El Ultrasonido Intraoperatorio tiene mejor sensibilidad que el Ultrasonido preoperatorio para detectar metástasis, es así como la mayoría de los centros quirúrgicos lo utilizan para completar la evolución del número y localizaciòn de las metástasis.
Con la ampliación de las indicaciones de resección hepática, nos planteamos la siguiente pregunta: ¿a qué pacientes con metástasis colo-rectal se les puede realizar la cirugía? Los datos recolectados sobre los factores pronóstico parecen indicar que la única contraindicación para realizar una resección es la enfermedad extrahepática, siempre y cuando se puedan resecar todas las lesiones con un margen negativo, y conservando una cantidad de parénquima hepático aparentemente normal superior al 25%.
En el Memorial Sloan Kettering Cancer Center de New York, se está utilizando la laparoscopia como método de estadificación en tumores hepatobiliares.
En 410 pacientes estudiados, encontraron que 153 tenían enfermedad irresecable, 84 de los cuales fueron identifi cados laparoscópicamente, aumentando la tasa de resecabilidad del 62% al 78%. El Ultrasonido laparoscópico sirve para efectuar una evaluación exacta mediante él se puede observar la capacidad del remanente hepático, así como las
metástasis intrahepática. Es menos sensible para determinar:
– La extensión de la invasión a los órganos adyacentes.
– Trombosis vascular en grandes vasos, ocasionados por el tumor Como limitaciones del Ultrasonido laparoscópicopodemos mencionar:
– la palpación de la lesión no es posible bajo laparoscopia.
– si se sospecha invasión de órganos adyacentes, no se puede realizar una disección de prueba.
– el ángulo y la dirección del Scan están limitados por el puerto de salida.
– el Ultrasonido laparoscópico es menos exacto en tumores grandes.
Finalmente existe la posibilidad de metástasis en los puertos de laparoscopia cuando se toman biopsias, sin embargo este riesgo parece ser muy bajo. El Ultrasonido Intraoperatorio tiene mejor sensibilidad que el Ultrasonido preoperatorio para detectar metástasis, es así como la mayoría de los centros quirúrgicos lo utilizan para completar la evolución del número y localizaciòn de las metástasis (Tabla 5).
Con la ampliación de las indicaciones de resección hepática, nos planteamos la siguiente pregunta: ¿a qué pacientes con metástasis colo-rectal se les puede realizar la cirugía? Los datos recolectados sobre los factores pronóstico parecen indicar que la única contraindicación
para realizar una resección es la enfermedad extrahepática, siempre y cuando se puedan resecar todas las lesiones con un margen negativo, y conservando una cantidad de parénquima hepático aparentemente normal superior al 25%.
La técnica quirúrgica requiere un equipo interdisciplinario que incluya: radiólogo, anestesiólogo, patólogo, oncólogo, cirujano e intensivista. Por ser una cirugía mayor, requiere de una buena evaluación funcional preoperatoria, y de una buena evaluación radiológica, para descartar otras lesiones y para aproximarse a la anatomía del paciente.
En la Figura 1, se observan las incisiones más utilizadas para las resecciones hepáticas, como son la incisión subcostal derecha (A-B), que puede extenderse hacia el lado izquierdo (B-C), hacia la línea media, en forma de Mercedes (B-D-E) o, hacia el tórax, con una incisión toracoabdominal (A-B-F).
* Basado en la anatomía portal y venosa.
* El hígado se encuentra dividido en 8 segmentos, por:
– 3 cisuras verticales.
– 1 cisura transversal.
En el hígado izquierdo la cisura portal izquierda, divide los segmentos 2 y 3, del segmento 4.
La cisura portal media divide el segmento 4 de los segmentos 5 y 8.
La cisura portal derecha divide los segmentos 5 y 8+ de los segmentos 6 y 7.
La extensión de la resección hepática, puede incluir desde un segmento hasta las resecciones mayores como la hepatectomía (lobectomía) derecha o izquierda, y la trisegmentectomía derecha o izquierda como nos permitimos presentarlas en las Figuras 4 y 5.
4 Fong Y. Ann of Surg, 1999; 230: 309-321.
5 Fong, 2003.
6 D’Angelica M, 2003.
7 Lo.C, 1998.
8 Velez Vergnaud, JP. 2001. Metástasis en los sitios de puertos de cirugía laparoscópica de cancer de colon.
9 MACHI J. ISOMOTO H, KUROHIJI T., et al. Accuracy of Intraoperative Ultrasonography in diagnosing liver metastases from colorectal
cancer: evaluation witb prospective follow-up results. World J. Surg . 1991 Jul-Aug; 15: 551-6.
10 Altendorf – Hoymann 2003 Surg Oncol Clin N. Ann. 2003; 12: 165-192

Imagen 10
IMAGEN 11. Trisegmentomía izquierda

IMAGEN 12.
A continuación se muestran tres imágenes de la misma paciente del scán anterior durante la cirugía (31/01/2004), Clínica San Pedro Claver, a la que tuve la oportunidad de asistir.
FIGURA 6. Medición de la superfi cie reseccionada del hígado

FIGURA 7. Técnica de disección hiliar tradicional
La correspondiente arteria hepática y el conducto biliar son ligados y cortados.(A) La vena portal correspondiente es ocluida usando un clamp, cortada y suturada con sustancias no absorbibles de tipo monofilamento antes de cortar el parénquima (B).
Para el control vascular del Hilio-hepático, hay dos técnicas principales: La disección individual de las estructuras (Portal, arterial e hilial), como se observa en la figura 7, o la sección con grapadora mecánica, sin disección individual de las estructuras, como se observa en la Figura 8.
El control de la Porta intra hepática se obtiene por hepatotomía cerca al pedículo portal correspondiente.
El TA-30 grapadora vascular es introducido para reparar el pedículo durante la transección con caucho para cortar el daño del conducto hiliar que confluye.
Algunos autores recomiendan el abordaje, rodeando la cápsula Glissoniana11 en la que van envueltos los pedículos hepáticos, lo cual permite su control y ligadura sin realizar una disección individual de las estructuras. Observar Figura 9.
Para la sección del parénquima, se ha utilizado la técnica de Kellyclasia, aplastando el parénquima hepático y visualizando las estructuras vasculares. Un avance importante en la técnica quirúrgica para resecciones hepáticas, ha sido el control vascular para prevenir el sangrado.
La Maniobra de Pringle es tradicionalmente usada durante la hepatectomía para reducir la pérdida de sangre, pero puede inducir a una lesión isquémica del hígado, por lo cual su uso era controversial hasta que se realizó un estudio prospectivo aleatorizado.
En el Departamento de Cirugía del Hospital Queen Mary de la Universidad de Hong Kong, en Hong Kong, se escogieron cien pacientes de manera aleatoria para practicar la Maniobra de Pringle; durante veinte minutos, con cinco minutos de intervalo vs paciente sin la Maniobra. Encontrándose que al efectuar dicho procedimiento, se observó:
una menor pérdida de sangre, expresada en milímetros por centímetro cuadrado de superficie de transección hepática. un menor tiempo quirúrgico una mejor preservación de la función hepática en el período post-operatorio inmediato que las tasas de complicación y mortalidad fueron similares’213. [Ver Figura 10].
En caso de lesiones muy cercanas a la vena cava inferior, se puede utilizar la exclusión vascular total, en la cual además de la Maniobra de Pringle, se realiza un c1ampeo de la vena cava en sus porciones infra y suprahepática.
Otro procedimiento empleado con el fin de controlar el sangrado en la transección del parénquima 17 Man,K et al, Ann Surg 1997; 226 704-713 Patiño J.F., Trauma de Higado, Capitulo 14, 2, PP 878-882 hepático es la aplicación del Cryo sellado (sellante de fibrina):
El sellante de fibrina es similar al último paso fisiológico de la cascada de coagulación para formar un coagulo de fibrina, independiente del proceso de coagulación del paciente. (Tabla 4).
TABLA 4.

Se describe como un gel adhesivo formado por la interacción de fibrinógeno concentrado y trombina en presencia del factor XIII (Hanneman), fibronectina y calcio ionizado. Es un efectivo agente hemostático, sellante y adhesivo al tejido en cirugía. Esta es su principal función. Tiene como virtud que se reabsorbe completamente en semanas, sin ninguna acción nociva para los tejidos, acelerando la cicatrización de ellos, y contribuyendo a la neoformación de vasos sanguíneos y a la proliferación tisular.
Este sistema del Crio sellado (sellante de fibrina),fue utilizado para la hemostasia durante la cirugía hepática en 150 pacientes escogidos al azar para un grupo de estudío en los hospitales Jackson Memorial de la Universidad de Miami, John Hopkins, Sloan Kettering, Universidad de Chicago, Universidad Sur Carolina (USC), Mont Sinai y UCLA.
Como punto final, el aspecto principal en este procedimiento debe considerarse el tiempo de la hemostasis determínado como el tiempo entre la aplicación del producto de estudio, y cuando la hemostasia es obtenida.
Como aspecto secundario, el porcentaje de la tabla de éxito para alcanzar la hemostasis en diez (10) minutos después de la primera aplicación del producto en estudio. Pérdida de sangre intraoperatoria, pérdida total de sangre por drenaje, necesidad de reoperación por sangrado, y utilización de productos sanguíneos.
Queda como objetivo, investigar la eficacia y seguridad del sellante de fíbrína preparado por el sistema FS de Cryosellado para detener el sangrado en el margen de la resección hepática durante la cirugía. Las principales complicaciones en el post-operatorio de la cirugía hepática son:
1. Insuficiencia hepática: 3-8%
2. Fístula biliar: 4%
3. Absceso perihepáticos: 2-10%
4. Hemorragia severa: 1-3%
5. Derrame pleural o lesiones perihepáticas
6. Insuficiencias respiratorias, neumonia y sangrado gastrointestinal.
Para el diagnóstico de la metástasis en carcinoma colo-rectal, en un estudio de 189 pacientes en el Departamento de Cirugia, Escuela de Medicina de la Universidad de Kurume, Fukuoka, Japón; se observó que los resultados en importancia de procedimientos empleados, fueron los siguientes.
En un análisis practicado en el Departamento de Cirugía del Memorial Sloan – Kettering Cancer Center de Nueva York, en los últimos diez años se estudiaron 1803 historias c1inícas; se encontró que los factores asociados con la mortalídad y la morbilidad son14: (Tabla 6).
TABLA 6.

Con todos estos progresos en la técnica y en el cuidado preoperatorio del paciente, ya se han reportado series como la del Hospital John Hopkins de Baltimore (Maryland) con una supervivencia a 5 años del 58%, en 133 pacientes operados entre los años de 1993 a 1999.
Las Terapias Coadyuvantes se utilizan en aquellos pacientes que están fuera del alcance de los procedímientas quirúrgicos y a los cuales se les puede aplicar con fines paliativos, son ellas:
1. La inyección de Etanol.
2. Crio-ablación.
3. Ablación Termal, Radiofrecuencia (RFA)
4. Aplicación de Microondas.
5. Láser.
6.Quimioterapia
Estos procedimientos tienen aplicación en:
1. Tumores múltiples que involucran ambos lóbulos.
2. En lesiones anatómicamente irresecables.
3. En pacientes con una reserva hepática disminuida (alterada) como es el caso de la cirrosis, y
4.Pacientes portadores de enfermedades concomitantes que impidan la resección hepática. También se indica en aquellos pacientes a los cuales se les practicó una resección hepática previa, quedando márgenes tumorales positivos.
Las técnicas coadyuvantes se utilizan de manera empírica, basándose en la preferencia o experiencia del médico tratante y no en los datos publicados. Ninguna de ellas han demostrado ser curativas, y la eficacia a largo plazo para controlar el tumor local, no se conoce aún.
11 JOAN FIGUERAS, MD. 2003.