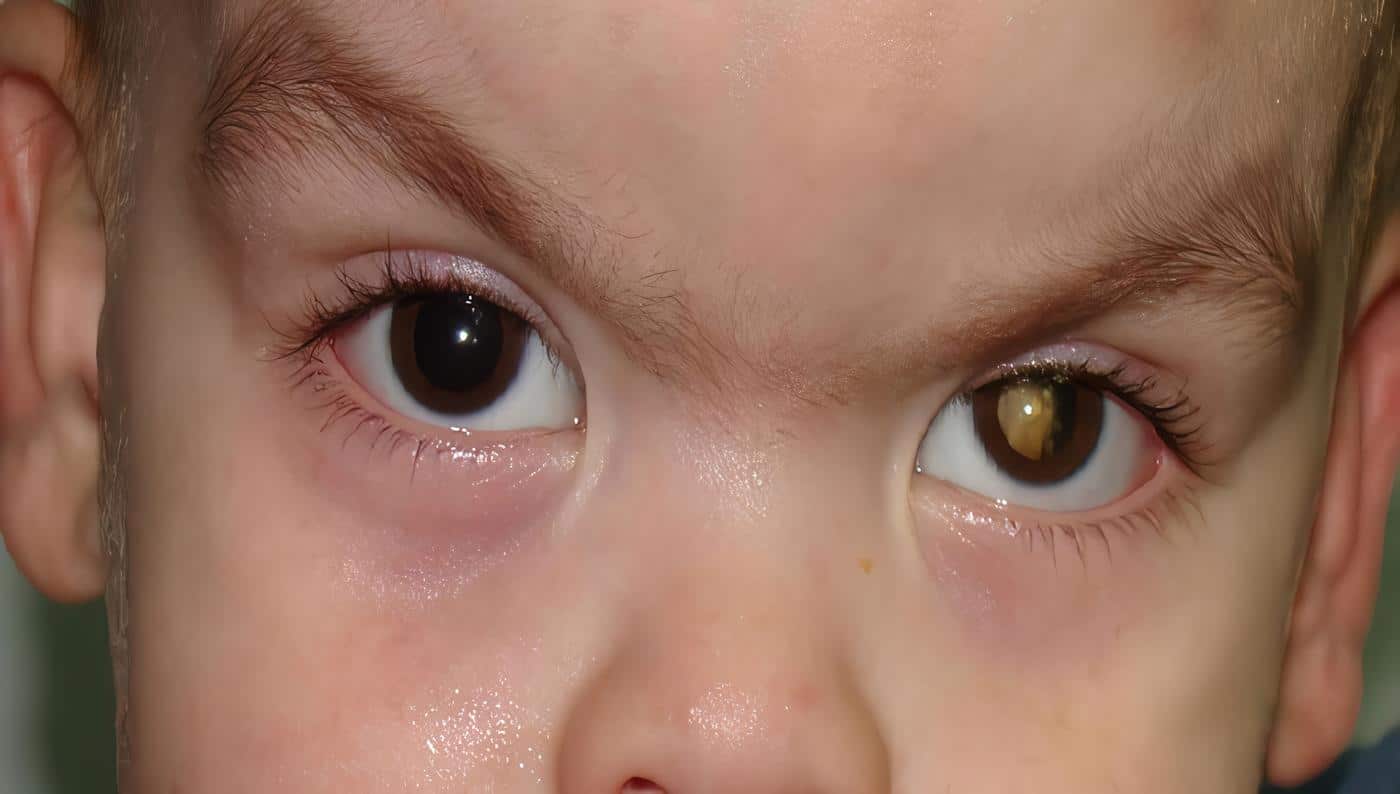
Enrique Constantin Jiménez M.D.
Resumen
El Retinoblastoma, representa un tópico de gran interés dentro de la patología tumoral, por sus características genéticas y por ser dentro de los cánceres un ejemplo de la importancia del diagnóstico precoz; detectado oportunamente, permite con los recursos científicos y técnicos de que disponemos, la sobrevida con conservación de la visión, hasta en un 90% de los casos.
Se enfatiza por lo anterior, en la responsabilidad del médico que atiende inicialmente al paciente; en los exámenes clínicos y para clínicos de importancia, en la necesidad de una clasificación que permita comparar resultados, orientar un tratamiento y establecer un pronóstico. Se propone la adopción del TNM.
Revisan las principales publicaciones sobre el tema y dentro de estas los trabajos elaborados en el Instituto Nacional de Cancerología. Se comentan las indicaciones de los diferentes tratamientos, los resultados y morbilidad de los mismos y los avances logrados con radioterapia externa como alternativa de la cirugía.
Introducción
Se pretende con el presente trabajo, actualizar y homologar los procedimientos diagnósticos, la clasificación y el tratamiento de un tumor, que a pesar de todas las facilidades de que ahora disponemos, continúa presentando en nuestro medio un panorama desolador, muy diferente al que se observa en otros países.
El retinoblastoma es un tumor maligno, poco frecuente, ya que solo representa el 1% de las neoplasias infantiles; es sin embargo el tumor ocular mas frecuente en el niño (l8,19). Se desarrolla en la retina durante los primeros años de la vida. Congénito, se transmite de padres a hijos hasta en un 50% de los casos cuando es bilateral o multicéntrico en aquellos y hasta en un 20% cuando es único y unilateral.
Sus características genéticas son de tipo autosómico dominante, de penetración casi completa. Los casos de retino- Estatuilla Maya. Corto M. Gaitán. blastoma hereditario pueden tener una mutación germinal; generalmente afectación del brazo largo del cromosoma 13 (6, 9 Y 15).
Tiene la afortunada característica de permanecer confinado al globo ocular durante un tiempo mas o menos largo, lo que abre la posibilidad de efectuar un diagnóstico oportuno, que actualmente permite salvar la vida del niño y conservar su visión hasta en el 90% de los casos, aún tratándose de tumores bilaterales. Sin embargo, cuando el tumor se extiende por fuera del globo ocular, sus posibilidades de curación se aproximan a cero, sea cual fuere el tratamiento que se practique ya que las medidas sistémicas de tipo inmunológico y la quimioterapia, hasta la fecha han sido muy poco eficaces. (4′, 8, 19).
Tumores menores de 4 discos
Los tumores menores de 4 discos de diámetro (6.4mms.) se controlan satisfactoriamente con procedimientos conservadores como la fotocoagulación, la diatermia, la crioterapia, la implantación de elementos radioactivos, bien sea en forma de semillas o de cobalto en aplicadores o discos. Es sin embargo la radioterapia externa, el tipo de tratamiento que ha mostrado un mayor desarrollo en los últimos años y se ha constituído en el tratamiento curativo de elección cuando se busca conservar la visión, como lo es en caso contrario la enucleación.
Este tumor, fué descrito por primera vez en 1.809 por James Wardrop.
La cultura Maya, ya lo había esculpido 2.000 años antes de Cristo. (Fig. No.1).

El primer reporte sobre radioterapia, data de 1.903, año en que Hilgartner trató exitosamente con RX un caso de retinoblastoma (19). En 1.929, Foster y Moore describieron su experiencia con implantes de Radón y en 1.948 Stallard desarrolló aplicadores de Radium, que posteriormente fueron reemplazados por discos de Cobalto 60 (19). 3214537170
Los actuales equipos para Teleterapia con radiación y principalmente los aceleradores lineales, se han perfeccionado hasta alcanzar una extraordinaria homogeneidad del haz y una precisión dosimétrica con fotones o electrones, con energía de 4 o mas MV., que permiten dar altas dosis al tumor y un máximo de protección a las estructuras vecinas.
Francois en los Estados Unidos, encontró una incidencia aproximada de un caso por cada 20.000 niños recién nacidos. La incidencia en Colombia en mas de 20.000 neoplasias vistas en el Instituto Nacional de Cancerología (INC), durante los años de 1.963 a 1.974 fué de 0.54%. Para el Registro Nacional de Cáncer, su frecuencia correspondió a 0.11 x 100.000 habitantes y constituyó el segundo tumor en frecuencia, después de los linfomas y leucemias, en niños menores de 3 años.
El INC atiende un promedio de 11 casos nuevos al año.
La mitad del tiempo transcurrido entre el primer síntoma y el diagnóstico, se debió a falla del médico. En la revisión de Castro, se detectó antes de los 3 años en el 85% de los pacientes; de 825 casos revisados por Stafford, el 14.9% demoró el tratamiento por error en el diagnóstico inicial ( 1,4,6), demora que en nuestro medio, desafortunadamente se presenta en la casi totalidad de los casos, con las implicaciones que esto conlleva sobre el tratamiento y el pronóstico.
Material y Métodos
Basándonos en las publicaciones previas sobre el tema, presentadas por Gaitán Yanguas, quien revisó 235 casos y por Castro sobre 110 casos ( 4, 8 ), casuística proveniente del INe., revisamos y analizamos con Pérez (18), para completar este estudio, 79 casos; 74 de ellos con confirmación histológica, atendidos en el INe., desde ello. De Enero de 1.974 hasta el31 de Diciembre de 1.983.
Los datos obtenidos sobre sexo y edad, fueron similares a los de los trabajos precedentes ( 41 niños y 38 niñas ), con ligero predominio por el sexo masculino; que era de 1.3/1 en la serie de Gaitán. La edad promedio fué de 30.83 meses, con una desviación de 14.86. E15% tenía antecedentes de retinoblastoma en la familia (4/79). Desde la presentación del primer síntoma hasta la remisión al INe., hubo una demora de 10 meses en promedio (18)
El síntoma ipicial mas frecuente, fué la leucocoria en 53/79 casos ( 67% ), ” Renejo de ojo de gato”. (Fig. No. 2).
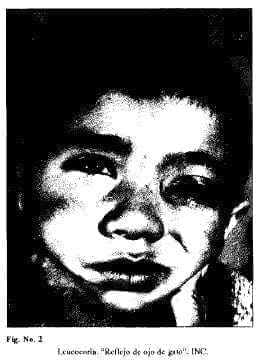
El segundo síntoma en frecuencia, fué el estrabismo en 8/79 casos ( 10.1%); masa intraocular presentaron 5 casos, edema e inflamación 5 casos, dolor y epífora 2 casos, exoftalmos y adenopatías cervicales 1 caso.
Respecto de los signos clínicos, 12 casos (15.18%) presentaban masa intrapalpebral; 10 casos (12.65%), masa reproducida postenucleación; 5 casos presentaban quemosis, buftalmos, destrucción del globo ocular o masa en los tejidos blandos del cuello respectivamente. En 3 casos se presentó exoftalmos, adenopatías cervicales o destrucción de la órbita; en 2 casos proptosis y en 1 caso atrofia del globo ocular.
La bilateralidad encontrada por Gaitán:
Fué del 25% y por Castro del 32.7%. En nuestra serie, encontramos una bilateralidad de 29/79 (24%). Merece destacarse en la casuística revisada, que para Castro, 66/110 casos eran localmente avanzados y 9 presentaban metástasis a distancia; en la de Gaitán, solamente 44/235 casos (18.7%) permanecieron confinados al globo ocular y en nuestra revisión, 31179 casos desarrollaron metástasis a distancia.
Actualmente, un equipo de oftalmólogos debidamente entrenados en este tipo de patología, es capaz de ofrecer una alta certeza diagnóstica, máxime si existen antecedentes familiares de retinoblastoma; por ello, puede en algunos casos prescindirse de la confirmación histológica, para no sacrificar un ojo que tiene posibilidades de conservar la visión (1).
Para efectuar el diagnóstico, es necesario elaborar una historia clínica enfatizando en los antecedentes familiares; practicar examen físico completo, que incluya fundoscopia bilateral bajo anestesia general, y dilatación pupilar máxima; documentación cuidadosa de todas las características oftalmoscópicas, clínicas y paraclínicas y examen oftalmológico a los hermanos del paciente.
El laboratorio, además de los estudios de rutina, debe complementarse con mielograma o biopsia de medula; estudio de cariotipo y citología del líquido cefalorraquídeo; dosificación de ácidos 5 vanilmandélico y homovanílico, que para algunos autores como Brown (1) han demostrado ser de utilidad diagnóstica y pronóstica.
La imagenología es decisiva para la correcta evaluación de la extensión y diseminación tumoral por continuidad y a distancia; por esto, además de los estudios radiológicos convencionales, tienen gran valor la ultrasonografía de órbita, la tomografía axial computarizada, (Fig. No. 3), la resonancia magnética nuclear y los estudios isotópicos con la utilización de gammacámaras.
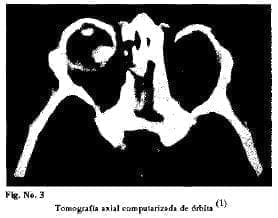
Para el diagnóstico diferencial, debe tenerse en cuenta si el crecimiento tumoral es exofítico o endofítico: en el primer caso, debe hacerse con hamartomas, granulomas o émbolos de endocarditis bacteriana subaguda. En el segundo caso, se hará con fibroplasia retrolental1 enfermedad de Coats e hiperplasia primaria del vítreo (1).
La clasificación de cada caso es fundamental para programar adecuadamente el tratamiento y para fijar su pronóstico.
En el trabajo de Castro(4), se evaluó retrospectivamente el material basándose en la clasificación de Pratt.
La clasificación internacionalmente mas aceptada, ha sido la de Reese Ellsworth, que podemos ver en la tabla No. 1. Gaitán Yanguas adicionó un grupo VI para incluir la propagación extraocular, diferenciando la invasión al nervio óptico, la invasión orbitaria o la presencia de metástasis a distancia. Esta clasificación es la que actualmente utiliza el INC.

La VICe. recomienda clasificar este tumor por el sistema 1NM (24),tanto clínico como patológico (tablas Nos. 2 y 3).


Los tratamientos efectuados en el INe., se limitaron a cirugía: enucleación o exenteración, radioterapia externa: exclusiva o post operatoria; fotocoagulación y quimioterapia.
La enucleación, se efectuó en casos confinados al globo ocular; la exenteración, cuando existía compromiso de tejidos orbitarios extraoculares o en casos de recidiva local ( 18 ). La radioterapia se empIcó con intención curativa o paliativa, dependiendo de la extensión de la enfermedad y de los tratamientos efectuados previamente. La fotocoagulación, se limitó a casos bilaterales previa enucleación del ojo mas afectado, buscando preservar alguna visión. La quimioterapia, se utilizó como tratamiento paliativo o adyuvante, con Trietilenomelamina ( TEM ) Y luego con esquemas de poliquimioterapia ( VAC Y VAC- Adria ); en algunos casos se empleó Methotrexate intratecal si había positividad en el líquido cefalorraquideo.
En la serie que presentamos con Pérez, sobre pacientes clasificables según los grupos de Reese Ellsworth, 11 pacientes se sometieron a enucleación exclusiva y 25 a enucleación y radioterapia con finalidad curativa – 21 de estos correspondían al grupo VIb – 16 casos muy avanzados recibieron radioterapia ¡>aliativa; la enucleación se efectuó en 60 ojos; la exenteración como tratamiento inicial se efectuó en 9 ojos y de rescate en 12.
El total de pacientes que recibieron radioterapia curativa post enucleación fué de 38.
Las técnicas de tratam iento con radiaciones variaron en las diferentes series analizadas: inicialmente se irradiaron con rayos X de ortovoltaje, posteriormente con cobalto y en la actualidad con fotones de 6 MV y electrones o rayos X superficiales.
Las figuras Nos. 4, 5, 6, 7 y 8 nos ilustran sobre las diversas técnicas de radioterapia indicadas, según los diferentes tipos de tratamiento de acuerdo con la situación tumoral.




 Los electrones se emplean cuando se desea limitar la zona irradiada a la órbita y tejidos periorbitarios, dando un máximo de protección a los tejidos subyacentes. (Fig. No. 9).
Los electrones se emplean cuando se desea limitar la zona irradiada a la órbita y tejidos periorbitarios, dando un máximo de protección a los tejidos subyacentes. (Fig. No. 9).

Para una adecuada aplicación de la radiación, los pacientes deben recibir previamente sedación con Hidrato de Cloral, una absoluta inmovilización – preferentemente empleando un colchón de vacío – y de ser necesario, anestesia superficial.
Generalmente empleamos un fraccionario de dosis de 300 cGy., dados 3 veces por semana, hasta una dosis total de 3.600 a 4.500 x cGy., administrados en 4 a 5 semanas. Los casos paliativos, pueden tratarse con dosis aproximadas de 3.000 cGy. No se ha visto en la literatura consultada, las ventajas de dar dosis mas elevadas y sí un aumento en la morbilidad y en la incidencia de segundos tumores (1) Abramson, reportó un aumento en la frecuencia de osteosarcomas del cráneo y el Columbian Presbyterian informó de un 11.6% de tumores secundarios.
Gaitán en su serie, encontró una supervivencia del 31% a 2 años y del 30% a 3 años sobre 235 pacientes.
La curva de supervivencia que él presenta, se hace perfectamente horizontal después de los 2 y hasta los 5 años, siendo durante este lapso excepcionales las recaídas (Fig. No. 10).
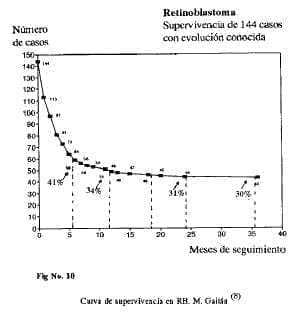
Los anteriores resultados, son muy similares a los que encontramos con Pérez, con una supervivencia absoluta libre de enfermedad, del 27.5% a 2 áños (19/70) y relativa del 36.5% (19/52). La sobrevida absoluta a 5 años en esta serie, fué del 20.5% y la relativa del 28%.
Como complicaciones solo se presentó una muerte, atribuida a intoxicación por Vincristina; dos casos irradiados requirieron reconstrucción de la órbita por falta de desarrollo de esta. En ningún caso se presentaron segundos primarios luego de más de 5 años de seguimiento en 44 pacientes.
Comentarios y Discusión
La incidencia de casos remitidos al INC. se ha mantenido con niveles ligeramente menores ahora, que en la década estudiada por Castro (1.964 a 1.973). Esto podemos explicarlo por la puesta en funcionamiento de doce centros oncológicos del Plan Nacional del Control del Cáncer en las principales ciudades.
En cuanto a la distribución por edad, sexo o bilateralidad, no encontramos diferencia con los estudios previos; sin embargo hay que destacar, que en nuestro medio, la edad de presentación tiene un máximo a los 30 meses; esto es, un año mas tarde que la reportada en países desarrollados.
La demora en consultar a personal especializado, puede en parte deberse a ignorancia o a dificultades socioeconómicas de los padres o familiares; pero sin duda, tienen gran responsabilidad los médicos que atienden inicialmente a estos pacientes, restándole en ocasiones importancia a los síntomas, no efectuando de rutina un examen de fondo de ojo o demorando por otros motivos su remisión.
La radioterapia externa, aplicada con cobalto o con acelerador lineal, permite obtener una distribución de dosis altamente homogénea y si es correctamente aplicada, una protección de la cámara anterior del ojo afectado y preservar el ojo contra lateral (en este caso, debe angulares el haz de 3 a 5 grados en sentido posterior al emplear un campo lateral).
Hay que relievar, que teniendo ahora en Colombia, personal altamente calificado y equipos tan evolucionados para permitir un correcto diagnóstico y tratamiento, estamos obligados a presentar cifras de supervivencia y de conservación de la visión similares a los de cualquier centro de Europa o de Norteamérica. Esto solo lo lograremos a través del diagnóstico temprano.
En el mismo orden de ideas, para poder efectuar el tratamiento mas indicado, es necesario unificar los diagnósticos y la clasificación.
La clasificación TNM, define en forma muy satisfactoria el compromiso de la retina, según el porcentaje de invasión y no medido por número de discos; el compromiso del vítreo, del nervio óptico, de la cámara anterior, la úvea y el compromiso extraocular. Es precisa además en cuanto al compromiso de los ganglios regionales (preauriculares, submandibular y cervicales) y sobre las metástasis a distancia.
La clasificación clínica, se correlaciona además con la patológica en los casos operados.
Por lo anterior, considero que es de todas, la que ofrece un mas objetivo enfoque desde el punto de vista oncológico.
En 1.983, propusimos a la UlCC por conducto de Kasdorf, de su Comité de Clasificación, la adopción de este sistema, que permite comparar resultados, elaborar protocolos de tratamiento y tener una idea más real sobre el pronóstico.
Agosto de 1990
Bibliografía
- 1.- ABRAMSOND., CancerJournalforClinicians; Pub!. Am. Cancer Soco pP. 26 – 34. May – Jun. 1.982.
- 2.- BERNAL Y COL., Retinoblastoma, Acta Médica del Valle, Vol. 2, págs. 148-54,1.972
- 3.- BRADY L. W. ; SIIIELDS J.A; AUSBURGER J.J. ; DA Y J.C, Malignant Intraocular Tumors, Cancer 49: 578-85, 1.982
- 4.- CASTRO J. Y COL., Retinoblastoma, 1.974
- 5.- CASSADY J.R; SAGERMAN R.H.; TlIELTER P. et al, Radiation therapy in Retinoblastoma, Radiology, 93: 405-4091.969
- 6.- CONSTANTlN E., Tratamiento del Retinoblastoma, presentado al XVI Congreso Nacional de Radiología, Madrid, septiembre, 1.982
- 7.-CLEAVER J.E. et al, Repair and Replicacion of DNA in hereditary ( Bilateral) Retinoblastoma cells after X irradiation, Canccr Research 42, 1.434-47, 1.982
- 8.- GAlTAN – YANGUAS M., Retinoblastoma:Analysis of235 cases, Int. J. Radiation Biol. Phys., Vo!. 4, pgs.35- 65, 1.978
- 9.- GALLIE B.L.; ELLSWORTlI R.M.; ABRAMSON D.n.; PHlLLIPS R.D.; Retinoma: spontaneus regression of retinoblastoma or benign manifestations of the mutation? Br. J, Cancer 45:5-13, 1.981
- 10.- ELSWORTll R.M., Tumors of the eye, In Cancer medicine, Holand & Frei (Ed.), pgs. 1,665-68, 1.982
- 11.- llOMA YOON S.; llORNBACK N.B.; IlELVESTON E.M.; GE1TLEN BNGER T.; BIGEAN AW., Treatment results ofretinoblastoma ofIndiana University Hospital, Cancer, 40:2.917-22, 1.977
- 12.- HOWARTlI C; MEYER D.; JlUSTU O,; JOIlNSON W.N.; SIIANKS E., PRA T. C. Stage-Related combined Modality treatment ofRetinoblastoma, Cancer 45:851-58, 1.980
- 13.-JENSEN R.D.; MILLER R W., Retinoblastoma: epidemiologic characteristics, N. Eng., J. Med., 283:307- 311, 1.971
Referencias
- 14.- LENNOX E.L.; DRAPER G.J., SANDERS B.M., Retinoblastoma, A study ofnatural history and prognosis of268 cases, Br. Med. J. Vo!. 3; 731-34,1.975
- 15.- KNUDSON AG. el. aL, Chromosomal deletion and retinoblastoma, N. Engl. J. Med., 295: 1120-23 1.976
- 16.- MERRJAM G., Int. J.R.B. ph., Vol. 4,pp 523 – 524. 1.978
- 17.- MOSS W.T., Retinoblastoma en Radioterapia Clínica, Salvat editores, pgs. 142-49, 1.973
- 18.- PEREZA; CONST ANTlN E.; Retinoblastoma: Diez años de experiencia en el Inst. Nal. de Cancerologín. Biblioteca INC. Bogotá. 1.986.
- 19.- PEREZ CA: BRADY L., PrincipIes and Practice of Radiation Oncology. Edil. Lippincot Phil., Vol. 1, pp. 462- 4631.987
- 20.- SCIOVILLE,S Tumores del ojo, Tribuna Médica Colombiana, No. 227, pgs. 6-9,1.966
- 21.- SIMONE J.; CASSADY R; F1LLER R, Cánceres infantiles en: Cáncer Principios y Práctica de Oncología, De Vita, (ed.) Salvat Editores, pgs, 1.200- 1.204, 1.984
- 22.- TAPLEY N.; DU V.; TRETTER P. Retinoblastoma, In Sutow (ed) Clinical Pediatrics Oncology, SI. Louis, CV, Mosby pgs. 411-430, 1.978
- 23.- TAPLEY N., Eye and Orbit in Text book of Radiotherapy, G. Fletcher (ed), pgs. 504-8, 1.978
- 24.- THOMPSON RW. et al, Treatment of Retinoblastoma, Am. J. Rocntgenol, 114:16-23, 1.972
- 25.- VICC., TNM. Clasificación de los Tumores Malignos. 4a. Edición Edil. P. Hermanek, L.H. Sobin.pp. 162- 165. Ginebra 1.987
- 26.- WEISS D.R; CASSADY J.R; PETERSEN R., Retinoblastoma, A modification in Radiation therapy technique Radiology, 114: 705- 708, 1.975