Objetivo
Objetivo
“Estudio de Biodisponibilidad Relativa entre dos formulaciones de Rosuvastatina Cálcica en comprimidos recubiertos de 20 mg, administrados en ayunas a voluntarios sanos de ambos sexos, con la formulación experimental producida por Sanofi-Aventis de Colombia, S.A.. Para Winthrop Pharmaceuticals de Colombia, S.A., y la formulación de referencia (Crestor®) fabricada por IPR Pharmaceuticals Inc. para AstraZeneca UK Limited”.
Conclusión
Centro Clínico Analítico: UNIFAG
Protocolo: ROSUVASTATINA CÁLCICA en comprimidos recubiertos de 20 mg – JPJ 08/12 Patrocinador: Medley Indústria Farmacêutica Ltda
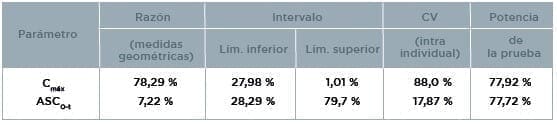
En el análisis estadístico se determinaron los intervalos de confianza. Los CV intraindividuales y la potencia de la prueba para los parámetros Cmáx y ASC0-1, como se aprecia en el resumen a continuación.
 Observando los resultados del estudio, se verifica que las formulaciones experimentales y de referencia son estadísticamente Bioequivalentes, pues satisfacen el Inciso 3.2 f) de la resolución RE n.° 1170, del 19/04/2006, es decir, los valores extremos del intervalo de confianza de 90 % de la razón de las medías geométricas (ASC0-t experimental/ASC0-t de referencia y Cmáx experimental/Cmáx de referencia) son mayores que 80 % y menores que 125 %.
Observando los resultados del estudio, se verifica que las formulaciones experimentales y de referencia son estadísticamente Bioequivalentes, pues satisfacen el Inciso 3.2 f) de la resolución RE n.° 1170, del 19/04/2006, es decir, los valores extremos del intervalo de confianza de 90 % de la razón de las medías geométricas (ASC0-t experimental/ASC0-t de referencia y Cmáx experimental/Cmáx de referencia) son mayores que 80 % y menores que 125 %.
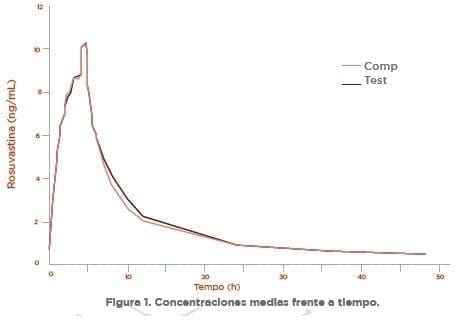
En la Figura 1 se presentan las curvas de las concentraciones plasmáticas medias de la Rosuvastatina Cálcica (medicamentos de referencia y experimental) frente al tiempo. De los 44 voluntarios sometidos al estudio.
 Según los resultados obtenidos, el medicamento experimental Rosuvastatina Cálcica en comprimidos recubiertos de 20 mg producida por Sanofi-Aventis de Colombia, S.A. para Winthrop Pharmaceuticals de Colombia, S.A., es estadísticamente Bioequivalente al medicamento de referencia Crestona® en comprimidos recubiertos de 20 mg fabricado por IPR Pharmaceuticals Inc. para AstraZeneca UK Limited, donde se evaluó en ambos el fármaco Rosuvastatina Cálcica, una vez que los valores extremos del intervalo de confianza de 90 % de la razón de las medias geométricas (ASC0-t experimental/ASC0-t de referencia y Cmáx experimental/Cmáx de referencia) son mayores que 0,8 y menores que 1,25, según se indica en el Inciso 3.2 f) de la resolución RE n.° 1170, del 19/04/2006.
Según los resultados obtenidos, el medicamento experimental Rosuvastatina Cálcica en comprimidos recubiertos de 20 mg producida por Sanofi-Aventis de Colombia, S.A. para Winthrop Pharmaceuticals de Colombia, S.A., es estadísticamente Bioequivalente al medicamento de referencia Crestona® en comprimidos recubiertos de 20 mg fabricado por IPR Pharmaceuticals Inc. para AstraZeneca UK Limited, donde se evaluó en ambos el fármaco Rosuvastatina Cálcica, una vez que los valores extremos del intervalo de confianza de 90 % de la razón de las medias geométricas (ASC0-t experimental/ASC0-t de referencia y Cmáx experimental/Cmáx de referencia) son mayores que 0,8 y menores que 1,25, según se indica en el Inciso 3.2 f) de la resolución RE n.° 1170, del 19/04/2006.
* En estudio por INVIMA


 Objetivo
Objetivo