 Informe Final
Informe Final
Estudio: Clorhidrato de Metformina en comprimidos de 500 mg
Código del estudio: JPJ 06/18 – BEQ15957
Patrocinador: Medley Farmacéutica Ltda.
Fecha: 10/07/2018 I Versión: 1.0
Farmacología I Gastroenterología
Estudio de Bioequivalencia entre dos formulaciones de Clorhidrato de Metformina en comprimidos de 500 mg, administradas de modo posprandial, en voluntarios sanos de ambos sexos, con la formulación experimental producida por Genfar, S.A., y la formulación de referencia (Glucophage® de 500 mg) producida por Merck, S.A.

Unidade do Laboratório de Análises Clínicas
(UNILAC) – UNIFAG Avenida São Francisco de Assis, 218 – Jardim São José, Bragança Paulista – SP C.P.: 12916-900
Objetivo
El objetivo de este estudio fue evaluar si la formulación de Clorhidrato de Metformina en comprimidos de 500 mg (formulación experimental), producida por Genfar, S.A.. Alcanzó niveles plasmáticos equivalentes a los del Clorhidrato de Metformina en comprimidos de 500 mg (Glucophage® formulación de referencia), producida por Merck, S.A., administrados de modo posprandial, en dosis únicas, a voluntarios sanos de ambos sexos.
El estudio se diseñó de tal forma que permitiera obtener los parámetros farmacocinéticos relevantes para la comparación estadística de Bioequivalencia. En su caso, tales parámetros se obtuvieron directamente a partir de la determinación de la concentración plasmática de Metformina, con base en la aplicación de un modelo no compartimental propio para la evaluación de estas concentraciones tras la administración del medicamento por vía oral.
Medicamentos:
 Resultados
Resultados
En el análisis estadístico se determinaron los intervalos de confianza, la potencia de la prueba y el valor P del efecto de secuencia de los parámetros Cmáx, ASC0-t y ASC0-inf, de la Metformina, como se puede apreciar en el resumen a continuación.
 Conclusión
Conclusión
Observando los resultados del estudio, se verifica que las formulaciones experimentales y de referencia son estadísticamente Bioequivalentes, pues satisfacen el Inciso 3.2 f) de la resolución RE n.° 1170, del 19/04/2006, es decir, los valores extremos del intervalo de confianza de 90 % de la razón de las medias geométricas (ASC0-t experimental/ASC0-t de referencia y Cmáx experimental/Cmáx de referencia) son mayores que 80 % y menores que 125 %.
* En estudio por INVIMA


 Informe Final
Informe Final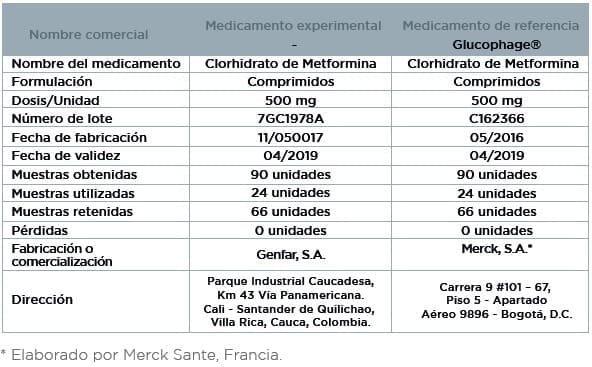 Resultados
Resultados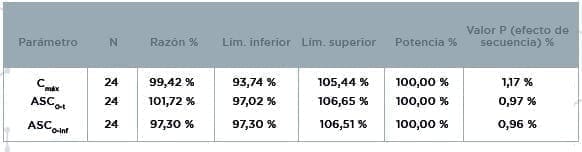 Conclusión
Conclusión

mi mama esta tomando Metformina de laboratorios GENFAR lote 9GC6154A
quiero saber si es ER O IR DEBIDO A ESTE ANUNCIO:
https://www.fda.gov/drugs/drug-safety-and-availability/fda-updates-and-press-announcements-ndma-metformin
Licy buenos días, te invitamos a comunicarte directamente con el laboratorio en su Servilínea 018000 911333 / página web: https://www.genfar.com.co/