El promedio de edades de los sujetos que participaron en el estudio fué en el grupo 1 de 8.5± 0.3 años (rango de 8.1 a 8.9), en el grupo 2 de 8.6± 0.3 (rango de 8.2 a 9.0) y en el grupo 3 de 8.6±0.2 (rango de 8.1 a 8.9). La proporción de varones y mujeres fué en el grupo 1 de 11 y 15, en el grupo 2 de 10 y 11 y en el grupo 3 de 15 y 13. No se encontraron diferencias en la edad, talla, peso e IMC entre los dos sexos de cada uno de los grupos (no se muestran los datos).
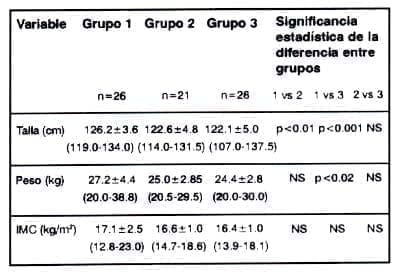
El grupo 1 presentó un promedio de talla significativamente mayor que el grupo 2 (p < 0.01 ) y que el grupo 3 (p < 0.001) mientras que no se observaron diferencias en la talla entre los grupos 2 y 3. El promedio de peso fué significativamente menor en el grupo 3 en relación al 1 (p < 0.02), sin observarse diferencia en el índice de masa corporal (Tabla Nº 1).
Tabla Nº 1. Variables clínicas de los tres grupos. Resultados se expresan como promedio + DS. Rangos entre paréntesis. NS: Diferencia estadísticamente no significativa (p>0.05).
No se encontraron diferencias estadística- mente significativas en los parámetros bioquímicos analizados entre los 2 sexos de cada uno de los 3 grupos (no se muestran datos).
El grupo 1 presentó concentraciones de zinc y de cobre mayores que el grupo 2 ( p < 0.005 y p < 0.0001 respectivamente) y que el grupo 3 ( p < 0.0001, p < 0.005 respectivamente). Los niveles séricos de zinc del grupo 2 fueron mayores a los del grupo 3 (p < 0.05). No se observaron diferencias significativas en los niveles de cobre entre los grupos 2 y 3. El contenido sérico de hierro, si bien tendió a ser mayor en el grupo 1 en relación al grupo 2, no alcanzó a ser significativamente diferente, en cambio si se observó un nivel significativamente menor de hierro en el grupo 3 en comparación al 1 ( p < 0.02). No se observaron diferencias significativas en los niveles de hierro entre los grupos 2 y 3. (Tabla Nº 2).
Tabla Nº 2. Niveles séricos de micronutrientes en los tres grupos. Los resultados se expresan como promedio +DS. Rangos entre paréntesis. NS: Diferencia estadísticamente no significativa (p>0.05).

Al considerar todos los sujetos, se encontró una correlación positiva de la talla con los niveles séricos de zinc (r = 0.29, p < 0.05) y de hierro (r = 0.32, p < 0.05), pero no con los de cobre. Además se observó una correlación positiva entre peso y zinc (r = 0.29, p < 0.05), peso y hierro (r = 0.39, p < 0.05), pero no entre peso y cobre. El índice de masa corporal se correlacionó positivamente con el hierro (r = 0.24, p < 0.05), pero no con el zinc, ni el cobre.
Discusión
El crecimiento y el desarrollo de los individuos dependen de factores genéticos y medioambientales.
Se ha descrito que a mayor pobreza existe mayor prevalencia de talla baja y se considera que la talla del niño es un indicador de calidad de vida19,38. En el presente estudio se encontró que el promedio de la talla de los escolares del colegio privado de la capital era mayor que la de los niños de la escuela pública de Santafé de Bogotá y a la de los del ámbito rural, mientras que no se encontraron diferencias estadísticamente significativas entre estos dos últimos.
El presente trabajo que lógicamente no pretendió abarcar todos los elementos nutricionales y cuyo diseño no incluyó el estudio de la calidad y cantidad de alimentos ingeridos, mostró diferencias en los niveles séricos de los micronutrientes medidos. Los escolares bogotanos del colegio privado presentaron niveles séricos de zinc y de cobre mayores que los niños de las escuelas públicas. Además los sujetos de la institución pública de Santafé de Bogotá presentaron concentraciones menores de zinc en comparación a los de la zona rural y niveles más bajos de hierro que los del colegio privado, sugiriendo que son los que están sometidos a la mayor carencia de estos micronutrientes. El fenómeno de la migración de las zonas rurales a las urbanas que se presenta en Colombia se ha acentuado en los últimos tres años. Se calcula que durante 1996 arribaron a Bogotá aproximadamente 9.700 hogares desplazados por la violencia política que integran un núcleo humano de 50 mil personas. Se estima que el desempleo, en el caso de los desplazados por la violencia en Santafé de Bogotá, alcanza la cifra del 29% y que un 25 % de los jefes de hogares desplazados se dedica a las ventas ambulantes mientras que otros trabajan en oficios varios, labores domésticas y empleos temporales39. La situación anterior determina un deterioro en la calidad de vida que incluye un acceso limitado a cierto tipo de nutrientes40.
En el presente estudio se encontró una correlación positiva de los niveles séricos de zinc con la talla y el peso. Esta relación parece estar mediada por el factor de crecimiento similar a la insulina (IGF-I). Investigaciones en ratas jóvenes han demostrado que la deficiencia de zinc provoca disminución del crecimiento corporal, de los niveles plasmáticos de IGF-I y de la proteína enlazante de la hormona de crecimiento (GH) con una reducción concomitante de las concentraciones hepáticas de los RNA mensajeros del IGF-I y del receptor de la GH (41,42). En un trabajo efectuado con niños japoneses que presentaban baja talla y deficiencia de zinc, la administración de este micronutriente fué seguida por un incremento significativo de IGF-I y un aumento de la velocidad de crecimiento corporal (43). En una investigación en la que se administró zinc a niños vietnamitas con retardo del crecimiento, se observó un mayor incremento de la talla, del peso, una menor frecuencia de los episodios de diarrea e infecciones respiratorias y una elevación significativa de las concentraciones circulantes de IGF-I en relación a niños de la misma edad y región que no recibieron suplementación10.
En este trabajo se encontró una correlación positiva de los niveles séricos de hierro con la talla, el peso y el índice de masa corporal. El déficit de este oligoelemento produce disminución del hierro intracelular y anemia ferropénica11. El hierro de la dieta se divide en dos categorías: el hierro heme, obtenido principalmente de las carnes y el hierro no-heme que se halla en otros alimentos tales como los cereales44. La absorción de hierro-heme es facilitada por proteínas animales, a su vez la de hierro no-heme es reducida por salvado, celulosa, pectina, fitatos y productos polifenólicos45. La deficiencia de hierro se acompaña de retardo del crecimiento corporal46. En los niños con carencia de hierro, la administración de este micronutriente se asocia con un incremento en la talla y en el peso14,47,48. Por otra parte se ha demostrado que la deficiencia de este micronutriente puede provocar alteraciones en los procesos de aprendizaje49, que incluyen dificultad para mantener la atención y resultados relativamente inadecuados en las pruebas de inteligencia50. Al parecer, el hierro es un elemento esencial para la actividad neurológica ya que interviene en la formación de mielina y en la síntesis de neurotransmisores como dopamina, serotonina y catecolaminas51. Estudios sobre suplementación de hierro han sido llevados a cabo en países en vía de desarrollo. Después de la administración de este micronutriente se ha observado un incremento de los niveles de hemoglobina y efectos benéficos -aunque sin significancia estadística- sobre el aprendizaje escolar52. A largo plazo, el rendimiento escolar se constituye en uno de los factores necesarios para lograr romper el ciclo de la pobreza y acceder a mejores condiciones de vida incluyendo una mejor nutrición53.
Si bien los sujetos del colegio privado presentaron niveles séricos de cobre significativamente mayores a los de los otros dos grupos, no se encontró una correlación de los niveles séricos de cobre con los parámetros antropométricos medidos. Se ha descrito la importancia del cobre en el crecimiento corporal, en la maduración de los glóbulos rojos y en el desarrollo del cerebro15,55. Además el cobre desempeña un papel en los mecanismos de defensa a las infecciones55. En un estudio -in vitro- realizado recientemente, con células T humanas, se demostró que la disminución de los niveles de cobre en el medio de cultivo es seguida por una reducción significativa de la producción de interleukina-2 en respuesta a la fitohemaglutinina56. Los hallazgos del presente trabajo no permiten establecer si las diferencias de cobre observadas entre los niños del colegio privado y los de las instituciones públicas tienen algún impacto sobre la susceptibilidad a las infecciones en los sujetos examinados.
En conclusión, en el presente trabajo se describen los niveles séricos de zinc, hierro y cobre en tres grupos de escolares colombianos. Se encuentra una correlación positiva de la talla y el peso con los niveles séricos de zinc y de hierro. Los escolares de la institución pública de la capital y de la zona rural presentan tallas menores a las de los niños del colegio privado de Santafé de Bogotá.
Si bien los sujetos de la zona rural evidencian concentraciones séricas de zinc y cobre menores a los niños de la institución privada de la capital, es el grupo de sujetos de la escuela pública de la capital el que muestra las concentraciones séricas más reducidas de zinc y de hierro, sugiriendo que de los tres grupos estudiados es el que tiene menor acceso a estos micronutrientes. Es necesario mencionar que se estudian niños que habitan una zona rural cercana a la capital y que probablemente los campesinos colombianos que viven en regiones alejadas están sometidos a situaciones económicas más difíciles. Considerando que la deficiencia de estos minerales, podría incidir negativamente sobre el crecimiento, la susceptibilidad a las infecciones y el rendimiento escolar57, la posibilidad de mejorar las condiciones de vida es limitada desde el punto de partida, desde la infancia, a menos de encontrar e implementar mecanismos que garanticen un aporte adecuado de micronutrientes a toda la comunidad.
Agradecimientos
Los autores agradecen a los niños que participaron en el estudio, a las Doctoras Magdalena Morales, Aurora Silva de Jiménez y a los maestros de las Escuelas de Cogua. Además expresan su gratitud al Profesor Fernando Britto (Universidad de la Habana, Cuba) por sus recomendaciones al inicio del presente trabajo, a Juan Carlos Rincón por el manejo estadístico de los datos, al profesor Humberto Trujillo por la revisión del texto y al CINDEC de la Universidad Nacional de Colombia por su apoyo financiero.-
Bibliografía
1. Eisenstein E. Chronic undernutrition during adolescence. Ann N Y Acad Sci 1997; 817: 138-61.
2. Chandra RK. Nutrition and the immune system: an introduction. Am J Clin Nutr 1997; 66: 460S-3S.
3. Rosado JL, Bourges H, Saint-Martin B. Deficiencia de vitaminas y minerales en México. Una revisión crítica del estado de la información: I. Deficiencia de minerales. Salud Pública Mex 1995; 37: 130-9.
4. Milne DB, Johnson PE. Assessment of copper status:effect of age and gender on reference ranges in healthy adults. Clin Chem 1993; 39: 883-7.
5. Gibson R. Content and biovailability of trace elements in vegetarian diets. Am J Clin Nutr 1994; 59: 12235-325.
6. Mill CF. Dietary interactions involving the trace elements. Annual Rev Nutr 1985; 5: 173-93.
7. Gibson RS, Smit Vanderkooy PD, MacDonald AC, Goldman A, Ryan BA, Berry M. A growth-limiting, mild zinc deficiency syndrome in some Southern Ontario boys with low height percentiles. Am J Clin Nutr 1989; 49: 1266-73.
8. Golden B, Golden MHN. Plasma zinc, rate of weight gain and energy cost of tissue deposition in children recovering from severe malnutrition on cow´s milk or soya protein based diet. Am J Clin Nutr 1981; 34: 892- 9.
9. Rivera Juan A, Ruel MT, Santizo MC, Lönnerdal, Brown KH. Zinc supplementation improves the growth of stunted rural guatemalan infants. J Nutr 1998; 128: 556-62.
10. Ninh NX, Thissen JP, Collette L, Gerard G, Khoi HH, Ketelslegers JM. Zinc supplementation increases growth and circulating insulin-like growth factor (IGF-I) in growth-retarded Vietnamese children. Am J Clin Nutr 1996; 63: 514-9.
11. Freire W. Strategies of the Pan American Health Organization/World Health Organization for the control of iron deficiency in Latin America. Nutr Rev 1997; 55: 183-8.
12. Underwood BA. From research to global reality: the micronutrient story. J Nutr 1998; 128: 145-51.
13. Cook JD, Skikne BS. Iron deficiency: definition and diagnosis. J Int Med 1989; 226: 349-55.
14. Lawless JW, Latham MC, Stephenson LS, Kinoti SN, Pertet AM. Iron supplementation improves appetite and growth in anemic Kenyan primary school children. J Nutr 1994; 124: 645-54.
15. Danks DM. Copper deficiency in humans. Annu Rev Nutr 1988; 8: 235-57.
16. Sherman AR. Zinc, copper and iron nutriture and immunity. J Nutr 1992; 122: 604-9.
17. Bradley J, Xu X. Diet, age, and the immune system. Nutr Rev 1996; 54: S43-50.
18. Brand Rosa N. El desplazamiento forzoso en Colombia. Santafé de Bogotá. Canal Ramírez Antares Ltda 1996; 1-108.
19. Tanner JM. Growth as a mirror of the condition of society: secular trends and class distinctions. En Demirjian A, ed. Human growth:a multidisciplinary review. 2a. ed. Cambridge. Taylor and Francis 1986; 3-34.
20. Stolzfus RJ, Albonico M, Tielsh JM, Chwaya HM, Savioli L. Linear growth retardation in Zanzibari school children. J Nutr 1997; 127: 1099-105.
21. Ivanovic D, Castro CG, Ivanovic R. Conocimientos alimentarios y nutricionales de madres de escolares de educación básica y media de diferentes niveles socioeconómicos. Arch Latinoam Nutr 1997; 47: 248-55.
22. Shamah T, Vásquez C, Cervantes L, Chávez A. Guías de alimentación y nutrición. Una propuesta didáctica. Arch Latinoam Nutr 1997; 47: 256-61.
23. Dirección Desarrollo Científico y Tecnológico. De los aspectos éticos de la investigación en seres humanos. En: Ministerio de Salud, ed. Normas científicas, técnicas y administrativas para la investigación en salud. Resolución N° 008430 de 1993 Santafé de Bogotá. D.C. 1993; 12-7.
24. Mockus I. Guía práctica para la valoración del crecimiento corporal y del desarrollo sexual. En: Nestlé, ed. Temas de pediatría 1995; 129: 3-14.
25. Hambidge KM, Goodall MJ, Stall C, Pritts J. Post-prandial and daily changes in plasma zinc. J Trace Elem Electrolytes Health Dis 1989; 3: 55-7.
26. Itriago A, Carrión N, Fernández A, Puig M, Dini E. Contenido de zinc, cobre, hierro, calcio, fósforo y magnesio en leche materna en los primeros días de lactación. Arch Latinoam Nutr 1997; 47: 14-22.
27. Carrión N, Itriago A, Murillo M, Eljuti E, Fernández A. Determination of calcium, phosphorus, magnesium, iron , copper and zinc in maternal milk by inductively coupled plasma atomic emission spectrometry. J Anal At Spectrom 1994; 9: 205-7.
28. Prasad AS. Discovery of human zinc deficiency and studies in an experimental human model. Am J Clin Nutr 1991; 53: 403-12.
29. Tershakovec AM, Weller SC. Iron status of inner-city elementary school children: lack of correlation between anemia and iron deficiency. Am J Clin Nutr 1991; 54: 1071-6.
30. Ferguson BJ, Skikne BS, Simpson KM, Baynes RD, Cook JD. Serum transferrin receptor distinguishes the anemia of chronic disease from iron deficiency anemia. J Lab Clin Med 1992; 19: 385-90.
31. Expert Scientific Working Group. Summary of a report on assessment of the iron nutritional status of the United States population. Am J Clin Nutr 1985; 42: 1318-30.
32. Turnlund JR, Keyes WR, Hudson CA, Betschart AA, Kretsch MJ, Sauberlich HE. A stable-isotope study of zinc, copper, and iron absorption and retention by young women fed vitamin B-6- deficient diets. Am J Clin Nutr 1991; 54: 1059-64.
33. Alarcón OM, Reinosa Fuller J, Silva TM, Angarita C, Terán E, Navas M, Solano P. Agostinelli M. Serum level of Zn, Cu and Fe in healthy schoolchildren residing in Mérida, Venezuela. Arch Latinoam Nutr 1997; 47: 118-22.
34. Amaya DC, Urrieta R, Gil NM, Molano NC, Medrano I, Castejón HV. Valores de zinc plasmático en una población infantil marginal de Maracaibo, Venezuela. Arch Latinoam Nutr 1997; 47: 23-8.
35. Meertens L, Solano L, Peña E. Evaluación del estado de zinc en adultos mayores institucionalizados. Arch Latinoam Nutr 1997; 47:311-4.
36. Gaetke LM, McLain CJ, Talwalkar RT, Shedlofssky SI. Effects of endotoxin on zinc metabolism in human volunteers. Am J Physiol 1997; 272: E952-6.
37. Bhattacharyya GK, Johnson RA. Nonparametric inference. En: Bhattacharyya GK, Johnson RA eds. Statistical Concepts and Methods. New York. John Wiley and Sons 1977; 505-49.
38. Kain J, Pizarro F. Efecto de un programa de refuerzo alimentario sobre el crecimiento en talla de una población infantil. Arch Latinoam Nutr 1997; 47: 101-4.
39. Grupo de Investigación Arquidiócesis de Bogotá. Desplazados por violencia y conflicto social en Bogotá. Santafé de Bogotá. Kimpress Ltda 1997; 1-93.
40. Martorell R. The role of nutrition in economic development. Nutr Rev 1996; 54: S66-71.
41. Roth HP, Kirchge(ner. Influence of alimentary zinc deficiency on the concentration of growth hormone (GH), insulin-like growth factor I (IGF-I) and insulin in the serum of force-fed rats. Horm Metab Res 1994; 26: 404-8.
42. Ketelslegers JM, Beauloye V, Defalque D, Brandt N, Maiter D, Maes M, Thissen JP. Starvation or sepsis as causes of growth hormone insensitivity. Endocrinol Metab 1997; 4: 71-80.
43. Nakamura T, Nishiyama S, Futagoishi-Suginohara Y, Matsuda Y, Higashi A. Mild to moderate zinc deficiency in short children:effect of zinc supplementation on linear growth velocity. J Pediatr 1993; 123: 65-9.
44. Cook JD, Dassenko SA, Lynch SR. Assessment of the role of non-heme-iron availability in iron balance. Am J Clin Nutr 1991; 54: 717-22.
45. Hurrell RF. Preventing iron deficiency through food fortification. Nutr Rev 1997; 55: 210-39.
46. Beard JL, Dawson H, Piñero DJ. Iron metabolism: a comprehensive review. Nutr Rev 1996; 54: 295-317.
47. Chwang L-C, Soemantri AG, Pollitt E. 1988 . Iron supplementation and physical growth of rural Indonesian children. Am J Clin Nutr 1988; 47: 496-501.
48. Tulchinsky TH, El Ebweini S, Ginsberg GM, Abed Y, Montano-Cuellar D, Schoenbaum M, Zansky SM, Jacob S, El Tibbi AJ, Abu Sha´aban D, Koch J, Melnick Y. Growth and nutrition patterns of infants associated with a nutrition education and supplementation programme in Gaza, 1987-1992. WHO Bulletin OMS 1994; 72: 869-75.
49. Pollitt E. Iron deficiency and educational deficiency. Nutr Rev 1997; 55: 133-41.
50. Sheard NF. Iron deficiency and infant development. Nutr Rev 1994; 52: 137-40.
51. Kretchmer N, Beard JL, Carlson S. The role of nutrition in the development of normal cognition. Am J Clin Nutr 1996; 63: S997-1001.
52. Pollitt E, Hathirat P, Kotchabhakdi NJ, Missell L, Valyasevi A. Iron deficiency and educational achievement in Thailand. Am J Clin Nutr 1989; 50: 687-97.
53. Brown JK, Pollit E. Malnutrition, poverty and intellectual development. Scientific American. 1996; 274: 38-43.
54. Linder MC, Hazegh-Hazam M. Copper biochemistry and molecular biology. Am J Clin Nutr 1996; 63: S797-811.
55. Lönnerdal B. Bioavailability of copper. Am J Clin Nutr 1996; 63: S821-9.
56. Hopkins RG, Failla ML. Copper deficiency reduces interleukin-2 (IL-2) production and IL-2 mRNA in human T-lymphocytes. J Nutr 1997; 127: 257-62.
57. Black MM. Zinc deficiency and child development. Am J Clin Nutr 1998; 68: S464-96.
