Dra. Susana Murcia de Onatra
Docente Unidad de Patología Pediátrica
Departamento de Patología, Facultad de Medicina
Universidad Nacional
Dra. Norma Villarraga
Residente III Departamento de Pediatría
Facultad de Medicina, Universidad Nacional
Hospital de la Misericordia
Motivo de Consulta
Niña de 18 meses de edad procedente de Bogotá, con cuadro de palidez progresiva, adinamia, petequias y equímosis de un mes de evolución. Tres días antes presentó vómito, fiebre de 38oC y epistaxis en varias ocasiones.
Antecedentes: producto de segundo embarazo normal, desarrollo sicomotor normal, desde los 13 meses camina sin apoyo, vacunas completas incluyendo primera dosis de hepatitis B y de hemófilus. Familiares: tía paterna murió de leucemia en edad adulta y prima del padre con historia de aplasia medular. Patológicos: bronconeumonía a los tres meses.
Examen Físico
Peso: 9500Gr; talla: 63cm; FC: 140xmin; FR: 40xmin; TA: 107/43; T: 38oC; hidratada, decaída, palidez generalizada, adenopatías móviles cervicales e inguinales menores de 1 cm, ruidos cardíacos rítmicos taqui-cárdicos, soplo sistólico II/VI, buena ventilación, no megalias, equímosis y petequias generalizadas, neurológico normal.
Evolución
EL CH inicial mostró Hto: 10.3%, Hb: 3.8Gr/l; blancos 6.2000, Seg: 6, linfos: 93; Monos: 1%, plaquetas de 30.000. Se trasfundieron GR empaquetados y plaquetas, y se inició cefalotina, amikacina, y trimetoprinsulfa.
El mielograma mostró celularidad muy escasa con predominio de linfocitos y plasmocitos, no se encontraron blastos.
Al cuarto día presentó rash cutáneo con eritema y descamación en palmas y plantas, que se interpretó como un reacción de hipersensibilidad; el hemocultivo inicial fue positivo para pseudomona pausimobilis, se cambió la cefalotina por ceftazidima y se suspendió la sulfa. Otros exámenes mostraron: biopsia ósea: celularidad de 15%, reemplazo graso sin fibrosis, relación mieloide eritroide 3/1 negativa para tumor, BUN 17, creatinina: 0.3, K: 3.7, Na: 133 meq/l, Rx de tórax y Eco abdominal normales. Urocultivos negativos, % de linfocitos T y B y relación CD4/CD8 normales. Cariotipo 46xx con fragilidad cromosómica. Hemoglobina fetal de 5.2, reticulocitos: 2.5%. Inmunoglobulina E elevada y PCR positiva.
El ecocardiograma descartó endocarditis. Persistieron picos febriles, cuadro hemorragíparo y severa anemia que obligó a nuevas transfusiones. Se inició metilprednisolona en bolos y ante la persistencia de picos febriles y la no respuesta a antibióticos, se agregaron netilmicina y fluconazol y factor estimulante de colonias. Hizo conjuntivitis, edema y eritema periorbitario; los Rx de Senos paranasales mostraron pansinusitis bilateral y el TAC de órbitas, celulitis periorbitaria derecha. Continuó con sangrado activo, consolidación basal de pulmón derecho, derrame pleural. Se inició anfotericina B, pero la paciente continúo con progresiva insuficiencia respiratoria y falleció.
Diagnósticos Clínicos Finales
Anemia aplástica tipo fanconi sepsis. Celulitis periorbitaria. Pansinusitis. Micosis sistémica?
Resultado de Autopsia
Se encontró cadáver de una niña lactante mayor, ictérica con marcada palidez de mucosas, petequias y equimosis, severa celulitis orbitaria derecha, con necrosis de la piel en el puente nasal. En el tórax: derrame pleural bilateral de líquido turbio, pleura opaca y lesiones múltiples amarillentas friables de bordes mal definidos, algunas confluentes en pulmón derecho y zonas periféricas de infartos recientes bilaterales (Figura No 1).
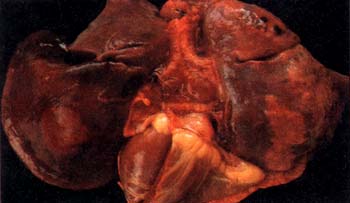
Figura No.1 Aspecto posterior del pulmón derecho con lesiones necróticas múltiples.
Iguales lesiones se vieron en hígado, bazo, riñón y en el ciego una amplia zona ulcerada. Los ganglios mediastinales grandes hemorrágicos y el timo pequeño fibroso. No se vieron lesiones cerebrales.
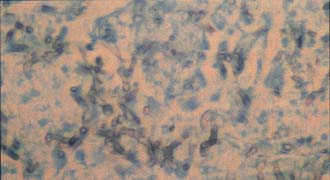
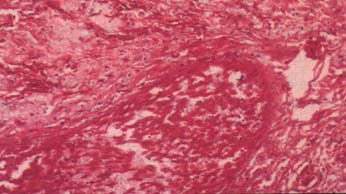
El estudio histiológico mostró en los órganos comprometidos y en la piel de la órbita, extensas zonas de necrosis de licuefacción con incontables hifas, esporas y conidias de Aspergillus (Figura No 2), que invadían además la pared y la luz de arterias (Figura No 3).
 |
 |
| Figura No. 2 Fotomicrografía del Aspergillus en las lesiones pulmonares Coloración de Grocott 40x. |
Figura No. 3 Fotomicrografía de Vasos Pulmonares con trombos micóticos Coloración de PAS 40x. |
La medula ósea presentaba un cuadro similar al encontrado en la biopsia.
Diagnóstico Definitivo
1 Anemia aplástica tipo fanconi (Fragilidad cromosómica, presencia de hemoglobina fetal y Reticulocitos elevados).
2 Aspergillosis diseminada con pnasinusitis, celulitis orbitaria y lesiones viscerales múltiples.
3 Infartos pulmonares múltiples por trombos micóticos.
4 Sindrome hemorragíparo con petequias, equí-mosis y hemorragias viscerarales múltiples.
Comentario
La Anemia aplástica es un síndrome de falla medular caracterizado por pancitopenia, por falla de la hemopoyesis a nivel de la medula ósea; puede ser adquirida o hereditaria y según su severidad se clasifica en Intensa, cuando el paciente presenta menos de 500 neutrófilos es sangre periférica, menos del 1% de reticulocitos y menos del 30% de células residuales en médula ósea y moderada, cuando presenta más del 2% de reticulocitos y más de 500 neutrófilos en sangre periférica con más de 10% de neutrófilos maduros en médula ósea. Su incidencia anual es de 5 a 6 por millón de habitantes1,2,3.
El 75 % de las anemias aplásticas son adquiridas principalmente por la exposición a radiación, agentes mielotóxicos, como el benzol y sus derivados, drogas como cloranfenicol, AINES, anti-neoplásicos, infecciones por Microbacterias, virus de ebstein bar, HIV, parvovirus y hepatitis3.
Entre el 20 y 25% de los casos es hereditaria y se ve en la disqueratosis congénita, en el Síndrome de Shwachman Diamond y en la Anemia de Fanconi. Esta última, presenta fragilidad cromosómica en lin-focitos periféricos, aumento de reticulocitos y presencia de hemoglobina fetal; un 30 % de los pacientes es fenotípicamente normal y el 70% restante, tiene otros defectos como hiperpigmentación cutánea, hipogenitalismo, baja talla, microcefalia, malformaciones de vías urinarias, paladar ojival, estrabismo, defectos de los dedos pulgares, del radio y de los arcos costales.
El tratamiento se realiza con medidas de sostén: transfusiones de glóbulos rojos y plaquetas, antibióticos profilácticos en casos de proceso febril y corticoterapia en megadosis, transplante de médula ósea, inmunoterapia con Globulinas antilinfocíticas y antimonocíticas, factores de crecimiento hematopoyético, como son el factor estimulante de colonias de granulocitos y macrófagos. La mortalidad es alta calculándose en un 50% 6 meses después de haberse hecho el diagnóstico; si solo se ha administrado tratamiento de sostén, la sobrevida a 5 años es del 25% pero esta cifra mejora a un 65% cuando se le realiza transplante de médula ósea o inmunoterapia.
El diagnóstico diferencial se hace con otras causas de Pancitopenia como los problemas carenciales, procesos infecciosos e inmunitarios, síndromes infiltrativos neoplásicos por leucemias, linfomas e Histiocitosis malignas y síndromes infiltrativos no neoplásicos por osteopetrosis maligna, proliferaciones histiocíticas y enfermedades de depósito de lípidos1,2,3.
La hemorragia intracraneana y las infecciones bacterianas diseminadas, constituyen las principales causas de muerte. La colonización y subsecuente superinfección con bacterias y hongos resistentes es un riesgo del uso prolongado de antibióticos; los cuadros de micosis profundas pueden ser producidos por cándida, Ficomicosis y Aspergilus3,4,5.
La ASPERGILLOSIS es producida por un moho cuyas especies Flavus y Fumigatus son patógenas para el individuo que padece una deficiencia inmunológica; pueden ocurrir brotes nosocomiales o adquirirse en áreas con defectos de ductos de ventilación o con remoción de escombros; la puerta de entrada suele ser el tracto respiratorio donde por inhalación da una infección localizada en aparato respiratorio, produciendo asma, expectoración mucosa parda, infiltrados pulmonares transitorios, eosinofilia y febrícula o diseminándose por vía hematógena afectando tejido subcutáneo (Aspergilomas) y múltiples órganos, Endocarditis, Osteomelitis, Meningitis, siendo fatal en la mayoría de los casos.
El hongo presenta gran afinidad por senos paranasales, conducto auditivo externo y región ocular cursando también con procesos de Pansinusitis y celulitis.
El diagnóstico se realiza por cultivo en agar-dextrosa de Sabouraud y examen directo por aislamiento en tejidos; solo se ha observado respuesta al tratamiento con Anfotericina B.
Bibliografía
1 Martinez A. Hematología y Oncología Infantil. Ed. Celsus 1992; 83-90.
2 Kupfer M, Naf D, Andrea AD. Molécular Biology of Fanconi Anemia. Hematol Oncol Clin N Am 1997; 6:1045-52.
3 Guinan EC. Clinical Aspects of Aplastic Anemia Hematol Oncol Clin N Am 1997; 6:1025-38.
4 Nash G, Irvine R, Kerschmann RL, et al. Pulmonary Aspergillosis in acquired Immune Deficiency Syndrome. Autopsy study of an emerging pulmonary co of human immunodeficiency virus infectionmplication Hum Pathol 28: 1268-75.
5 Rippon J. Aspergillosis in Rippon J: Medical Mycology N York W.B. Saunders Co 3th Ed 1988; 618-50.
