Agradecemos a los laboratorios Wyeth su colaboración al autorizar la publicación de esta información científica de importancia para la educación médica continuada.
Preguntas
Lea las siguientes preguntas e indique la respuesta o respuestas que seleccione para cada una. La clave para la respuesta y los comentarios comienzan luego de las preguntas.
Pregunta 1
Una mujer de 53 años, con historia de histerectomía por miomas uterinos, pide reemplazo de estrógenos. La dosis cardioprotectora diaria mínima de estrógenos necesaria en su caso es:
- 0,625 mg de estrógenos equinos conjugados (EEC)
- 0,2 mg de 17 B- estradiol
- 0,035 mg de etinilestradiol
- 0,05 mg de mestranol
Pregunta 2
Una mujer de 54 años, con una historia familiar de coronariopatía prematura, pide reemplazo hormonal. ¿Cuál de los siguientes regímenes logra el máximo de efectos positivos sobre los lípidos y lipoproteínas más eficazmente?
- Estrógenos equinos conjugados (EEC) y acetato de medroxiprogesterona (AMP) continuo por vía oral
- EEC y progesterona micronizada cíclica por vía oral
- EEC y AMP cíclico por vía oral
- Parche transdérmico de estrógenos y AMP cíclioco por vía oral.
Pregunta 3
Una mujer de 50 años, cuyo último periodo menstrual ocurrió hace 2 meses, le consulta sobre la terapia de reemplazo hormonal.
Algunas de sus amigas toman reemplazo de hormonas y ella tiene varias preguntas. En particular, está buscando información para comparar la terapia cíclica con estrógeno y progestina con la terapia continúa con estrógeno y progestina combinados. Cada una de las declaraciones siguientes es correcta, excepto:
- El riesgo de hiperplasia endometrial es similar con ambos regímenes.
- La terapia continua combinada probablemente cause amenorrea durante los primeros 3 meses de tratamiento.
- La terapia continua continua combinada con una dosis de progestina no ha demostrado efectos adversos sobre los lípidos.
- Tanto la terapia combinada continua como la cíclica con estrógeno y progesterona son eficaces en la prevención de la osteoporosis.
Pregunta 4
Una mujer de 50 años planifica comenzar la terapia de reemplazo hormonal. La paciente conserva su útero. Usted le recomienda la terapia con progestina cíclica. ¿Qué duración es óptima para evitar la hiperplasia endometrial?
- 5 días
- 7 días
- 10 días
- 14 días
Pregunta 5
Una mujer posmenopáusica de 40 años ha estado tomando 0,9 mg de estrógenos equinos conjugados por 3 meses. Sus bochornos y otros síntomas de deficiencia aguda de estrógenos se han resuelto completamente. El nivel de hormona foliculoestimulante (FSH), tomado antes del tratamiento como parte de la evaluación de amenorrea secundaria, fue de 95 UL/ ml. ¿Cuál sería la interpretación más probable de un valor de seguimiento de 45 UL/ ml para la FSH?
- La dosis es inadecuada
- La paciente tiene un problema de absorción
- El valor se encuentra entre los límites esperados
- Un error de laboratorio
Pregunta 6
Una mujer de 53 años está por iniciar la terapia combinada con estrógeno y progestina. Se preocupa acerca de la cardiopatía debido a que una amiga murió recientemente de un ataque cardíaco. ¿Cuál de las siguientes progestinas más probablemente ejerza efectos adversos sobre el perfil de los lípidos?
- Acetato de megestrol
- Desogestrel
- Progesterona micronizada oral
- Acetato de medroxiprogesterona
- Noretindrona (también llamada noristerona)
Pregunta 7
Una mujer de 62 años se queja de sequedad vaginal y de coito doloroso, que han empeorado durante los 5 años transcurridos desde su último período. El examen muestra una mucosa vaginal fina, roja y frágil. ¿Cuál es el tratamiento inicial más eficaz para esta paciente?.
- Estrógeno oral
- Parche transdérmico de estrógeno
- Crema vaginal de estrógeno
- Estrógeno intramuscular
- Gel transdérmico de estrógeno
Pregunta 8
Una mujer de 35 años fue sometida a histerectomía abdominal total con salpingo ooferectomía bilateral hace 6 meses para el tratamiento de endrometrosis. Desde entonces, se ha mantenido con 2 mg de estradiol por vía oral diariamente, pero se queja de varios síntomas persistentes. ¿Para cuales de los siguientes síntomas es probable que la metiltestosterona sea de mayor beneficio?
- Bochornos
- Insomnio
- Libido baja
- Depresión
- Distensión absominal
Respuestas
Pregunta 1 (Dosis cardioprotectora mínima)
Una mujer de 53 años, con historia de histerectomía por miomas uterinos, pide terapia de remplazo de estrógeno. La dosis cardioprotectora diaria mínima de estrógeno necesaria en su caso es:
- 0,625 mg de estrógenos equinos conjugados (EEC) *
- 0,02 mg de 17 B- estradiol
- 0,035 mg de etinilestradiol
- 0,05mg de mestranol
Comentarios
La mayoría de las investigaciones sobre los efectos cardioprotectores del estrógeno se basan en 0,625 mg de estrógenos equinos conjugados (EEC) por vía oral tomados diariamente, que es el régimen empleado más ampliamente en los Estados Unidos. Esta posología reduce el riesgo relativo de coronariopatía a 0,50. La gran mayoría de los estudios, sin embargo, no han comparado a preparaciones científicas. Los pocos estudios que compararon posologías hallaron una tendencia no significativa hacia una mayor protección a partir de la dosis diarias de 0,625 mg de EEC frente a dosis de 1,25 mg o más, lo que sugiere que las posologías mayores pueden presentar un efecto decereciente sobre la cardioprotección.
La hipótesis central que explica el efecto cardioprotector del estrógeno declara que a absorción oral y el metabolismo hepático aumentan con las concentraciones de lipoproteínas de alta densidad (HDL). La adición de una progestina no debe reducir ese grado de protección, pero no conferiríoa beneficios adicionales en una paciente que no conserve su útero. El mismo mecanismo hepático de “primer pasaje” que parece conferir la mayoría de la cardioprotección también es responsable de los riesgos potenciales, incluso la síntesis hepática de los subtratos de renina, que pueden asociarse con aumentos de la presión sanguínea, así como los factores de coagulación de la sangre circulatoria que aumentan el riesgo relativo de trombosis coronaria y cerebrovasculares. Los estrógenos naturales parecen reducir el mínimo estos últimos efectos.
Cuando se compara de acuerdo con el peso molecular:
El etinilestradiol oral tiene una potencia relativa de 232,0 y el sulfato de estrona piperacínica oral tiene una potencia relativa de 1’0 para elevar los substratos de renina sérica. Los EEC, que se derivan de la orina de yeguas preñadas, típicamente contiene estrona, quilina y una mezcla de otros metabolitos del estrógeno. Su potencia relativa para la producción de substratos de renina, 3,5 es baja y, como se absorben y se almacenan bien en el tejido adiposo, los EEC son más potentes y de acción más prolongada que los estrógenos naturalmente conjugados. Estos factores los han convertido en el agente de primera elección.
Por consiguiente, cuando se decide entre los tipos de estrógeno y las estrategias posológicas para esta paciente (Cuadro 6.1), el etinilestradiol y el mestranol pueden descartarse debido a que son compuestos sintéticos. Aunque tienen mayor potencia, también representan riesgos mayores incluso de tipo cardiovascular. Cuando el etinilestradiol se usa para el reemplazo hormonal posmenopáusico, una posología de 0,02 a 0,05 mg es normal. La posología de 0,035 mg para el etinilestradiol, reflejada en la opción c, típicamente se usa para la anticoncepción oral sistémica.
Cuadro 6.1. Dosis equivalentes aproximadas de estrógenos de uso común.
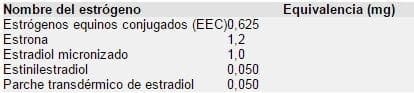
El mestranol también se usa como anticonceptivo en combinación con el noretinodrel o la noretindrona . LA posología estándar de mestranol para tal propósito es de 0,1 mg. Un estudio sobre el uso de mestranol para el reemplazo hormonal posmenopáusico mostró que la posología de 0,025 mg eliminó eficazmente la pérdida de hueso. Por consiguiente, la posología de 0,05mg de mestranol declarada en la opción d es la mitad de la usada para la anticoncepción oral, pero el doble de la que ha demostrado beneficios preventivos en el reemplazo hormonal. El efecto del mestranol sobre el riesgo cardiovascular no ha sido evaluado en ningún estudio importante.
Algunos autores han sugerido que es prematuro llegar a la conclusión de que un perfil favorable de lípidos es principalmente responsable del efecto cardioprotector del estrógeno, lo que también podría ser mediado por factores tales como la vasodilatación, las prostaglandinas y el metabolismo de la glucosa sanguínea.
El estradiol sintético, un 17 B- estrógeno, esta disponible tanto en aplicaciones orales como transdérmicas. La posología transdérmica típica es de 0,05 mg dos veces por semana, que es 2,5 veces la posología declarada en la opción b. A tal posología, un régimen con parche de estradiol mostró un efecto sobre los val
ores de lípiudos y lipoproteínas similar al régimen oral diario de 0,625 mg de EEC, pero presento la ventaja de reducir los trigklicéridos plasmáticos, que se sospechan como factores independientes de riesgo cardiovascular. Puede haber un papel mayor para las rutas de administración no orales (parches transdérmicos, granulaciones subcutáneas y cremas vaginales) que soslayen los efectos cardiovasculares de tales métodos todavía no han sido establecidos firmemente.
Bibliografía
- 1. Crook, D., Cust, MP., Gangar, KF y colab., Compariso of transdermal and oral estrogen/progestogen replacement therapy: Effects on serum lipids and lipoproteins. Am J Obstet Gynecol 1992; 166: 950-955.
- 2. Ellerington, MC., Whitecroft, SIJ., Whitehead, MI. Therapeutic and preventive aspects of estrogen and progesterone therapy, en Lorrain J y colab. (ed), Comprehensive Management of Menopause. Nueva York: Springer-Verlang 1994; págs. 269-285.
- 3. Leach, RE., Hendrix, SL. Hormone replacement therapy, en Hajj SN, Evans WJ (ed), Clinical Postreproductive Gynecology. Norwalk, Connecticut: Appleton & Lange 1993; págs. 59-73.
- 4. Lindsay R., Aitken, JM., Anderson, JB y colab. Long-term prevention of postmenopausal osteoporosis by oestrogen. Lancet 1: 1976; 1038-1041.
- 5. Mashchak, CA.,m Lobo, RA. Estrogen replacement therapy and hyperten. J Repro Med 1985; 30 (10 Supl): 805-810.
- 6. Ross, RK., Paganini_Hill, A., Mack, TM., Henderson, AM. Menopausal oestrogen therapy and protection from death from ischaemic heart disease. Lancet 1981; 1: 858-860.
- 7. Stampfer, MJ., Colditz, GA. Estrogen replacement therapy and coronary heart diseacse: A quantitative assessment of the epidemiologic evidence. Prev Med 1991; 20: 47-63.
- 8. El grupo de escritores para la prueba REPI, Effects of estrogen or estrogen/progestin regimens on heart disease risk factors in postmenopaujsal women: The Postmenopausal Estrogen/Progestin Interventions (PEPI) Trial. JAMA 273: 199-208.
Pregunta 2 (Obtención del efecto positivo máximo sobre los lípidos séricos)
Una mujer de 54 años, con una historia familiar de coronariopatía prematura, pide reemplazo hormonal.
¿Cuál de los siguientes regímenes logra el máximo de efectos positivos sobre los lípidos y lipoproteínas más eficazmente?
- Estrígenos equinos conjugados (EEC) y acetato de medroxiprogesterona(AMP) continuo por vía oral.
- EEC y progesterona micronizada cíclica por vía oral *
- EEC y AMP cíclico por vía oral
- Parche transdérmico de estrógeno y AMP cíclico por vía oral
Comentarios
La administración oral de la terapia de reemplazo hormonal es más eficaz que la administración transdérmica o subdérmica para elevar las concentraciones sanguíneas de lipoproteínas de alta densidad (HDL) y reducir las de lipoproteínas de baja densidad (LDL). La síntesis de HDL ocurre en el hígado.
El denominado efectro heático de “primer pasaje” con el estrógeno oral da lugar a la entrega de estrógeno a concentraciones mayores que las que estarían disponibles después de su metabolismo parcial en la corriente sanguínea a través de la administración transdérmica o subdérmica.
Después de la ingestión oral, las concentraciones de estrógeno en la circulación portal son cuatro a cinco veces más elevadas que las de la sangre periférica.
El efecto de primer pasaje se considera como el mecanismo primario detrás del efecto favorable del estrógeno sobre el metabolismo de los lípidos y liproteínas.
Sin embargo se cuentan con datos que indican que el metabolismo de lípidos también podría ser afectado favorablemente por las rutas de administración no orales, como las aplicaciones percutáneas y subcutáneas.
También es importante observar que se ha atribuido a las concentraciones de HDL, sólo la mitad de la cardioprotección proporcionada por el reemplazo de estrógeno, y que otros mecanismos, tales como la vasodilatación, el metabolismo de los carbohidratos y factores de coagulación, también podrían contribuir.
Los estrógenos naturales:
Han surgido como los agentes preferidos para la terapia de reemplazo hormonal posmenopáusica.
Los estrógenos sintéticos se absorben con mayor facilidad y son más potentes, pero se han asociado con un aumento en la producción hepática de substratos de renina, que pueden elevar la presión arterial, y con procoagulantes que pueden aumentar el riesgo de una apoplejía.
En un importante estudio reciente, el uso de estrógenos equinos conjugados (EEC) tuvo un efecto neutro sobre tales riesgos.
Como otra alternativa, la administración transdérmica de estrógeno sintético se está explorando como un medio de evitar estos productos secundarios hepáticos que constituyen los aspectos negativos del efecto del primer pasaje.
Los estudios han demostrado que la progestina se opone a los efectos favorables del estrógeno sobre el metabolismo de los lípidos. Este efecto parece relacionarse con el potencial androgénico de la progestina.
El acetato de medroxiprogesterona (AMP) y otras progestinas C-21 han demostrado u efecto menor que los derivados de la 19-nortestosterona y, por consiguiente, han sido empleados ampliamente en los Estados Unidos.
En un ensayo extenso reciente, hubo diferencias despreciables conectadas con la administración cíclica en comparación con la continuada de AMP. Sin embargo, el mismo ensayo demostró conclusivcamente que la progesterona micronizada conserva más de los efectos favorables del estrógeno oral sobre las concentraciones de HDL que el AMP.
Bibliografía
- 1. Jul, H. Pharmacokinetics of oestrogens and progestogens. Maturitas 1990; 12: 171-197.
- 2. Lobo, RA. Estrogen and cardiovascular disease. Ann N Y Acad Sci 1990; 592: 286-294.
- 3. Mashchak, CA., Lobo RA. Estrogen replacement therapy and hyperrtensio. J Repro Med 1985; 30 (10 Supl): 805-810.
- 4. Moorjani, S., Dupont, A., Labrie, F y colab. Changes in plasma lipoprotein and apolipoprotein composition in relation to oral versus percutaneous administration of estrogen alone or in cyclic association with autrogestan in menopausal women. J Clin Endocrinol Metab 1991; 73: 373-379.
- 5. Notelovitz, M., Kitchens, CS., Ware, MD. Coagulation and fibronolysis in estrogentreated surgically menopausal women. Obstet Gynecol 1983; 3: 621-625.
- 6. Noyes, MA., Demmier, RW. Estrogen therapy during menopause and the treatment of osteoporosis. Prim Care 1990; 17: 647-665.
- 7. El grupo de escritores para la prueba PEPI. Effects of estrogen or estrogen/progestin regimens on Herat disease risk factors in postmenopausal women: The Postmenopausal Estrogen/Progestin Interventions (PEPI) Trial. JAMA 1995; 273: 199-208.
- 8. Whitehead, MI. Effects of hormone replacement therapy on cardiovascular disease: An interview. Am J Obstet Gynecol 1988; 158: 1658-1661.
- 9. Whitehead, MI., Fraser, D., Schenkel, L., Crook, D. Transdermal administration of oestrogen /progestogen hormone replacement therapy. Lancet 1990; 335: 310-312.
Pregunta 3 (Comparación de regímenes de estrógeno-progestina)
Una mujer de 50 años, cuyo último periódo menstrual ocurrió hace 2 meses, le consulta sobre la terapia de reemplazo hormonal. Algunas de sus amigas toman reemplazo de hormonas y ella tiene varias preguntas. En particular, está buscando información para comparar la terapia cíclica con estrógeno y progestina con la terapia continua con estrógeno y progestina combinados. Cada una de las declaraciones siguientes es correcta, excepto:
- El riesgo de hiperplasia endometrial es similar con ambos regímenes.
- La terapia continua combinada probablemente cause amenorrea durante los primeros 3 meses de tratamiento.*
- La terapia continua combinada con una dosis baja de progestina no ha semostrado efectos adversos sobre los lípidos.
- Tanto la terapia combinada continua como la cíclica con estrógeno y progestina son eficaces en la prevención de la osteoporosis.
Comentarios
La ventaja principal de la terapia continua combinada con estrógeno y progestina sobre la terapia cíclica es la inducción final de amenorrea.
Muchas mujerea hallan que la hemorragia se asocia con la terapia cíclica es indeseable y, para ellas, la suspensión del período menstrual con el régimen continuo probablemente sea un factor importante para fomentar el cumplimiento con la terapia hormonal.
En las pacientes tratadas con el régimen continuo, la hemorragia irregular es común durante los primeros 3 a 4 meses de tratamiento. Después de haberse inducido un endometrio atrófico, el régimen combinado continuo mantiene el endometrio de esa manera. No obstante, algunas mujeres continuarán presentando hemorragia de un endometrio atrófico y estas probablemente no sean buenas candidatas para el régimen continuo.
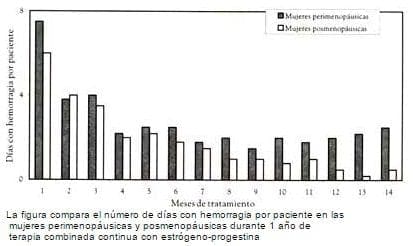
Además, no es tan probable que la terapia combinada continua induzca amenorrea en las mujeres perimenopáusicas como en las posmenopáusicas. En la figura 6.2 se presentan los episodios de hemorragias presentados por pacientes en un estudio. Las mujeres que han pasado la menopausia de 5 años atrás presentan menos episodios de hemorragias que las que han pasado más recientemente.
Por consiguiente, el uso del régimen combinado continuo probablemente deba ser desalentado en los primeros 1 a 2 años después de la menopausia. La mujer descrita probablemente no sea una buena candidata para el régimen continuo en este momento.
Se considera que el efecto beneficioso de los estrógenos:
sobre el riesgo cardiovascular se asocia con un efecto sobre el perfil de los lípidos: con la terapia estro génica sin oposición, las concentraciones de lipoproteínas de alta densidad (HDL) aumentan y las de baja densidad (LDL) disminuyen.
Hasta la fecha, no se han evaluado estudios a largo plazo sobre el impacto de la terapia combinada continua sobre el riesgo cardiovascular, aunque una serie de investigadores han observado los perfiles de los lípidos asociados con tales regímenes.
En un estudio, 92 pacientes tratadas con un régimen continuo de 0.625 mg por día de estrógenos quinos conjugados y 2,5 o 5 mg por día de acetato de medroxiprogesterona fueron observadas durante un período de 12 meses. Se observó una reducción en el colesterol total (2,8%) y LDL (7,6%) y un aumento HDL (4,5%) y HDL2 (6,3%).
La protección del sistema cardiovascular por HDL se ha atribuido mayormente a HDL2. Estos hallazgos de un efecto benigno sobre el perfil de los lípidos con el acetato de medroxiprogesterona a dosis bajas de encuentran en oposición con la evidencia de que en el régimen cíclico, la administración de 10 mg de acetato de medroxiprogesterona durante 10 días de cada ciclo ejerce un efecto negativo sobre las concentraciones de colesterol HDL.
Dos estudios recientemente evaluaron la densidad ósea en pacientes bajo terapia hormonal continua.
En un estudio, la terapia continua demostró evitar la pérdida de hueso completamente durante un período de 5 años, en comparación con una pérdida del 10% en la densidad ósea después de 4 años en el grupo testigo no tratado.
Otro grupo de investigadores comparo los regímenes secuencial y continuo y comunicó un aumento en la densidad ósea y una reducción del recambio óseo en las pacientes en cualquiera de los regímenes. La tasa de aumento en la densidad ósea varió solamente con la dosis de estrógeno.
Además, las muestras de biopsia endometrial en las pacientes que recibían terapia de reemplazo hormonal fueron negativas para la hiperplasia y neoplasia. El régimen continuo demostró proporcionar los mismos efectos saludables que la terapia cíclica sobre el hueso, el endometrio y los síntomas menopáusicos, mientras que reducía al mínimo la ocurrencia de manchas y hemorragia vaginales.
El gráfico compara el número de días con hemorragia por pacientes en las mujeres perimenopáusicas y posmenopáusicas durante 1 año de terapia combinada continua con estrógeno-progestina. [Fuente: Berg G, Amar M, The Modern Management of the Menopause: A Perspective for the 21 st Century. Las actas del VII Congreso Internacional de la Menopausia, Estocolmo, Suecia, 1993. Londres: The Pathernon Publishing Group, 1994, págs. 456].

Figura 6.2. Episodios hemorrágicos presentados por pacientes tratadas
con terapia continua combinada de estrógeno-progestina
Bibliografía
- 1. Berg, G., Hammar, M. The Moder Management of the Menopause: AS Perpective for the 21 st Century. Las actas del VII Congreso Internacional de la Menopausia, Estocolmo, Suecia, 1993. Londres: The Partenón Publishing Group 1994; pág.456.
- 2. Christiansen, C., Rii, BJ. Five years with continous combined oestrogen/progestogen therapy. Effects on calcium metabolism, lipoproteins, and bleeding pattern. Br J Obstet Gynaecol 1990; 97: 1087-1092.
- 3. Mattsson, L-A. Continuous combined HRT: A possible way to avoid uterine bleeding? En Berg G, Hammar M (ed). The Modern Management of the 21st Century. Las actas del VII Congreso Internacional de al Menopausia, Estocolmo, Suecia, 1993. Londres : The Partenón Publishing Group 1994; págs. 453-462.
- 4. Samsioe, GN., Mattsson, L-A. Regimenes for today and the future, en Lobo RA (ed), Treatment of the Postmenopausal Woman: Basic and Clinical Aspects. Nueva York: Raven Press 1994; Pág. 421-426.
- 5. Session, DR.k, Kelly, AC., Jewelewicz, R., Current concepts in estrogen replacement therapy in the menopause. Fertil Steril 1993; 59: 277-284.
- 6. Weinstein, L., Bewtra, C., Gallagher, JC. Evaluation of continuous combines lowdose regimen of estrogen-progestin for treatment of the menopausal patient. Am J Obstet Gynecol 1990; 162: 1534-1542.
- 7. Williams, SR., Frenchek, B., Speroft, T y colab. A study of combined continuous ethinyl estradiol and norethindrone acetate for postmenopausal hormone replacement. Am J Obstet Gynecol 1990; 162: 238-446.
Pregunta 4 (Prevención de la hiperplasia endometrial)
Una mujer de 50 años planifica comenzar la terapia de reemplazo hormonal. La paciente conserva su útero. Usted le recomienda la terapia con progestina cíclica. ¿Qué duración de la administración mensual de progestina es óptima para evitar la hiperplasia endometrial?
- 5 días
- 7 días
- 10 días
- 14 días *
Comentarios
LA hiperplasia endometrial significa, literalmente, el crecimiento excesivo malignidades posteriores, variando del 10 al 15% con atipia leve, al 25% con atipia moderada y al 50 % con atipia severa en estudios a corto plazo, y al 100% en estudios a largo plazo.
La hiperplasia atípica se caracteriza por atipia nuclear, pseudoestratificación y hacinamiento glandular.
La administración de estrógenos sin oposición se ha asociado sólidamente con la hiperplasia endometrial y el cáncer de endometrio. Algunos estudios han demostrado que la incidencia de hiperplasia es de 18% con la administración diaria de 0,625 mg de estrógenos equinos conjugados y del 32% con 1,25mg diarios . Hasta un tercio de estas hiperplasias son atípicas.
La incidencia de hiperplasia se reduce significativamente al agregar una progestina. Los estudios han demostrado que al adición de progestina durante 7 días de cada mes reduce la tasa de hiperplasia a un 3% a 4% .
Cuando la administración de progestina se extiende a 10 días, la incidencia de hiperplasia disminuye al 2%, y cuando la progestina se administra por 12 0 más días por mes, la incidencia es de cero.
Aunque la terapia cíclica con progestina tradicionalmente ha sido administrada por duraciones menores, por ejemplo 7 o 10 días por mes, el reconocimiento reciente de los efectos protectores de la terapia con progestina de más larga duración ha causado que los expertos recomienden a la progestina por 12 o más días del mes.
Bibliografía
- 1. Spcroff, L., Glass, RH., Case, NG. Clinical Gynecologic Endocrinology & Infertility, 5a ed. Bartimore: Williams & Wilkins, 1994; pág. 620.
- 2. Whitehead MI. Prevention of endometrial abnormalities. Acta Obstet Gynecol Scand Supl 1986; 134: 81-90.
- 3. Whitehead, M., Godfree, V. Hormone Replacement Therapy: Your Questions Answered. Londres: Churchill Livingstone, 1992; págs. 115-117.
Pregunta 5 (Interpretación de la concentración de FSH)
Una mujer posmenopáusica de 40 años ha estado tomando 0,9 mg de estrógenos equinos conjugados por 3 meses. Sus bochornos y otros síntomas de eficiencia aguda de estrógenos se han resuelto completamente.
El nivel de hormona folículo estimulante (FSH), tomado antes del tratamiento como parte de la evaluación de amenorrea secundaria, fue de 95 Ul/ml.
¿Cuál sería la interpretación más probable de un valor de seguimiento de 45 Ul/ml para la FSH?
- La dosis es inadecuada
- LA paciente tiene un problema de absorción
- El valor se encuentra entre los límites esperados *
- Un error de laboratorio
Comentarios
Durante la menopausia, las concentraciones de FSH se elevan hasta 18 veces por encima de los niveles premenopáusicos, a medida que las gonadotropinas se liberan para estimular el ovario que esta fallando.
stas concentraciones pueden llegar a sus niveles máximos a los 2 a 3 años después de la menopausia y luego declinar gradualmente durante los 20 a 30 años siguientes.
Las gonadotropinas plasmáticas fluctúan ampliamente durante la menopausia. Es común observar concentraciones de FSH de 30 a 100 unidades, por lo que un valor de 45 estaría dentro de lo esperado.
No es útil usar las concentraciones séricas de FSH para tratar de determinar si el reemplazo de estrógeno es adecuado. La FSH es regulada por otros factores además de los estrógenos: la inhibina, progestinas y andrógenos.
El reemplazo de estrógeno no reducirá la FSH a los valores premenopáusicos, y los esfuerzos por lograr esto resultarían en tratamiento excesivo.
Los valores de FSH son útiles solamente para diagnosticar la menopausia prematura espontánea o la insuficiencia ovárica después de la histerectomía, o para confirmar la menopausia cuando el diagnóstico es incierto.
La mejor manera de determinar si la posología del estrógeno que se administra es apropiada es verificar que haya aliviado los síntomas de la paciente. Las concentraciones séricas de estradiol también pueden medirse para determinar si entran dentro de los límites normales (40 a 60 pg/ml para la fase folicular). Si una paciente que toma la posología oral normal (0,625 a 1,25 mg de estrógenos conjugados diariamente) presenta concentraciones bajas de estradiol sérico, puede presentar un problema de absorción y tal vez sea útil encontrar otra ruta de administración.
Bibliografía
- 1. Jones, KP. Estrofgens and progestins: GAT to use and how to use it. Clin Obstet Gynecol 1992; 35(4): 871-883.
- 2. Speroff, L., Glass, RH., Case, NG. Clinical Gynecologic Endocrinology & Infertility, 5a ed. Baltimore: Williams & Wilkins, 1994; pág. 620.
- 3. Whitehead, M., Godfree, V. Hormone Replacement Therapy: Your Questions Answered. Londres: Churchill Livingstone, 1992; pág. 169.
Pregunta 6 (Fórmulas de progestina)
Una mujer de 53 años está por iniciar la terapia combinada con estrógeno y progestina . Se preocupa acerca de la cardiopatía debido a que una amiga murió recientemente de un ataque cardíaco. ¿Cuál de las siguientes progestinas más probablemente ejerza efectos adversos sobre el perfil de los lípidos?
- Acetato de megestrol
- Desogestrel
- Progesterona micronizada oral
- Acetato medroxiprogesterona
- Noretindrona (también llamada noretisterona) *
Comentarios
Aunque el estrógeno presenta un impacto favorable sobre las concentraciones de lipoproteína y el riesgo de cardiopatía, la adición de progestina a la terapia hormonal disminuye los efectos beneficiosos del estrógeno sobre las lipoproteínas. Las tres categorías distintas orales con la progesterona natural, los compuestos C-21 (entre ellos el acetato de medroxiprogesterona y el acetato de megestrol) y las 19- norprogestinas (también llamadas progestinas 19- nortestosterónicas) tales como las usadas en los anticonceptivos orales.
Todas las progestinas en este último grupo se derivan de la noretindrona. Las estructuras químicas de las diversas. 19- norprogestinas son similares, pero las pequeñas alteraciones estructurales entre ellas pueden dar lugar a diferencias drásticas en la actividad bioquímica. Dentro de este grupo se encuentran las nuevas progestinas gonádicas, todas ellas derivadas del norgestrel, que incluyen el disogestrel, norgestimato y gestodene.
Las progestinas presentan diferentes potencias.
Cuando se administran por vía oral, la mayoría sufre un efecto de primer pasaje en el hígado, que resulta en variaciones en la biodisponibilidad entre las usuarias. De las dos clases de progerstinas sintéticas, el acetato de medroxiprogesterona presenta las propiedades más cercanas a la progesterona producida naturalmente por el cuerpo. El agente se absorbe rápidamente y presenta una vida media de aproximadamente 8 horas. Sin embargo se han notado variaciones significativas entre las pacientes. Para muchas mujeres, una dosis de 5 mg administrada durante 12 días por mes es adecuada para proteger al endometrio, pero en otras es necesaria una dosis de 10 mg por 12 días al mes es suficiente.
Las 19- norprogestinas se usan más a menudo en Europa que en los Estados Unidos para la terapia de reemplazo hormonal. Normalmente se combinan en anticonceptivos orales debido a su mayor actividad progestacional y eficacia oral.
Una preocupación durante la administración a largo plazo se las 19- norprogestinas es su efecto adverso sobre las lipoproteínas. Ese grupo de progestinas ha demostrado reducir las concentraciones de lipoproteínas de alta densidad (HDL) más que otros agentes.
Si se usan estas progestinas, deben administrarse a la menor dosis necesaria para proteger al endometrio, por ejemplo, 2,5 mg de noretindrona durante 12 días de cada mes.
Cuadro 6.3. Fórmula de peogestina
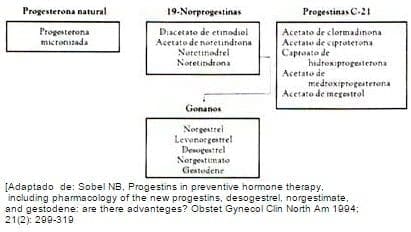
La progesterona natural ha demostrado no ejercer efectos adversos sobre los cambios beneficiosos en los lípidos producidos por el estrógeno. La progesterona oral se absorbe ineficazmente y se metaboliza con rapidez. Cuando la progesterona es micronizada, se absorbe con mayor eficiencia.
De acuerdo con un resumen reciente de datos disponibles, los efectos sobre los lípidos, similares a los observados con el estrógeno sin oposición, fueron producidos por dosis diarias de 2,5 y 5 mg de acetato de medroxiprogesterona, por 200mg de progesterona micronizada diariamente y por una dosis secuencial de 0,15 mg de desogestrel.
Muchos expertos creen que las nuevas progestinas gonánicas tal vez demuestren ventajas sobre las usadas ampliamente en la actualidad, tales como menos cambios en el metabolismo de los lípidos. En un estudio reciente, por ejemplo, el desogestrel demostró no causar efectos negativos en la acción del estrógeno sobre lípidos plasmáticos en 30 mujeres perimenopáusicas que recibieron 0,02 mg de etinilestradiol y 0,15 mg de desogestrel durante 6 meses.
Bibliografía
- 1. Jones, KP. Estrogens and progestins: what to use and how to use it. Obstet Gynecol 1992; 35 (4): 871-883.
- 2. Porcile, A., Gallardo, E., Onetto, P y colab. Very low estrogen-desogestrel contraceptive in perimenopausal hormonal replacement. Maturitas 1994; 18: 93-103.
- 3. Sobel, NB. Progestins in preventive hormone therapy, including pharmacology of the new progestins, desogestrel, norgestimate, and gestodene: are there advantages? Obstet Gynecol Clin North Am 1994; 21(2): 299-319.
Pregunta 7 (Tratamiento de la vaginitis atrófica)
Una mujer de 62 años se queja de sequedad vaginal y de coito doloroso, que han empeorado durante los 5 años transcurridos desde su último periodo. El examen muestra una mucosa vaginal fina, roja y frágil. ¿ Cuál es el tratamiento inicial más eficaz para esta paciente?
- Estrógeno oral
- Parche transdérmico de estrógeno
- Crema vaginal de estrógeno *
- Estrógeno intramuscular
- Gel transdérmico de estrógeno
Comentarios
Los cambios en el tracto genital inferior comienzan durante la menopausia, normalmente desarrollándose en forma gradual a lo largo de varios años. La vulva pierde la mayor parte de su colágeno, adiposidad y capacidad de retener el agua y toma un aspecto aplanado y fino.
LA vagina se acorta y adelgaza y sus paredes se vuelven más delgadas, menos elásticas y pálidas. La vagina secreta menos lubricante y el inicio de la lubricación con el estimulo sexual es más lento.
Debido a que el contenido de glucógeno de las células epiteliales vaginales se reduce, la población de lactobacilos disminuye y el PH aumenta. Generalmente, el resultado es sequedad vaginal, coito doloroso y mayor vulnerabilidad a la infección vaginal y al traumatismo.
Aunque la administración de estrógenos por vía oral, transdérmica o intramuscular tiene efectos beneficiosos, en todos los casos, sobre la vaginitis atrófica, la ruta que actúa con mayor rapidez es la aplicación intravaginal. Los estrógenos aplicados vaginalmente son absorbidos con facilidad por la mucosa en las mujeres con deficiencias de estrógeno y, en realidad, se absorben a una velocidad significativamente mayor en la vagina atrófica que en la sana. La absorción disminuye a medida que la mucosa vaginal se cornifica, lo que ocurre en unos 3 a 4 meses. Después de este tiempo, ocurre menos absorción, pero la cantidad todavía es significativa.
Las cremas vaginales que contienen estrógeno:
Han sido usadas ampliamente para tratar la atrofia vaginal debida a da deficiencia de estrógeno. Los estrógenos mezclados con una base de crema producen inmediatamente una concentración elevada del agente en la vagina. Originalmente se creía que los estrógenos vaginales actuaban sólo localmente, pero los estudios más recientes han demostrado que una cantidad significativa, aunque variable, de estrógeno se absorbe en la corriente sanguínea cuando el medicamento se administra vaginalmente.
Las cremas vaginales pueden contener cualquiera de varias formas de estrógeno, incluso el dienestrol, estradiol, estrógenos conjugados, estropipato o estrona. Las preparaciones disponibles varían según el país. La posología recomendada es similar para los tipos.
En general, se aconseja a las pacientes que se inserten un aplicador lleno (1 a 2 g de la crema, dependiendo de la preparación) 1 ó 2 veces al día, durante una o dos semanas. Una vez que los síntomas de la atrofia vaginal se han revertido, la posología normalmente se reduce a un aplicador lleno una a tres veces por semana.
El medicamento de mantenimiento se aplica a menudo en ciclos de tres semanas, suspendiéndose durante la cuarta semana. Otra opción es cambiar a la terapia oral, transdérmica o intramuscular después de haberse logrado la maduración vaginal.
Las mujeres que se quejan solamente de cambios atróficos del tracto urogenital inferior con frecuencias:
han pasado la menopausia varios años atrás, y pueden preferir la administración vaginal de estrógeno debido a su preocupación acerca de la posibilidad de hemorragia vaginal imprevisible, que ocurre en el 35 al 40 % de las mujeres con útero intacto que reciben terapia estrogénica por vía sistémica.
Las rutas sistémicas incluyen tabletas orales, inyecciones, implantación de granulación que liberan estrógeno, el parche transdérmico de estrógeno y los geles transdérmicos, que se frotan en la piel sobre una parte extensa del cuerpo.
Otra manera eficaz de tratar la vaginitis atrófica son los anillos vaginales y los supositorios vaginales que contienen estradiol. Sin embargo, estas formas posológicas solamente están disponibles en algunos países.
Bibliografía
- 1. Jones, KP. Estrogens and progestins: what to use and how to use it. Clin Obstet Gynecol 1992; 35(4) 871-883.
- 2. Bachmann, GA. Vulvovaginal complaints, en lobo RA (ed), Treatment of the Postmenopausal Woman: Basic and Clinical Aspects. Nueva York: Raven Press, 1994; 140.
- 3. Rigg, LA., Hermann H., Yen SS. Absorptin of estrogens from vaginal creams. New Engl J Med 1978; 298(4): 195-197.
- 4. Speroff, L., Glass, RH., Case, NG. Clinical Gynecologic Endocrinology & Infertility, 5a ed. Bartimore: Williams & Wilkins, 1994; 630.
- 5. Whitehead, M., Godfree, V. Hormone Replacement Therapy: Your Queations Answered. Londres: Chuchill Livingstone, 1992; 108-109.
- 6. USPDI-Drug Information lar the Health Care Professional. Rockville, Maryland: The United States Pharmacopeial Convention, Inc., 1992; 1349.
Pregunta 8 (Terapia combinada con estrógeno-metiltestosterona)
Una mujer de 35 años fue sometida a histerectomía abdominal total con salpingoooforectomía bilateral hace 6 meses para el tratamiento de endrometriosis.
Desde entonces, se ha mantenido con 2 mg de estradiol por vía oral diariamente, pero se queja de varios síntomas persistentes. ¿Para cuales de los siguientes síntomas es probable que la metiltestosterona sea de mayor beneficio?
- Bochornos
- Insomnio
- Libido baja*
- Depresión
- Distensión abdominal
Comentarios
La testosterona, que influye sobre la libido, es liberada por los ovarios durante toda la vida, incluso después de la menopausia. Las concentraciones de testosterona no se reducen apreciablemente después de la menopausia; de hecho, durante los primeros años después de la menopausia, los ovarios de muchas mujeres secretan más testosterona que antes de la menopausia.
Los estudios realizados en mujeres que pasan por la menopausia natural indican una asociación positiva entre las concentraciones plasmáticas de andrógeno y el interés sexual, la respuesta sexual y la frecuencia del coito. Sin embargo, no se ha hallado una relación entre las concentraciones de estrógeno y la libido.
LA ooforectomía bilateral elimina una fuente importante de producción de andrógeno en las mujeres. Dentro del primer día después de la cirugía, las concentraciones plasmáticas de estradiol y testosterona se reducen significativamente.
La terapia estrogénica puede aliviar muchos síntomas de la menopausia, incluso los bochornos, el insomnio y la depresión. Si la distensión abdominal no se resuelve con el pasaje del tiempo, puede tratar de corregirse reduciendo la ingestión de sal o agregando un fármaco diurético suave.
El reemplazo de estrógeno puede realzar la libido en mujeres cuyo interés sexual han menguado debido a atrofia vaginal o dispareunia, pero mayormente no se ha demostrado que tenga un efecto positivo sobre el deseo sexual.
Una mujer joven, como la paciente descrita:
que ha sido sometida resientemente a histerectomía abdominal total con salpingoooforectomía bilateral, y que esta recibiendo reemplazo de estrógeno, tiene muy poca probabilidad de presentar atrofia vagianl l La causa básica de la reducción de su libido probablemente sea una deficiencia de andrógeno.
Un estudio de mujeres que han sido sometidas a histerectomía abdominal total y salpingo-ooforectomía bilateral halló que las tratadas con una preparación de estrógeno y andrógeno presentaban mayor deseo sexual, excitación sexual y fantasías que las que no fueron tratadas o las que recibieron estrógeno solamente.
Los estudios también demostraron que la libido de mujeres que pasaron a través de la menopausia natural fue afectada positivamente agregando testosterona a sus regímenes de estrógeno.
Se dispone de varios tipos de testosterona, entre ellos la metiltestosterona para administración oral y el enantato de testosterona para inyección. En algunos países se usan los implantes de granulaciones subcutáneas que contienen testosterona.
También se dispone de productos combinados que incluyen estrógeno y testosterona. Se han llevado a cabo pocos estudios concernientes a la posología de la testosterona y a sus efectos sobre la libido.
Las posologías recomendadas para la testosterona inyectable:
Varían de 75 a 150 mg una vez al mes. Para la terapia oral, la posología es generalmente de 1,25 a 10 mg diarios.
Los efectos secundarios de la terapia con testosterona en las mujeres pueden incluir hirsutismo, acné y profundización de la voz.
En un estudio canadiense, nueve mujeres menopáusicas que recibieron inyecciones mensuales de andrógeno y esdrógeno durante varios meses a varios años presentaron un virilismo severo. La posología que recibieron 150 mg de bencilácido hidrozona de enantato de testosterona es equivalente a 69 mg de testosterona.
Otro estudio en que se usó la misma combinación y posología durante cuatro años halló que del 15 al 20% de las pacientes desarrollaron hirsutismo facial leve que se abatió cuando la posología fue modificada. El mejor enfoque es usar la menor dosis posible y reducir la posología si ocurren síntomas de virilización.
Las dosis mayores de testosterona pueden causar lesión hepática, especialmente cuando se administran por vía oral. No se ha demostrado que las dosis menores lesionen al hígado.
La administración Xde testosterona:
Puede tener efecto adverso sobre los lípidos séricos, disminuyendo potencialmente los efectos cardiovasculares positivos del estrógeno. En un estudio reciente, 13 mujeres postmenopausicas que tomaron estrógenos conjugados (0,625 mg diariamente) se compararon con un grupo similar que tomaba una combinación de estrógeno y metil-testosterona (o,625 mg y 1,25 mg diariamente).
Los perfiles de los lípidos al iniciarse el estudio eran similares para ambos grupos pero al cabo de 6 meses el que tomo metiltestosterona mostró una reducción significativa de las lipoproteínas de alta densidad (HDL)- un efecto que no se observo en el grupo tratado solamente con estrógeno. No se hallaron diferencias en los triglicéridos o en las lipoproteínas de baja densidad (LDL).
Como se sabe que el proceso de la aterosclerosis está relacionada con un aumento en las concentraciones de LDL y una reducción en las de HDL, las concentraciones de lípidos deben vigilarse en las mujeres tratadas con testosterona, aún a posologías bajas.
Bibliografía
- 1. Burger, H.G., Hailes, J., Menelaus M. Y Colab. The management of persistent menopausal symptoms with oestradiol-testosterone implants: clinical, lipid and hormonal results. Maturitas 1984; 6: 351-358.
- 2. Burger, H. G., Hailes, J., Nelson,J. Effect of combined implants of oestradiol and testosterone on libido in postmenopausal women. BMJ 1987; 294: 936-937.
- 3. Hickok, L.R., Toomey, C., Speroff, L. A comparison of esterified estrogens with and without methyltestosterone: effects on endometrial histology and serum lipoproteins in postmenopausal women. Obstet Gynecol 1993; 82(6): 919-924.
- 4. Sherwin, B.B. Affective chages with estrogen and androgen replacement therapy in surgically menopausal women. J Affect Disord 1988; 14: 177-187.
- 5. Sherwin, B.B., Gelfand, M.M. Differential symptom response to parenteral estrogen and/or androgen administration in the surgical menopause. Am J Obstet Gynecol 1985; 151: 153-160.
- 6. Sherwin, B.B., Gelfand M.M. The role of androgen in the maintenance of sexual functioning in oophorectomized women. Psychosomatic Med 1987; 49: 397-409.
- 7. Speroff, L., Glass, R.H., Case N.G. Clinical Gynecologic Endocrinology & Uinfertility, 5a ed. Baltimore: Williams & Wilkins, 1994; 623-624.
- 8. Urman, B., Pride, S.M., Yuen, B.H. Elevated serum testosterone, hirsutism, and virilism associated with combined androgen-estrogen hormone replacement therapy. Obstet Gynecol 1991; 77(4): 595-597.
- 9. USPDI-Drug Information for the Health Care Professional. Rockville, Maryland: The United States Pharmacopeial Convention, Inc., 1992; 193-201.