Artículos Originales
María Isabel Barona C.*
* Docente adjunto. Dermatología. Universidad del Valle _ Cali. Colombia.
Correspondencia: Carrera 38A No. 5A-100 Torre B. 604 e-mail: mabarona@andinet.com
Resumen
La piel es un órgano complejo que refleja la salud general, se relaciona con diferentes clases de células para mantenerse sana y constituye el blanco de diferentes hormonas1,2; en ella se han identificado receptores específicos para estrógenos y otras hormonas que corresponden a la superfamilia de las esteroideas/tiroideas, los cuales dejan de activarse cuando no hay estrógenos que los estimule produciendo una reducción de las funciones cutáneas que están bajo el control estrogénico3.
La menopausia se define como la suspensión permanente de la menstruación debido a la pérdida de la función folicular de los ovarios4, lo cual implica la caída abrupta en la producción de estrógenos.
Se ha sugerido que durante la menopausia las alteraciones hormonales que ocurren aumentan el proceso de envejecimiento cutáneo5, y por tanto, se puede pensar que la terapia hormonal de reemplazo también mejorará los diferentes síntomas de envejecimiento que aparecen en las mujeres posmenopáusicas, tales como sequedad y disminución de la firmeza y elasticidad de la piel. Sin embargo, es importante considerar que hay factores intrínsecos y extrínsecos implicados en el proceso de envejecimiento que deben tenerse en cuenta, como la influencia genética y la exposición solar1,5.
Palabras clave: Piel, menopausia, hormonas, colágeno, envejecimiento.
Abstract
The skin is a complex organ that reflects general health, maintains relation with different types of cells for its own health and is the target for numerous hormones1,2. Estrogens receptors have been identified in human skin and other specific receptors which belong to the steroid/ thyroid hormones superfamily. A decrease in estrogen influences might induces a reduction of those skin functions that are under estrogen control3.
Menopause is the permanent cessation of menstruation due to loss of ovarian follicular function4, with a sudden fall of estrogen production.
It has been suggested that during the menopause hormonal changes lead to increase in the aging cutaneous process5 and therefore if the hormone replacement therapy also improves the different aging simptoms that appear during the post-menopause, such as skin dryness and decrease in skin firmness and elasticity.
However, it is important to consider that there are other intrinsic and extrinsic factors that influence the aging process, as genetics and ultraviolet light exposure5.
Key words: Skin, menopause, hormones, colagen, aging.
Capas de la Piel
La piel está compuesta por una variedad de células de diferente origen embriológico, y posee dos capas principales: la epidermis es la más externa y está compuesta de queratinocitos de origen ectodérmico, entremezclados con melanocitos provenientes de la cresta neural, un tejido embriogénico ectodérmico especializado2.

Figura 1. Hematoxilina-eosina 4x. Panorámica de piel joven, con epitelio ondulante, linearidad fina evidente en la superficie, crestas interpapilares prominentes. La dermis papilar y adventicial es fibrilar, la dermis reticular tiene colágenos tipos I y II rugosos gruesos. El detalle resalta las características del epitelio y de la dermis ya descritas.
La otra capa más profunda es la dermis, un estroma que constituye el principal volumen de la piel, de origen mesodérmico, está íntimamente unida a la epidermis y compuesta predominantemente por tejido conectivo y vasos sanguíneos. Procesos digitiformes o papilas dérmicas se proyectan hacia la epidermis. Contiene estructuras derivadas del ectodermo, como folículos pilosos y glándulas sudoríparas. El colágeno y la elastina son las principales fibras dérmicas presentes en su interior, siendo el colágeno el más abundante, 70-80% del peso seco de la piel humana5, producido por los fibroblastos, que se organiza de manera paralela a la superficie cutánea, y es el responsable de la flexibilidad de la dermis. Existen por lo menos ocho clases diferentes de colágenos, todos ellos formados por cadenas de polipéptidos, siendo el más abundante el tipo I y el único detectado en hueso. El tipo III también es común, está distribuido por todo el cuerpo, aunque en menor cantidad que el tipo I. El colágeno tipo IV es el mayor componente estructural de la membrana basal, y es el responsable de su estabilidad mecánica6. Las fibras de elastina forman una red delgada sub-epidérmica, constituyen el 5% de la dermis, y está conformada por una proteína elástica que contribuye a mantener la tensión normal de la piel.
El tejido conectivo también contiene glicosaminoglicanos (GAGs), que consisten en cadenas largas de disacáridos repetidos, unidos a proteínas específicas que atraen gran cantidad de iones osmóticamente activos y, con ellos, agua a la matriz extracelular que le confieren la turgencia e hidratación a la piel2.
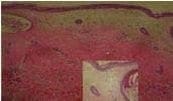
Figura 2. Hematoxilina-eosina 4x. Piel no expuesta con rasgos de envejecimiento intrínseco. Epitelio atrófico, sin crestas interpapilares. Dermis papilar hipocelular homogenizada, ensanchada. Dermis reticular fragmentada, la dermis adventicial ha sido reemplazada por este mismo tipo de colágeno. El detalle en 10x resalta la hipocelularidad, el colágeno homogéneo y la ausencia de soporte a los anexos cutáneos.
Tanto los queratinocitos epidérmicos como los fibroblastos dérmicos poseen receptores para estrógenos y andrógenos. Los folículos pilosos, glándulas sebáceas, sudoríparas y vasos sanguíneos también presentan receptores estrogénicos en su superficie7.
Sin embargo, el epitelio vaginal tiene la más alta concentración de estos receptores, siendo muy alta la relación para receptores de estrógenos: andrógenos, la cual se invierte en la vulva, donde es mayor la densidad de receptores androgénicos8. En la posmenopausia se ha encontrado en la piel del pubis una disminución de casi un 50% de los receptores para andrógenos, lo cual puede ser relevante en el tratamiento de las dermatosis vulvovaginales de las mujeres posmenopáusicas9.
Epidermis
Investigaciones histológicas realizadas han demostrado adelgazamiento de la epidermis, aplanamiento de la membrana basal y de las papilas dérmicas después de la castración y durante el proceso de envejecimiento, que se revierte después de administrarse estrógenos durante 3 meses, y persisten aún después de 6 meses10-11.
Sin embargo, los estudios en la epidermis son todavía insuficientes y se espera la aplicación de todos los nuevos avances tecnológicos, que permitan progresar en la demostración de los efectos de los estrógenos, particularmente en esta capa de la piel2.
Dermis
El grosor de la dermis ha sido estudiado empleando diferentes métodos como el ultrasonido de alta frecuencia; se ha demostrado su adelgazamiento durante la menopausia y la mejoría con la terapia hormonal12-13.
Algunos autores han mostrado que después del tratamiento con estrógenos se aumenta la tasa de producción de colágeno y la síntesis de ácido hialurónico, mejorando con esto la capacidad higroscópica e hidratación de la piel14. Otros componentes de la dermis, también mejoran con el tratamiento hormonal, por ejemplo, en ratones castrados se ha demostrado un aumento del 70% de GAGs después de dos semanas de tratamiento con estrógenos14.
Las fibrillas de colágeno se han encontrado menos fragmentadas en la dermis de mujeres tratadas con estrógenos15. Holland y col. demostraron una reducción en el recambio de colágeno, como también la formación de fibras de colágeno más maduras durante la posmenopausia en mujeres que reciben terapia hormonal de reemplazo16.
Sin embargo, hay controversias respecto a los cambios del colágeno de la piel relacionados con la edad y la terapia hormonal. Para Shuster y col.17, la cantidad de colágeno, medida mediante el cálculo de éste por milímetro cuadrado en una biopsia de piel, fue mayor en hombres que en mujeres, independientemente de la edad, mientras que para Hall y col.18 estos hallazgos no fueron confirmados. Otros autores como Oikarinen A5 y Haapasaari y col19 no encuentran cambios en la cantidad ni en la síntesis de colágeno, en mujeres durante la posmenopausia, quienes han recibido tratamiento con estrógenos solos o asociados con progestágenos durante un año.
Diferentes estudios2,8,20 han demostrado que la disminución del contenido de colágeno en la piel ocurre mucho más rápido en los primeros años de la posmenopausia, casi 30% en los primeros 5 años y que el aumento del colágeno después de 6 meses de tratamiento con terapia hormonal de reemplazo depende del contenido de colágeno al inicio del tratamiento. En mujeres con un bajo contenido de colágeno, los estrógenos son inicialmente de valor terapéutico y luego profiláctico, mientras que en mujeres con una cantidad moderada de colágeno el tratamiento con estrógenos en las primeras etapas de la menopausia son sólo de valor profiláctico. De esta manera, la deficiencia de colágeno será corregida pero nunca en exceso.
El contenido de colágeno medido radiológicamente está directamente relacionado con el grosor de la piel. Utilizando diferentes dosis de estradiol, ya sea tópico o en implantes, se ha encontrado un aumento significante en el grosor de la piel, especialmente durante los primeros 6 meses de tratamiento. El seguimiento de pacientes que reciben estrógenos en la posmenopausia ha revelado que el contenido de colágeno y el grosor de la piel continúan aumentados, comparados con mujeres que no reciben tratamiento2, 20-21.
En un estudio prospectivo, Savvas y col.22 reportan un aumento en la proporción del colágeno tipo III en mujeres que reciben terapia hormonal de reemplazo.
Por otro lado, se observa que durante el envejecimiento se produce un aumento en la glicosilación del colágeno cutáneo, posiblemente responsable del entrecruzamiento entre las diferentes moléculas de colágeno, de igual manera se ha demostrado una disminución en la cantidad de GSGs favoreciendo la resequedad de la piel23-24, pero mejoran cuando se administran estrógenos.
Respecto a los lípidos de la superficie cutánea, se ha encontrado que la terapia hormonal combinada con progestágenos1, no los estrógenos solos, los aumenta especialmente en las áreas de la piel con mayor número de glándulas sebáceas, como la frente y la región preesternal, y por tanto debe tenerse en cuenta en pacientes con acné a quienes se les administre el tratamiento.
Vascularización Capilar de la Piel
Respecto a la vasculatura dérmica, la información disponible está aumentando y se ha encontrado una interacción importante con las hormonas femeninas, demostrando que la reactividad de los vasos sanguíneos de la piel normal de las mujeres varía durante el ciclo menstrual. Estos hallazgos tienen manifestaciones clínicas, tales como la disminución de la temperatura en las manos y pies o la sudoración en la cara25.
Las alteraciones en el flujo sanguíneo cutáneo comprometen dos vías importantes del sistema nervioso simpático: primero, un efecto vasoconstrictor adrenérgico, que es tónicamente activo y cuenta para la mayoría de los cambios sutiles que ocurren durante el curso de actividades diarias y es responsable del control de la temperatura corporal en estado de reposo; segundo, el sistema vasodilatador, no adrenérgico, aunque no tónicamente activo, es responsable del aumento en más del 90% del flujo sanguíneo cutáneo durante el estado de hipertermia. Este sistema es apoyado por el ÓXIDO NÍTRICO, ejerciendo vasodilatación aguda. Otro factor determinante del flujo sanguíneo de la piel es la exposición al calor o al frío locales y, como ya se mencionó, el influjo de las variaciones hormonales26.
Cuando la temperatura corporal es monitoreada en mujeres premenopáusicas, se observa un aumento de 0.3-0.5°C en la fase luteal, donde los niveles de hormonas sexuales son altos y hay predominio de progesterona, comparada con la fase folicular, cuando la secreción de estradiol y progesterona es baja25.
En mujeres que reciben terapia hormonal de reemplazo, el flujo sanguíneo capilar se aumenta en un 20 a 30%, debido a la vasodilatación que ocurre mediante el mecanismo de relajación de la microcirculación cutánea dependiente del endotelio, comprobada por Doppler27,28 y no por reclutamiento adicional de vasos sanguíneos. Por otro lado, se cree que las hormonas sexuales esteroideas femeninas también actúan centralmente, influyendo en las neuronas dependientes de la temperatura en el hipotálamo anterior preóptico29. Simultáneamente, los estrógenos favorecen la producción y liberación de óxido nítrico endotelial, que aumenta la vasodilatación25.
Sin embargo, durante la posmenopausia, después de 2 años de tratamiento, no se ha observado ninguna alteración del flujo sanguíneo máximo adquirido, cuando se compara con mujeres posmenopáusicas que no reciben tratamiento30. Otros autores31, sí han encontrado, en mujeres posmenopáusicas que reciben tratamiento hormonal, una disminución de la vasoconstricción cuando se les administra noradrenalina.
Las oleadas de calor se consideran como uno de los síntomas más característicos de la menopausia. Se presentan casi en un 75% de las mujeres durante la menopausia temprana y un 25% de todas las mujeres los experimentan 5 años más tarde. Diferentes estudios han revelado que se deben a la vasodilatación de la red vascular de las papilas dérmicas y del tejido celular subcutáneo, particularmente los de la cara, el cuello, el tórax y las palmas y plantas. Reflejan el pobre control vascular periférico que se sucede debido a la deprivación de estrógenos, ya que éstos actúan como neurotransmisores directos en los capilares terminales, ejerciendo un control neurovascular32.
Pelo
Los folículos pilosos poseen tres fases: anágena o de crecimiento, catágeno o de reposo y telógeno o de caída y están influenciados por un microambiente hormonal. Se han identificado receptores para estrógenos en los folículos pilosos que regulan su paso de la fase telógena a anágena33.
La pérdida del pelo del cuero cabelludo y púbico se ha asociado con el inicio de la menopausia, al igual que el aumento del pelo facial que se acentúa en la posmenopausia34.
Se cree que los estrógenos durante el período premenopáusico actúan como antiandrogénicos, protegiendo los folículos pilosos35; sin embargo, como los niveles circulantes de testosterona disponible, androstenediona, dehidroepiandrosterona y dehidroepiandrosterona sulfato disminuyen después de la menopausia, los cambios en el pelo durante esta etapa podrían ser explicados, no sólo por el influjo hormonal sino como consecuencia de otros factores tales como el envejecimiento y factores genéticos36-37.
Los estrógenos permiten que la duración del ciclo de vida del folículo piloso se aumente, propiciando la prolongación de la fase anágena del ciclo de crecimiento del pelo2-4.
Conclusiones
La piel, al igual que otros órganos, posee receptores hormonales, donde éstos se acoplan y realizan funciones importantes. Por tanto, durante períodos de cambios en la producción y en los niveles circulantes de hormonas como la menopausia, se afecta morfológica y funcionalmente. Los diferentes estudios, reportados algunos de ellos en esta revisión, demuestran que la terapia hormonal de reemplazo contribuye a mejorar las deficiencias que se presentan en las distintas capas de la piel, ayudando a mantener el equilibrio que la piel necesita para mantenerse sana y ejercer su función de barrera cutánea apropiada frente a las injurias externas e internas. Aunque para algunos autores los resultados no han sido replicables respecto a los beneficios de la terapia hormonal, el mayor número de estudios, llevados a cabo con un número de pacientes significante, sí lo demuestra, de ahí el valor que tiene este tratamiento.
En una segunda parte, se describirán las manifestaciones clínicas cutáneas que se presentan durante la menopausia y, posteriormente, la respuesta de ellas ante la terapia hormonal.
Bibliografía
1. Sator PG, Schmidt JB, Sator MO, et al. The influence of hormone replacement therapy on skin ageing. A pilot study. Maturitas 2001; 39: 43-55.
2. Brincat MP ed. Hormone replacement therapy and the skin. Parthenon Publishing Group U.K. 2001; 1-17.
3. Schmidt JB, Lindmaier A, Spona J. Hormone receptors in pubic skin of premenopausal and postmenopausal females. Gynecol Obstet Invest 1990; 30: 96-100.
4. Gail AG, Lee NP, Arriola ER. The menopause. The Lancet 1999; 353(9152): 571-80.
5. Oikarinen A. Systemic estrogens have no conclusive beneficial effect on human skin connective tissue. Acta Obstet Gynecol Scand 2000; 79(4): 250-4.
6. Castelo-Branco C. Skin collagen changes related to age, menopause and hormone replacement therapy. En: Brincat MP. Hormone Replacement Therapy and the Skin. Parthenon Publishing Group U.K. 2001; 19-37.
7. Alberts B, Bray D, Lewis J et al, eds. Molecular Biology of The Cell. New York: Garland Publishing.
8. McLean AB, Nicol LA, Hodgins MB. Immunohistochemical localization of estrogen receptors in the vulva and vagina. J Reprod Med 1990; 35: 1015-16.
9. Hodgins MB, Spike RC, Mackie RM, et al. An immunohistochemical study of androgen, oestrogen and progesterone receptors in the vulva and vagina. Br J Obstet Gynaecol 1998; 105: 216-22.
10. Rauramo L, Punnonen R. Wriking einer oralen estrogentherapie mit oestriolsuccinat auf die Aut. Hastierter [Effect of oral oestrogen treatment with estriol succinate on the skin of castrated women]. Z Haut Geschlechtskr 1969; 44: 463-70.
11. Punnonen R. On the effect of astration and peroral estrogen therapy on the skin. Acta Obstet Gynecol Scand 1971; 9 (Suppl 9): 32.
12. Brincat M, Moniz CJ, Studd JW, et al. Long-term effects of the menopause and sex hormones on skin thickness. Br J Obstet Gynaecol 1985; 92: 256-259.
13. Meschia M, Bruschi F, Amicarelli F, et al. Transdermal hormone replacement therapy and skin in postmenopausal women, a placebo controlled study. Menopause 1994; 1: 79-82.
14. Grosman N, Hvidberg E, Schou J. The effect of oestrogenic treatment on the acid mucopolysaccharide pattern in skin of mice. Acta Pharmacol Toxicol (Copenh) 1971; 30: 458-64.
15. Goldzieher MA. The effects of oestrogens on the senile skin. J Gerontol 1946; 1: 196.
16. Holland EF, Studd JW, Mansell JP, et al. Changes in collagen composition and cross-links in bone and skin of osteoporotic postmenopausal women treated with percutaneous estradiol implants. Obstet Gynaecol 1994; 83: 180-3.
17. Shuster S, Black MM, McVitie E. The influence of age and sex on skin thickness, skin collagen and density. Br J Dermatol 1975; 6: 639-43.
18. Hall DA, Reed FB, Nuki G, et al. The relative effects of age and corticosteroid therapy on the collagen profiles of dermis from subjects with rheumatoid arthritis. Age ageing 1974; 3: 15-22.
19. Haapasaari KM, Raudaskoski T, Kallioinen M, et al. Systemic therapy with estrogen or estrogen with progestin has no effect on skin collagen in postmenopausal women. Maturitas 1997; 27: 153-62.
20. Brincat M, Moniz CF, Studd JW, et al. Sex hormones and skin collagen content in postmenopausal women. Br Med J (Clin Res Ed) 1983; 287: 1337-8.
21. Brincat M, Versi E, Moniz CF, et al. Skin collagen changes in postmenopausal women receiving different regimens of estrogen therapy. Obstet Gynecol 1987; 70: 123-7.
22. Savvas M, Bishop J, Laurent G, et al. Type III collagen content in the skin of postmenopausal women receiving oestradiol and testosterone implants. Br J Obstet Gynaecol 1993; 100: 154-6.
23. Kohn RR, Schnider SL. Collagen changes in aging skin. En Balin AK, Kligman AM eds. Aging and the skin. New York: Raven Press 1989; 121-42.
24. Monnier VM, Cerami A. Nonenzymatic browning in vivo : possible process for aging of long – lived proteins. Science 1981; 211: 491-3.
25. Gruber C, Huber J. Capillary blood flow in the skin. En: Brincat MP. Hormone Replacement therapy and the Skin Parthenon Publishing 2001; 77-84.
26. Johnson JM, Proppe DW. Cardiovascular adjustments to heat stress. En: Handbook of Physiology. Environmental Physiology. 1st ed. Bethesda, MD: American Physiology Society, 1996: 215-44.
27. Haenggi W, Linder HR, Birkhaeuser MH, et al. Microscopic findings of the nail-fold capillaries_dependence on menopausal status and hormone replacement therapy. Maturitas 1995; 22: 37-46.
28. Arora S, Veves A, Caballaro AE, et al. Estrogen improves endotelial function. J Vasc Surg 1998; 27: 1141-6; discusión 1147.
29. Stephenson LA, Kolka MA. Thermoregulation in women. Exerc Sport Sci Rev 1993; 21: 231-62.
30. Brooks Asplund EM, Kenney WL. Chronic hormone replacement therapy does not alter resting or maximal skin blood flow. J Appl Physiol 1998; 85: 505-10.
31. Sudhir K, Esler MD, Jennings GL, et al. Estrogen supplementation decreases norepinephrine-induced vasoconstriction and total body norepinephrine spillover in perimenopausal women. Hypertension 1997; 30: 1538-43.
32. Ginsburg J, Hardiman P, O’Reilly B. Peripheral blood flow in menopausal women
33. who have hot flushes and in those who do not. Br Med J 1989; 298: 1488-90.
34. Oh HS, Smart RC. An estrogen receptor pathway regulates the telogen-anagen hair follicle transition and influences epidermal cell proliferation. Proc Natl Acad Sci USA 1996; 93: 12525-30.
35. Palacios S, Cifuentes I. Hair and hormone replacement therapy. En: Brincat MP. Parthenon Publishing UK 2001; 145-54.
36. Venning VA, Dawber RPR. Patterned androgenic alopecia in women. J Am Acad Dermatol 1988; 18: 1073-7.
37. Rannevik G, Carlstrom K, Jeppsson S, et al. A prospective long-term study in women from pre-menopause to post-menopause: changing profiles of gonadotrophins, oestrogens and androgens. Maturitas 1986; 8: 297-307.
38. Laughlin GA, Barret-Connor E, Kritz-Silverstein D, et al. Hysterectomy, oophorectomy, and endogenous sex hormone levels in older women: the Rancho Bernardo Study. J Clin Ecdocrinol Metab 2000; 85: 645-51.
