Endocrinología Ginecológica
MARÍA ALEJANDRA YÉPEZ GALINDO,* GUSTAVO GÓMEZ TABARES**
Introducción
La prolactina (PRL) es una hormona secretada por la hipófisis anterior, y las variaciones en su secreción siguen el ritmo circadiano, caracterizado por niveles superiores durante la fase MOR (movimientos oculares rápidos) del sueño, con concentraciones pico entre las 2 a. m. y las 5 a. m., y durante la ovulación; niveles inferiores de PRL se evidencian durante la vigilia.1,2 La producción extra hipofisiaria se llevará a cabo en los ovarios, las glándulas mamarias y el endometrio; adicionalmente, existen otros sitios de origen como próstata, linfocitos, células hematopoyéticas, piel, tejido adiposo, timo, sistema linfático, endotelio y cerebro.2
Esta hormona, en términos generales, ejerce funciones sobre la reproducción, la lactancia y el metabolismo.3 En las mujeres, la PRL está involucrada en el desarrollo folicular y el mantenimiento del cuerpo lúteo y también actúa sobre la glándula mamaria para inducir y mantener la lactancia.2
La hiperprolactinemia (HPRL) se define como cualquier situación en la que los niveles circulantes de prolactina son más altos que los de la población de referencia.4 En la práctica clínica, el término se utiliza generalmente cuando el nivel de PRL se encuentra crónicamente elevado. Valores mayores de 20-25 ng/ml (420-500 mUI/l) son considerados patológicos, pero el valor de referencia depende del tipo de ensayo utilizado para su determinación.4
Es un motivo de consulta frecuente tanto para ginecólogos como para endocrinólogos y médicos generales.
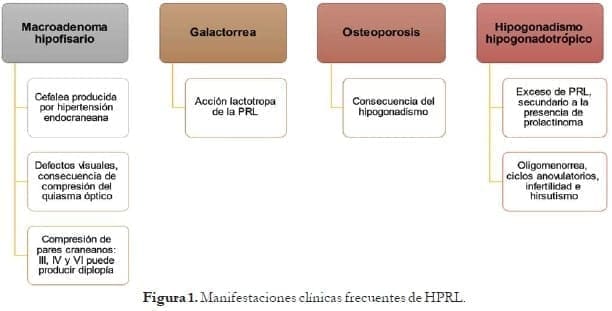
La HPRL se encuentra en el 15 al 20% de las mujeres que se someten a estudios para infertilidad.5 Las manifestaciones clínicas incluyen galactorrea, alteraciones del ciclo menstrual, infertilidad y osteoporosis; de acuerdo con los síntomas más comunes, las anormalidades menstruales pueden incluir ciclos irregulares desde 6 semanas hasta 6 meses de periodos caracterizados por amenorrea, oligomenorrea, hipomenorrea, ciclos menstruales cortos, regresión prematura del cuerpo lúteo, síndrome disfórico premenstrual, disminución de la libido, dispareunia, hirsutismo, acné, cefalea, y en presencia tumoral, puede ocasionar síntomas visuales cuando el prolactinoma alcanza un diámetro superior a 1 cm. Todas las alteraciones descritas anteriormente se encuentran en estrecha relación con el sistema reproductivo y en consecuencia repercuten en la fertilidad.6
Se calcula que la alteración de esta hormona afecta principalmente a mujeres entre los 25 y los 34 años, con una prevalencia de 10 a 90 de cada 100.000 personas; también ocurre en hombres, pero es cuatro veces menos frecuente.1
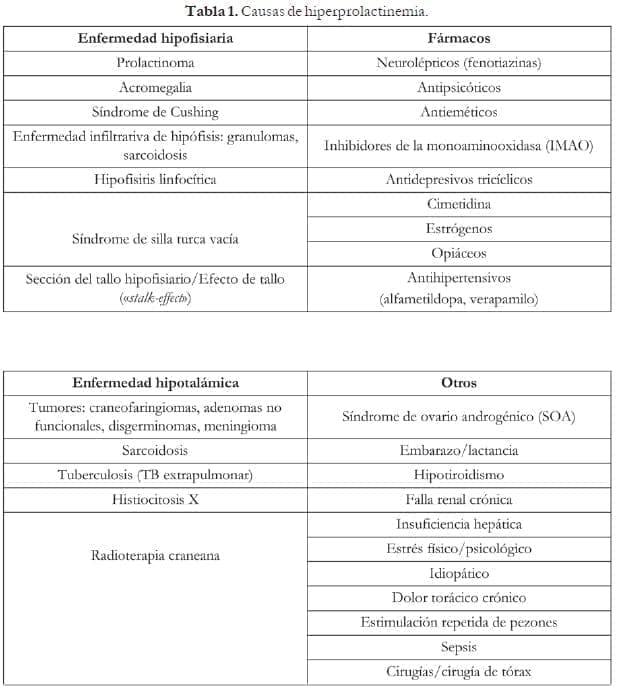
Entre las diversas causas de la HPRL se pueden encontrar embarazo, consumo de ciertos fármacos, trastornos tiroideos, y enfermedad renal y hepática; pero la causa más frecuente son los adenomas hipofisiarios productores de prolactina (prolactinomas).2,7,8 Estos se clasifican en microadenomas (menores de 10 mm), que constituyen el 90% de los casos y se manifiestan con disfunción menstrual e infertilidad. Los tumores con más de 10 mm se llaman macroadenomas, son menos frecuentes y se asocian con niveles más altos de PRL, usualmente en presencia de disfunción neurológica e hipogonadismo.5
Además de los factores fisiológicos que podrían causar su alteración, también hay condiciones patológicas que llevan a HPRL.
Estas incluyen enfermedades que ocasionan lesión de las células hipofisiarias o de otras estructuras del sistema nervioso central (SNC).1 Algunas de las causas tanto fisiológicas como patológicas se presentan en la tabla 1.
No es usual hablar de hiperprolactinemia como una enfermedad en sí misma, sino como un hallazgo o síntoma, el cual nos lleva a sospechar alteraciones patológicas en los órganos donde ejerce su función fisiológica. Por esta razón el manejo de la alteración de los niveles de la prolactina, e indirectamente de la infertilidad por esta causa, debe iniciar con la búsqueda activa de un diagnóstico integral, que corresponda a la causa de la elevación de la concentración de prolactina.1
Prolactinomas
La HPRL es causada por adenomas hipofisiarios productores de prolactina (denominados prolactinomas) en alrededor de un 50% de los casos.4
Se clasifican, según su tamaño, en microprolactinomas (menores de 1 cm) y macroprolactinomas (mayores de 1 cm). Rara vez se presentan los prolactinomas gigantes (mayores de 4 cm), que son más frecuentes en hombres.9 Su incidencia es de 27 casos por millón por año.9
El 70% de los prolactinomas se presenta en mujeres9 y el 64% al 90% son microprolactinomas intraselares que no crecerán durante el seguimiento.9,10
En mujeres, dado que la mayoría de los prolactinomas son microprolactinomas, suelen producirse alteraciones endocrinológicas (trastornos del ciclo menstrual e infertilidad). En mujeres posmenopáusicas prevalece la clínica de efecto de masa sobre otras alteraciones.10
Por su parte, en los hombres, el 80% de estos tumores son macroprolactinomas, por lo que presentan síntomas de efecto de masa como alteraciones visuales (incluyendo pérdida visual) y cefalea.10 Así mismo, pueden presentarse otras manifestaciones secundarias a la afectación de otros ejes hipofisiarios. En ellos, la HPRL produce disminución de la libido, disfunción eréctil, oligospermia e infertilidad y, con menos frecuencia, ginecomastia y galactorrea.10 Figura 1.
Fisiopatología
La prolactina es una hormona polipeptídica de cadena sencilla y existen diferentes isoformas de esta, cada una con funciones biológicas distintas. La isoforma principal tiene una masa molecular de 23,4 kDa, está formada por 199 aminoácidos y contiene tres enlaces bisulfuro.1,6
Es producida y secretada mayoritariamente por células acidófilas lactotróficas del lóbulo anterior de la adenohipófisis. 1,7 Esta hormona pertenece a la familia de la hormona de crecimiento (GH) y del lactógeno placentario, cuyos miembros comparten propiedades estructurales, funcionales y de unión, así como el mismo ancestro genético.2
Además de esta prolactina monomérica de 23 kDa, se encuentran en la circulación otras dos formas principales de la proteína, conocidas como «PRL grande» y «PRL muy grande» (también conocida como macroprolactina).11
Estas son complejos de masa molecular grande (mayor de 100 kDa) compuestos por la PRL de 23 kDa y autoanticuerpos IgG o IgA (o por agregados poliméricos conformados por monómeros de PRL altamente glicosilados)(2), que pueden ser detectados por inmunoensayos de PRL.11 Sin embargo, estas formas de PRL tienen una actividad biológica mínima in vivo y no se conocen efectos patológicos asociados.11
Regulación de PRL
En ausencia de hormonas de una glándula blanco para hacer un control por retroalimentación con los lactotropos, la PRL regula su propia liberación actuando en los sistemas dopaminérgicos hipotalámicos. Este tipo de interacción se ha llamado «retroalimentación de asa corta» y es el principal responsable de mantener la homeostasis de la PRL.
Muchos estudios muestran que un aumento en PRL endógena o exógena resulta en una mayor actividad de las neuronas dopaminérgicas tuberoinfundibulares (TIDA), mientras una disminución de PRL circulante resultante de una hipofisectomía, la inmunoneutralización o el uso de agonistas dopaminérgicos bajan su actividad.
Las neuronas TIDA responden a los cambios agudos y crónicos de PRL con pocas excepciones como el embarazo, la lactancia y los prolactinomas, cuando las neuronas dopaminérgicas se vuelven refractarias a los niveles de PRL, permaneciendo, por lo tanto, hiperprolactinemia fisiológica o patológica.23
Los estrógenos son responsables por mayores niveles de PRL en el suero, la respuesta aumentada de la PRL a los secretagogos, y la mayor incidencia de prolactinomas en mujeres que en hombres. Los niveles circulantes de PRL no se aumentan (en humanos contrario a las ratas) durante el pico de LH, están básicamente estables durante el ciclo menstrual.24
La regulación es compleja e involucra factores inhibidores, así como estimuladores; están involucrados el sistema endocrino clásico y los sistemas paracrino (liberado localmente desde una célula para actuar sobre otra) y autocrino (que actúa sobre la célula de la cual proviene).
En esta compleja interacción participan diversos neurotransmisores, hormonas peptídicas y hormonas esteroides. El sistema de control endocrino es el que se comprende mejor.2)
A. Inhibidores de la PRL
- Dopamina: Tiene receptores de alta afinidad en los lactotropos. Aquí la dopamina inhibe la trascripción del gen de la PRL al disminuir la actividad de la adenilciclasa.
- GABA: Tiene actividad de factor inhibidor de PRL (PIF). Hay neuronas GABAérgicas en la eminencia media y receptores del GABA en el lóbulo anterior de la hipófisis.
- GAP: Péptido asociado a la hormona liberadora de gonadotropinas; es un polipéptido de 56 aminoácidos, el cual es la porción carboxilo-terminal de la proteína precursora de la GnRH. El GAP tiene actividad inhibidora de la PRL, así como estimuladora de las gonadotrofinas, y se halla en el hipotálamo y en la placenta humana. Figura 2.
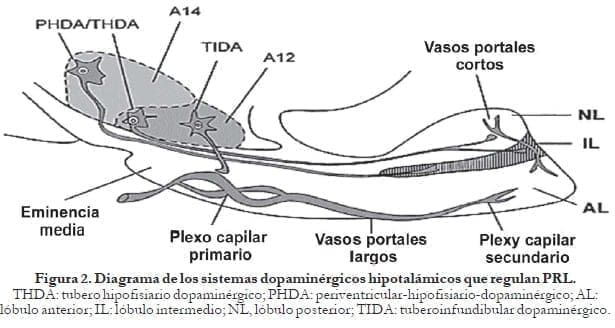
B. Liberadores de la PRL
Hay situaciones que pueden actuar directamente sobre la pituitaria, y bloquean la inhibición dopaminérgica, o indirectamente, por depleción de niveles hipotalámicos.
Estos incluyen la succión, el estrés, el sueño, la alimentación, el dolor y la hipoglicemia. Todos están mediados por centros cerebrales superiores. La succión es un estímulo potente que da como resultado un marcado aumento de la PRL sérica en 5 minutos. Los cambios de la secreción hipotalámica de la dopamina no son suficientes para mediar esta respuesta. Esto sugiere la presencia de uno o varios factores liberadores (PRF) que puede incluir varios péptidos:
- TRH: Hormona liberadora de la tirotropina responsable del aumento de la PRL en el hipotiroidismo primario. La proTRH, de 256 aminoácidos, tiene 2 péptidos que estimulan la producción de PRL (pFE22 y pSE14).
- VIP: Péptido intestinal vasoactivo.
- Oxitocina.
- Angiotensina II.
Se ha identificado, además, mediación de neurotransmisores en la liberación de la PRL: serotonina, opioides endógenos, histamina, neurotensina y sustancia P.
Algunas sustancias actúan en el control autocrino y paracrino de la liberación de la PRL, entre las cuales figuran glucocorticoides, vitamina D, progesterona y estrógenos. Este último es el principal regulador periférico de la secreción de PRL que estimula directamente su producción.
La acción de la histamina a través de los receptores H1 puede estimular la secreción de PRL, mientras que su acción a través de los receptores H2 puede inhibir la secreción de PRL, lo cual puede explicar la mayor secreción de PRL observada con el uso de fármacos antagonistas H2 (antagonista de los receptores H2 de la histamina).24 Figura 3.
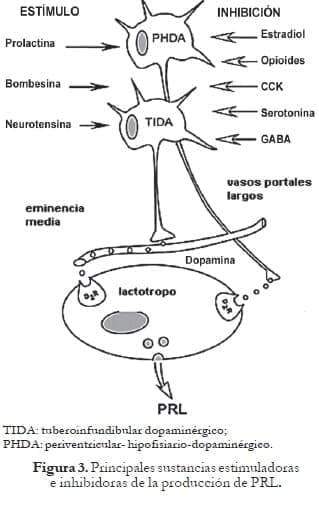
Relación PRL-gonadotropinas
La relación de hiperprolactinemia e hipogonadotropinemia es manifiesta en los síndromes de amenorrea-galactorrea. El descubrimiento de una prohormona precursora de GnRH llamada GAP (GnRH Adjunct Polipeptide) con importante actividad inhibitoria de prolactina ha generado la explicación para esa relación inversa entre las dos hormonas. Figura 4.
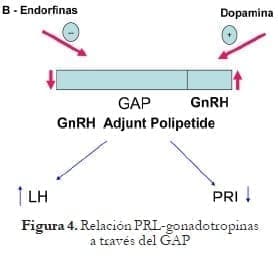
Macroprolactina
En la mayoría de los individuos, alrededor del 85% de la prolactina sérica es monomérica, pero en otros predomina la macroprolactina, lo cual se conoce como macroprolactinemia.
Esta también es conocida como hiperprolactinemia analítica y se ha reportado con una frecuencia del 4 al 40% entre los casos de HPRL, siendo en estos casos generalmente asintomática y no asociada con patología hipofisiaria habitualmente.2,3,11
Su presencia a nivel sérico puede generar dificultades en la clínica debido a una interpretación errónea de la prueba bioquímica, por lo que hoy en día se recomienda fraccionar el suero mediante precipitación con polietilenglicol (PEG) para aumentar la calidad de la medición de la proteína monomérica biológicamente activa (la de 23 kDa).11
Tras el proceso de centrifugación y precipitación con PEG, la obtención de PRL libre superior al 60% del total es sugestivo de hiperprolactinemia monomérica, mientras que una obtención menor del 40% es compatible con macroprolactinemia.2
La macroprolactinemia se asocia por lo general con actividad de gonadotropinas y función gonadal normal.3 (Lea También: Hiperprolactinemia e Infertilidad Femenina)
Funciones de la prolactina
Filogenéticamente, la prolactina ha sido llamada la hormona más antigua de la glándula hipófisis durante décadas, debido a la estimulación y el efecto que ejerce sobre las células de múltiples órganos,1 pero exhibe principalmente acción mamotrófica, lactogénica y lactopoyética.1,3
Es decir, su órgano diana son las glándulas mamarias, pues participa en la hipertrofia de estas y en el estímulo y mantenimiento de la lactancia en el puerperio.1,3
No se puede dejar de lado el papel que juega en el desarrollo del apego y el instinto materno (es la hormona responsable de estos) y la tolerancia inmunológica durante el embarazo.1,2 En niveles bajos o incluso fisiológicos, la PRL puede presentar un comportamiento «luteotrópico », ejerciendo un papel similar a las gonadotropinas, y en altas concentraciones, inhibiendo la secreción de gonadotropinas hipofisarias.1,2
Sin embargo, existen condiciones diferentes al embarazo, el parto y la lactancia que pueden influir en su secreción en otras circunstancias fisiológicas y patológicas, como una dieta de alto contenido proteico, estrés, fase MOR del sueño, ejercicio físico, hipoglicemia, relaciones sexuales, enfermedades inflamatorias, enfermedades sistémicas crónicas, cambios en hormonas tiroideas (en hipotiroidismo, las concentraciones de TSH y de PRL están elevadas) e ingesta de fármacos.1
La síntesis y la secreción de la PRL son mediadas por factores inhibitorios y de liberación.
La dopamina, el ácido gamma-aminobutírico (GABA) y la somatostatina ejercen el efecto inhibitorio, siendo la dopamina la protagonista en este último caso. Se ha sugerido el papel de varias hormonas y neuropéptidos como promotores de la liberación de PRL, incluyendo la hormona liberadora de tirotropina (TRH), opioides endógenos, oxitocina, serotonina, vasopresina, péptido intestinal vasoactivo (VIP por sus siglas en inglés), neurotensina, galanina y salsolinol.2 Sin embargo, la PRL se diferencia de otras hormonas hipofisiarias en que no se ha identificado un factor fisiológico liberador de la misma.2
Como se había mencionado antes, la PRL también puede ser secretada por los ovarios, las glándulas mamarias, el endometrio, la placenta, las células del sistema reticuloendotelial y en ocasiones por células neoplásicas.1,4 Esta PRL es estructuralmente idéntica a la PRL hipofisiaria y se une al mismo receptor.2 Su regulación es sitio-específica y es diferente de la de la PRL hipofisiaria.
El receptor de PRL es estructural y funcionalmente similar al receptor de la GH y es expresado en la hipófisis y en muchos otros tejidos como la glándula mamaria, endometrio, ovarios, corazón, pulmón, timo, bazo, hígado, páncreas, riñón, glándula suprarrenal, músculo esquelético, cerebro, piel y osteoblastos.2
Las acciones lactotróficas y reproductivas de la PRL han sido bien establecidas, y en los últimos años se ha logrado una mejor comprensión de los efectos de la PRL extrahipofisiaria en humanos.2
En las mujeres, como se mencionó inicialmente, juega un papel en el desarrollo folicular y en el mantenimiento del cuerpo lúteo. A nivel suprarrenal, estimula la secreción de andrógenos (incluyendo dehidroepiandrosterona (DHEA), cortisol y aldosterona. La PRL también ha sido implicada en la activación inducida por estrés del eje hipotálamo-hipófisissuprarrenal (HHS).2 Aumenta la secreción de corticotropina (ACTH), induce hipertrofia suprarrenal y el almacenamiento de ésteres de colesterol, así como estimula la producción de cortisol.2
Por otro lado, ejerce un efecto variable sobre el hueso durante el desarrollo y la reproducción: en el feto, promueve el crecimiento óseo y la mineralización, mientras que durante la gestación, contribuye a la resorción ósea acelerada en la materna para proporcionar micronutrientes al feto.2,12 Adicionalmente, tiene acción vasoconstrictora y se ha postulado su posible papel en la hipertensión y la preeclampsia.2,12
La hipersecreción de PRL suprime directamente la producción de la hormona liberadora de gonadotropinas (GnRH), lo cual lleva a una disminución en la amplitud y la frecuencia de los pulsos de la hormona luteinizante (LH).1,2,13
Sin embargo, la PRL también ejerce un efecto inhibitorio directamente sobre el ovario, de manera que disminuye la producción de estrógenos.1, 3 La síntesis de estrógenos y progesterona disminuye en células ováricas humanas cuando estas se exponen a concentraciones suprafisiológicas de PRL, resultando en anovulación e hipoestrogenismo.
1,3,13 Estos cambios generan irregularidad menstrual (amenorrea u oligomenorrea, a veces flujos abundantes, y ciclos menstruales cortos, entre otras alteraciones), hirsutismo, acné, infertilidad, disminución del deseo sexual resequedad vaginal y dispareunia poscoital, así como alteraciones en la fase de excitación y de orgasmo.1,2,13 La galactorrea, espontánea o provocada, es una manifestación común en mujeres en edad fértil con HPRL, hasta en el 90% de casos, y puede ocurrir en presencia o ausencia de disfunción menstrual.1,2,13
Ante la presencia de un prolactinoma como causa de la HPRL, puede haber además cefalea y alteraciones visuales (diplopía y amaurosis, entre otras), sobre todo en el contexto de macroprolactinomas (diámetro mayor de 1 cm) por su efecto compresivo.1,2,13
En ratas con hipogonadismo, se ha evidenciado que la secreción de GnRH a nivel del hipotálamo aumenta el número de receptores de GnRH a nivel de la hipófisis. Por el contrario, las ratas con hipogonadismo e hiperprolactinemia tienen menos receptores hipofisiarios para GnRH, una respuesta disminuida del receptor de GnRH a la GnRH y una caída de la frecuencia y amplitud de los pulsos de la hormona luteinizante, factores que revierten tras la corrección de la HPRL.13
El hipoestrogenismo provoca indirectamente una alteración en la regulación del metabolismo de los lípidos, osteoporosis (varios estudios han demostrado que mujeres y hombres con HPRL e hipogonadismo tienen una densidad mineral ósea disminuida y un riesgo aumentado de fracturas vertebrales),4 cambios atróficos en el sistema genitourinario, aumento de la secreción de ACTH y andrógenos suprarrenales.
Así mismo, pueden alterarse funciones pancreáticas como la secreción de insulina, y disminuye la síntesis de globulina transportadora de hormonas sexuales a nivel hepático.1,2
En resumen, se ha considerado que existe una asociación importante entre HPRL y mortalidad por cualquier causa así como mortalidad por enfermedad cardiovascular.14
Sin embargo, la literatura resulta contradictoria respecto a la afirmación anterior, pues hay autores que, por el contrario, reportan que la HPRL relacionada con tumores hipofisiarios no se asocia con morbilidad aumentada ni mortalidad por cualquier causa.4
Particularmente, reportan que no hubo riesgo aumentado de diabetes, enfermedad cardiovascular, cáncer en general ni cáncer de mama, resultados que coincidieron con aquellos obtenidos por el estudio del corazón Framingham.4
Autores
* MARÍA ALEJANDRA YÉPEZ GALINDO. Residente de cuarto año de Ginecología y Obstetricia. Universidad Libre, Seccional Cali.
**GUSTAVO GÓMEZ TABARES. Ginecólogo endocrinólogo, Infertilidad, Laparoscopia; profesor titular de la Universidad del Valle y la Universidad Libre; Unidad de Medicina Reproductiva, Clínica Imbanaco, Quirón Salud.