José Saulo Torres R. MD.*
Resumen
Se analizan conceptos de ´como interpretar la citología vaginal según el Sistema Bethesda, importancia del virus del papiloma humano como posible factor desencadenante de los procesos displásicos, el compromiso humano que debe existir desde la toma citológica hasta la decisión final de manejo, esto último según protocolo del Hospital Universitario Evaristo García de la ciudad de Cali.
Palabras Claves: Lesiones Intraepiteliales Cervicales (L.I.C.) – Sistema Bethesda – Virus del Papiloma Humano, Protocolo de manejo
Summary
This articles privides guidelines for interpreting vaginal cytologies using the bethesda System. It also discusses the importance of both human papilomas as a possible unchaining factor of displasic processes and the human commitment needed from taking the cytological sample to making the final treatment decision. Following the protocol of Evaristo García University Hospital in Cali.
Key words: Cervical Intraepithelial Lessions (C.I.L.) – Bethesda System – Human Papiloma Virus – Treatment Protocol.
Lesión Escamosa Intraepitelial Cervical: (L.E.I.C)
Concepto: La lesión escamosa intraepitelial en el cuello uterino varía de un crecimiento anormal mínimo (bajo grado), progresando en espesor hasta llegar a la capa más superficial del epitelio (alto grado). La actividad mitótica está confinada a la capa basal y a las capas celulares por encima de ella sin compromiso del estroma. Coilocitos, discariocitos son más frecuentes en lesiones de bajo grado (16).
Bajo Grado: Significa Lesiones intraepiteliales que afectan sólo el tercio inferior del grosor total del epitelio y las alteraciones celulares asociadas al Virus del Papiloma Humano.
Alto Grado: Las alteraciones afectan desde los dos tercios hasta todo el espesor del epitelio.
Las anormalidades que fundamentalmente comprometen el epitelio son:
1. Presencia de Coilocitos y Disqueratocitos.
2. Pérdida de estratificación y polaridad.
3. Ausencia de diferenciación y maduración.
4. Alteración en la relación Núcleo-Citoplasma.
5. Alteraciones nucleares ( Hipercromatismo, y distribución anormal de la cromatina.)
6. Aumento de mitosis
Epidemiología: Los factores que se han encontrado asociados con la existencia de lesiones premalignas son:
1. Inicio de relaciones sexuales a edad temprana: Se acepta actualmente como factor de riesgo elevado de padecer lesiones premalignas y cáncer de cuello uterino el inicio de relaciones sexuales antes de los 20 años.
2. Primer embarazo a edad temprana. Aparentemente debido a inmadurez de las células del cuello, durante el trauma obstétrico
3. Promiscuidad sexual de alguno de los cónyuges: El individuo promiscuo está más expuesto a adquirir infecciones de transmisión sexual las que a su vez parecen jugar papel importante en la transformación neoplásica cervical.
4. Infecciones por virus del Papiloma Humano: Existe una asociación causal entre el desarrollo de lesiones intraepiteliales y el Virus del Papiloma Humano.
5. Cigarrillo: existen elevadas concentraciones de Nicotina en moco cervical y disminución de células de Langerhans en tejido cervical en pacientes fumadoras. El antecedente de tabaquismo incrementa el riesgo de infección por V.P.H.
6. lngesta de anticonceptivos orales. En algunos estudios epidemiológicos se ha encontrado un riesgo mayor en quienes toman anticonceptivos orales, al controlar por la presencia del Virus del Papiloma Humano.
Edad: La prevalencia de las lesiones intraepiteliales ocurren en el grupo de edad entre los 20-40 años con un pico de Incidencia a los 30 años de edad.
El tiempo para que una lesión preinvasiva pase a invasiva se ha calculado entre 3 a 10 años.
Etiología: Es desconocida la causa etiológica del cáncer cervical. Parece existir una asociación entre un agente infeccioso transmitido sexualmente que actúa sobre el epitelio metaplásico o zona de transformación, produciendo alteración en la madurez celular del epitelio.
La mujer desde su vida intrauterina presenta constantes modificaciones del epitelio cérvico-vaginal el cual está conformado por epitelio escamoso y epitelio cilíndrico o columnar; el sitio de unión de estos epitelios es conocida como Unión Escamo-Columnar o Escamo-Cilíndrica. Es en esta unión y en la zona de transformación donde presumiblemente actúan los agentes con potencial carcinogénico dando origen a la metaplasia atípica, Lesiones Intraepiteliales Cervicales y carcinomas invasivos.
Antes del quinto mes gestacional, la vagina y el exocervix son cubiertos por epitelio columnar, después de lo cual el epitelio escamoso reemplaza al epitelio columnar en vagina y exocervix. Durante la adolescencia como en el primer embarazo el epitelio escamoso reemplaza al epitelio columnar vía metaplasia formándose una nueva unión Escamo-Columnar, progresivamente más próxima al orificio cervical externo. Esta nueva Unión Escamocolumnar es llamada zona de transformación, la que es más susceptible al efecto carcinogénico de los agentes transmitidos sexualmente. Entre estos agentes se han involucrado al Virus del Papiloma Humano (V.P.H.), tricomonas, clamidia, y D.N.A del espermatozoide.
Las observaciones de varios estudios sugieren que después de la infección por virus del Papiloma Humano (VPH) muchos individuos no desarrollan signos clínicos o síntomas, pero guardan el virus por períodos variables. Los cambios morfológicos que ocurren en las células epiteliales durante la infección por el VPH se relacionan con neoplasia intraepitelial cervical de bajo grado (CIN-1). Muchas de estas lesiones regresarán espontáneamente pero una pequeña proporción progresará a CIN de alto grado (CIN II-III) y eventualmente a cáncer invasivo. Se ha estimado que se requieren 4 a 5 años para la transición de CIN-1 a ClNlll, 9 a 10 años de CIN-lll a carcinoma invasivo subclínico y 4 a 5 años de invasivo subclínico a cáncer invasivo sintomático (2). Los estimados anteriores se basan en datos de estudios de seguimiento y de registros selectos y programas de tamizaje. La existencia de un continuum morfológico de cambios progresivos y consecutivos llevando hasta cáncer cervical invasivo ha cambiado recientemente. Se ha propuesto que CIN-1 y CIN-lll pueden ser dos entidades separadas y que solamente CIN II-III son precursores reales de cáncer cervical (3).
Virus del Papiloma Humano (V.P.H.): Las infecciones del V.P.H son clasificadas en:
• Clínica: La infección se evidencia a simple vista, como el condiloma exofítico
• Subclínica: Evidenciada a través del colposcopio.
• Latente: Detectado sólo por técnicas de hibridación molecular. (4)
Asociación entre VPH y neoplasia cervical: Se han caracterizado más de 75 tipos de VPH y cerca de 30 de ellos se sabe que infectan el cuello uterino. Algunos de los tipos de VPH que infectan el cérvix (tipos asociados a cáncer o de alto riesgo) se aceptan corrientemente como el factor etiológico central para cáncer invasivo y sus lesiones precursoras (5). Puesto que las intervenciones deben ser tipo específicas es importante considerar la prevalencia de los tipos de VPH relevantes. Un estudio internacional de tipos de VPH en cáncer cervical en 22 países alrededor del mundo reveló que el VPH 16 es responsable del 54% de los cánceres asociados a tipos de VPH, seguido del VPH 18 (15%), VPH 45 (9%) y VPH 31(6%) (6). Así, los 4 tipos de VPH anteriores son responsables del 84% de todos los cánceres asociados a tipos de VPH y las intervenciones contra el VPH 16 deberán tener impacto considerables en la reducción del cáncer cervical.
Las evidencias epidemiológicas de la asociación entre el VPH y la neoplasia cervical incluyen un conjunto impresionante y ampliamente consistente de series de casos, estudios de casos y controles y algunos estudios de cohortes que han sido revisados recientemente (7).
Los datos epidemiológicos disponibles indican que la asociación entre ciertos tipos de VPH y cáncer cervical cumple completamente con los criterios aceptados de causalidad propuestos por Sir Bradford Hill:
1. Es muy fuerte, con OR superiores a 15 y todos los estudios de casos y controles metodológicamente sólidos utilizaron métodos confiables para la detección del ADN del VPH. La fuerza de la asociación descarta la posibilidad de que se pueda explicar por sesgo, azar o confusión.
ll. Es consistente, asociaciones igualmente fuertes se han encontrado tanto en países de alto como de bajo riesgo para cáncer cervical.
III. Hay una relación dosis-respuesta entre la carga viral y el riesgo de desarrollar neoplasia cervical.
IV. Los resultados de unos pocos estudios de cohorte indican que la infección con ciertos tipos de VPH precede el desarrollo de lesiones CIN II-III.
V. La asociación es específica para ciertos tipos de VPH denominados tipos de VPH de alto riesgo. Además de los 30 tipos de VPH que infectan el cérvix uterino, el VPH 16 aporta la proporción mayor de cáncer cervical, seguido del VPH 18.
VI. La evidencia epidemiológica está apoyada por un gran número de investigaciones de laboratorio que indican un potencial carcinogénico de los tipos de VPH implicados en la neoplasia cervical.
Estas conclusiones han sido apoyadas por un grupo multidisciplinario internacional reunido recientemente en Lyon para evaluar la carcinogenicidad del VPH (5).
En humanos la infección ocurre en piel, mucosas, conjuntivas, cavidad oral, laringe, árbol traqueobronquial, esófago, vejiga, ano y tracto genital.
En la actualidad han sido aislados alrededor de 30 tipos de V.P.H capaces de infectar el tracto ano-genital; basados en su comportamiento biológico se han dividido en serotipos de:
• Bajo riesgo (6, 11, 40, 42, 43, 44, 57).
• Alto riesgo (16, 18, 30, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59, 66).
El contagio de la infección genital por H.P.V. se produce mediante el contacto sexual directo o indirecto, por fragmentos de tejido infectado que penetra a través de microabrasiones. Se admite la transmisión mediante fómites como son instrumentos de uso ginecológico o guantes inadecuadamente esterilizados.
El virus penetra en las células del estrato basal expuestas a una serie de microtraumatismos, los viriones pierden su involucro proteico y el genoma viral llega al núcleo de la célula donde se establece en forma episómica. El período de incubación varía entre tres semanas y ocho meses para condiloma, alrededor del 70% de compañeros sexuales de mujeres con H.P.V y neoplasia intraepitelial son diagnosticados como subclínica. El semen y la uretra actúan como reservorio del virus (8). La inmunidad celular desempeña un papel fundamental en la defensa contra la infección por H.P.V. El primer encuentro entre el virus y el sistema inmunológico se produce en el epitelio. La primera línea de defensa del huésped son las células de Langerhans intraepiteliales que desempeñan un papel en la activación de los linfocitos T.
Coilocitosis: El diagnóstico de infección por virus del papiloma en citologías cervico-uterinas sólo debe ser emitido cuando se observan coilocitos o disqueratocitos. El cambio citológico diagnóstico del V.P.H es la célula coilocítica, cuyas características morfológicas completas se consideran patognomónicas de la infección. Los coilocitos son células superficiales o intermedias con un gran espacio vacío irregular rodeando completamente el núcleo.
Características de Coilocitos:
1. Halo Perinuclear amplio irregular.
2. Condensación citoplasmática periférica.
3. Agrandamiento, hipercromasia y angulaciones nucleares con o sin multinucleación. El segundo tipo de célula asociado a la infección son los disqueratocitos, pequeñas células queratinizantes con núcleos picnóticos agrupadas en nidos o sabanas.
Características de los Disqueratocitos:
1 . Acúmulos celulares.
2. Núcleos picnoticos.
3. Citoplasma acidofilo intenso.
El tercer tipo de célula asociado es la parabasal. Difícil de diferenciar de células provenientes de lesiones de alto grado, su apariencia es más de tipo degenerativo que neoplásico. Son características morfológicas:
1. Citoplasma denso sucio.
2. Halo perinuclear pequeño.
3. Núcleos atípicos sin angulaciones (9)
Frotis citológico:
La citología cérvico-vaginal es un test de screening diseñado para identificar pacientes quienes podrían tener lesiones premalignas y malignas ocultas que requieren evaluación cuidadosa posterior (10).
En 1945 la Sociedad Americana de Cáncer apoyó el uso de la citología vaginal como un examen preventivo efectivo para el Cáncer Cervical. El Doctor Charles Cameron, quien fue el primer director científico de la sociedad y amigo cercano del Doctor George N. Papanicolaou impulsó dicha iniciativa. lnicialmente la toma se realizaba del fondo vaginal lo que hacia el examen microscópico tedioso, consumía tiempo, y requería mayor cuidado en el screening como evidencia de lesiones premalignas. Un seguidor del Dr. Papanicolaou, Ernest Ayre, propuso la toma de muestras con bajalenguas directamente del cérvix, tomándolo bajo control visual mejorando dramáticamente la calidad de la muestra facilitando así su lectura e interpretación (11).
La significante caída de la tasa de cáncer invasivo del cuello uterino en los Países donde el Screening citológico fue aplicado en gran escala, es un testimonio de la eficacia del extendido cervical (10).
La citología tiene todas las cualidades necesarias de una buena técnica de screening. Es fácil de realizar, aceptado por las pacientes, económico y certero. Sin embargo en ocasiones es pobremente entendido y severamente cuestionado (12).
Frecuencia de la citología vaginal: La citología vaginal de acuerdo con la Sociedad Americana de Cáncer (Nov. 1988) se recomienda sea tomada anualmente a “Todas las mujeres que sean o hayan sido activas sexualmente o que hayan alcanzado los 18 años de edad, conjunto con un examen pélvico. Después que una mujer haya tenido tres o mas exámenes anuales consecutivos normales satisfactorios, el Pap puede ser hecho menos frecuente a discreción de su médico mas aún si es catalogada de bajo riesgo”.
Son consideradas pacientes de alto riesgo para desarrollar lesiones intraepiteliales y cáncer cervical todas aquellas mujeres que iniciaron relaciones sexuales antes de los 18 años, tuvieron múltiples compañeros sexuales, su compañero sexual es promiscuo, antecedente de infección por virus del papiloma humano y tabaquismo.
Son de bajo riesgo las célibes y cuando ambos compañeros son monógamos.
Las pacientes histerectomizadas por patología benigna son consideradas de riesgo bajo (13).
Pasos para una adecuada interpretación del informe citológico: Existen múltiples pasos para que una citología conduzca a un exitoso manejo:
1. Toma Adecuada: Debe tomarse muestras celulares de la unión escamocolumnar, de la zona de transformación y del canal endocervical.
2. Adecuada Fijación: Debe fijarse en el instante de haber terminado la toma citológica.
3. Practicar la Interconsulta: Se debe enviar un informe como si se tratara de una interconsulta médica.
4. Citotecnólogos: Se debe contar con un grupo de citotecnólogos calificados, sin sobrecargas de lecturas, y con un plan de educación médica continuada.
5. Informe Citológico: Que proporcione tanto al clínico como al patólogo una efectiva comunicación.
6. Conocimientos Clínicos Suficientes: Los que permiten una adecuada interpretación citológica y a su vez una conducta adecuada.
Si se es fiel a estos pasos los falsos negativos que podrían ser del orden del 50% pueden disminuirse a un 5% (14).
Toma Adecuada
La eficacia de la citología en los screening es dependiente de la calidad de la muestra. La citología ha sido informada como técnicamente inadecuada en el 12.3%, y los hallazgos podrían subestimar las lesiones intraepiteliales en el 17.5% de los casos. Se ha estimado que entre el 15 al 25% de los pacientes con lesiones intraepiteliales tienen resultados como normales. Tales resultados pueden ser minimizados aplicando una técnica adecuada para obtener la muestra citológica (10).
La zona de transformación, la cual está entre el epitelio escamoso del exocervix y el epitelio columnar del endocervix es el sitio mas común para el desarrollo de lesiones intraepiteliales. Los resultados falsos negativos podrían deberse a la muestra inadecuada de la zona de transformación, la cual frecuentemente progresa en el canal endocervical en la mujer post-menopáusica. Siempre debe tomarse muestra del canal endocervical con cepillo lo que se complementa con la espátula para el exocervix (15). En un estudio practicado por el Doctor Carlos Cuello enfatiza lo anterior cuando demuestra como citologías tomadas por personal entrenado frente a personal inexperto la relación de citologías no satisfactorias es de 1/100 frente a 40/100 (Cuadro 1) señalando cuales son las causas más frecuentes de muestras no satisfactorias (Cuadro 2).

El Dr. Cuello presenta la localización del Cáncer Cervical in situ en 100 especímenes de histerectomías practicadas en el Hospital Universitario del Valle donde no encontró en ningún espécimen compromiso aislado del exocérvix escamoso, 18% compromiso de la Unión Escamo-Columnar, 64% en la zona de transformación, 8% en endocérvix, 10% compromiso del exocervix+unión escamo-columnar y endocervix (cuadro 3). Esto demuestra claramente como debe dirigirse la toma de la citología (16).
Fijación de la citología: Las fijaciones más comunes son las de alcohol-éter consiste en la introducción del portaobjeto en una solución de alcohol etílico de 96° y éter a partes iguales, que tiene un pH de 6.8 a 7, por eso debe cambiarse la solución con cierta frecuencia, pues la evaporación del éter forma ácido acético capaz de acidificar el fijador, lo que cambiaría la capacidad tintorial de las células. El tiempo de fijación es de 15 minutos como mínimo y 6 días como máximo. También pueden fijarse sólo con alcohol etílico al 96°.
Puede usarse también como fijador la nebulización del frotis con una mezcla de alcohol isopropilo y una materia plástica (Polietilenglicol). Para una buena fijación se debe colocar el nebulizador frente al portaobjetos a una distancia de 20 – 30 cm para evitar barrer las células. Se deja secar al aire unos siete minutos antes de transportar o colorear (17).
Informe anexo a la citología: El clínico debe ser consciente que la citología debe ir acompañada de un resumen de los datos más relevantes de la paciente, pues lo que se está pidiendo es una interconsulta médica para que a su vez el citopatólogo pueda realizar una evaluación citológica adecuada (14).
Citotecnólogos con Experiencia: La muestra debe ser adecuadamente procesada. Su trabajo es examinar la totalidad de la placa e identificar cualquier célula anormal. Este trabajo es difícil y tedioso cuando uno considera que hay 50.000 – 300.000 células por placa y cada célula debe ser categorizada. Más de 100 placas pueden ser tamizadas cada día.
Es probable que muchos de los falsos negativos sea debido a la monotonía y la fatiga de este trabajo mas que a la falta de experiencia.
Toda citología detectada anormal debe ser revisada por un cito-patólogo (11-12).
Reporte Citológico: Uno de los aspectos más críticos en la valoración de la citología es la comunicación de los hallazgos del citopatólogo y el clínico la que se debe desarrollar en términos no ambiguos con una buena relevancia clínica. Esto es lo que ha originado a través del tiempo las distintas modificaciones citológicas desde Papanicolaou hasta llegar al sistema Bethesda de diciembre de 1988 siendo reformado en el 91 (14,18).
Haciendo un recuento histórico vemos como en 1910 Rubin introdujo la denominación Carcinoma in Situ, hasta Broders, en 1932 no se generalizó este término. En el año 1961 durante el Primer Congreso Internacional de Viena, se adoptó la definición de Ca in Situ de cérvix la que posteriormente, con los términos de displasia, (término acuñado por Reagan en 1953) y definido en el congreso como “Todo epitelio escamoso situado sobre la superficie o en las glándulas, que muestra alteraciones en la diferenciación sin alcanzar el grado de perturbación que caracteriza al carcinoma in Situ”, fueron explicados en dos volúmenes publicados por la O. M.S (19).
Koss en 1963 considera que la displasia grave y el Ca in Situ debían superponerse y Richard en 1966 lanza el concepto de Neoplasia Intraepitelial Cervical (N.I.C:) eliminando así el concepto separado de displasia grave y Ca in Situ.
En 1972 Nyirjesy llama la atención acerca de los frotis Pap, 11 atípicos persistentes podían corresponder no sólo a un proceso de cervicitis (22.8%), sino a procesos Displásicos (45.6%), Carcinomas in Situ (24.6%), Cáncer cervical invasivo 3.5%. Adeno Carcinoma Endometrial 3.5% (20).
Hacia finales de los 70 Meissels y Elbe, observaron que la mayoría de las infecciones ginecológicas por virus del papiloma humano son subclínicas y que se reconocen por citologías anormales con la presencia de koilocitosis, disqueratocitos, anfofilia, hipercromasia y binudeación; y que su distinción con los procesos displásicos se superponían. Ya en 1956 Koss había descrito el efecto citopático viral (21, 11).
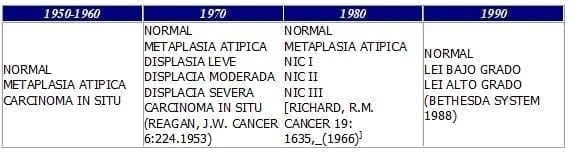
Sistema Bethesda
En ese intento por unificar criterios sobre terminología en citología cervical, el National Cáncer Institute estableció una reunión de trabajo en Bethesda, Maryland, en 1988. El segundo taller se celebró en abril de 1991, a esa nomenclatura se le designa usualmente ” Sistema de Bethesda”.
En cuanto al sistema Bethesda para el reporte diagnóstico citológico se reconoce que:
1. Proporciona una efectiva comunicación entre el citólogo y el médico.
2. Facilita la correlación Citológica-Histopatológica.
3. Facilita la investigación epidemiológica, biológica y patológica de la enfermedad cervical.
4. Proporciona datos para análisis estadísticos y comparaciones nacionales e internacionales (14).
El sistema Bethesda introdujo nuevos términos como fueron:
Lesiones Intraepiteliales Escamosas de Bajo Grado que abarca lesiones cervicales del tipo displasia leve o N.I.C I e infección por virus del papiloma humano.
Lesiones Intraepiteliales Escamosas de Alto Grado. Que corresponden a displasia moderada, severa y carcinoma in Situ (CIS), como, N.I.C II, N.I.C III.
El sistema Bethesda limita el uso del término “atipia celulares” a aquellos casos en los cuales los hallazgos citológicos son de significancia indeterminada. “Atipia” no debe ser usado como un diagnóstico para definir cambios celulares inflamatorios, preneoplásicos, o neoplásicos. Para ayudar al clínico en un reporte que incluya la palabra “atípico” debe hacer una recomendación para una evaluación adicional que puede ayudar a determinar la significancia de las células atípicas. Por ejemplo “Células escamosas atípicas de significancia no determinada (Ascus o Agus), asociadas con atrofia la recomendación puede ser “sugerimos administrar estrógenos y repetir la citología (21).
Conocimientos Clínicos Suficientes:
Toda paciente con citología cervico-vaginal anormal exige del clínico un cuidadoso examen ginecológico, encaminado a precisar el diagnóstico. En caso de confirmar una lesión macroscópica “inequívoca” de tumor, el paso a seguir es la biopsia; si por el contrario el aspecto del cuello es sano se practicará: colposcopia y biopsia dirigida.
Si la colposcopia es satisfactoria, es decir se observa bien la unión escamocolumnar, la lesión no penetra en el canal, no hay estenosis del orificio cervical externo, el cérvix es regular y no existe ni atrofia ni inflamación severa; se toma la biopsia muestreando el sitio de mayor representatividad de acuerdo con los criterios colposcópicos para estudio histológico, además del legrado endocervical; si no es satisfactoria por inflamación o atrofia se prescribe tratamiento médico indicado y se cita en un futuro próximo, si corresponde a otras causas se realiza cono diagnóstico.
Son considerados criterios colposcópicos de anormalidad después de aplicar el ácido acético:
1. Epitelio acetoblanco: se produce por deshidratación de las células, causando un incremento en el reflejo de la luz de las áreas de densidad nuclear aumentada-corresponde a L.I.C.
2. Patrones vasculares: referidos a punteado y mosaico. Estos son causados por capilares vistos al final, como señales, tal como llegan mas apretados al epitelio de superficie.
3. El mosaico es causado por capilares alineados paralelamente a la superficie del epitelio. Entre más blanca es la lesión más avanzada es la L.I.C. Los colposcopistas pueden biopsiar la lesión y clasificarla acertadamente en un 95 – 98%.
Si por el contrario la paciente presenta criterios colposcópicos de invasividad, o la lesión se introduce dentro del canal no visualizándose la parte más cefálica; o no se visualiza la unión escamo-columnar recomendamos el cono lletz de tipo diagnóstico que en algunos casos servirá como terapéutico.
Todos los informes con diagnósticos de adeno -ca in Situ, legrado endocervical positivo, microinvasión o falta de correlación entre la citología, colposcopia y biopsia, donde la primera surgiera mayor lesión amerita cono diagnóstico.
Cuando el informe histológico es de una lesión de alto grado, con una citología concordante, se procederá a practicar cono con intención terapéutica; (bordes de sección libres de enfermedad) la cual es una opción de manejo a cualquier edad o paridad.
Los casos informados por Cono como microinvasión, ( compromiso del estroma menor de 3 mm en profundidad y hasta 7 mm en extensión), con bordes libres de lesión, y a su vez la paciente desee conservar su útero y sea fácil su seguimiento el cono es una medida terapéutica adecuada.
En caso que la paciente tenga paridad satisfecha, acepte la histerectomía, o sea incierto su seguimiento, se optará por la histerectomía ampliada, se propondrá anexectomía bilateral como profilaxis oncológica si sobrepasa los 45 años, la cual se realizará siempre que la paciente apruebe el procedimiento.
Aquellas pacientes con lesiones intraepiteliales o microinvasivas, menores de 3 mm, con bordes de resección comprometidos; podrían manejarse con reconización cuando desean conservar el útero si es técnicamente posible.
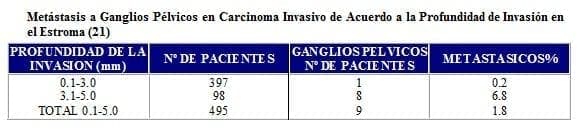
Las pacientes con infiltración mayor de 3 mm, se manejarán como verdaderos tumores invasivos, por su compromiso metastásico ganglionar pélvico y para-aórtico proponiéndose cirugía oncológica especializada vs radioterapia radical dependiendo del caso en particular.
Ayuda a comprender los anteriores conceptos el conocer el porcentaje de compromiso ganglionar en lesiones invasivas tempranas, la cual se estipula de la siguiente manera:
Seguimiento: El seguimiento se hará con citología vaginal, examen físico cuidadoso con énfasis en cúpula vaginal y parametrios con una periodicidad de cada tres meses el primer año, cada 4 meses el segundo año, cada seis meses el tercero cuarto y quinto año, se solicitará Radiografía de tórax cada seis meses los dos primeros años y posteriormente en forma anual (22-23).
Lesiones Intraepiteliales Cervicales asociadas a embarazos: El cáncer cervical es la malignidad genital más comúnmente asociada con el embarazo, reportan un promedio de un embarazo complicando cada 34 casos de cáncer invasivo (2.9%) lo cual contrasta con que por cada 220.2 embarazos se acompaña de un carcinoma cervical (0.45 por 1000) (24).
Las pacientes con citología compatibles con L.I.C durante el embarazo deben practicársele colposcopia y biopsia dirigida, una vez se confirme el diagnóstico de L.I.C por estudio histológico deberá seguirse con colposcopia cada 6-8 semanas, hasta el final del embarazo. Se repetirá la biopsia sólo en caso de encontrar en un control posterior hallazgos colposcópicos sospechosos de invasión, el Cono sólo se realizará para descartar invasión. (Cono Diagnóstico); el cono con fines terapéuticos no está indicado en embarazo. Seis semanas post-parto será reexaminada la paciente para definir conducta.
La vía de evacuación al momento del parto la define el criterio puramente obstétrico.
Bibliografía
1. Jo Ann Benda. Seminars in Oncology 1994; 21: 3.
2. Pontén J., Adami HO., Bergström R., Dillner J., Friberg LG., Gustafsson L., Miller AB., Parkin DM., Sparén P., & Trichopoulos D. Strategies for global control of cervical cancer. lnt. J. Cancer, 1995; 60: 1-26.
3. Kiviat NB & Koutsky L. Do our current cervical cancer control strategies still make sense? J. Natl Cancer Inst., 1996; 88: 317-318.
4. Luna JG. Curso de Patología del Tracto Genital Inferior. H.U.V. 1995; 28.
5. Cannistra SA. & Nilofl JM. The N Engl J of Med. 1996; 1031.
6. IARC. Monographs on the Evaluation of the Carcinogenic Risks to Humans, Human papillomaviruses, Vol 64, International Agency for Research on Cancer, Lyon Koss L. G. (1993) Cancer Supplement. 1995; 71: 1406.
7. Bosch FX., Manos MM., Muñoz N., Sherman M., Jansen AM., Peto J., Schiflman MH., Moreno V., Kurman R., Shah KV & The IBSCC Study Group. Prevalence of human papillomavirus in cervical cancer: a worlwide perspective. J. Natl Cancer Inst., 1995; 87: 796-802.
8. Muñoz N. & Bosch FX. Current views on the epidemiology of HPV and cervical cancer. In: Lacey, C. ed., Papillomavirus Reviews: Current Research on Papillomaviruses. Leeds, Leeds University Press, 1996; 227-237.
9. Schneider A. J Obstetrics and Ginecology 1994; 14: 82-86.
10. Carrascal E. Curso de Patología del Tracto Genital Inferior. H.U.V. 1995; 26.
11. Koss LG. Cancer Supplement. 1993; 71: 1406.
12. Pap Smear or Pap Test for patients, Internet http:1www erinet.com/fnadoc/pap.
13. Hempling RE. Preinvasive Lesions of the Cervix: Diagnosis and management Steven Piver. Handbook of Gynecologic-Oncology.
14. El sistema de Bethesda de 1988 para el repone de la citología diagnostica de cervix y vagina. Human Patology, 1990: 21 N° 7.
15. De Palo Giuseppe. MD. Colposcopia y patología del tracto genital inferior. 1996; 91.
16. Cuello C. Curso de Patología del Tracto Genital Inferior. Informe citológico y patológico de lesiones intraepiteliales cervico-uterinos. Clasificación actual. Curso de Patología del Tracto Genital Inferior. H.U.V: 1996; 16-17.
17. Fernández C., López L. Citopatología Ginecológica y Mamaria. Pág 15.
18. Jones HW. lmpact of the Bethesda System. Cancer Supplement 1995; 76: 10.
19. M. Puig-Tintore. Oncología Ginecológica. González Merlo, 1995; 87.
20. Rodríguez A. Recuento Histórico de la patología del tracto genital inferior. 1996. lnédito.
21. Kurman RJ. y Col. Del Pap al Bethesda. Las explicaciones para una nueva clasificación de citología cervical. Obst. y Ginecología 1991; 77: 779-780.
22. Torres JS. Manejo de la citología cervical anormal en el Hospital Universitario del Valle. Curso de Patología del Tracto Genital Inferior. HUV: 1996; 43-44.
23. Grupo de Oncología Ginecológica Hospital Universitario del Valle. Protocolos de Manejo en Patología Gineco – Oncológica. 1995; 8-10.
* Ginecólogo-Oncólogo. Hospital Universitario del Valle.

Buenos días un trabajo excelso e impecable que disfrute de principio a fin, nutrido en información y detalles como sugerencia en mi opinión debe incluirse la tipificación del VPH para determinar si es de Bajo o Alto Riesgo, eso nos va enfocar en las posibles terapeuticas, el estudio de la citología debe ser descriptivo ya que el Sistema Bethesda su eficacia depende de la experiencia del citotecnologo y el especialista esta en la capacidad de leer en forma descriptiva los resultados de la citología, hace mas de 25 años que el VPH esta en estudio y ya no es considerado un enfermedad netamente de transmicion sexual, se han reportado casos de pacientes núbiles con NIC I-II, por otro lado estudios han reportado que la nicotina causa mutacion de las células cervicales, otra herramienta importante es el Video Colposcopio la tecnología con sus filtros de luz azul y roja y el entrenamiento adecuado nos da una herramienta clínica que no da ningún otro estudio y esto tiene que ver porque al tomar las citologías el mecanismo de defensa del cérvix es el de descamar todos los días sus células y muchos resultados de citología no se correlacionan con lo encontrado en la Video Colposcopia, sin mas que agregar felicitaciones por su trabajo