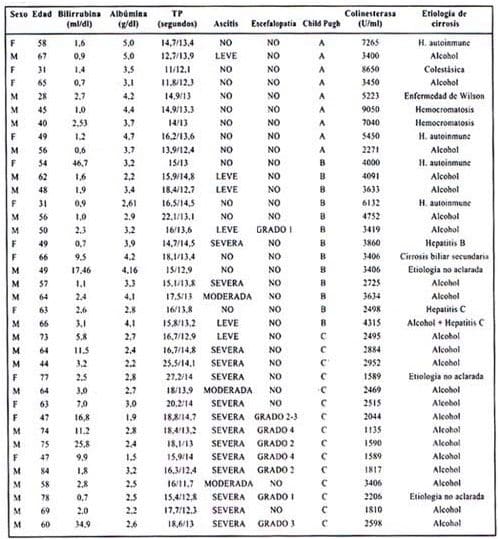
Resultados con diagnóstico de cirrosis hepática
Se estudiaron 37 pacientes con diagnóstico de cirrosis hepática, con un promedio de edad de 57,5 años (rango 28-84 años), de los cuales 13 (35,13%) eran mujeres y 24 (64,86%) hombres.
TABLA 1. Clasificación de Child-Pugh
| 1 punto | 2 puntos | 3 puntos | |
| Bilirrubina (mg/dl) | menor de 2 | 2 a 3 | mayor de 3 |
| Albúmina (g/dl) | mayor de 3,5 | 2,8 a 3,5 | menor de 2,8 |
| Tiempo de protombina | |||
| (segundos) | 1 a 3 seg. | 4 a 6 seg. | mayor de 6 seg. |
| Ascitis | No | Leve | Moderada a Severa |
| Encefalopatía | No | Grado 1-2 | Grado 3-4 |
Método estadístico: la información se presenta en tablas; se emplearon métodos de validez epidemiológica.
Los pacientes se distribuyeron en tres grupos de acuerdo con el puntaje de Child-Pugh (tabla 2). El grupode pacientes clasificados con el índice de Child A se compuso de nueve enfermos, 4 mujeres y 5 hombres. La etiología de la cirrosis en 3 de los pacientes fue secundaria a alcohol, en 2 de los pacientes lo fue a hepatitis autoinmune, en 2 casos fue secundaria a hemocromatosis, en 1 caso a enfermedad de Wilson y en 1 caso colestásica.
El grupo de pacientes clasificados con el índice Child B estuvo compuesto por 13 enfermos, 5 mujeres y 8 hombres. La cirrosis fue secundaria a alcohol en 7 de los pacientes, a hepatitis autoinmune en 2, a hepatitis viral (B o C) en 3, a cirrosis biliar secundaria en 1 y de etiología no aclarada en 1. Vale la pena mencionar que en uno de los pacientes incluidos en este grupo, se documentó infección por hepatitis C y tenía antecedentes de ingestión importante de alcohol.
Finalmente, el grupo de pacientes clasificados con el índice de Child C, se constituyó por 15 personas, 4 mujeres y 11 hombres, 13 de los cuales presentaron cirrosis atribuida a alcohol y en 2 no se logró esclarecer la etiología.
A todos los pacientes se les realizó medición de bilirrubina total, albúmina sérica, tiempo de protrombina y seudocolinesterasa sérica y, clínicamente, se evaluó la presencia o ausencia y grado de severidad en caso de presentarse ascitis o encefalopatía hepática (Tabla 2).
Se revisó la curva de desviación de los informes de seudocolinesterasa sérica:
Con respecto al grado de Child-Pugh de cada uno de los pacientes, obteniéndose un rango de valor de la misma para cada uno de los grupos de pacientes (Tabla 3).
Se evaluó la validez epidemiológica del nivel sérico de seudocolinesterasa con respecto al índice de Child-Pugh del grupo determinado de pacientes mediante el cálculo de sensibilidad, encontrándose que para el grupo de pacientes con Child A el nivel de la seudocolinesterasa encontrado tuvo una sensibilidad de 66%; en el grupo de pacientes con Child B, la sensibilidad de la prueba fue de 84,6%, y en el grupo de pacientes con Child C, la sensibilidad de la prueba fue del 93,3%.
La validez de la seudocolinesterasa con relación al grado de Child-Pugh mostró que la mayor sensibilidad fue para el grupo Child C.
Conclusiones
Independientemente de la causa de la cirrosis, el pronóstico de la enfermedad está determinado por el grado de falla hepatocelular.
En este estudio, se ha aplicado la clasificación de Child-Pugh para evaluar la reserva funcional hepática, comparado con el nivel de actividad de seudocolinesterasa sérica, proteína sintetizada en el hígado y que se ha llegado a considerar un predictor independiente de función hepatocelular de acuerdo con lo revisado en la literatura.
Al evaluar la validez epidemiológica del nivel sérico de la seudocolinesterasa con respecto al índice de Child-Pugh, luego de haber establecido rangos de actividad de la enzima para cada grado de la clasificación de Child-Pugh, se encontró que la mayor sensibilidad (93,3%) fue para el grupo Child C, aunque la encontrada para el grupo Child B (84,6%) también tuvo una sensibilidad importante.
Lo cual conlleva a concluir que el papel de la seudocolinesterasa como indicador de función hepatocelular tendría mayor validez en pacientes cirróticos Child B y C, lo que tiene implicaciones pronósticas.
Actividad de la seudocolinesterasa
Al tenerse en cuenta los rangos de actividad de la seudocolinesterasa de más de 4.700 U/ml para los pacientes con Child A, de 3.200 a 4.500 U/ml para los pacientes con Child B y de menos de 3.200 U/ml para los pacientes con Child C, podría tenerse un punto de corte para la actividad de la seudocolinesterasa de 3.400 U/ml, valor por debajo del cual los pacientes tendrían peor pronóstico, lo que estaría acorde con la literatura, en donde se atribuye compromiso hepático funcional significativo y enfermedad descompensada para los pacientes con Child grado B y grado C, respectivamente.
Seguimiento de los pacientes con diagnóstico de cirrosis hepática
De esta forma, se podría incluir la medición de actividad de seudocolinesterasa sérica en el seguimiento de los pacientes con diagnóstico de cirrosis hepática, independientemente de la causa de la misma, como factor pronóstico en un momento dado, para evaluar el grado de función de síntesis hepatocelular.
Dado que el número de pacientes incluidos en el estudio es pequeño, no se pretende generalizar los resultados a toda la población de pacientes con diagnóstico de cirrosis hepática; por el contrario, se puede considerar como un trabajo pionero en nuestro medio para el desarrollo de posteriores estudios que conlleven a una mayor representatividad de la muestra.
Agradecimientos
A las bacteriólogas del laboratorio clínico del Hospital de San José, por el procesamiento de las muestras.
Al doctor William Rojas G., asesor metodológico y con quien se llevó a cabo el proceso de análisis estadístico de las variables consideradas en el estudio.
TABLA 2

TABLA 3
| Indice de Child-Pugh | Punto de corte para la seudocolinesterasa (U/ml) |
| A | Mayor de 4.700 |
| B | 3.200 – 4.500 |
| C | 0 – 3.199 |
Referencias Bibliografícas
- 1. Sherlock S, Dooley J. Enfermedades del hígado y vías biliares. Novena edición. Madrid: Marban libros SL; 1996.
- 2. Bodily O, Fitz G. Approach to the patient with suspected liver disease. In: Diagnosis and treatment in gastroenterology. Stanford: Appleton and Lange; 1996.
- 3. Castera L, Pauwels A, Levy VG. Indicateurs pronostiques chez les malades atteints de cirrhose admis en service de Réanimation. Gastroenterol Clin Biol 1996; 20: 263-8.
- 4. Pugh RNH, et al. Transection of the oesophagus for bleeding oesophageal varices. Br. J Surg 1973; 60(8): 646-9.
- 5. Saunders JB, et al. A 20-year prospective study of cirrhosis. Br Med J 1981; 282: 263-6.
- 6. Infante-Rivard CL, et al. Clinical and statistical validity of conventional prognostic factors in predicting short-term survival among cirrhotics. Hepatology 1987; 7(4): 660-4.
- 7. Child CG, Turcotte JG. Surgery in portal hypertension. In: Child CG, editor. Major problems in clinical surgery: the liver and portal hypertension. Saunders; 1964.
- 8. Christensen E, et al. Prognostic value of Child-Turcotte criteria in medically treated cirrhosis. Hepatology 1984; 4: 430-5.
- 9. Christensen E, et al. Updating prognosis and therapeutic effect evaluation in cirrhosis with Cox’s multiple regression model for time-dependent variables. Scand J Gastroenterol 1986; 21: 163-74.
Fuentes Bibliográficas
- 10. Weston SR, et al. Pseudocolinesterase is a simple, independent indicator of hepatocellular synthetic function in patients with advanced liver disease. Hepatology 1997; 26(4): 289 A.
- 11. Vorhaus LJ, Kark RM. Serum cholinesterase in health and disease. Am J Med 1953; 14: 707-19.
- 12. Hashizuma N, et al. Blood amino acid levels in sarin poising patients. Rinsho-Byori 1997; 45(8): 785-9.
- 13. Devlin JC, et al. Pharmacodynamics of mivacurium chloride in patients with hepatic cirrhosis. Br J Anaesth 1993; 71(2): 227-231.
- 14. Head-Rapson AG, et al. Pharmacokinetics of the three isomers of mivacurium and pharmacodynamics of the chiral mixture in hepatic cirrhosis. Br J Anaesth 1994; 73(5): 613-8.
- 15. Hirata N, Matsuda H. Cardiovascular surgery in patients with liver disfunction. Nippon-Geka-Gakkai-Zasshi 1997; 98(8): 671-5.
- 16. Evans DB, Lehmann H. Pseudocholinesterase activity in liver transplantation. The Lancet 1971; 1: 1040-44.