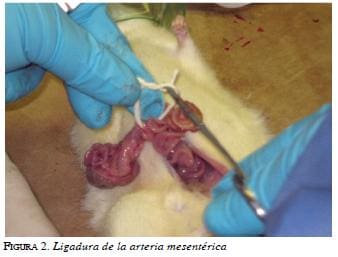
PULGAR GLADYS, CAÑADAS RAUL, ALVARADO JAIME, HANI ALBIS, RODRIGUEZ ALBERTO, SANMIGUEL CLAUDIA
Paciente de 36 años, sexo masculino, con cuadro clínico de 12 días de evolución consistente en fiebre de 39 °C de predominio nocturno, astenia, adinamia y, en las últimas 48 horas, dolor en hemiabdomen superior de predominio en hipocondrio derecho, tipo cólico, asociado a deposiciones líquidas (3/día) de moderada cantidad, sin moco, ni sangre, sin pujo ni tenesmo.
Tres días previo al inicio de la enfermedad actual (EA) estaba en el Magdalena medio, por lo cual se realizaron dos gotas gruesas (negativas) y un cuadro hemático informado como normal.
Antecedentes Personales
Patológicos: cefalea crónica recurrente de 10 años de evolución, sin tratamiento actual.
Revisión por Sistemas
Pérdida de 4 kg de peso con la E A.
No hay historia previa de dolor abdominal.
Examen Físico
Paciente en adecuadas condiciones generales!
SV: TA: 120/80, FC: 110/min; FR:16; t °: 36 °C.
Escleras anictéricas, conjuntivas normocrómicas, mucosa oral seca.
Campos pulmonares bien ventilados, RsCsRs sin soplos.
Abdomen: no distendido, RsIs (+), normales, dolor difuso a la palpación, principalmente en HCD. Murphy dudoso. Sin megalias ni signos de irritación peritoneal.
Extremidades: normal.
Neurológico: sin alteración.
Impresión Diagnostica
- Estado febril en estudio
- Enfermedad diarreica aguda
- Paludismo?
- Fiebre tifoidea?
- Colecistitis?
- Deshidratación.
Estudios paraclínicos
CH: leucocitos: 8000, N: 51%, L: 37%, M: 9,2%, E: 0,2%, B:1%. Hcto: 48%, Hb: 17, PLT: 135.000, VSG: 17.
Parcial de orina: turbio, pH: 5,5, D: 1015, cetonuria, leucocitos: 0-1.
B.T: 0,92, B.D: 0,22, B.I: 0,7, AST: 107, ALT: 205, F.A: 102, LDH: 449.
Glicemia: 82; Cr: 1,3, BUN: 13; Na: 135, K: 4.1
Gota gruesa: (negativa)
Antígenos febriles negativos
Placa de tórax: normal.
La ecografía de abdomen mostró lesión focal hiperecoica con áreas hipoecoicas en su interior en segmento 6: 32x37x26 en lóbulo derecho que sugiere absceso hepático amebiano, por lo que se inicia metronidazol, 250 mg c/8h.
En las primeras 24 horas, evoluciona con deterioro del estado general, con dolor y distensión abdominal, fiebre, con signos de irritación peritoneal. Se realiza TAC de abdomen que muestra imágenes alteradas de las ramas portales y el confluente esplenoportal que sugieren trombosis venosa de la porta. Se corrobora este hallazgo con doppler venoso y se descarta absceso hepático, confirmando el diagnóstico de trombosis.
Con impresión diagnóstica de trombosis de la porta de etiología séptica con foco intraabdominal no aclarado se decide llevar a laparotomía, encontrándose trombosis venosa mesentérica, con intestino isquémico desde el ángulo de Treitz hasta los 20 cm de la válvula ileocecal; ascitis, hígado normal, no se identifica foco séptico intraabdominal; se deja abdomen abierto para una segunda revisión. Se continúa anticoagulación, antibioticoterapia (ceftriaxona) y se inicia soporte nutricional parenteral.
Mejoría de la isquemia mesentérica
A las 24 y 48 horas del postoperatorio se lleva a revisión, encontrándose mejoría de la isquemia mesentérica, realizándose cierre de laparostomía. Presenta derrame pleural derecho con disnea que hacen necesario el manejo con toracostomía cerrada.
Se inicia el estudio de hipercoagulabilidad solicitando antitrombina III: 80% (VN: 80-120%), proteína C: 75% (VN: 70-130%), y anticuerpos antifosfolípidos.
El día 11 postoperatorio, el paciente presenta nuevamente picos febriles, y disnea; se documenta derrame pleural derecho tabicado que requiere nuevo paso de sonda a tórax.
El paciente persiste febril por lo cual se realiza TAC toracoabdominal que confirmó la presencia de derrames pleurales, de líquido ascítico en moderada cantidad, dilatación de asas delgadas con engrosamiento de sus paredes y falta de opacificación de la vena esplénica, confluente esplenoportal y parcialmente la porta (figura 1) y aumento de realce de la grasa mesentérica, hallazgos relacionados con cambios isquémicos intestinales secundarios a trombosis de la vena mesentérica y confluente esplenoportal. (gráfica 2).
Se documenta radiológicamente un proceso neumónico bibasal como causa de la fiebre persistente: entra en insuficiencia respiratoria y es trasladado a UCI. Presenta incremento de los infiltrados, leucocitosis; se aisla Staphylo-coccus aureus y se inicia vancomicina. Por infiltrados pulmonares múltiples y con sospecha de endocarditis infecciosa, se realiza ecocardiograma que muestra hipertensión pulmonar moderada, ligero engrosamiento de la valva anterior de la válvula mitral, sin franca vegetación.
Riesgo conocido de empeorar la isquemia mesentérica
Posteriormente, presenta hemorragia digestiva alta que hace necesario suspender la anticoagulación a pesar del riesgo conocido de empeorar la isquemia mesentérica. No fue posible realizar endoscopia por el compromiso respiratorio.
Evoluciona con deterioro del compromiso respiratorio atribuido a derrames pleurales tabicados que requieren punción; un nuevo cuadro hemático mostró leucocitosis, anemia, dímero D positivo, tiempos de coagulación prolongados y el paciente se halla en malas condiciones generales con aumento del perímetro abdominal y distensión abdominal, por lo que se decide llevar a cirugía con sospecha de hemorragia intraabdominal encontrándose abundante líquido seroso en cavidad, asas intestinales viables y se realiza empaquetamiento.
Se reciben resultados de estudio antifosfolípidos:
- Primero, Antifosfolípido: 1:400 (+)
- Segundo, Anti cardiolipina: 1:400 (+)
- Tercero, Anti fosfatidiletanolamina: 1:400 (+)
- Cuarto, Anti fosfatidilglicerol: 1:400 (+)
- Quinto, Anti acidofosfatídico: 1:400 (+)
- Sexto, Anti fosfatidilinositol: 1:400 (+).
Presenta coagulación intravascular diseminada, inestabilidad hemodinámica que necesita apoyo inotrópico, insuficiencia renal aguda, edema pulmonar, que requiere hemofiltración. Evoluciona a una falla orgánica múltiple dada por compromiso renal, hepático, hematológico y pulmonar. Presenta choque séptico con hipotensión refractaria y fallece.
Diagnostico definitivos
- Falla orgánica múltiple
- Choque séptico refractario
- Endocarditis por S. aureus.
- Neumonía nosocomial
- Trombosis venosa mesentérica secundaria a sindrome de Anticuerpos antifosfolípidos.
Patología Post-Mortem
Se lleva a cabo autopsia, con estudio macroscópico y microscópico que concluye lo siguiente:
1. Enfermedad tromboembólica generalizada secundaria a síndrome de anticuerpos antifosfolípidos, con compromiso de pulmón, vena mesentérica superior, esplénica, porta y suprarrenal.
2. Sepsis secundaria a focos intraabdominales múltiples y endocarditis bacteriana de válvula mitral con infarto séptico cerebral secundario, hepatitis, esplenitis séptica y CID.
Trombosis Venosa Mesentérica
La trombosis venosa mesentérica (TVM) es una rara, pero potencialmente letal, forma de isquemia mesentérica, cuya presentación puede variar desde una forma completamente asintomática hasta una forma aguda y catastrófica, con infarto intestinal (1-3).
Incidencia
La TVM fue descrita por primera vez por Elliot en 1895, como trombosis del sistema portomesentérico. En las primeras publicaciones como la de Cokkinis, publicada en 1926, se consideró que la TVM era la principal causa de isquemia mesentérica aguda (1-3,5). Sin embargo, la mayoría de estos casos probablemente eran secundarios a isquemia mesentérica no oclusiva, entidad descrita por primera vez por Ende en 1958 (4-5). Hoy en día, se sabe que 5-15% de los pacientes con isquemia mesentérica aguda tiene TVM (1, 4, 6).
Esta patología constituye tan sólo 0,01% de todos los ingresos en los servicios de urgencias quirúrgicas, 0,006% de las admisiones hospitalarias, y menos del 2% de las autopsias. El infarto intestinal debido a TVM se encuentra en menos de 1 en 1000 laparotomías en casos de abdomen agudo (7). La relación hombre/ mujer varía de 1,5 :1 a 1:1; y la edad promedio es de 48-60 años (menor que la observada en otras formas de isquemia mesentérica) (4, 8).
Etiología
De acuerdo con su etiología, la TVM puede dividirse en primaria, espontánea o idiopática (25% de los casos) y secundaria (1, 4) (tabla 1). Inicialmente se identificaba la causa de la TVM en menos de 50% de los casos; sin embargo, con la descripción de los estados de hipercoagulabilidad y de otras condiciones protrombóticas, la causa puede establecerse actualmente en más de 80% de los casos (8).
Los estados de hipercoagulabilidad pueden representar hasta 42% de las causas de TVM y consisten en la presencia de anticuerpos anticardiolipina (tipos I-IV, cada uno con distintas manifestaciones trombóticas) (9), anticoagulante lúpico, deficiencias de proteína C o S, disfibrinogenemia, plasminógeno anormal, disfunción de antitrombina III o del cofactor II de la heparina, policitemia vera, trombocitosis, anemia de células falciformes y mutaciones del factor V Leiden (1-2, 4).
(Lea También: Manifestaciones Clínicas en Isquemia Mesentérica)
Historia natural de la TVM
Numerosos estudios experimentales, ocluyendo la vena mesentérica superior en perros (2, 4), han contribuido al conocimiento actual sobre la fisiopatología de esta entidad. Los cambios visibles consistieron en dilatación de la vena mesentérica, hemorragia hacia el mesenterio, cianosis del intestino con congestión y espasmo, íleo paralítico y exudación de líquido serosanguinolento desde el intestino y el mesenterio hacia la cavidad peritoneal. De manera constante, se observaron hipovolemia y hemoconcentración notables y reducción del flujo a nivel de la arteria mesentérica superior por vasoconstricción o por trombosis de la misma. Al final del proceso, ocurre infarto intestinal transmural haciendo imposible diferenciar la trombosis arterial de la trombosis venosa; sin embargo, el infarto rara vez ocurre a menos que se encuentren comprometidas las ramificaciones de las arcadas periféricas y la vasa recta (5).
TABLA 1. Trastornos relacionados con TVM
| Estados de hipercoagulabilidad Trombosis venosa profunda periférica Neoplasias Deficiencia de antitrombina III Deficiencia de proteína C y S Ingestión de anticonceptivos Embarazo Policitemia vera TrombocitosisHipertensión portal Cirrosis Esplenomegalia congestiva Después de escleroterapia de várices esofágicas |
Inflamación Pancreatitis Peritonitis (apendicitis, víscera perforada) Enfermedad intestinal inflamatoria Absceso pélvico o intraabdominal Enfermedad diverticularEstado postoperatorio o trauma Trauma abdominal cerrado Esplenectomía u otros estados postoperatoriosOtros trastornos Enfermedad por descompresión |
La hipoxia celular causa disminución en la síntesis de ATP y aumento en su degradación, con la consiguiente elevación en la concentración de productos de la degradación del ATP tales como H+ (una de las causas de acidosis celular), fosfato inorgánico y derivados de purinas que intervienen en la formación de radicales libres de oxígeno e incremento en la glicólisis anaerobia con la consiguiente producción de lactato (2, 5, 10). El aumento en la concentración de H+ por los mecanismos ya mencionados conlleva a la generación de una gran cantidad de CO2 (hipercarbia celular) en el proceso de neutralización de estos H+. Es posible que, en conjunto con la hipoxia tisular, la hipercarbia contribuya a la producción de los cambios funcionales y anatómicos que caracterizan los estados de isquemia (10).FISIOPATOLOGIA DE LA ISQUEMIA MESENTERICA
Los cambios isquémicos son más intensos en la punta de las vellosidades y ocurren tempranamente. Después de 3 a 4 horas, la necrosis de la vellosidad es completa y se asocia con necrosis de las criptas, comprometiendo la regeneración epitelial. La mucosa intestinal lesionada queda expuesta a los efectos digestivos de las proteasas pancreáticas y las sales biliares, causando su autodigestión (11).
Por otra parte, la alteración del pH y la disminución del potencial redox se asocia con un desequilibrio de la naturaleza y densidad de la flora intestinal, con proliferación y migración proximal de las bacterias anaerobias. La mucosa lesionada permite la translocación bacteriana hacia el peritoneo y la circulación portal y sistémica favoreciendo la aparición de sepsis en estos pacientes (10-11).
La lesión por reperfusión, también descrita, se caracteriza por vasoespasmo intenso, permeabilidad mucosa aumentada, infiltrado leucocitario y agregación plaquetaria, Durante la reperfusión existe mayor disponibilidad de oxígeno para convertirse en radical superóxido (O2) que luego de varios pasos metabólicos puede generar radicales hidroxilo (OH-), altamente reactivos y tóxicos. El efecto final es un incremento en la permeabilidad vascular y de la mucosa que conllevan a la formación de un tercer espacio, hipovolemia, translocación bacteriana y sepsis (10).