Diagnóstico y Tratamiento de los Tumores de la Unión Esofagogástrica. Experiencia en el Instituto Nacional de Cancerología
Diagnosis and treatment of esophagogastric junction tumors. Experience at the National Cancer Institute
Resumen
Introducción. El diagnóstico adecuado de los tumores de la unión esofagogástrica es esencial para el tratamiento de estos pacientes. La clasificación propuesta por Siewert-Stein define las características propias, factores de riesgo y estrategias quirúrgicas según la localización. El objetivo de este estudio fue describir las características de los pacientes con adenocarcinoma de la unión esofagogástrica tratados en nuestra institución.
Métodos. Estudio retrospectivo, descriptivo, de corte longitudinal, que incluyó los pacientes con diagnóstico de adenocarcinoma de la unión esofagogástrica intervenidos quirúrgicamente en el Instituto Nacional de Cancerología, Bogotá, D.C., Colombia, entre enero de 2012 y mayo de 2017.
Resultados. Se operaron 59 pacientes (84,7 % hombres), con una edad media de 62,5 años. En su orden de frecuencia los tumores fueron tipo II (57,6 %), tipo III (30,7 %) y tipo I (11,9 %). El 74,6 % recibieron neoadyuvancia y se realizó gastrectomía total en el 73 % de los pacientes.
La concordancia diagnóstica moderada con índice Kappa fue de 0,56, difiriendo con la endoscópica en 33,9 %. El 10,2 % de los pacientes presentó algún tipo de complicación intraoperatoria. La supervivencia a tres años en los tumores tipo II fue del 89,6 % y del 100 % en aquellos con respuesta patológica completa.
Conclusión. Es necesario el uso de diferentes estrategias para un proceso diagnóstico adecuado en los tumores de la unión esofagogástrica. En esta serie, los pacientes Siewert II, aquellos que recibieron neoadyuvancia y los que obtuvieron una respuesta patológica completa, tuvieron una mejor supervivencia a tres años.
Palabras clave: unión esofagogástrica; neoplasias esofágicas; neoplasias gástricas; clasificación; supervivencia.
Abstract
Introduction: Proper diagnosis of gastroesophageal junction tumors is essential for the treatment of these patients. The classification proposed by Siewert-Stein defines its own characteristics, risk factors and surgical strategies according to the location. This study describes the characteristics of patients with adenocarcinoma of the esophagogastric junction treated at our institution.
Methods. Retrospective, descriptive, longitudinal study, which includes patients diagnosed with adenocarcinoma of the esophagogastric junction who underwent surgery at the National Cancer Institute in Bogotá, Colombia, between January 2012 and May 2017.
Results. Fifty-nine patients (84.7% men) were operated on, with a mean age of 62.5 years. In their order of frequency, the tumors were type II (57.6%), type III (30.7%) and type I (11.9%). 74.6% received neoadjuvant therapy and total gastrectomy was performed in 73% of the cases. The moderate diagnostic concordance with the Kappa index was 0.56, differing from the endoscopic one in 33.9%. 10.2% of the patients presented some type of intraoperative complication. Three-year survival in type II tumors was 89.6% and 100% in those with complete pathologic response.
Conclusion. The use of different strategies is necessary for an adequate diagnostic process in tumors of the esophagogastric junction. In this series, Siewert II patients, those who received neoadjuvant therapy, and those who obtained a complete pathological response had a better three-year survival.
Keywords: esophagogastric junction; esophageal neoplasms; gastric neoplasms; classification; survival.
Introducción – Diagnóstico y Tratamiento de los Tumores de la Unión Esofagogástrica
El cáncer gástrico corresponde a la cuarta causa de mortalidad por cáncer a nivel mundial, mientras que el esofágico ocupa la sexta posición; en los países occidentales su incidencia ha aumentado rápidamente, por una mayor prevalencia de la enfermedad por reflujo gastroesofágico 1,2,3.
La literatura en Latinoamérica es muy limitada a este respecto; en una institución de referencia en Brasil, se informó una prevalencia del 15 % en biopsias de lesiones de esófago y estómago, y otras series describen la experiencia en algunos centros oncológicos, con desenlaces que parecen no diferir de los reportados a nivel mundial 4,5,6.
En Colombia esta patología esofágica tiene una menor incidencia, mientras que el cáncer gástrico representa la primera causa de mortalidad 1.
Las implicaciones de un diagnóstico preciso en los tumores de la unión esófago gástrica (UEG) obligan al conocimiento de esta patología, ya que los errores en la clasificación y la inadecuada elección del tratamiento son frecuentes en el manejo de estos pacientes 7.
Siewert y Stein desarrollaron una clasificación endoscópica, basándose en la ubicación del tumor según la UEG 8, sin embargo, en la más reciente edición de la American Join Cancer Committee (AJCC), se define como adenocarcinomas de la UEG a aquellos con centro del tumor a dos cm proximal y distal del cardias, lo que puede ser un complemento con la clasificación de Siewert para la toma de decisiones quirúrgicas, considerando estadificar a los tumores que se encuentran en los primeros dos cm del estómago proximal (tipos I y II) como cánceres de esófago y a los más distales como gástricos o tipo III 9,10 (Tabla 1).
Tabla 1. Clasificación de Siewert-Stein para los tumores de la unión esófago gástrica 8.

Tradicionalmente, las lesiones Siewert I han sido tratadas como cáncer de esófago y las tipo III como cáncer gástrico, pero en cuanto a los tumores Siewert II existen aún controversias, tanto en la estrategia de manejo neoadyuvante como en el abordaje quirúrgico, sin que hasta el momento exista un consenso para su abordaje 11.
Con el manejo neoadyuvante con quimioterapia, sola o asociada a radioterapia, se han informado tasas adecuadas de respuesta con reducción del tamaño tumoral, aumento de las tasas de resecciones R0 y mejoría de los desenlaces en supervivencia, sin embargo, se observa una importante heterogeneidad de los estudios, sin lograr discriminar estos desenlaces asociados a un tipo de abordaje quirúrgico específico 12.
La esofagectomía por toracotomía se ha aceptado ampliamente como el tratamiento para los tumores Siewert I, así como la gastrectomía total o proximal por abordaje abdominal para los tipo III.
No se ha definido la mejor estrategia quirúrgica para los pacientes con tumores Siewert II; una gastrectomía proximal con un abordaje transhiatal resecando los ganglios mediastinales según la longitud del compromiso esofágico, puede ser un punto de partida oncológico para estas lesiones 13, sin embargo, teniendo en cuenta que la cirugía radical exige una resección con márgenes libres de mínimo dos cm proximales y un margen circunferencial mayor de 1 mm, asociado a una linfadenectomía de más de 15 ganglios 14, la resección a nivel del esófago y su anastomosis, requiere en la mayoría de los casos un abordaje torácico adicional 15.
En la revisión inicial, Siewert no encontró diferencias en la supervivencia a cinco años entre el abordaje torácico o el transhiatal 8.
Algunos estudios han buscado encontrar beneficios en la supervivencia de acuerdo al abordaje quirúrgico según el tipo de tumor; Parry et al. compararon los desenlaces según el manejo quirúrgico (esofagectomía contra gastrectomía) para los tumores tipo II y, aunque no se encontraron diferencias en la supervivencia a cinco años, informaron una mayor presentación de borde circunferencial positivo y un menor número de ganglios paraesofágicos resecados en los pacientes a quienes se les realizó solo gastrectomía 16.
Otros estudios han evaluado los desenlaces según el tipo de abordaje en tórax, encontrando una mayor disección de ganglios mediastinales en el abordaje toracoabdominal comparado con el transhiatal, pero con una morbilidad mayor (49 % vs 34 %), sin impacto en la supervivencia para estos pacientes 17,18,19.
Recientemente Kurokawa et al, basados en el compromiso de los ganglios linfáticos mediastinales y abdominales, encontraron que un abordaje abdominal transhiatal es adecuado para los tumores con un compromiso esofágico menor a tres cm, a diferencia de aquellos con una extensión esofágica mayor, donde se hace necesario adicionar un abordaje torácico derecho 14.
No se encontró una publicación nacional que describa la experiencia en el manejo de los pacientes con tumores de la UEG.
El objetivo de este trabajo fue presentar la experiencia del Instituto Nacional de Cancerología en Bogotá, D.C., Colombia, en el diagnóstico y manejo de los pacientes con tumores de la UEG, analizando una de las series con mayor representación de pacientes con Siewert tipo II, en quienes existe la mayor controversia en cuanto a su manejo.
Métodos – Diagnóstico y Tratamiento de los Tumores de la Unión Esofagogástrica
Estudio retrospectivo, observacional, descriptivo, de corte longitudinal, que incluyó pacientes con diagnóstico de adenocarcinoma de la unión esofagogástrica, intervenidos quirúrgicamente en el Instituto Nacional de Cancerología, entre enero de 2012 y mayo de 2017.
Se excluyeron pacientes con histología escamocelular y aquellos con pérdida de seguimiento antes de tres años.
A partir de las historias clínicas y teniendo en cuenta los informes endoscópicos, descripciones quirúrgicas, reportes de patología quirúrgica y seguimiento posoperatorio, se elaboró una base de datos utilizando la plataforma Research Electronic Data Capture (REDCap).
Para la caracterización demográfica y descripción de la población, se utilizaron medidas de frecuencia para el caso de variables categóricas y medias o medianas, con sus correspondientes medidas de dispersión, en el caso de variables continuas. Con el objetivo de evaluar la concordancia entre la clasificación endoscópica y la patológica se estimaron coeficientes de concordancia (kappa ponderado).
Para describir la supervivencia global, se utilizaron las curvas de Kaplan Meier y se reportaron las tasas de densidad de incidencia junto con sus intervalos de confianza del 95 %. Todos los análisis estadísticos fueron realizados en el software R – Project v4.1.1 (R Core Team®, 2021).
Resultados – Diagnóstico y Tratamiento de los Tumores de la Unión Esofagogástrica
Características clínicas
Se incluyeron en total 59 pacientes (84,7 % hombres). La edad media fue de 62,5 años (DE 34–81 años) (tabla 2).
Tabla 2. Características demográficas, clínicas y quirúrgicas de los pacientes con tumores de la unión
esófago gástrica intervenidos quirúrgicamente en el Instituto Nacional de Cancerología.
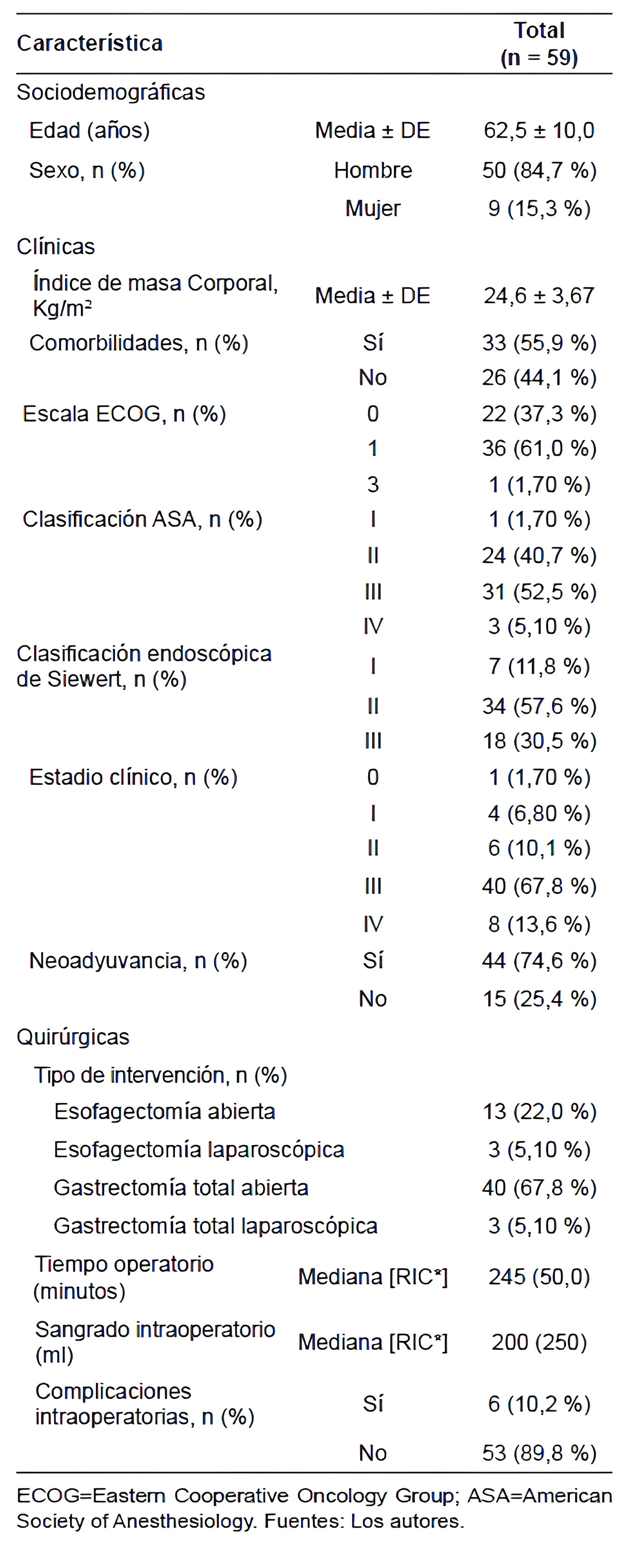
El índice de masa corporal (IMC) medio fue de 24,6 ± 3,67 Kg/m2, con un IMC mínimo de 17,6 y un máximo de 34,7 Kg/m2.
Se encontraron comorbilidades en 33 pacientes (55,9 %), siendo las de tipo vascular las más frecuentes (45,5 %); otras patologías subyacentes correspondieron a alteraciones inmunológicas, endocrinológicas, neurológicas y respiratorias. De acuerdo con el Eastern Cooperative Oncology Group (ECOG), la mayoría de los pacientes (n=36) tenía una escala de 1 (61 %).
Según la clasificación Siewert-Stein endoscópica, la mayoría de los pacientes (n=34) eran tipo II (57,6 %) y 40 pacientes se encontraban en el estadio clínico III (67,8 %).
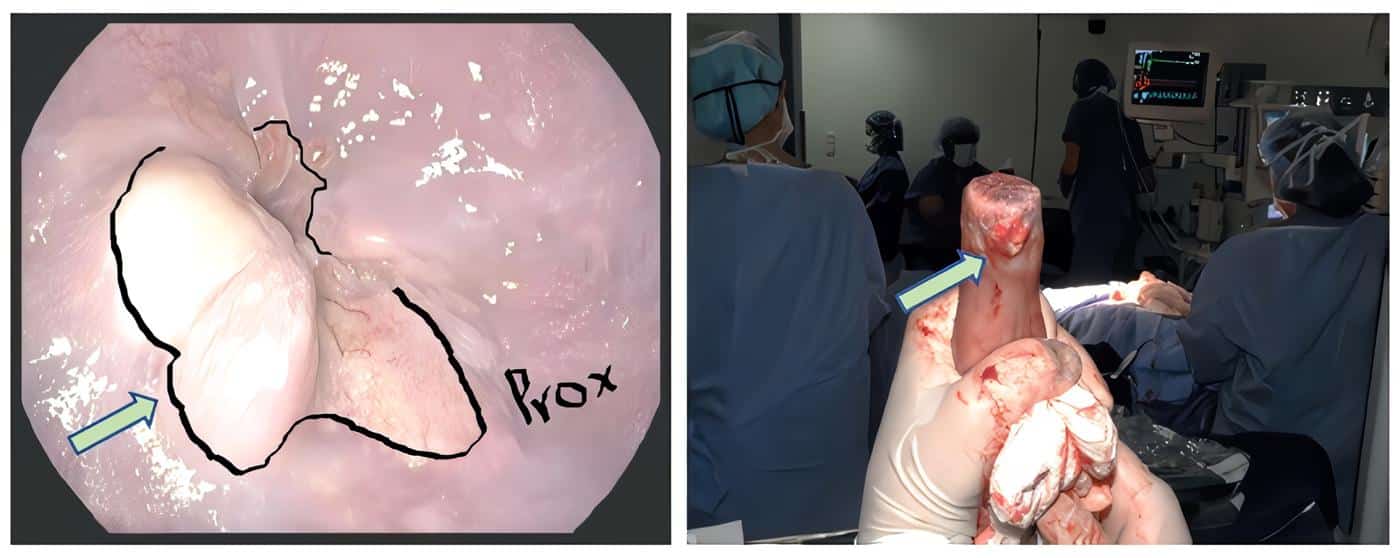
Figura 1. Imagen de correlación endoscópica y quirúrgica de un paciente con tumor de la unión
gastroesofágica Siewert II. Lesión tumoral señalada con las flechas. Fuentes: Los autores.
El tratamiento neoadyuvante fue administrado a 44 pacientes (74,6 %), siendo el esquema del protocolo CROSS (carboplatino u otro platino + taxano + radioterapia) el más frecuentemente usado, en 21 pacientes (47,7 %), seguido del protocolo CALGB 9781 (cispaltino + 5FU + radioterapia) en nueve (20,4 %); los esquemas de quimioterapia perioperatoria en dupleta (11,3 %) o tripleta (13,6 %) se aplicaron en menor porcentaje.
El 85 % de los pacientes Siewert I recibieron algún esquema de quimiorradioterapia; el 65 % de los pacientes con Siewert II recibieron neoadyuvancia, al igual que el 23 % de los Siewert III. La mediana de tiempo entre la neoadyuvancia y el momento de la cirugía fue de 2,7 meses (RIC: 1,17), y varió entre 0,9 y 18,1 meses.
La mitad de los pacientes (50,8 %) recibieron tratamiento adyuvante, siendo la dupleta capecitabina y oxaliplatino el esquema más utilizado (43,3 %), seguido del protocolo McDonald (20 %).
Manejo quirúrgico
La gastrectomía total con margen esofágico transabdominal se realizó en 43 pacientes (73 %) y en los restantes 16 pacientes se realizó esofagectomía mediante las técnicas de Mckeown, Ivor Lewis, mínimamente invasiva o transhiatal abierta sin toracotomía. La clasificación endoscópica difirió de la clasificación intraoperatoria en el 38 % de los casos, siendo del 43,2 % para los pacientes tipo II, del 33 % para los tipo I y del 23,5 % para los tipo III.
En cuanto a la clasificación tipo Siewert, el 66,7 % de los pacientes con el tipo I fueron tratados con esofagectomía por dos o tres vías y el 33,3 % por gastrectomía y esofagectomía distal transabdominal.
Los pacientes con tipo II, se llevaron a gastrectomía total más esofagectomía distal transabdominal en el 76,7 % de los casos, 9 % con esofagectomía Ivor Lewis, el 11,7 % con esofagectomía por tres vías y un solo paciente con esofagectomía más ascenso gástrico transhiatal.
Al 88,2 % de los pacientes con una clasificación Siewert III se les realizó gastrectomía total, con abordaje de Ivor Lewis o con esofagectomía transhiatal.
La mediana del tiempo quirúrgico fue de 245 minutos (RIC: 50,0), con un tiempo mínimo de 120 y un tiempo máximo de 500 minutos. El sangrado promedio durante el procedimiento quirúrgico fue de 200 ml. El tipo de sutura más utilizado fue la grapadora circular de 25 mm en esofagectomía tipo Ivor Lewis, gastrectomía total abierta y total laparoscópica.
Desenlaces tempranos
Ocurrieron complicaciones intraoperatorias en seis pacientes (10,2 %): sangrado en tres, lesión de estructuras adyacentes en dos, y lesión de la vía aérea en uno. Luego de la cirugía, 28 pacientes requirieron traslado a la Unidad de Cuidados Intensivos (47,5 %), con una estancia media de 9,5 días. En cuanto a la estancia hospitalaria, la mediana fue de 11 días.
Veintidós pacientes (37,3 %) presentaron algún tipo de complicación postoperatoria, con una tasa de reintervención del 15,3 % debida a colección torácica en cuatro pacientes, fuga de la anastomosis en tres, obstrucción intestinal en un paciente y colección abdominal en otro. La tasa de fuga anastomótica fue del 6,8 %, sin diferencias según el tipo de abordaje realizado.
Las complicaciones ocurrieron por igual en paciente sometidos a gastrectomía o esofagectomía transhiatal y esofagectomía por dos o tres vías, sin embargo, del total de pacientes con complicaciones cardiopulmonares (n=11), el 63,6 % habían tenido un abordaje transtorácico asociado. La mortalidad en los primeros 30 días se presentó en dos pacientes (3,4 %) (Tabla 3).
Tabla 3. Características postoperatorias y patológicas de los pacientes con tumores de la unión esófago
gástrica intervenidos quirúrgicamente en el Instituto Nacional de Cancerología.

Características patológicas
La mayoría de los pacientes presentaron estadio patológico IIIb (n=20, 33,9 %), seguido del estadio IIb (20,3 %). El 8,3 % de los pacientes tuvieron una respuesta patológica completa, el 80 % de ellos tenía una clasificación endoscópica de Siewert tipo II y habían recibido neoadyuvancia con protocolo CALGB 9781. El grado de diferenciación histológico fue moderado en el 44,1 % de los pacientes.
Se encontró un margen positivo en la pieza quirúrgica o en la dona esofágica en 12 pacientes (20,3 %): en cuatro en la dona esofágica, en cuatro en el margen proximal, en tres en el circunferencial y en uno en el distal. Todos los pacientes con margen positivo proximal, incluyendo la dona esofágica, fueron manejados con gastrectomía total más esofagectomía distal transabdominal.
De los pacientes con margen circunferencial positivo, el 66,7 % habían sido llevados a esofagectomía por tres vías.
En promedio, el número de ganglios resecados fue de 20 (DE: 9,56), con un número mínimo de tres y un máximo de 47. El número de ganglios resecados fue mayor en la clasificación III (media= 22, DE:8,64); 22 pacientes (37,3 %) tuvieron una linfadenectomía menor a 15 ganglios.
En cuanto a la vía de abordaje, el promedio de ganglios resecados fue de 21,1 en los pacientes llevados a gastrectomía total por abordaje transhiatal, con menos de 15 ganglios en el 30,4 % de los casos.
En los pacientes llevados a esofagectomía por 2 vías, el promedio fue de 10,8 ganglios, con un 80 % de linfadenectomías menor a 15 ganglios. Y en los pacientes llevados a esofagectomía por tres vías, el promedio fue de 19, con menos de 15 en el 42,8 % de los pacientes.
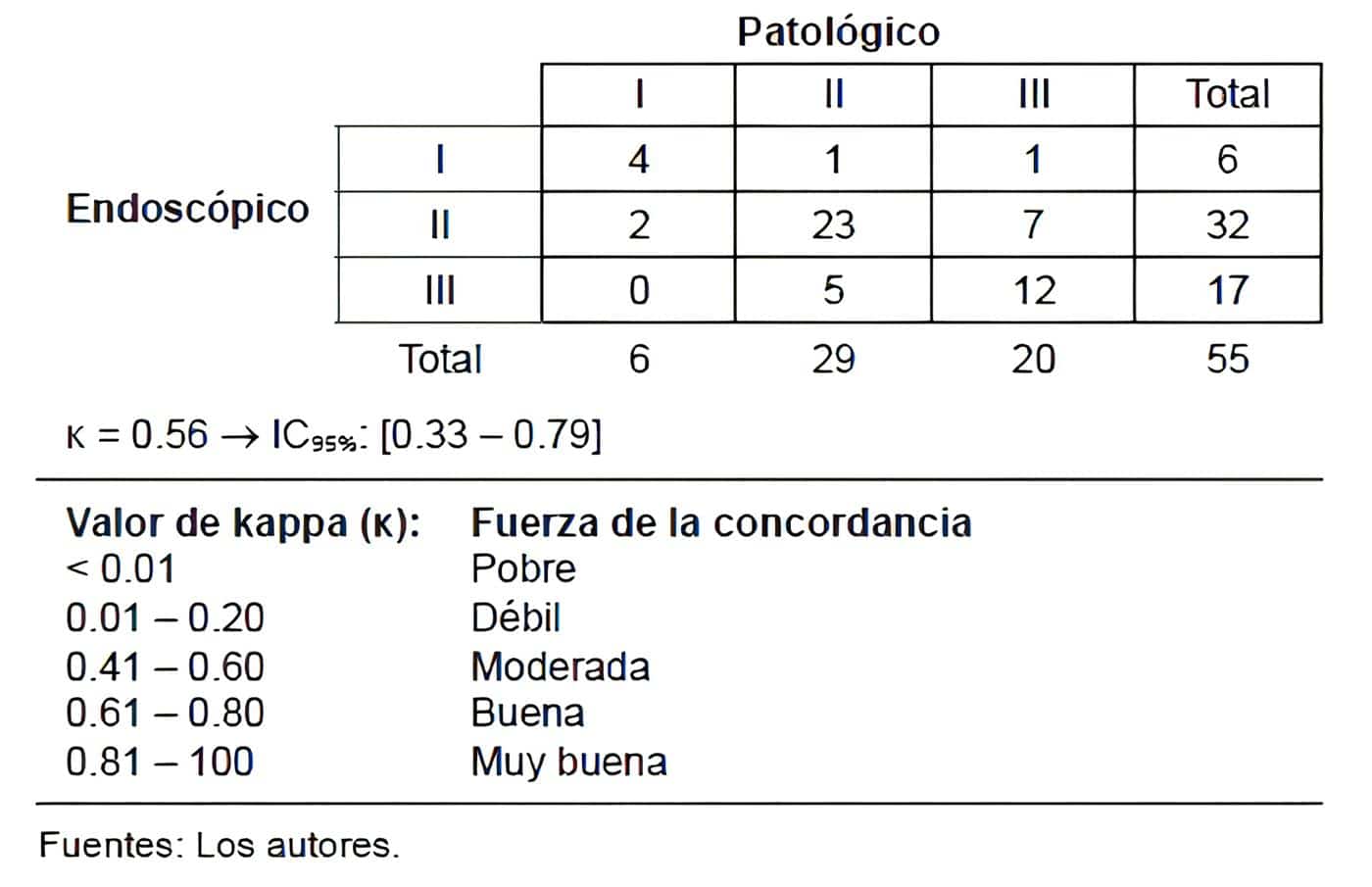
La clasificación patológica de Siewert tuvo una concordancia moderada, con un índice Kappa de 0,56 (IC95% 0,33–0,79), difiriendo de los hallazgos endoscópicos en el 33,9 % de los pacientes, que fue mayor para los pacientes con Siewert I (66 %) y II (32,4 %) y menor en el tipo III (23,5 %).
La concordancia de la clasificación intraoperatoria con la patológica fue mayor, difiriendo solo en el 15,2 % de los pacientes, con una menor discordancia al comparar con el diagnóstico endoscópico en los tumores tipo II (16 % vs 32,4 %) (Tabla 4).
Tabla 4. Concordancia con relación al tipo de clasificación Siewert endoscópica y patológica en
pacientes con diagnóstico de adenocarcinoma de la unión esofagogástrica.
La mediana de la extensión del esófago resecado fue de 37,5 mm (DE:10-150 mm); en el caso del margen de resección proximal, la mediana fue de 24 mm (RIC: 26,2), con un tamaño mínimo de tres y máximo de 120 mm.
Desenlaces a largo plazo
La mediana del período de seguimiento fue de 31,5 meses (RIC: 39,0). Hubo recaída en 16 pacientes (27 %), de estos, el 43 % había presentado alguna complicación postoperatoria temprana. Solo dos de ellos tenían margen positivo (proximal y circunferencial).
La mediana de ganglios resecados para estos pacientes fue de 19,5, sin diferencia con los pacientes que no recayeron 19,8. Dos pacientes (12,5 %) tenían una clasificación Siewert tipo I, 10 tipo II (62,5 %) y cuatro pacientes tipo III (25 %).
El 75 % de los pacientes que recayeron habían sido manejados con gastrectomía total más esofagectomía distal transhiatal. Como hallazgo importante se encontró que, de los pacientes tratados con esofagectomía por tres vías, el 43 % presentaron recaída, en tanto que de los operados con técnica de Ivor Lewis solo el 14 % la sufrió.
La supervivencia global, definida como el tiempo transcurrido desde la fecha de la cirugía hasta la fecha de la muerte (o de último contacto), a dos años fue del 74,9 % (IC95%: 63,9–88,0) y a tres años del 68,2 % (IC95%: 55,5–83,9).
La supervivencia global a tres años para los pacientes con Siewert tipo I fue de 68,6 % (IC95%: 40,3–100), para el tipo II fue 89,6 % (IC95%: 79,0–100) y para el tipo III del 51,8 % (IC95%: 32,4–82,7). En los pacientes que recibieron neoadyuvancia, la supervivencia fue de 76,3 % (IC95%: 63,7–91,4) y del 70,9 % (IC95%: 50,4–99,8) en los que no la recibieron.
Todos los pacientes con respuesta patológica completa estaban vivos y sin recaída al momento de la recolección de datos.
La supervivencia en relación con el tipo de tratamiento quirúrgico recibido fue de 65,3 % (IC95%: 44,5–95,8) para los pacientes a quienes se les realizó esofagectomía y de 78,5 % (IC95%: 66,2–93,1) en los pacientes manejados con gastrectomía total.
Los pacientes con margen positivo presentaron una supervivencia menor a la reportada para la serie en general, con un 41,6 % a tres años. De los 59 pacientes, fallecieron 16 (27,1 %).
Dentro de las variables asociadas a un aumento en la mortalidad, se encontró que la mitad de los pacientes con linfadenectomía menor a 15 ganglios y todos los pacientes con recaída fallecieron en el seguimiento a tres años.
Discusión – Diagnóstico y Tratamiento de los Tumores de la Unión Esofagogástrica
La incidencia de los tumores de la unión esófago gástrica, ha venido aumentando a nivel mundial, y se estima un incremento progresivo hasta el año 2030 6.
En esta serie se observó un predominio de pacientes de género masculino, con una edad promedio de presentación (62,5 años), similar a lo reportado en los estudios de caracterización de la población europea y norteamericana 20-22.
En la década de 1980, ante la creciente confusión del área específica de la UEG como una zona más allá de una estructura anatómica, Siewert y colaboradores propusieron una clasificación para los tumores de esta localización, con la intención de dividir esta zona en tres tipos de tumores, cada uno con unas características, factores de riesgo y estrategias quirúrgicas diferentes.
Y en nuestra serie, llama la atención la distribución en la clasificación de estos pacientes, con más del 60 % diagnosticados endoscópicamente como Siewert II, en comparación con la serie chilena publicada en el 2010, donde el 70 % de los pacientes fueron clasificados como Siewert III 4.
Sin embargo, las publicaciones recientes enfatizan que los tumores tipo II son los verdaderos tumores del cardias, y es este grupo el que requiere mayor estudio debido a sus dificultades en el manejo quirúrgico y multimodal.
Ante la dificultad de la clasificación adecuada de estos tumores, se quiso analizar la concordancia de la clasificación de Siewert endoscópica, intraoperatoria y patológica.
En esta serie, la endoscopia logró una clasificación adecuada al compararse con el reporte de patología en 20 pacientes (66 %), resultado similar a los reportados en otros estudios 23,24. Se encontró además una mayor eficacia de la endoscopia para la clasificación de los tumores tipo III (76,5 %).
Cuando se comparó el diagnóstico intraoperatorio realizado por el cirujano con el reporte de patología, este presentó una concordancia del 85 %, con una diferencia más significativa a favor de los tumores tipo II (84 % vs 67,6 %) comparado con el diagnóstico endoscópico, lo cual es esperado ante la posibilidad de una mejor evaluación anatómica.
Esta discordancia indica que se debe propender por el uso de herramientas combinadas para la clasificación y evaluación preoperatoria, teniendo en cuenta que un diagnóstico inadecuado podría llevar a un cambio en la indicación del tipo de manejo neoadyuvante e implicaciones en la posibilidad de adyuvancia.
Por otra parte, la planeación del abordaje quirúrgico, transabdominal o toracoabdominal, está basado en la longitud del compromiso esofágico de más o menos tres cm, que determinaría la extensión de la linfadenectomía según las recomendaciones de las publicaciones de Yamashita y Kurokawa basadas en el compromiso linfático de los tumores de la UEG 14,25.
El manejo multimodal de los pacientes con tumores de la UEG es actualmente el estándar en los estadios localmente avanzados, debido a las altas tasas de falla en el tratamiento con solo manejo quirúrgico.
El manejo neoadyuvante, con o sin radioterapia, se recomienda en los pacientes con estadios superiores a T3 y N+, logrando aumento en la tasa de resecciones R0 y beneficios en la supervivencia de 49 vs 24 meses 24.
En esta serie, un 74,6 % de los pacientes recibieron manejo neoadyuvante, siendo más frecuente para los pacientes Siewert I y II localmente avanzados. La frecuencia de respuesta patológica completa fue del 8,3 %, con un 80 % de tumores tipo II.
Estos resultados que corresponden a un grupo de pacientes con adenocarcinoma están cercanos a lo reportado en algunos estudios para este subgrupo (9-18 %), pero difieren de las tasas de respuesta patológica completa referidas en otros estudios donde se incluyeron pacientes con carcinomas escamocelulares y adenocarcinomas (26-28 %) 26,27.
El manejo quirúrgico en esta serie de pacientes está acorde a lo reportado en la literatura, con una tendencia al abordaje toracoabdominal con esofagectomía por dos o tres vías para los Siewert I y gastrectomía total para los tumores tipo III.
Por otra parte, se observa una tendencia al manejo con gastrectomía total y margen esofágico transabdominal para los tumores Siewert II (76,7 %), distribución similar a la que se encuentra en otros estudios 28.
Sin embargo, a la fecha, la evidencia que apoya la esofagectomía o la gastrectomía total para este grupo de pacientes, sigue siendo heterogénea y las dos revisiones sistemáticas con este objetivo informaron tasas de supervivencia a tres y cinco años similares para ambos abordajes, con diferencias que no exceden el 10 % 19,29.
La tasa de complicaciones en este estudio (37,3 %) no difiere de otros 18.
Contrario a otras series donde se ha descrito un aumento en la morbilidad superior al 50 % para el abordaje transtorácico, en esta serie no se encontraron diferencias significativas entre los tipos de abordajes y la presentación de complicaciones; sólo las complicaciones cardiopulmonares fueron más frecuentes en el abordaje transtorácico, con implicaciones en la estancia hospitalaria y requerimiento de intervenciones adicionales durante la hospitalización.
Una de las complicaciones más estudiadas en estos pacientes es la fuga de la anastomosis, sin embargo, identificamos solo un 6,7 %, valor inferior al 12 % mencionado en otras series 18,30, y no se encontró asociación con el tipo de abordaje realizado o un impacto en la recaída o supervivencia.
Los desenlaces de los pacientes oncológicos están directamente relacionados con las resecciones no curativas, por tanto, lograr una resección R0 es el objetivo principal en el tratamiento quirúrgico de los tumores de la UEG.
Se han descrito algunos estándares mínimos, uno de ellos es la extensión del margen proximal mayor de cinco cm in vivo o de dos cm ex-vivo 11,31.
En este estudio los datos para esta variable fueron obtenidos del reporte de patología con una mediana superior a dos cm, y una incidencia de márgenes positivos (longitudinal o circunferencial) del 20 %, encontrándose una asociación con la vía transabdominal en todos los casos, lo que refleja la dificultad técnica que puede tener este abordaje para lograr un margen seguro en algunos pacientes con tumores Siewert II.
En la literatura se reporta una incidencia de márgenes positivos en el rango del 3-40 % 32, con un impacto negativo en los desenlaces a largo plazo, sobre todo en los pacientes en estadios tempranos. Así mismo, para esta serie la supervivencia a tres años fue significativamente menor en estos pacientes comparados con el grupo general (41,6 % vs 68,2 %), sin relación con la recaída locorregional.
Otro de los estándares en el manejo quirúrgico de los tumores de la UEG es la linfadenectomía radical, enfatizando no solo en la necesidad de un mínimo de 15 ganglios resecados, sino también en una disección acorde con la ubicación del tumor y su extensión esofágica.
Este objetivo al igual que el margen adecuado se ha estudiado con relación al tipo de abordaje, debido a que la vía transabdominal podría limitar la disección de los ganglios mediastinales medios y superiores, subestimando su compromiso 11,31. Para esta serie, la media de ganglios resecados fue de 20 y se reportó un 37 % de pacientes con una linfadenectomía inferior a 15 ganglios, siendo más frecuente para el abordaje por esofagectomía de dos y tres vías, sin embargo, esta variable no tuvo asociación con la recaída locorregional o a distancia.
Conclusiones – Diagnóstico y Tratamiento de los Tumores de la Unión Esofagogástrica
A pesar de que los resultados de esta serie corresponden a un estudio retrospectivo, aportan una información valiosa y fácilmente reproducible en otras instituciones del país.
En esta serie encontramos que la mortalidad estuvo directamente relacionada con la recaída, mientras que las variables asociadas a una mayor supervivencia fueron los tumores Siewert II, pacientes que recibieron neoadyuvancia y quienes presentaron respuesta patológica completa.
También encontramos que a pesar de tener una linfadenectomía inferior en el abordaje combinado y un margen positivo más frecuente en el abordaje transabdominal, la diferencia en la supervivencia no fue significativa con la reportada en otros estudios, por tanto, podríamos concluir que no es solo uno, sino varios los factores que en conjunto influyen en los desenlaces oncológicos de los pacientes.
Cumplimiento de normas éticas – Diagnóstico y Tratamiento de los Tumores de la Unión Esofagogástrica
Consentimiento informado: este trabajo de investigación siguió los principios establecidos en los lineamientos de Buenas Prácticas Clínicas del Comité Internacional de Armonización y los principios éticos de la Declaración de Helsinki, y de acuerdo a la resolución 008430 de 1993 del Ministerio de Salud de la República de Colombia, se considera un estudio sin riesgo.
El comité de ética en Investigaciones del Instituto Nacional de Cancerología aprobó este trabajo de investigación.
Conflicto de interés: los autores declararon no tener conflictos de interés.
Fuente de financiación: los recursos de financiación de este proyecto de investigación provienen en su totalidad de aportes de los autores.
Contribución de los autores:
– Concepción y diseño del estudio: Raúl Pinilla-Morales, Jorge Vélez-Bernal.
– Adquisición de datos: Jorge Vélez-Bernal, Julián Meza- Rodríguez, Jairo Ospina-Gaitán, Jenith Lagos, Angélica Rodríguez–Peralta.
– Análisis e interpretación de datos: Raúl Pinilla-Morales, Silvia Guerrero-Macías, Ricardo Oliveros-Wilches, Angélica Rodríguez–Peralta.
– Redacción del manuscrito: Raúl Pinilla-Morales, Silvia Guerrero-Macías, Jorge Vélez, Angélica Rodríguez– Peralta.
– Revisión crítica: Raúl Pinilla-Morales, Ricardo Oliveros- Wilches, Silvia Guerrero-Macías.
Referencias – Diagnóstico y Tratamiento de los Tumores de la Unión Esofagogástrica
1. International Agency for Research on Cancer. IARC: Global Cancer Observatory, Cancer Today: GCO. Fecha de consulta 20 de julio de 2022. Disponible en: https://gco.iarc.fr/today
2. Zhang Y. Epidemiology of esophageal cancer. World J Gastroenterol. 2013;19:5598-606. http://dx.doi.org/10.3748/wjg.v19.i34.5598
3. Arnold M, Laversanne M, Brown LM, Devesa SS, Bray F. Predicting the future burden of esophageal cancer by histological subtype: international trends in incidence up to 2030. Am J Gastroenterol. 2017;112:1247-55. https://doi.org/10.1038/ajg.2017.155
4. De Barros SG, Vidal RM, Luz LP, Ghisolfi ES, Barlem GG, Komlós F, et al. Prevalência de adenocarcinoma do esôfago e da junção esofagogástrica durante 10 anos num centro de referência para câncer no sul do Brasil. Arq Gastroenterol. 1999;36:32-6. https://pubmed.ncbi.nlm.nih.gov/10511877/
5. Ulloa-Ochoa P, Palomeque-Bueno J, Vecilla-Chancay J. Adenocarcinoma de la unión esofagogástrica y su resolución quirúrgica en Guayaquil, Ecuador. Revista Médica Sinergia. 2019;4:e276. https://doi.org/10.31434/rms.v4i9.276
6. Butte JM, Becker F, Visscher A, Waugh E, Meneses M, Court I, et al. Adenocarcinoma of the esophagogastric junction: retrospective analysis of 39 patients. Rev Med Chile. 2010;138:53-60. https://dx.doi.org/10.4067/s0034-98872010000100007
7. Grotenhuis BA, Wijnhoven BP, Poley JW, Hermans JJ, Biermann K, Spaander MC, et al. Preoperative assessment of tumor location and station-specific lymph node status in patients with adenocarcinoma of the gastroesophageal junction. World J Surg. 2013;37:147- 55. https://doi.org/10.1007/s00268-012-1804-9
8. Siewert JR, Stein HJ. Classification of adenocarcinoma of the oesophagogastric junction. Br J Surg. 1998;85:1457- 9. https://doi.org/10.1046/j.1365-2168.1998.00940.x
Bibliografías – Diagnóstico y Tratamiento de los Tumores de la Unión Esofagogástrica
9. Escrig-Sos J, Gómez-Quiles L, Maiocchi K. The 8th edition of the AJCC-TNM classification: New contributions to the staging of esophagogastric junction cancer. Cir. Esp. 2019;97:432-7. https://doi.org/10.1016/j.ciresp.2019.03.006
10. Kumagai K, Sano T. Revised points and disputed matters in the eighth edition of the TNM staging system for gastric cancer. Jpn J Clin Oncol. 2021;51:1024-7. https://doi.org/10.1093/jjco/hyab069
11. Hayashi T, Yoshikawa T. Optimal surgery for esophagogastric junctional cancer. Langenbecks Arch Surg. 2022;407:1399-1407. https://doi.org/10.1007/s00423-021-02375-7
12. Zhao X, Ren Y, Hu Y, Cui N, Wang X, Cui Y. Neoadjuvant chemotherapy versus neoadjuvant chemoradiotherapy for cancer of the esophagus or the gastroesophageal junction: A meta-analysis based on clinical trials. PLoS One. 2018;13:e0202185. https://doi.org/10.1371/journal.pone.0202185
13. Kurokawa Y, Takeuchi H, Doki Y, Mine S, Terashima M, Yasuda T, et al. Mapping of lymph node metastasis from esophagogastric junction tumors: a prospective nationwide multicenter study. Ann Surg. 2021;274:120-7. https://doi.org/10.1097/sla.0000000000003499
14. Mine S, Sano T, Hiki N, Yamada K, Kosuga T, Nunobe S, Yamaguchi T. Proximal margin length with transhiatal gastrectomy for Siewert type II and III adenocarcinomas of the oesophagogastric junction. Br J Surg. 2013;100:1050-4. https://doi.org/10.1002/bjs.9170
15. Okereke IC. Management of gastroesophageal junction tumors. Surg Clin North Am. 2017;97:265-75. https://doi.org/10.1016/j.suc.2016.11.004
16. Parry K, Haverkamp L, Bruijnen RC, Siersema PD, Ruurda JP, van Hillegersberg R. Surgical treatment of adenocarcinomas of the gastro-esophageal junction. Ann Surg Oncol. 2015;22:597-603. https://doi.org/10.1245/s10434-014-4047-1
Lecturas Recomendadas – Diagnóstico y Tratamiento de los Tumores de la Unión Esofagogástrica
17. Hulscher JB, van Sandick JW, de Boer AG, Wijnhoven BP, Tijssen JG, Fockens P, et al. Extended transthoracic resection compared with limited transhiatal resection for adenocarcinoma of the esophagus. N Engl J Med. 2002;347:1662-9. https://doi.org/10.1056/nejmoa022343
18. Sasako M, Sano T, Yamamoto S, Sairenji M, Arai K, Kinoshita T, et al; Japan Clinical Oncology Group (JCOG9502). Left thoracoabdominal approach versus abdominal-transhiatal approach for gastric cancer of the cardia or subcardia: a randomised controlled trial. Lancet Oncol. 2006;7:644-51. https://doi.org/10.1016/s1470-2045(06)70766-5
19. Heger P, Blank S, Gooßen K, Nienhüser H, Diener MK, Ulrich A, et al. Thoracoabdominal versus transhiatal surgical approaches for adenocarcinoma of the esophagogastric junction-a systematic review and meta-analysis. Langenbecks Arch Surg. 2019;404:103-13. https://doi.org/10.1007/s00423-018-1745-3
20. Verlato G, De Manzoni, G. Epidemiology and risk factors. In: Giacopuzzi S, Zanoni A, de Manzoni G, eds. Adenocarcinoma of the Esophagogastric Junction. Cham: Springer; 2017. https://doi.org/10.1007/978-3-319-28776-8_1
21. Carneiro F, Moutinho C, Pera G, Caldas C, Fenger C, Offerhaus J, et al. Pathology findings and validation of gastric and esophageal cancer cases in a European cohort (EPIC/EUR-GAST). Scand J Gastroenterol. 2007;42:618- 27. https://doi.org/10.1080/00365520601101641
22. El-Serag HB, Mason AC, Petersen N, Key CR. Epidemiological differences between adenocarcinoma of the oesophagus and adenocarcinoma of the gastric cardia in the USA. Gut. 2002;50:368-72. https://doi.org/10.1136/gut.50.3.368
23. Pedrazzani C, Bernini M, Giacopuzzi S, Pugliese R, Catalano F, Festini M, et al. Evaluation of Siewert classification in gastro-esophageal junction adenocarcinoma: What is the role of endoscopic ultrasonography? J Surg Oncol. 2005;91:226-31. https://doi.org/10.1002/jso.20302
24. Chevallay M, Bollschweiler E, Chandramohan SM, Schmidt T, Koch O, Demanzoni G, et al. Cancer of the gastroesophageal junction: a diagnosis, classification, and management review. Ann N Y Acad Sci. 2018;1434:132- 8. https://doi.org/10.1111/nyas.13954
Fuentes Bibliográficas – Diagnóstico y Tratamiento de los Tumores de la Unión Esofagogástrica
25. Yamashita H, Seto Y, Sano T, Makuuchi H, Ando N, Saako M, et al. Results of a nation-wide retrospective study of lymphadenectomy for esophagogastric junction carcinoma. Gastric Cancer. 2017;20(Suppl 1):69-83. https://doi.org/10.1007/s10120-016-0663-8
26. Charalampakis N, Tsakatikas S, Schizas D, Kykalos S, Tolia M, Fioretzaki R, et al. Trimodality treatment in gastric and gastroesophageal junction cancers: Current approach and future perspectives. World J Gastrointest Oncol. 202215;14:181-202. https://doi.org/10.4251/wjgo.v14.i1.181
27. Kamarajah SK, Griffiths EA; Oesophago-Gastric Anastomotic Audit (OGAA) Collaborative, Writing group list in the end of manuscript & co-authors listed in the Appendix. Postoperative and pathological outcomes of CROSS and FLOT as neoadjuvant therapy for esophageal and junctional adenocarcinoma: an international cohort study from the Oesophagogastric Anastomosis Audit (OGAA). Ann Surg. 2022; Online ahead of print. https://doi.org/10.1097/sla.0000000000005394
28. Kamarajah SK, Phillips AW, Griffiths EA, Ferri L, Hofstetter WL, Markar SR. Esophagectomy or total gastrectomy for Siewert 2 Gastroesophageal Junction (GEJ) Adenocarcinoma? A registry-based analysis. Ann Surg Oncol. 2021;28:8485-94. https://doi.org/10.1245/s10434-021-10346-x
29. Haverkamp L, Ruurda JP, van Leeuwen MS, Siersema PD, van Hillegersberg R. Systematic review of the surgical strategies of adenocarcinomas of the gastroesophageal junction. Surg Oncol. 2014;23:222-8. https://doi.org/10.1016/j.suronc.2014.10.004
Reseñas Bibliográficas – Diagnóstico y Tratamiento de los Tumores de la Unión Esofagogástrica
30. Takeuchi M, Kawakubo H, Matsuda S, Mayanagi S, Irino T, Okui J, et al. Association of anastomotic leakage with long-term oncologic outcomes of patients with esophagogastric junction cancer. World J Gastrointest Surg. 2022;14:46-55. https://doi.org/10.4240/wjgs.v14.i1.46
31. Groth SS, Virnig BA, Whitson BA, DeFor TE, Li ZZ, Tuttle TM, et al. Determination of the minimum number of lymph nodes to examine to maximize survival in patients with esophageal carcinoma: data from the Surveillance Epidemiology and End Results database. J Thorac Cardiovasc Surg. 2010;139:612-20. https://doi.org/10.1016/j.jtcvs.2009.07.017
32. Barbour AP, Rizk NP, Gonen M, Tang L, Bains MS, Rusch VW, Coit DG, Brennan MF. Adenocarcinoma of the gastroesophageal junction: influence of esophageal resection margin and operative approach on outcome. Ann Surg. 2007;246:1-8. https://doi.org/10.1097/01.sla.0000255563.65157.d2
Autores – Diagnóstico y Tratamiento de los Tumores de la Unión Esofagogástrica
1 Raúl Pinilla-Morales, Médico, especialista en Cirugía general y en Gastroenterología y endoscopia digestiva; jefe, Departamento de Cirugía Gastrointestinal,
Instituto Nacional de Cancerología; profesor asistente, Facultad de Medicina, Universidad Nacional de Colombia, Bogotá, D.C., Colombia.
2 Silvia Guerrero-Macías, Médico, especialista en Cirugía general, fellow Cirugía Oncológica, Universidad Militar Nueva Granada, Instituto Nacional de
Cancerología, Bogotá, D.C., Colombia.
3 Jorge Vélez-Bernal, Médico, especialista en Cirugía general, Instituto Nacional de Cancerología, Bogotá, D.C., Colombia.
4 Julián Meza-Rodríguez, Médico, especialista en Cirugía general y en Cirugía oncológica, Clínica La Estancia, Popayán, Colombia.
5 Jairo Ospina-Gaitán, Médico, especialista en Cirugía general y Cirugía gastrointestinal y endoscopia digestiva, Liga de Lucha Contra el Cáncer, Seccional
Bogotá, Bogotá, D.C., Colombia.
6 Jenith Lagos, Médica, especialista en Cirugía general, fellow Cirugía Vascular, Universidad de Antioquia, Medellín, Colombia.
7 Angélica Rodríguez–Peralta, Médica, Departamento de Cirugía Gastrointestinal, Instituto Nacional de Cancerología, Bogotá, D.C., Colombia.
8 Ricardo Oliveros-Wilches, Médico, especialista en Cirugía general y en Cirugía gastrointestinal y endoscopia digestiva, Departamento de Cirugía Gastrointestinal, Instituto Nacional de Cancerología, Bogotá, D.C., Colombia.
Fecha de recibido: 08/09/2022 – Fecha de aceptación: 22/11/2022 – Publicación en línea: 29/04/2023
Correspondencia: Angélica Rodríguez–Peralta, Calle 1 # 9-85, Instituto Nacional de Cancerología, Bogotá, D.C., Colombia. Teléfono: +57 312 5170622. Dirección electrónica: angiemeponasi@hotmail.com
Citar como: Pinilla-Morales R, Guerrero-Macías S, Vélez-Bernal J, Meza-Rodríguez J, Ospina-Gaitán J, Lagos J, Rodríguez–Peralta A, Oliveros-Wilches R. Diagnóstico y tratamiento de los tumores de la unión esofagogástrica. Experiencia en el Instituto Nacional de Cancerología. Rev Colomb Cir. 2023;38:447-58. https://doi.org/10.30944/20117582.2209
Este es un artículo de acceso abierto bajo una Licencia Creative Commons – BY-NC-ND https://creativecommons.org/licenses/by-nc-nd/4.0/deed.es