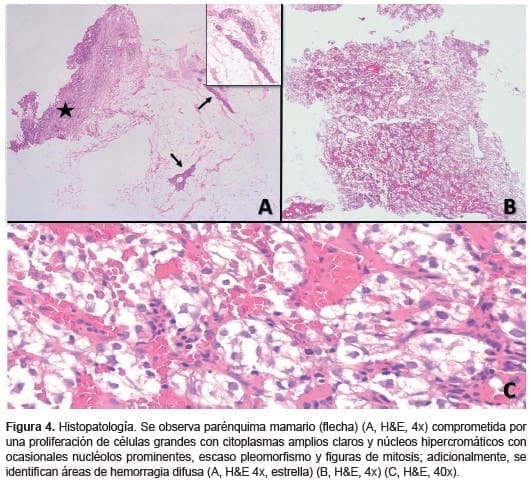
En los cortes histopatológicos de la biopsia se observó proliferación de células con citoplasmas claros, con poco pleomorfismo y figuras de mitosis (figura 4). Se acompañó con estudios de inmunohistoquímica que mostraron positividad para CK, CD10 y RCC, con un índice de proliferación del 10 % (figura 5). Adicionalmente, se observó positividad para CD68 en histiocitos difusos acompañantes de las células neoplásicas. Se encontró, así mismo, positividad débil focal para S100; el CD34 fue positivo en los espacios vasculares. No se observó reactividad en las células tumorales para HMB45, p63, y miosina de cadenas pesadas.
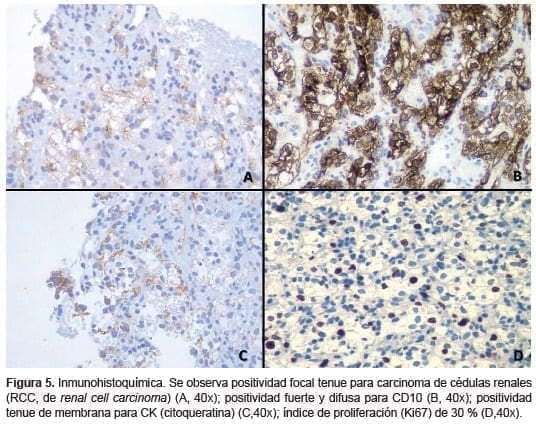
Teniendo en cuenta los antecedentes de la paciente, y apoyados en la histopatología de la lesión y los estudios de inmunohistoquímica, se concluyó que la paciente cursaba con metástasis mamaria de carcinoma de células claras del riñón.
Discusión
En 1903, Trevisthick reportó la primera metástasis a la mama de un tumor extramamario identificado como un linfoma de alto grado2; sin embargo, algunos autores excluyen los casos de infiltración por linfomas, al considerar que el tejido linfoide se encuentra en cualquier parte del organismo, por lo que no cumplen todos los criterios para clasificarlos como verdaderas metástasis y por tanto se le calificarían como infiltraciones secundarias. En 1936, Dawson describió el caso de una mujer de 25 años con compromiso difuso de ambas mamas por un adenocarcinoma gástrico de células en anillo de sello, considerándose el primer caso descrito de un tumor sólido con metástasis en mama1.
El carcinoma de células renales representa aproximadamente el 5 % de todas las neoplasias epiteliales en el mundo, de las cuales el carcinoma de células claras del riñón es el tercer tumor más común del tracto genitourinario, dando cuenta de aproximadamente el 3 % de todas las neoplasias y el 85 % de los carcinomas de células renales6-9. Es más común en hombres que en mujeres, en una proporción de 1.5:1, y la mayoría de los casos ocurren entre los 50 a 70 años de edad. El cuadro clínico clásico está conformado por dolor, hematuria y masa palpable en flanco, que se observa en hasta un 9 % de los casos10.
Cerca del 25 al 30 % de los pacientes tienen tendencia a metastatizar usualmente pulmón (70 %), ganglios linfáticos (55 %), hueso (42 %), hígado (41 %), glándula adrenal (15 %) y cerebro (11 %), y otro 20 % experimentan recurrencia o enfermedad metastásica después de la nefrectomía6-9. Se han descrito otros casos de metástasis en lugares poco frecuentes como páncreas (0,25-3 %)11,12, cabeza y cuello (8-14 %)13-17 y ovario18.
Las metástasis mamarias de origen renal corresponden sólo al 3 % de todos los tumores metastásicos en esta localización6-9.
En la literatura se han descrito aproximadamente 25 casos de metástasis de carcinoma de células claras del riñón a la mama, 11 de los cuales acaecieron con una metástasis como signo inicial de la enfermedad y 14 como una lesión metacrónica posterior a una nefrectomía y de estos, 2 fueron lesiones bilaterales6.
Desde el punto de vista clínico, las lesiones metastásicas a la mama se manifiestan con edema no doloroso con rápido crecimiento7. A diferencia de las neoplasias primarias, la piel frecuentemente no está involucrada y el compromiso axilar es variable, describiéndose entre un 14 a 42 % de los casos; se ha detectado presentación bilateral en un 8 a 26 % de los casos descritos7,8.
De otro lado, para la valoración radiológica de la mama se requieren tres herramientas diagnósticas: mamografía, ecografía mamaria y resonancia magnética nuclear, que ayudaría a definir cuáles lesiones requerirán evaluación con métodos invasivos que incluyan aspiración con aguja fina, biopsias con aguja gruesa o biopsias escisionales3. En la mamografía se observan lesiones bien circunscritas, sin evidencia de microcalcificaciones7. En las ecografías mamarias suele observarse una lesión con características morfológicas sospechosas debido a vascularización intensa y ausencia de elasticidad. Por su parte, en la resonancia magnética nuclear, se observa captación rápida del agente de contraste en el sitio de la lesión, lo cual confirmaría la hipótesis de una lesión expansiva3.
Desde el punto de vista histológico, el carcinoma de células renales recuerda a un carcinoma mamario de células claras, por tanto se requieren estudios de inmunohistoquímica para PAX2, PAX8, MUC1, CD10, y anticuerpo monoclonal del carcinoma de células renales (RCCma), que ayudan a confirmar el origen renal1.
El curso del carcinoma de células claras renales es extremadamente variable e impredecible, tanto en cuanto a su clínica como a sus metástasis. Muchos pacientes con carcinoma de células renales desarrollan múltiples metástasis y es frecuente la muerte en los siguientes diez años7. El 60 % presenta en algún momento de la evolución de su enfermedad una metástasis a distancia, con una mediana de supervivencia a 3 y 5 años del 4,4 % y 17 % de los casos, respectivamente. El tratamiento de las lesiones secundarias de la mama difiere del de los tumores primarios. Por un lado, los márgenes de una lumpectomía deben ser muy amplios debido a que las lesiones metastásicas tienden a ser múltiples, así que con frecuencia es difícil conseguir un margen quirúrgico libre. Por otro lado, la valoración de ganglios linfáticos axilares aún es controvertida; sin embargo, se cree que debido al mecanismo de diseminación, al tratarse de una lesión metastásica, no es útil la biopsia de ganglio centinela ni el vaciamiento ganglionar. El tratamiento de elección para pacientes con metástasis aisladas es la mastectomía sin vaciamiento axilar5,6,8. Pese a lo anterior, en una serie de casos de metástasis mamarias, como aquella publicada en 2013 por DeLair et al. evidenciaron que en un 14 % de los casos se podía encontrar lesión que involucraba la mama y los ganglios axilares ipsilaterales, y hasta en un 8% se halló compromiso solamente de ganglios axilares4. De lo expuesto, es posible concluir que aún se requiere mayor estudio de estas lesiones de modo que puedan dilucidarse las mejores estrategias para el manejo quirúrgico de las metástasis mamarias con base en el origen histológico de las mismas.
En cuanto al tratamiento quimioterapéutico y con hormonoterapia para las metástasis de carcinoma de células claras del riñón, se considera ineficaz, con tasas de respuesta inferiores al 5 % y de corta duración. Con la inmunoterapia se han logrado tasas de respuesta del 15 al 20 %, algunas de ellas de larga duración6,8. La introducción de inhibidores de la tirosina kinasa (TKIs) y mTOR ha modificado el escenario terapéutico en pacientes con carcinoma de células renales metastásico, reemplazando la inmunoterapia como tratamiento de elección; no obstante, se requieren nuevos estudios clínicos y moleculares con el fin de optimizar el uso de esos nuevos agentes terapéuticos para las metástasis de carcinomas de células renales9.
Conclusión
Las metástasis a mama de otras neoplasias, son infrecuentes; sin embargo, deben formar parte de los diagnósticos diferenciales planteados en casos donde previamente se conozca la historia oncológica, y en aquellos en los cuales los hallazgos histológicos no sean los esperados en una neoplasia primaria.
Referencias
1. Hoda S. Metastases in the breast from nonmamary neoplasms. In: Hoda S, Brogi E, Koerner F, Rosen P. Rosen’s Breast Pathology. Fourth edition. Philadelphia: Lippincott Williams & Wilkins; 2014. p. 937-55.
2. Pinto D, Carballo P, Lamas G, Montesinos M, Debonis D. Metástasis en la mama de carcinoma renal. Rev Argent Cirug. 2011;100(1-2):36-8.
3. Botticelli A, De Francesco G, Di Stefano D. Breast metastasis from clear cell renal cell carcinoma. J Ultrasound. 2013;16:127-30.
4. DeLair D, Corben A, Catalano J, Vallejo C, Brogi E, Tan L. Non-mammary metastases to the breast and axilla: a study of 85 cases. Mod Pathol. 2013;26:343-9. doi: 10.1038/ modpathol.2012.191.
5. Bortnik S, Cohen D, Leider-Trejo L, Ron I. Breast metastasis from a renal cell carcinoma. IMAJ. 2008;10:736–7.
6. Falcoa G, Buggib F, Sannab P, Dubinic A, Folli S. Breast metastases from a Renal Cell Carcinoma. A case report and review of the literature. Int J Surg Case Rep. 2014;5:193–5. doi: 10.1016/j.ijscr.2014.01.019.
7. Alzaraa A, Vodovnik A, Montgomery H, Saeed M, Sharma N. Breast metastasis from a renal cell cancer. World J Surg Oncol. 2007;5:1-4. doi: 10.1186/1477-7819-5-25.
8. Fírvida J, Calvo J, Martínez F, Salgado M. Metástasis mamaria como manifestación inicial de un carcinoma renal. Arch Esp Urol. 2005;57; 67-9.
9. Santoni M, Conti A, Procopio G, Porta C, Ibrahim T, Barni S, et al. Bone metastases in patients with metastatic renal cell carcinoma: are they always associated with poor prognosis? J Exp Clin Cancer Res. 2015;34:1-9. doi: 10.1186/s13046-015-0122-0.
10. Shuck C, Morales G, Fernández A, Vázquez, Castellano M., Pacheco C, et al. Metástasis de carcinoma de células claras de riñón a bazo. Rev Mex Urol. 2007;67:124-8.
11. Oneil N, Chopra P. Pancreatic metastasis from renal carcinoma managed by whipple resection. A case report and literature review of metastatic pattern, surgical management and outcome. J Pancreas (Online) 2009;10:413-8.
12. Markinez I, Jiménez R, Ruiz I, Villarreal E, Lizarazu A, Borda N, et al. Pancreatic metastases due to renal carcinoma: our cases and a literature review. Cir Esp. 2013;91:90–5. doi: 10.1016/j.cireng.2012.07.003.
13. Ramôa F, Souza R, Ficarra G, Silveira A, Carlos R, Kowalski LP, et al. Metastatic renal cell carcinoma to the oral cavity and clear cell mucoepidermoid carcinoma: comparative clinicopathologic and immunohistochemical study. Oral Surg Oral Med Oral Pathol Oral Radiol Endod. 2010;109:22-7. doi: https://doi. org/10.1016/j.tripleo.2009.12.006.
14. Jayasooriyaa P, Gunarathnaa I, Attygallab A, Tilakaratne W. Metastatic renal cell carcinoma presenting as a clear cell tumour in the head and neck región. Oral Oncology. 2004;40:50–3. Doi: 10.1016/j.ooe.2003.12.005.
15. Patiño B, Lorenzo F, Martín R, Alvarez A, López-Cedrún J. Metastasic renal cell carcinoma presenting as a parotid tumor. Oral Surg Oral Med Oral Pathol Oral Radiol Endod. 2005;99:554-7. doi: 10.1016/j.tripleo.2004.08.007.
16. Abbaszadeh H, Motallebnejad M, Rajabi M. Metastatic renal cell carcinoma presenting as a clear-cell tumor in tongue: a case report. Iran J Otorhinolaryngol. 2014;26:185-90.
17. Mogedas A, Rubio J, Gutiérrez J, Bordonaba S, Pamias J, Raspalla G, et al. Metástasis parotídea de un carcinoma renal: A propósito de un caso. Rev Esp Cir Oral Maxilofac. 2013;35:83–6. doi:10.1016/j.maxilo.2011.08.009.
18. Ruiz-Reyes R, Jordán-Alonso A, Madruga-Vásquez K, Fernández-Cedeño O. Metástasis ovárica de carcinoma de células renales: presentación de un caso y revisión de la literatura. Rev Med Electrón. 2012;34:609-702. Fecha de consulta: 17 de diciembre de 2017. Disponible en: http://www.revmatanzas.sld.cu/revista%20medica/ano%202012/vol6%202012/tema08.htm.
