Existen menos de 50 casos reportados en la literatura científica y se ubican principalmente en la cola del páncreas; entre el 60 y el 90 % de estos tumores son malignos. Corresponden a menos del 1 % de los carcinoides gastrointestinales y son de mejor pronóstico. Estos tumores secretan serotonina y taquicininas, lo cual causa rubor o rubefacción, diarrea y dolor abdominal.
Evaluación bioquímica y hormonal
Los biomarcadores consisten en expresiones celulares, bioquímicas o moleculares que se pueden rastrear o medir mediante herramientas tecnológicas que facilitan la predicción, aclarar la etiología, hacer el diagnóstico, y valorar la evolución (progresión o regresión) de la enfermedad y el resultado del tratamiento 25.
Los biomarcadores permiten integrar la génesis tumoral y las manifestaciones clínicas, lo cual repercute en la estrategia terapéutica; sin embargo, en forma aislada, no permiten hacer el diagnóstico. Entre sus ventajas están: se correlacionan con la carga tumoral, conducen al diagnóstico temprano, evalúan la enfermedad residual mínima, apoyan la elección de determinada modalidad diagnóstica compleja, y pueden demostrar el éxito o el fracaso del tratamiento 26.
Entre sus desventajas, se incluyen: no estar disponible en todos los centros, los altos costos, su difícil uso en enfermedades avanzadas, y la variabilidad en la sensibilidad y la especificidad. Debido a la complejidad, la heterogeneidad y el fenotipo de los tumores neuroendocrinos de páncreas, no existe un único biomarcador para ellos; son múltiples y se pueden evaluar en tejidos, sangre y orina, así como con imágenes combinadas con radionúclidos, con gran variabilidad en la sensibilidad, la especificidad y la reproducibilidad debido a cambios en la metodología y la estandarización de las técnicas.
Biomarcadores generales
Cromogranina A. Es un marcador ampliamente usado en la última década en tejido y en sangre; se expresa en los sujetos sanos, en enfermedad neoplásica y no neoplásica. Su rendimiento es superior cuando se ha confirmado el tumor neuroendocrino y es ineficaz como marcador diagnóstico aislado. Se correlaciona con la carga tumoral, con la enfermedad metastásica y con el pronóstico. No se correlaciona con la funcionalidad ni la localización tumoral. Las muestras sanguíneas se deben tomar en ayunas con suspensión previa de los inhibidores de bomba de protones, por lo menos, dos semanas antes 27.
Hay gran variabilidad entre los ensayos comerciales para la cromogranina A 28.
Pancreastatina. Es el polipéptido más corto de la cromogranina A y se encuentra elevada en 58 a 81 % de los tumores neuroendocrinos; se puede medir en sangre y orina 29. No se correlaciona con la carga tumoral, la localización, la agresividad ni la supervivencia. Se afecta por la ingestión de alimentos o la hiperglucemia 30.
Cromogranina B y C. El rendimiento de las cromogranina B y C en tumores neuroendocrinos es inferior al de la cromogranina A. Al parecer, no se afectan por el deterioro de la función renal o el uso de inhibidores de bomba de protones 31.
Enolasa neuronal específica. Está presente en neuronas y células neuroendocrinas. Hasta el momento, no tiene una buena utilidad clínica 32.
Biomarcadores específicos
Polipéptido pancreático. Se produce en las células neuroendocrinas del páncreas y del colon, desempeñando un papel en la autorregulación de la secreción. Su utilidad clínica es limitada 33,34.
Gastrina. Es un marcador que se puede evaluar en sangre y tejido. En caso de gastrinoma, la gastrina sérica en ayunas es mayor de 100 pg/ml o más de 10 veces el límite superior, el pH gástrico es menor de 2, la salida de ácido basal es mayor de 15 mEq/L y la prueba de secretina muestra un aumento de la secreción de gastrina.
Es importante recordar que la gastrinemia es alta en la atrofia gástrica y que los inhibidores de la bomba de protones se deben suspender, al menos, una semana antes de la toma de exámenes y, los antagonistas H2, dos días antes 4,21,35.
Insulina y prueba en ayunas. El diagnóstico y el seguimiento de los insulinomas requieren confirmar: valor de glucosa inferior a 40 mg/dl, insulina mayor de 36 pmol/L, péptido C mayor de 200 pmol/L, proinsulina de más de 5 pmol/L y β-hidroxibutirato inferior a 2,7 mmol/L. Además, se debe documentar la ausencia de sulfonilureas o sus metabolitos en plasma u orina y una buena respuesta terapéutica con el glucagón 21.
Glucagón. Es un marcador que se puede evaluar en sangre y tejido. El síndrome de glucagonoma conlleva valores de glucagón plasmático por encima de 500 pg/ml y elevación de la glucosa en sangre 7,21.
Péptido intestinal vasoactivo. Este marcador se evalúa en sangre. Los niveles encontrados en caso de VIPoma son mayores de 500 pg/ml y, en la diarrea secretoria aguda, mayores de 700 ml/d 21.
Somatostatina. Es un marcador que se evalúa en sangre y tejido. Para el diagnóstico del somatostatinoma, se requiere elevación de la somastotatina sérica y la inmunohistoquímica positiva en el tejido.
Otros biomarcadores menos frecuentes y su síndrome
GRFoma. Causa aumento de la hormona del crecimiento, elevación de la somatomedina C y hábito acromegálico. La prueba de supresión de glucosa para la hormona del crecimiento es positiva, con imágenes que descartan tumores hipofisiarios.
ACTHoma. Produce elevación de la ACTH sérica, del cortisol libre en orina de 24 horas y del cortisol salival de las 11 p.m. La prueba de supresión con dexametasona es positiva y existe hábito cushingoide con coloración parda de la piel. Se deben descartar tumores hipofisiarios y, por medio del cateterismo de los senos petrosos, confirmar la producción extrahipofisiaria.
PTHrp-oma. Produce hipercalcemia, elevación de la PTH-rp y supresión de la PTH endógena.
Tumor neuroendocrino de páncreas que causa síndrome carcinoide asociado a elevación de serotonina y sus metabolitos. Se puede medir el ácido 5-hidroxiindolacético en orina de 24 horas.
Biomarcadores emergentes
Células tumorales circulantes. La detección de células tumorales circulantes se basa en la tecnología que captura la expresión celular de las moléculas de adhesión celular epitelial en varios tumores sólidos. En los tumores neuroendocrinos metastásicos se encuentran células tumorales circulantes detectables en el intestino medio (43 %) y el páncreas (21 %), sin correlación con el índice Ki-67 y la cromogranina A sérica 36. Alrededor del 50 % de los pacientes con tumores neuroendocrinos tienen células tumorales circulantes detectables y se correlacionan con el compromiso hepático 37.
MicroARN. Son ARN no codificantes de pequeño tamaño (19 a 25 nucleótidos) que regulan los mecanismos posteriores a la transcripción en diversos procesos; se encuentran alterados en neoplasias y son potenciales biomarcadores y agentes terapéuticos. Se pueden evaluar en sangre y en tejido, pero hay dificultades para su estandarización y reproducibilidad.
En los tumores neuroendocrinos de páncreas se ha encontrado aumento de la regulación de miR-2, miR-103, miR107, miR-193b. La sobreexpresión de miR-21 se asocia con un alto índice Ki-67 y metástasis hepáticas. La expresión de miR-642 se correlaciona con el índice Ki-67 y la expresión de miR-210 se asocia con enfermedad metastásica. Se ha encontrado disminución de la regulación de miR-584, miR- 1285, miR-550-002410, miR-1290 y miR-1825; la disminución de la regulación sérica del miR- 1290 discrimina los tumores neuroendocrinos de páncreas de los adenocarcinomas 38-40.
Análisis genético por transcripción por PCR, microarreglos. La tasa de mutaciones de los tumores neuroendocrinos de páncreas es de 0,82 por megabase (rango de 0,04 a 4.56) y es baja al compararse con la del adenocarcinoma de páncreas, que reporta 2,64 (rango de 0,65 a 28,2). Múltiples genes candidatos asociados se pueden medir en sangre o tejido fresco. Las pruebas de PCR son estandarizadas y reproducibles, con un coeficiente de variabilidad entre ensayos e intraensayos inferior al 2 %; y no se afectan por edad, sexo, etnia, ayuno o medicación 41,42.
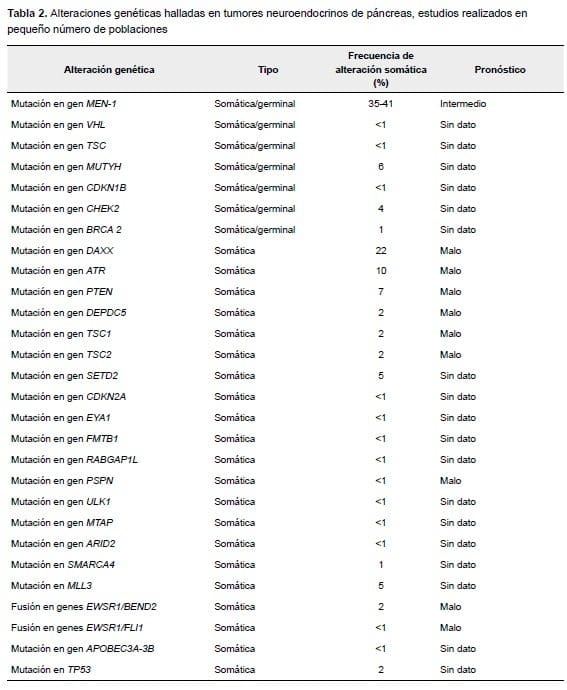
En los tumores neuroendocrinos de páncreas bien diferenciados, se pueden encontrar genes con mutaciones somáticas múltiples, como: MEN1, DAXX, ATRX, TSC, NF1 y MUTYH (tabla 2) 43.
NETest. Permite evaluar, en sangre periférica, la expresión de ARN de 51 genes para identificar tumores neuroendocrinos gastroenteropancréaticos. Ha demostrado buen rendimiento en pacientes con tumores bien y moderadamente diferenciados de intestino medio y páncreas metastásicos 41,42. Hasta marzo de 2018, se había evaluado en 5.207 pacientes de 106 instituciones de Estados Unidos y Europa con una probabilidad diagnóstica mayor del 90 %, un valor predictivo positivo mayor del 92 % y valor predictivo pronóstico mayor del 95 %; se ha evaluado en pretratamiento para la predicción de la respuesta a la terapia con radionúclidos con una exactitud del 93 % 44.
Evaluación radiológica
La evaluación de la estadificación tumoral inicial y el seguimiento recae principalmente en las imágenes diagnósticas como la tomografía computadorizada (TC) y la resonancia magnética (RM). Las técnicas de medicina nuclear combinadas (imágenes híbridas) con TC y RM mejoran la localización de los tumores ocultos y mejoran la estadificación, como la SPECT (TC de emisión monofotónica), la gammagrafía con análogos del receptor de somatostatina (RSST), la tomografía con emisión de positrones (PET) con análogos del RSST y, en algunas ocasiones, la PET con 18F-DOPA o con 18F-FDG. Las innovaciones en medicina nuclear con antagonistas para el RSST y agonistas del receptor GLP-1 (Glucagon-Like Peptide-1), podrían mejorar las imágenes de los tumores neuroendocrinos de páncreas 45.