Guía de Manejo y Revisión de la Literatura
AnaMaríaAristizábal1, YulianaCastrillón1, TatianaGil1, DavidRestrepo1, Katherine Solano2, MarcelaGuevara1, Karen Torres3, Santiago Cuenca3, Jhon Ortiz3, Gabriel J. Echeverri4
Palabras clave: trasplante; trasplante de órganos; selección de donante; obtención de tejidos y órganos; muerteencefálica.
Resumen
El trasplante de órganos es, en muchos casos, la única opción terapéutica para pacientes con enfermedades terminales de diversos órganos esenciales, sin embargo, existe un acentuado desequilibrio entre el número de órganos disponibles y el de potenciales receptores a nivel mundial.
Los donantes con muerte cerebral son la principal fuente de órganos de trasplante y son esenciales las medidas que promueven su reconocimiento temprano para realizar una gestión clínica apropiada. En este contexto, se sabe que el manejo clínico agresivo del donante potencial y el uso de protocolos orientados a determinados objetivos se asocia con un mayor número de órganos trasplantados por donante y a la reducción de las pérdidas de potenciales donantes por paro cardiaco.
Colombia es un país con bajos índices de donación y grandes necesidades de trasplantes, con una lista de espera que cada año aumenta exponencialmente. En esta revisión se exponen las recomendaciones internacionales para el manejo del donante potencial con muerte cerebral, las cuales esperamos se puedan adoptar en los protocolos institucionales para optimizar el manejo de nuestros potenciales donantes en Colombia y, así, aumentar los trasplantes y suplir las necesidades de nuestros pacientes.
Introducción
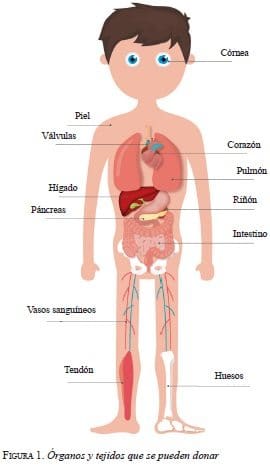
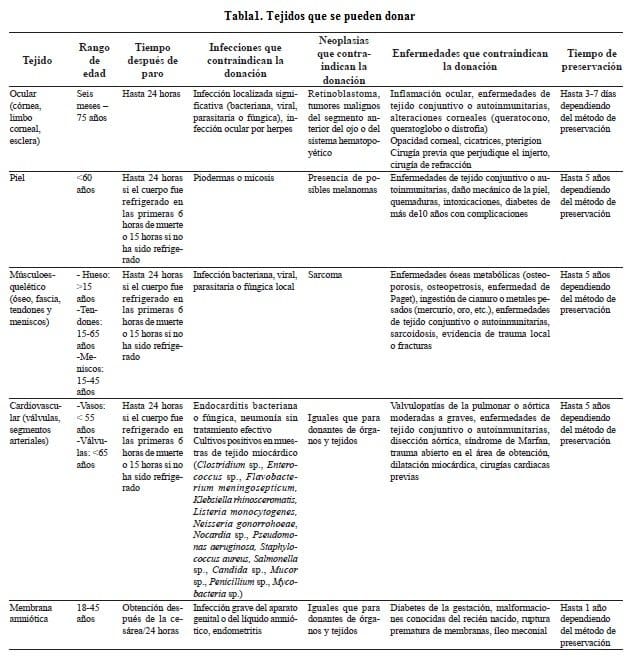
El trasplante de órganos es, en muchos casos, la única opción terapéutica para pacientes con enfermedades terminales de diversos órganos 1 (figura 1, tabla 1). Existe un acentuado desequilibrio entre el número de órganos disponibles y el de potenciales receptores 2. En el Reino Unido, Estados Unidos y Europa, el número de potenciales receptores de trasplantes ha aumentado a más de 133.000, mientras que el número de órganos donados de todas las fuentes no está aumentando lo suficiente para mantener este ritmo de crecimiento 3-5.
Los donantes con muerte cerebral son la principal fuente de órganos de trasplantes. Sin embargo, con la reducción de la mortalidad hospitalaria y el número de pacientes con lesión cerebral que progresa a muerte cerebral en los últimos años, las donaciones después de muerte cerebral también han disminuido, aumentando la disparidad entre la demanda de órganos y el número de trasplantes efectivos 2,6.
Es importante promover medidas que ayuden al reconocimiento temprano de la muerte cerebral, con el fin de realizar una gestión clínica apropiada y ayudar a mitigar esta disparidad 7. En este contexto, se sabe que el manejo clínico agresivo del potencial donante y el uso de protocolos orientados a determinados objetivos se asocia con un mayor número de órganos trasplantados por donante y a la reducción de las pérdidas de potenciales donantes por paro cardiaco 8-11.
El 25 % de los fracasos en la obtención de órganos de donantes con muerte cerebral se le atribuye a la falta de soporte hemodinámico adecuado 5. El inicio temprano de las acciones de mantenimiento facilita el control hemodinámico y la restauración de la función de los órganos que se van a trasplantar, lo cual permite, en teoría, la planificación de la extracción de los órganos en el momento más oportuno 12. No obstante, el retrasar su obtención puede conducir a una mayor inflamación sistémica y a un aumento del riesgo de futuro deterioro clínico y paro cardiaco 2.
Aunque no hay evidencia sobre el efecto del tiempo de mantenimiento en la aparición de paro cardiaco en el donante potencial, las posibilidades de deterioro funcional del injerto justifica la obtención temprana de órganos dentro de un periodo entre 12 y 24 horas después del diagnóstico de muerte cerebral 13.
Las guías de manejo de donantes con muerte cerebral destacan la importancia de un manejo multidisciplinario en la unidad de cuidados intensivos 14,15. Se enfatiza la necesidad de la monitorización temprana para guiar la administración de líquidos y evitar la sobrecarga hídrica. Además, se exalta la importancia de que un intensivista experimentado esté directamente involucrado en el cuidado del donante potencial 16.
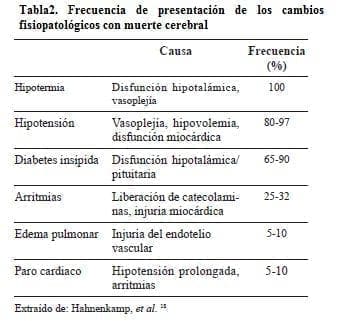
Las consecuencias fisiopatológicas típicas de la muerte cerebral incluyen disfunción cardiovascular (hipotensión y arritmias), pulmonar (edema pulmonar, lesiones pulmonares asociadas al respirador), endocrina (diabetes insípida, hiperglucemia), de la termorregulación (poiquilotermia), renal (daño renal agudo), electrolítica (hipernatremia, hiperpotasemia e hipotasemia), hematológica (coagulación intravascular diseminada) y sistémica (reacción inflamatoria sistémica) 17. En la tabla 2 se muestra la frecuencia de presentación de los diferentes cambios fisiopatológicos 18.
Trasplantes en Colombia
Según cifras del Instituto Nacional de Salud de Colombia, entidad de referencia nacional en donación y trasplante de órganos, en el año 2015 hubo un total de 405 donantes reales de órganos, para una tasa nacional de 8,4 donantes por millón de población, en su mayoría, a expensas de donantes cadavéricos 19.
La lista de espera del Instituto Nacional de Salud al 31 de diciembre del 2015, reportaba 2.029 pacientes que necesitaban órganos sólidos para trasplante y se practicaron 1.204 trasplantes en el país en ese año 19, lo que demuestra la carencia de órganos suficientes para suplir las necesidades. En las figuras 2 y 3 se evidencia la variación de la tasa de donantes y de trasplantes, y el aumento de la lista activa de espera de trasplantes en los últimos años en Colombia.
[enc_su_row][enc_su_column size=”1/2″]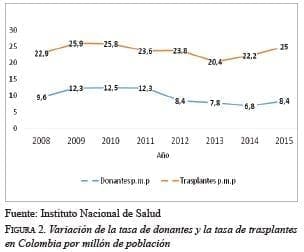 [/enc_su_column]
[/enc_su_column]
[enc_su_column size=”1/2″]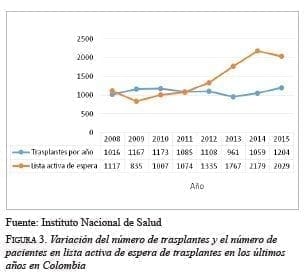 [/enc_su_column][/enc_su_row]
[/enc_su_column][/enc_su_row]
Legislación colombiana
En Colombia existe una amplia reglamentación de todos los aspectos relacionados con la donación y el trasplante de componentes anatómicos, entre ellas, la Ley 73 de 1988, la Ley 919 de 2004 y el Decreto 2493 de 2004, como las más importantes. El Decreto 2493 de 2004, “Regula la obtención, donación, preservación, almacenamiento, transporte, destino y disposición final de componentes anatómicos y los procedimientos de trasplante o implante de los mismos en seres humanos”.
Estas normativas regulan los procesos para la donación de órganos y tejidos de personas fallecidas o vivas con fines de trasplante, los mecanismos de donación, los aspectos técnico-científicos y las medidas sanitarias en caso de incumplimientos.
Recientemente, el Congreso de la República expidió la Ley 1805 de 2016, por medio de la cual se modifican la Ley 73 de 1988 y la Ley 919 de 2004, ampliando la presunción legal de componentes anatómicos para fines de trasplantes u otros usos terapéuticos. Esta ley pretende brindar mayores oportunidades para aquellas personas que padecen enfermedades crónicas termina¬les, atribuyendo la facultad de oponerse a la donación de componentes anatómicos únicamente a la persona que en vida así lo hubiere manifestado formalmente. Además, exige a las instituciones prestadoras de salud (IPS) contar con la capacidad técnica necesaria para detectar oportunamente a los potenciales donantes de acuerdo con los criterios y competencias que establezca el Instituto Nacional de Salud.
1 Médico general, estudiante de diplomado en Coordinación Operativa de Trasplantes, Universidad Icesi, Cali, Colombia
2 Enfermera profesional, estudiante de diplomado en Coordinación Operativa de Trasplantes, Universidad Icesi, Cali, Colombia
3 Médico general, Coordinación Operativa de Trasplantes, Clínica Fundación Valle del Lili, Cali, Colombia
4 Especialista en Cirugía de Trasplante de Órganos Abdominales; director, Centro para la Investigación en Cirugía Avanzada y Trasplantes (CICAT), Universidad Icesi, Cali, Colombia
Fecha de recibido: 22 de enero de 2017
Fecha de aprobación: 21 de febrero de 2017
Citar como: Aristizábal AM, Castrillón Y, Gil T, Restrepo D, Solano K, Guevara M, et al. Manejo actual del donante potencial de órganos y tejidos en muerte cerebral: guía de manejo y revisión de la literatura. Rev Colomb Cir. 2017;32:128-45.
Red de trasplantes en Colombia.
La Red de Donación y Trasplantes de Órganos y Tejidos fue creada por el Ministerio de la Protección Social en el año 2004, mediante el Decreto 2493. Es un sistema de integración de los Bancos de Tejidos y Médula Ósea, IPS habilitadas con programas de trasplantes o implantes, el Instituto Nacional de Salud, las Direcciones Departamentales y Distritales de Salud, y demás entidades del sistema. Busca la coordinación de actividades relacionadas con la promoción, la donación, la extracción, el trasplante y el implante de órganos y tejidos, con el objeto de hacerlos accesibles en condiciones de calidad, en forma oportuna y suficiente a la población, siguiendo los principios de cooperación, eficacia, eficiencia, equidad y solidaridad.
El Instituto Nacional de Salud, como coordinador de la Red, realiza sus funciones de coordinación nacional; para su funcionamiento se dividió al país en seis regionales:
- Regional 1: con sede en Bogotá, D.C., está integrada por Cundinamarca, Tolima, Boyacá, Casanare, Meta, Caquetá, Vichada, Vaupés, Guaviare, Guainía, Putumayo y Amazonas.
- Regional 2: con sede en Medellín, está integrada por Antioquia, San Andrés y Providencia, Chocó, Córdoba y Caldas.
- Regional 3: con sede en Santiago de Cali, está integrada por el Valle del Cauca, Cauca, Nariño, Risaralda y Quindío.
- Regional 4: con sede en Bucaramanga, está integrada por Santander, Norte de Santander, Cesar y Arauca.
- Regional 5: con sede en Barranquilla, está integrada por Atlántico, Bolívar, Magdalena, La Guajira y Sucre.
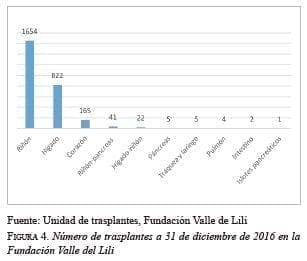
- Regional 6: con sede en Neiva, corresponde al departamento del Huila.Cada regional cuenta con una coordinación regional y, a su vez, con coordinadores operativos de trasplantes en las principales ciudades que, unidos a la coordinación nacional, vigilan el adecuado funcionamiento de la Red.Las IPS donde exista un potencial donante de órganos deben notificar a la red regional de trasplantes a través del personal médico responsable del paciente; de igual forma, deben permitir los procedimientos requeridos por los médicos coordinadores operativos, y por el personal médico y paramédico que realice el rescate de dichos órganos y tejidos (Decreto 2493, artículo 23). Dicha reglamentación fortalece el desarrollo del procedimiento en todo el territorio colombiano, generando un ámbito de seguridad y claridad en las IPS.Experiencia en la Clínica Fundación Valle del LiliEn el año 2015, la principal ciudad generadora de donantes fue Medellín (27,4 %). Sin embargo, la Clínica Fundación Valle del Lili de Cali generó la mayor cantidad de donantes (7,9 % de los donantes reales), seguida del Hospital Pablo Tobón Uribe y el Hospital Universitario San Vicente de Paúl de Medellín, con el 5,4 % cada uno 19.La Fundación Valle del Lili cuenta con una amplia experiencia en trasplantes 20-30. Es una institución en donde desde hace más de 20 años está en marcha el programa de trasplantes; es la única IPS en Colombia donde se practica el trasplante de riñón y páncreas y, en la actualidad, se realizan trasplantes de hígado, páncreas, islotes pancreáticos, riñones, intestino, pulmón y corazón (figura 4).
Diagnóstico de muerte por criterios cerebrales
Con el advenimiento de la tecnología en las unidades de cuidados intensivos y, particularmente, del pulmón artificial en 1959, el cual permitió el control externo de la función respiratoria sin que para ello medie la voluntad del individuo o el mecanismo reflejo de la respiración, se evidenció una nueva situación clínica neurológica a la que Goulon y Mollaret en Francia denominaron ‘coma depassé’ (del que no se regresa) 31,32. Este se caracteriza por un coma profundo arreactivo con ausencia de reflejos del tallo cerebral, en el cual la función respiratoria y el estado hemodinámico del paciente se mantienen por medios externos artificiales.
Sistemáticamente, se fue comprobando por todo el mundo, que este coma depassé representaba una situación neurológica irrecuperable y que inexorablemente estaba seguida, en cuestión de horas o días, por la asistolia irreversible, a pesar de las más concienzudas medidas de mantenimiento. El examen histopatológico de estos individuos mostraba necrosis y descomposición del sistema nervioso central, similar a lo observado en los pacientes que sufren muerte clásica por paro cardiorrespiratorio. Finalmente, el concepto de coma depassé dio paso al de muerte cerebral, según los criterios de Harvard, en 1968 33.
Desde entonces, el concepto de muerte cerebral se ha ido construyendo y modificando a lo largo del tiempo, y ha sido aceptado por la comunidad científica y la legislación de diferentes países. Actualmente, se entiende como “el cese irreversible de todas las funciones del tallo cerebral y la corteza comprobado por un examen neurológico clínico” 34. Dicho diagnóstico cumple los siguientes criterios: lesión estructural cerebral definitiva y de etiología conocida, ausencia de reflejos del tallo encefálico y apnea 35.
Dada la importancia ética y médico-legal, para hacer el diagnóstico se debe certificar la exclusión de condiciones clínicas que simulen la muerte cerebral, como: alteraciones en la oxigenación-hipoxemia, graves alteraciones electrolíticas, metabólicas o endocrinas (hipotermia <32 °C, hipoglucemia, hipofosfatemia, hipotiroidismo), intoxicación o estar bajo efecto de medicación neurodepresora (sedantes, anestésicos, barbitúricos o relajantes musculares) 16,34.
La legislación colombiana a lo largo del tiempo ha establecido quiénes pueden ser donantes y los criterios clínicos que deben cumplir. Actualmente, el Decreto 2493 del 2004 rige las pautas que se deben tener presentes para el diagnóstico de muerte cerebral en Colombia. Indica que debe hacerse por dos o más médicos, uno de los cuales debe ser neurólogo o neurocirujano. Ninguno de ellos puede pertenecer al programa de trasplantes, ya que esto podría generar conflicto de interés. Dichas actuaciones deben constar por escrito en la historia clínica, indicando la valoración de los siete signos y el diagnóstico definitivo de muerte cerebral 36.
El objetivo de la evaluación neurológica es determinar la ausencia de los reflejos de tallo encefálico en la muerte cerebral:
1. pupilas persistentemente dilatadas,
2. ausencia de reflejos pupilares a la luz,
3. ausencia de reflejo corneano, 4.
susencia de reflejos óculo-vestibulares,
5. ausencia de reflejo faríngeo o nauseoso,
6. ausencia de reflejo tusígeno, y
7. ausencia de respiración espontánea.
Prueba de Apnea
Se recomienda continuar la valoración del potencial donante realizando el test de apnea. Su objetivo es estimular el centro respiratorio del tronco encefálico para corroborar la ausencia de respiración espontánea. Es necesario conseguir un estímulo suficiente para activar el centro respiratorio; generalmente, esto se logra al alcanzar una presión parcial de dióxido de carbono (PaCO2)≥60 mm Hg 34.
Inicialmente, se debe verificar la estabilidad hemodinámica del paciente (presión arterial sistólica≥100 mm Hg), habiendo administrado previamente, por lo menos durante 10 minutos, oxígeno al 100 % para alcanzar una presión parcial de oxígeno (PaO2)≥200 mm Hg.
Seguidamente, se debe realizar una gasometría arterial para verificar la cifra de PaCO2 y calcular el tiempo que el paciente debe estar desconectado del respirador para alcanzar niveles de PaCO2 suficientes para estimular el centro respiratorio (generalmente, entre 8 y 10 minutos) 35.
Posteriormente, se desconecta al paciente del respirador y se introduce a través del tubo endotraqueal una sonda de nélaton delgada (máximo 30 % del diámetro del tubo) conectada a una fuente de oxígeno a 6 litros por minuto. Se deben observar el tórax y el abdomen, comprobando que no exista ningún tipo de movimiento respiratorio durante el tiempo previamente calculado para lograr la estimulación del centro respiratorio. Durante este periodo, debe haber monitoría continua de la saturación de oxígeno, la presión arterial y el ritmo cardiaco. Inmediatamente después, se toma una nueva gasometría arterial, previa a la reconexión del respirador. Esta prueba se interpretará como correspondiente a muerte cerebral si hay ausencia de movimiento o esfuerzo respiratorio y si se provoca un aumento de la PaCO2≥60 mm Hg o superior a 20 mm Hg de su valor basal 35.
Si se considera que el potencial donante cumple los criterios para la donación de pulmón, se debe procurar al máximo no desconectarlo del respirador. En estos casos, se puede practicar la prueba de apnea con una válvula de presión positiva continua en la vía aérea, con el fin de asegurar una mejor oxigenación y disminuir el riesgo de complicaciones que se pueden presentar con el método tradicional, tales como la despresurización en la vía aérea y el aumento del colapso alveolar 37.
Se deben tener en cuenta algunos requisitos previos al test de apnea, para disminuir los riesgos de complicaciones y evitar lesiones iatrogénicas durante el mismo; entre estos, están mantener la euvolemia, la normocapnia, la normoxemia y una temperatura ≥36 °C 16. En caso de que durante la prueba se presente una arritmia cardíaca, hipotensión con PAS≤90 mm Hg, desaturación significativa (SpO2≤85 %) o presencia de movimientos respiratorios autonómicos, se debe suspender de inmediato el procedimiento 3.
Prueba de certeza
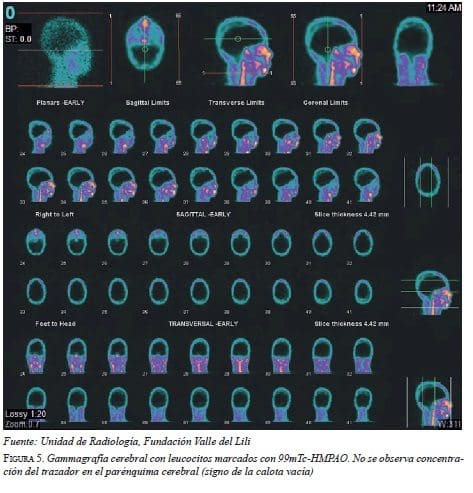
Cuando no sea posible valorar algún reflejo o practicar la prueba de apnea, el Decreto 2493 del 2004 recomienda aplicar una prueba de certeza o estudio imagenológico complementario, tal como la ecografía Doppler transcraneal, la arteriografía cerebral por sustracción digital o la gammagrafía de perfusión cerebral, las cuales evaluarían el paro circulatorio sanguíneo cerebral (figura 5). También, pueden hacerse pruebas que midan la actividad eléctrica neuronal, como el electroencefalograma o los potenciales auditivos evocados 35,38,39.
En el caso del diagnóstico de muerte cerebral en pacientes pediátricos, se tienen en cuenta consideraciones especiales sujetas a la legislación colombiana 36,40. El periodo de observación varía con la edad. En niños entre siete días y dos meses de edad, se requieren dos exploraciones clínicas con electroencefalogramas separados por 48 horas. En niños de dos meses a dos años, se realizan dos exploraciones clínicas con electroencefalogramas separados por 24 horas. En los mayores de dos años, es válido aplicar los mismos criterios diagnósticos que en el adulto.