Óscar Guevara
Palabras clave: colecistectomía laparoscópica; hepatectomía; curva de aprendizaje; historia.
Primero que todo quiero agradecer a la Asociación Colombiana de Cirugía, al Consejo Asesor de Expresidentes y a su Junta Directiva, por el honor de designarme para dictar esta conferencia; al profesor Oswaldo Borráez, por su introducción y por la remembranza del profesor Rafael Casas Morales.
Solamente quiero agregar aquí, la presentación del acta de grado de médico de la Universidad Nacional de Colombia (figura 1), imagen gentilmente cedida por el doctor Herley Aguirre (profesor de Cirugía Plástica y candidato a doctorado en Historia). Cabe destacar el Acta de Grado Nº 2860 del 7 de noviembre de 1952, que tuvo categoría de “Mención Honorífica”, por sus exámenes y por la tesis de grado, titulada “Estudio y plan de fomento del sistema hospitalario en Colombia”. El presidente del acto de graduación era el Ministro de Higiene del momento, doctor Alejandro Jiménez Arango, a quien, paradójicamente, el doctor Casas Morales reemplazaría como Decano de Medicina de la Universidad Nacional de Colombia en 1965, durante la rectoría del doctor José Félix Patiño (El Tiempo, 29 de noviembre de 1965). Notablemente, llevaba apenas 13 años de graduado como médico, cuando se posesionó en la decanatura y ya había sido Secretario General de la Universidad Nacional de Colombia, como muestras de su brillante carrera universitaria.

A continuación se presenta la evolución de la cirugía desde las técnicas de la colecistectomía y la hepatectomía, pasando por la colecistectomía laparoscópica, y cómo la evolución ha llevado al desarrollo de la hepatectomía laparoscópica, procedimiento impensable hace algunos años; todo esto, enmarcado en la importancia del paciente, por lo cual al final se presenta una reflexión sobre la atención centrada en el paciente.
El desarrollo de la colecistectomía laparoscópica
Hoy en día, la colecistectomía es una de las cirugías más practicadas en el mundo. No obstante, para llegar a este punto de la evolución de la técnica, se debe recordar que primero tuvieron que desarrollarse la anestesia, en el siglo XIX 1, y la técnica aséptica, por Lister 2, para que, posteriormente, se empezaran a realizar las cirugías abdominales mayores.
En Berlín, el 15 de julio de 1882, Carl Johan August Lagenbuch realizó la primera colecistectomía y, aunque él describía que la paciente al otro día pudo sentarse a fumar, la cirugía fue realizada en julio y la paciente salió del hospital en septiembre de ese mismo año, es decir que la estancia fue de alrededor de dos meses 3,4.
Posteriormente, hubo otros aportes importantes de cirujanos como John Murphy y Hans Kehr, quien desarrolló el tubo en T, denominado dren de Kehr. Grandes maestros de la cirugía, como William Mayo y Frank Lahey, aportaron al desarrollo de la cirugía de la vesícula y de las vías biliares 5,6. No se puede pasar por alto la contribución de un latinoamericano, Pablo Mirizzi, cirujano argentino quien realizó la primera colangiografía transoperatoria, fundamental en el desarrollo de la cirugía biliar y poseedor de uno de los pocos epónimos que persisten aún en nuestros días: el síndrome de Mirizzi 7.
En Colombia, algunas fuentes mencionan al doctor Zoilo Cuéllar como el primero en practicar una colecistectomía, en 1902 8, y casi todos coinciden en que el doctor Pompilio Martínez, en 1915, realizó la segunda colecistectomía, lo cual indica que pasaron diez años sin que se practicara esta cirugía en el país. Vale la pena mencionar el desarrollo en otras ciudades fuera de Bogotá, pues el doctor Pablo García, en Cali en 1888, ya había realizado la primera colecistostomía.
Una vez aumentó el número de colecistectomías, empezaron a aparecer las dificultades intraoperatorias y posoperatorias. William Mayo, en un artículo en 1905, describió cómo después de practicar 1.100 operaciones de la vesícula biliar con su hermano Charles, hubo varios casos en los cuales tuvieron que resecar el conducto biliar; en uno de ellos, se seccionó accidentalmente el colédoco y se requirió una anastomosis al duodeno, convirtiéndose, tal vez, en el primer reporte de una lesión de la vía biliar 6.
Un poco más adelante, en 1937, Frank Lahey, otro prohombre de la cirugía americana y mundial, describió las estenosis del conducto colédoco después de la cirugía biliar debida a varios factores causales. Presentó una serie de casos muy detallada, con sus respectivos dibujos de lo que él había encontrado en la cirugía y cómo lo había resuelto. De manera interesante, aparece esquematizado el mecanismo de lesión de la vía biliar consistente en la tracción excesiva del cístico en medio de las adherencias, donde el cirujano inadvertidamente pinza la vía biliar común, la secciona y queda ligada 5. Este fue el mismo mecanismo principal de lesión de la vía biliar descrito décadas más tarde, al inicio de la experiencia de la colecistectomía laparoscópica 9.
Dando un salto a los años 80 con la colecistectomía, se llegó al dominio de la técnica con una mortalidad de 0,1 a 0,6 %, una morbilidad de 10 a 15 % y una incidencia de lesiones de la vía biliar de 0,1 a 0,2 %. La estancia hospitalaria era de cuatro días en promedio 10. Con variaciones entre países y entre escuelas, las incisiones que más se utilizaban eran la subcostal derecha y la laparotomía mediana. Recuerdo perfectamente que, al inicio de la residencia, la incisión estándar de una colecistectomía debía ir desde el xifoides hasta el ombligo. Una de las frases preferidas del profesor Federico Peñalosa (q.e.p.d.) era el viejo adagio quirúrgico: “Para cirugías grandes, incisiones grandes”, a lo cual el agregaba… “y cirujanos grandes” (él medía cerca de 1,90 m de estatura).
Pero es, en ese momento, después de tener el dominio de la técnica quirúrgica y el manejo perioperatorio de las colecistectomías, que empezaron a aparecer algunos desarrollos que buscaban reemplazar la colecistectomía. Por ser una cirugía muy frecuente en la población económicamente activa, causaba muchas incapacidades laborales y se empezaba a buscar algo menos cruento que una cirugía y, entonces, aparecieron reportes de tratamientos médicos con disolución de los cálculos, como el ácido ursodesoxicólico 11, la litotripsia extracorpórea con ondas de choque 12 e, inclusive, la instilación directa en la vesícula biliar de sustancias como el metil-ter-butil éter para disolver los cálculos 13. Es decir, a pesar de que la morbimortalidad era tan baja, de todas maneras se consideraba una cirugía muy cruenta para los pacientes y se buscaban opciones médicas diferentes a la colecistectomía como tratamiento.
Empezaron a aparecer alternativas quirúrgicas como la minicolecistectomía, desarrollada por Dubois en Francia 14, pero poco extendida en el mundo. En Colombia, posteriormente, en 1991, se publicó el artículo del doctor José Félix Patiño sobre una colecistectomía practicada mediante una incisión de 4 o 5 cm, buscando que el paciente tuviera una estancia más corta y una recuperación más rápida 15. Por otro lado, hay que darle el reconocimiento aquí al profesor Stevenson Marulanda, quien desarrolló la técnica de la minilaparotomía mediana subxifoidea, con la cual ganó el Premio Nacional de Gastroenterología, en 1995.
Simultáneamente con esto que estaba ocurriendo en los años 80, había un desarrollo paralelo muy silencioso de la laparoscopia. Se utilizaba con fines diagnósticos en casos de ascitis, principalmente por los gastroenterólogos. Kurt Semm era un ginecólogo alemán quien hizo grandes aportes, en su momento no muy reconocidos, pero la historia le ha ido dando ese papel fundamental en el desarrollo de la cirugía por laparoscopia. El doctor Semm hacía liberación de adherencias pélvicas y luego cirugía de los anexos, para lo cual necesitó desarrollar el instrumental e introdujo algunos avances a la técnica, como eran la adopción del nudo de Roeder que se utilizaba en otras circunstancias y el desarrollo de la termocoagulación para hacer hemostasia, pues si no se lograba hacer hemostasia en la laparoscopia era imposible avanzar. Desarrolló, además, el neumoinsuflador electrónico que evitaba perder la presión cada vez que se sacaban los instrumentos. Y finalmente, en sus últimos aportes, implementó la sutura intracorpórea, lo cual en esa época era algo completamente revolucionario. En 1980, practicó la primera apendicectomía por laparoscopia, pero fue muy criticada y poco utilizada por casi dos décadas 16,17.
En Alemania, el 12 de septiembre de 1985, Erich Mühe practicó la primera colecistectomía (hace 30 años) con un dispositivo llamado el “Galloscope”, en la cual, a través de un solo orificio, introducía los instrumentos, y disecaba y colocaba los clips para el cístico y para la arteria, y utilizaba dos pequeños puertos laterales en el abdomen inferior para poder separar y ayudar. Requirió de una pistola desarrollada por Reynolds Jr. con la cual podía poner clips y coagular también 18. Un poco después de las primeras cirugías, le parecía dispendioso entrar por el ombligo y esperar la insuflación del neumoperitoneo; y se dio cuenta de que, si entraba por la región subcostal, con el mismo separador podía hacer espacio y no necesitaba gas, entonces, hacía la cirugía sin neumoperitoneo y entonces, la denominó la “colecistectomía abierta por el tubo”; todo lo operaba por ahí y esto fue un factor importante para que no tuviera tanta atención en su momento. Él presentó las fotos de su primer caso que después se publicaron, con la incisión en el ombligo y dos incisiones en el abdomen inferior; después, en otra paciente, lo pasó al hipocondrio derecho y mostró que eran incisiones muy pequeñas. A pesar de esto, fue muy criticado cuando reportó estos primeros casos, en 1986. Se decía que no respetaba los principios quirúrgicos e, inclusive, la llamaron “la cirugía de Mickey Mouse”, “cerebros pequeños, incisiones pequeñas” 19. Solamente una década después, la Society of American Gastrointestinal and Endoscopic Surgeons (SAGES) le reconoció en sesión plenaria este desarrollo como la primera colecistectomía laparoscópica 20,21.
Apenas dos años después, Philippe Mouret, un ginecólogo en Lyon, también tenía la costumbre de revisar la cavidad peritoneal, incluyendo las asas intestinales, y liberaba algunas adherencias, de manera que estaba familiarizado con la visión por laparoscopia de la cavidad peritoneal 22. En 1987, una paciente le pidió que, ya que le iba a operar las trompas por esos “orificios pequeños”, de una vez le realizara la colecistectomía para sus cálculos. Finalmente, él decidió hacerlo; una vez que terminó la cirugía ginecológica, giró su lente, le cambió la posición a la paciente y pudo hacer la colecistectomía. Al otro día, cuando fue a ver la paciente al pasar su ronda matinal, estaba ya estaba cambiada y vestida, y se iba para su casa muy disgustada porque decía que no le había realizado la cirugía de la vesícula y parece que los primeros días ¡la paciente no lo creyó que sí lo había hecho! 23.
La historia se encarga de hacer las conexiones: François Dubois era un cirujano en París, que desde 1973 practicaba colecistectomías a través de incisiones de 3 a 5 cm, a las que llamaba la minicolecistectomías; utilizaba luz frontal y unos instrumentos especiales para separar. En el año 1987, mientras hacía una de estas cirugías, la enfermera del quirófano le comentó que había visto en Lyon al doctor Mouret hacerla por un orificio más pequeño, con un lente. Ante esto, Dubois quedó sorprendido y contactó al doctor Mouret. Se encontraron en París y Mouret le mostró un vídeo que había hecho con las cámaras que había disponibles en esa época. Se interesó tanto el doctor Dubois, que hizo unos procedimientos en animales y, en 1988, los primeros en humanos 24.
Cuando envió su primer artículo reportando los primeros 30 casos, este fue rechazado por la revista médica más importante que había en Francia. En ese momento, la nota de respuesta le decía: “… es una técnica peligrosa, no difundir”. Él siguió insistiendo y, finalmente en 1989, en otra revista francesa se lo aceptaron y, al tiempo, se lo estaban aceptando en la revista Annals of Surgery; realmente, los mismos franceses reconocen que, si no hubiera sido porque la técnica llegó a Estados Unidos, seguramente en Francia no le hubieran prestado toda la atención y difusión que finalmente tuvo 25. El primer artículo muestra que, en la técnica francesa, se utiliza el puerto epigástrico para introducir la succión y separar el hígado; el cirujano se sitúa entre las piernas del paciente, con la mano izquierda ejerce tracción sobre la bolsa de Hartmann, con la mano derecha está disecando, mientras que el ayudante lleva la cámara con una mano y, con la otra, separa el hígado 26.
Posteriormente, en 1995, se publicó la experiencia en 2.655 casos, demostrando que era una técnica replicable, que se podía continuar haciendo y difundiendo en el mundo 27. Como muchos avances en la ciencia y en la técnica, simultáneamente otros cirujanos estaban desarrollando algo similar. En Burdeos, Jacques Perissat, utilizaba una técnica de litotripsia mediante laparoscopia; destruía los cálculos y extraía la vesícula biliar 28,29. Casi al mismo tiempo, en 1989 en Estados Unidos, Reddick y Olsen desarrollaron una técnica laparoscópica utilizando el láser 30. Esta técnica fue muy conocida como la cirugía con láser. Posteriormente, se dieron cuenta de que no era necesario utilizarlo, pero los pacientes en su imaginario todavía siguen mencionando “la cirugía con láser para la vesícula” 31.
Se produjo enseguida la gran explosión de la cirugía laparoscópica de los años 90. Rápidamente, se difundió en el mundo como ninguna otra técnica quirúrgica en tan corto tiempo y tan ampliamente. En algunos artículos empezaron a aparecer titulares sobre la llamada “segunda revolución francesa”, la “perestroika biliar” 32. Si la historia debe contrastarse siempre con lo que está ocurriendo en la sociedad, en esos momentos se producían la caída del muro de Berlín y la perestroika; los historiadores dirán que esto tuvo alguna influencia para favorecer los cambios en los paradigmas de la cirugía.
Tampoco puede pasarse por alto el papel de la industria de insumos quirúrgicos; por un lado, con el desarrollo de los instrumentos y equipos necesarios para el crecimiento de las técnicas laparoscópicas y, por otro lado, con el patrocinio de los cursos y formación de los cirujanos en las nuevas técnicas. Al mismo tiempo, hubo un cambio nada menor en el uso del instrumental, pasando de los utilizables por décadas a los instrumentos desechables.
Después de los primeros años de introducción de la técnica y de las publicaciones iniciales europeas 33, en Estados Unidos se publicaron las experiencias iniciales de instituciones a la vanguardia, así como trabajos multicéntricos que mostraban la relativa seguridad de la técnica, pero también, las nuevas complicaciones con la laparoscopia 9,34. En Colombia, se publicó la primera experiencia institucional, los primeros 60 casos en la Clínica del Country, en 1991 35. El doctor Abaúnza lideró un interesante artículo publicado en 1992 en la Revista de la Asociación Colombiana de Cirugía, con los resultados de un estudio cooperativo en el cual recolectaron 1.078 pacientes, con resultados similares a los de la literatura mundial, con tasas de conversión del 5 %, de mortalidad de 0,1 %, de complicaciones mayores del 0,6 % y de lesión de la vía biliar de 0,4 % 36. En Medellín, también se publicó la experiencia inicial por el grupo encabezado por el doctor Carlos Morales, con 328 casos, quienes de manera muy juiciosa recolectaron sus estadísticas y las compararon con lo publicado en la literatura científica 37.
Profesor asociado, Universidad Nacional de Colombia, Instituto Nacional de Cancerología, Bogotá, D.C., Colombia
Fecha de recibido: 17 de noviembre de 2016
Fecha de aprobación: 25 de enero de 2017
Citar como: Guevara O. De la colecistectomía laparoscópica a la hepatectomía laparoscópica: 30 años de evolución quirúrgica en beneficio del paciente. Conferencia honorífica “Rafael Casas Morales, 2016”. 2017;32:12-21.En el mundo, entonces, empezaron a hacerse otras cirugías por laparoscopia; la cirugía antirreflujo, la cirugía para la acalasia, la esplenectomía, la herniorrafia inguinal y la apendicectomía, aunque ninguno de estos procedimientos era para el cáncer, ni implicaban resecciones complejas. También, aparecieron las complicaciones y las lesiones de la vía biliar; hubo artículos en que casi condenan la colecistectomía laparoscópica por el mayor riesgo de lesiones de la vía biliar. Aparecieron las explicaciones, como el cambio en la percepción, la visión en dos dimensiones y la pérdida de la sensación táctil del cirujano, todo esto para enfatizar en la precaución en el desarrollo de las nuevas técnicas quirúrgicas 38. No obstante, las evaluaciones, el balance riesgo-beneficio a favor de la colecistectomía laparoscópica, la economía de las incisiones en la pared, la reducción del dolor y el retorno más rápido a la actividad de los pacientes, terminaron inclinando la balanza a favor de un menor trauma para el paciente 39.
Al final de la década de los noventa y comienzos de este siglo, surgió la pregunta de si esto se podía aplicar en las cirugías más complejas y, especialmente, en las oncológicas. Se reportaron algunos casos de siembras en la pared en resecciones de cáncer de colon y, entonces, se produjo una gran oposición al desarrollo de la cirugía laparoscópica en oncología, hasta que se encontró que, realmente, tenía el mismo riesgo que la cirugía abierta, pero que sí se debían tomar ciertas medidas de precaución para evitar dichas siembras 40. Posteriormente, se publicaron ensayos clínicos de asignación aleatoria sobre cáncer de colon, que mostraron resultados adecuados y, así, esta técnica fue validada y aceptada con una buena calidad de la evidencia 41. Para el cáncer gástrico ha sido mucho más lento el desarrollo, principalmente en Asia, pero aun en Japón, donde son muy conservadores, ha venido aumentando la proporción de gastrectomías por laparoscopia para esta neoplasia.
Un cirujano muy reconocido en Estados Unidos daba por terminada la era de las “grandes incisiones”, en un artículo titulado “La disminución y la caída de las incisiones quirúrgicas”, en 2006 42. Sin embargo, uno de los últimos reductos de esas “grandes incisiones” era y sigue siendo la cirugía hepato-pancreato-biliar, por la complejidad de los procedimientos. Sin embargo, a continuación se presenta cómo ha cambiado este panorama en los últimos años.
Desarrollo de la hepatectomía laparoscópica
Como órgano sólido con múltiples vasos arteriales, venosos portales, venosos suprahepáticos y conductos biliares, el hígado ha representado un reto quirúrgico, especialmente sobre cómo dividir este órgano. Se requirieron grandes avances en el conocimiento anatómico y en la técnica misma, para poder avanzar en las resecciones hepáticas. Uno de estos aportes lo hizo James Cantlie en el siglo XIX, pues antes se creía que los lóbulos hepáticos estaban divididos por el ligamento falciforme y él describió una línea divisoria entre el lóbulo derecho y el izquierdo, que va desde el fondo de la vesícula hasta la mitad de la vena cava inferior (línea de Cantlie). Estando en Hong Kong, un preso se suicidó al colgarse de una cuerda; él hizo la autopsia y le llamó mucho la atención que su porción derecha estaba completamente atrófica y, la izquierda, hipertrófica, como si hubiera tenido alguna una enfermedad que causara esto, seguramente una colangitis, que en esa época era muy frecuente. Con esto se inició su teoría de que la línea divisoria del hígado era ahí y no en el ligamento falciforme 43. Otro aporte importante fue el reconocimiento de la capacidad del hígado de hipertrofiarse 44, que permitió posteriormente el desarrollo de la cirugía.
En 1952, Jean Louis Lortat-Jacob publicó la primera resección anatómica del hígado en París 45. Fue una hepatectomía derecha en una paciente de 42 años con metástasis de cáncer de colon; mediante un abordaje toraco-abdominal derecho muy extenso, hizo el control de los vasos y luego la sección del parénquima 46. Apenas un año después, en Estados Unidos, Julian Quattlebaum publicó un artículo donde utilizaba también el control de los vasos inicialmente y de la vía biliar, y después, con el mango del bisturí iba disecando las estructuras dentro del parénquima, sin cortarlas, y donde encontraba vasos sanguíneos o canalículos biliares hacia el control mediante ligadura. Juan Manuel Sarmiento, cirujano hepatobiliar colombiano y profesor en la Universidad de Emory, escribió un artículo con la historia de Quattlebaum. En los dibujos que ilustran el artículo se observa la extensa incisión toraco-abdominal utilizada para la resección. Al final, mencionó esta frase de Quattlebaum: “yo soy el hombre más rico de mi condado, el más rico en amigos a cada paso que doy…”, prueba de la sencillez de este cirujano que hizo su aporte aún viviendo en una población pequeña 47.
En las siguientes dos décadas, no hubo mayores desarrollos en la cirugía hepática, pero sí un gran aporte en la anatomía, con el libro de Claude Couinaud publicado en 1957. En él hizo una recopilación de sus disecciones anatómicas sobre sus modelos que le permitieron plantear la existencia y describir los ocho segmentos que hoy se reconocen, según la división dada por la circulación portal. En alguna época, se dijo que se parecía a la distribución de los distritos de París, pero el mismo Couinaud negó esta relación 48.
Hay que mencionar, también, a un gran cirujano en Vietnam, Ton-Tan-Tung, quien por esta época desarrolló las resecciones hepáticas, sin tener mucho contacto con el mundo occidental. En la región de Indochina era muy frecuente el hepatocarcinoma y él decía que “la cirugía del hígado es una cirugía delicada y peligrosa”. Su técnica consistía en el control intraparenquimatoso de las estructuras vasculares y biliares 49.
El gran desarrollo de las resecciones hepáticas se produjo en los años ochenta y noventa, principalmente por el aporte de tres grandes cirujanos: Henri Bismuth, en Francia, Leslie Blumgart, en el Reino Unido y Estados Unidos, y Masatoshi Makuuchi, en Japón 50,51. Todos hicieron aportes muy importantes para el desarrollo y la difusión de la cirugía hepática. Esta época coincide con un análisis bibliométrico con series de tiempo, que permitió mostrar que el gran incremento en las publicaciones en cirugía hepatobiliar se presentó entre los años 1987 y 1995, planteando este periodo como la consolidación de este campo del conocimiento 52. Fue así como, en 1987, en un editorial se mencionó por primera vez la cirugía hepatobiliar como especialidad 53 y, en 1988, se publicó la primera revista de la especialidad 54.
Entonces, se produjeron desarrollos técnicos en la resección hepática, que requiere básicamente de dos momentos: la disección de las estructuras vasculo-biliares y su control. Hoy en día, se pueden fusionar en el mismo momento, pero, inicialmente, la disección se hacía con los dedos (“digitoclasia”) y, luego, aplastando el tejido con la pinza de Kelly (“kellyclasia”) y ligando o coagulando los vasos y conductos biliares, y posteriormente, con un disector ultrasónico principalmente 55. En cuanto a la hemostasia, hoy en día tenemos una gran cantidad de dispositivos y de equipos para hacerla, incluyendo desde las ligaduras y clips hasta los equipos de tijera ultrasónica, sellador bipolar y disector con radiofrecuencia, entre otros 56.
Después de 30 años, en 1989, Couinaud publicó otro libro que se llamaba “La anatomía quirúrgica revisada”. En uno de sus dibujos, se mostraba la vena cava inferior y se afirmaba que, en el espacio entre la línea media de la vena cava retrohepática y el hígado, casi no había venas colaterales, que podía considerarse un espacio avascular, y ese espacio estaba justo entre la llegada de la vena suprahepática derecha y el tronco de la suprahepática media izquierda.
Unos años después, el profesor Jacques Belghiti empezó a pensar que, si se disecaba este espacio desde arriba y desde abajo, podría pasarse un hiladillo para tener un control del plano posterior del hígado, principalmente en las resecciones de las hepatectomías derechas. De esta manera, no habría necesidad de movilizar el hígado lo cual podría tener ventajas oncológicas. El video de la técnica se presentó por primera vez en el Congreso Mundial de la International Hepato-Pancreato-Biliary Association del 2000 en Brisbane (Australia), técnica que él llamo la maniobra del colgamiento del hígado (liver hanging maneuver). Después de recibir los comentarios, se preparó el artículo que, finalmente, se publicó en 2001 57.
Esta maniobra ha sido muy utilizada en el mundo y ahora se presentan artículos sobre cómo realizarla mediante laparoscopia. Sirvió como puente híbrido entre la cirugía abierta y la laparoscopia, en la cual se liberaban los ligamentos del hígado por laparoscopia y, luego, se hacía la sección transversal del parénquima a través de una pequeña incisión; esta técnica ha servido de puente para el desarrollo de la resección laparoscópica. Quien más la impulsó fue el cirujano japonés Go Wakabayashi 58.
Con el avance de la cirugía laparoscópica, en algún momento debía llegarse a las resecciones hepáticas; sin embargo, se requería previamente un desarrollo especial, pues el riesgo de sangrado siempre fue una limitación. Se debe destacar aquí que Michel Gagner fue el primero que realizó una resección laparoscópica de un tumor hepático. Posteriormente, en 1996, Azagra y Goergen desarrollaron la primera resección anatómica del lóbulo izquierdo por laparoscopia. No obstante, seguían inquietando dos problemas importantes: el primero era el riesgo de embolia aérea, al cortar el hígado y cortar una vena trabajando con neumoperitoneo, y el segundo era cómo controlar el sangrado durante la laparoscopia cuando no se podían introducir las manos para comprimir el hígado o realizar la hemostasia. En los años siguientes, se fue demostrando que el riesgo de embolia aérea clínicamente relevante era mínimo, ya que la misma presión intraabdominal hacía que se colapsaran las venas y evitaba que se presentara una embolia aérea masiva y, luego, tomó más tiempo desarrollar las técnicas de control del sangrado por laparoscopia 59.
Hacia el año 2000 y con el grado de desarrollo de la cirugía hepática, el panorama fue similar al mencionado previamente para la colecistectomía: se lograron buenas cifras de mortalidad, aceptables cifras de morbilidad 60 y dominio de la técnica, y entonces, ¡resultaba que se debía implementar una técnica nueva por laparoscopia! Se empezaron a publicar las primeras series de casos, pero había muchas dudas sobre la reproducibilidad de la técnica, la selección de pacientes, si eran adecuadas oncológicamente y si se tenía el instrumental adecuado. En el 2000 en París, Daniel Cherqui publicó una serie de 30 casos de resecciones hepáticas por laparoscopia, la mayoría en el lóbulo izquierdo, y el resto en la parte anterior del segmento 4 y en los segmentos 5 y 6. Esas eran las indicaciones que él tenía en ese momento, es decir, la resección de los segmentos con mejor acceso por laparoscopia 61.
Poco a poco la laparoscopia fue ganando terreno, inicialmente, en muy pocos centros. Uno de estos fue el del profesor Gayet en París, quien publicó que, de las últimas 250 hepatectomías practicadas hasta el año 2004, 113 habían sido por laparoscopia, mostrando cómo cada vez más pacientes se podían intervenir por vía laparoscópica con una tasa de conversión del 10 % y con un solo caso de mortalidad Aseguraba que los resultados tempranos podían ser similares a los de la técnica abierta, siempre y cuando estuvieran en manos expertas 62.
Las publicaciones sobre resecciones laparoscópicas con buenos resultados tempranos, siguieron aumentando. En el año 2008, cuando ya había un buen conocimiento, se llevó a cabo un consenso de expertos internacionales en Louisville (Estados Unidos), en el cual se propusieron como sus primeras indicaciones la resección de tumores menores de 5 cm y localizados en los segmentos 2 al 6 para que fueran abordables. Para entonces, se consideró como método estándar la resección lateral izquierda de los segmentos 2 y 3 por laparoscopia; las resecciones hepáticas mayores debían ser reservadas para cirujanos con experiencia 63.
En los años siguientes, se fueron demostrando las ventajas de la técnica, como la visión amplificada del parénquima y los vasos, el acceso a sitios difícilmente visibles en la cirugía abierta y las ya conocidas ventajas en la obtención de bordes libres de tumor, aún mayores por las usualmente extensas incisiones para la cirugía hepática. Además, se demostró que la visión caudal (vía laparoscópica) en lugar de la anterior (cirugía abierta), permitía un mejor control de los vasos 64. Por supuesto, también se mostraron las limitaciones conocidas, como la falta de sensación táctil y de visión bidimensional, y la dificultad para acceder a los posteriores, la cual se ha ido superando con los cambios de posición del paciente y, también, con ingeniosos accesos transdiafragmáticos.
Aún quedaban sin resolverse las dudas sobre los resultados oncológicos. En los últimos años, se han publicado series más grandes que han mostrado, al menos, equivalencia en los resultados respecto a la cirugía abierta, aclarando que aún no se cuenta con ensayos clínicos de asignación aleatoria, aunque sí hay algunos en curso. En Seúl, se publicó que en los hepatocarcinomas menores de 5 cm, la supervivencia a cuatro años con la técnica laparoscópica y con la abierta fue similar 65. En Bélgica, se reportó que la supervivencia global y la libre de recaída habían sido muy similares con la técnica laparoscópica y con la cirugía abierta, en casos de resección de metástasis hepáticas de carcinoma colorrectal 66.
En el 2014 se llevó a cabo The Second International Consensus Conference on Laparoscopic Liver Resection (ICCLLR) en Morioka, Japón, liderado por el profesor Wakabayashi 67. Después de una revisión sistemática de la literatura publicada y de encuestas globales, se concluyó que las resecciones hepáticas se pueden hacer con resultados a corto plazo iguales o mejores que los de la cirugía abierta y con resultados a largo plazo que, hasta ahora, son al menos iguales 68.
En el consenso quedaron anotadas tres requisitos importantes para proteger a los pacientes en este nuevo procedimiento: que haya registros prospectivos con transparencia de los datos, que haya un puntaje que permita clasificar la dificultad de los pacientes para decidir si se someten inicialmente a cirugía laparoscópica, y que se cree una estructura formal de educación 69. Se espera que en los próximos años se publiquen los resultados de, por lo menos, dos ensayos clínicos de asignación aleatoria sobre hepatocarcinoma y metástasis de carcinoma colorrectal. El análisis del número de artículos que aparecen en PubMed demuestra el gran aumento de las publicaciones sobre hepatectomías y el número de publicaciones sobre hepatectomías laparoscópicas, mostrando su tendencia clara a aumentar (figura 2). Seguramente, la literatura científica nos aportará más información en los siguientes años, pero la tendencia al aumento de las hepatectomías laparoscópicas es clara también.
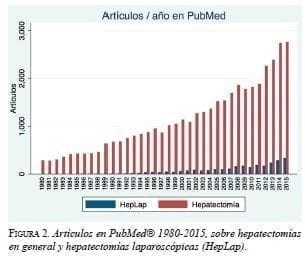
Atención centrada en el paciente
Al final, la pregunta es ¿y dónde queda el paciente? Hay que regresarle el papel de protagonista de la atención en salud. Muchos pacientes sienten que no son escuchados por el médico y tampoco le entienden lo que dice. Entonces, ¿será ventajoso para el paciente el abordaje laparoscópico? En principio parece que sí. Cambiar las incisiones extensas que normalmente hacemos en cirugía abierta, por otras más pequeñas parecería justificado para el paciente, siempre que se tengan la misma seguridad y los mismos resultados a corto y a largo plazo.
Quiero dejar estas dos reflexiones, para recordar cada vez que nos comunicamos con un paciente:
- El paciente no sabe lo que el médico sabe.
Al hablar con el paciente y explicarle su diagnóstico y las opciones de tratamiento, no hay que olvidar que él no sabe ni siquiera el 1 % de lo que el médico sabe de medicina; hay que pensar en eso, hay que explicarle todo y con el lenguaje apropiado. Es posible que se requiera repetir más de una vez una explicación. A manera de comparación, solamente hay que recordar cuando un abogado empieza a hablar con su jerga jurídica., ¡casi siempre estamos perdidos después de la segunda frase! Pues lo mismo les pasa a los pacientes con los términos médicos.
- El médico no logra imaginarse ni siquiera la mitad de lo que el paciente siente…
Cuando el paciente cuenta sus dolencias, no logramos realmente imaginarnos la magnitud y la relevancia de cada síntoma. Entonces, debemos darle importancia a cada molestia del paciente, así a veces con ligereza creamos que no son muy importantes.
Para terminar, quiero volver sobre la memoria del profesor Rafael Casas Morales, quien escribió un artículo titulado “Universidad y servicios hospitalarios”, en 1973, en el cual hace unas reflexiones sobre la necesidad de un hospital universitario para la Universidad Nacional de Colombia 70. En Colombia se han cerrado muchos hospitales universitarios. El Hospital San Juan de Dios, que era el hospital principal de la Universidad Nacional, se cerró hace 16 años y ahora la Universidad tiene un gran peso sobre los hombros, porque acaba de abrirse el Hospital Universitario Nacional de Colombia, gracias al esfuerzo y la tenacidad de muchas personas. El profesor Rafael Casas Morales fue fundador, también, de la Asociación de Exalumnos de la Universidad Nacional (AEXMUN), que fue primordial para que se pudiera abrir este hospital. Por lo tanto, quiero destacar cómo su legado está presente aún en nuestros días y es nuestra responsabilidad sacar adelante este hospital.
Mis agradecimientos infinitos a mi familia, a mis profesores, compañeros y alumnos en la Universidad Nacional de Colombia y en el Instituto Nacional de Cancerología.
Bibliografía
1. Abaúnza H. Evolución de la cirugía de algunos órganos. Desde sus pioneros hasta los cirujanos actuales. Rev Colomb Cir. 1996;11:66-74.
2. Toledo-Pereyra LH. Joseph Lister’s surgical revolution. J Inves¬tig Surg Off J Acad Surg Res. 2010;23:241-3.
3. Rains AJ. A thought for Carl Langenbuch (1846-1901): A cen¬tenary. Ann R Coll Surg Engl. 1982;64:268-9.
4. Dannenberg S, Eder F. 130 Jahre Gallenwegschirurgie – ein kurzer historischer Rückblick auf die Pioniertaten in der Chirurgie der Galle und der Gallenwege durch Professor Carl Langenbuch und Professor Hans Kehr. Zentralblatt Für Chir. 2012;137:16-9.
5. Lahey FH. Strictures of the common and hepatic ducts. Ann Surg. 1937;105:765-90.
6. Mayo WJ. VI. Some remarks on cases involving operative loss of continuity of the common bile duct: With the report of a case of anastomosis between the hepatic duct and the duodenum. Ann Surg. 1905;42:90-6.
7. Quintero G. Cirugía hepatobiliar: historia y perspectiva. Medi¬cina (Mex). 2004;26:244-8.
8. Andrade E. La cirugía en Colombia en el siglo XX. Pasado, presente y futuro. Rev Colomb Cir. 1986;1:99-105.
9. Peters JH, Gibbons GD, Innes JT, Nichols KE, Front ME, Roby SR, et al. Complications of laparoscopic cholecystectomy. Sur¬gery. 1991;110:769-78.
10. Shea JA, Berlin JA, Bachwich DR, Staroscik RN, Malet PF, McGuckin M, et al. Indications for and outcomes of cholecys¬tectomy: A comparison of the pre and postlaparoscopic eras. Ann Surg. 1998;227:343-50.
11. Schoenfield LJ, Marks JW. Oral and contact dissolution of gallstones. Am J Surg. 1993;165:427-30.
12. Nahrwold DL. Gallstone lithotripsy. Am J Surg. 1993;165:431-4.
13. Allen MJ, Borody TJ, Bugliosi TF, May GR, LaRusso NF, Thistle JL. Rapid dissolution of gallstones by methyl tert-butyl ether. Preliminary observations. N Engl J Med. 1985;312:217-20.
14. Dubois F, Berthelot B. Cholecystectomy through minimal inci¬sion (author’s transl). Nouv Presse Médicale. 1982;11:1139-41.
15. Patiño JF, Londoño E, García LG. Colecistectomía “Mini¬traumática”. Hospitalización de corta estancia. Rev Col Cir. 1991;6:70-5.
16. Litynski GS. Kurt Semm and an automatic insufflator. JSLS. 1998;2:197-200.
17. Litynski GS. Kurt Semm and the fight against skepticism: En¬doscopic hemostasis, laparoscopic appendectomy, and Semm’s impact on the “laparoscopic revolution.” JSLS. 1998;2:309-13.
18. Reynolds W. The first laparoscopic cholecystectomy. JSLS. 2001;5:89-94.
19. Litynski GS. Erich Mühe and the rejection of laparoscopic cholecystectomy (1985): A surgeon ahead of his time. JSLS. 1998;2:341-6.
20. Blum CA, Adams DB. Who did the first laparoscopic cholecys¬tectomy? J Minimal Access Surg. 2011;7:165-8.
21. Mühe E. Long-term follow-up after laparoscopic cholecystec¬tomy. Endoscopy. 1992;24:754-8.
22. Litynski GS. Profiles in laparoscopy: Mouret, Dubois, and Pe¬rissat: The laparoscopic breakthrough in Europe (1987-1988). JSLS. 1999;3:163-7.
23. Mouret P. Celioscopic surgery. Evolution or revolution?. Chir Memoires Acad Chir. 1990;116:829-33
24. Dubois F, Berthelot G, Levard H. Laparoscopic cholecystectomy: Historic perspective and personal experience. Surg Laparosc Endosc. 1991;1:52-7.
25. Polychronidis A, Laftsidis P, Bounovas A, Simopoulos C. Twenty years of laparoscopic cholecystectomy: Philippe Mouret–March 17, 1987. JSLS. 2008;12:109-11.
26. Dubois F, Icard P, Berthelot G, Levard H. Coelioscopic cholecys¬tectomy. Preliminary report of 36 cases. Ann Surg. 1990;211:60- 2.
27. Dubois F, Berthelot G, Levard H. Coelioscopic cholecystectomy: Experience with 2006 cases. World J Surg. 1995;19:748-52.
28. Perissat J, Collet D, Vitale G, Belliard R, Sosso M. Laparoscopic cholecystectomy using intracorporeal lithotripsy. Am J Surg. 1991;161:371-6.
29. Périssat J. Laparoscopic surgery: A pioneer’s point of view. World J Surg. 1999;23:863-8.
30. Reddick EJ, Olsen DO. Laparoscopic laser cholecystectomy. A comparison with mini-lap cholecystectomy. Surg Endosc. 1989;3:131-3.
31. Reddick EJ, Olsen DO. Outpatient laparoscopic laser cholecys¬tectomy. Am J Surg. 1990;160:485-9.
32. Liguory C, Vitale GC. Biliary perestroika. Am J Surg. 1990;160:237-8.
33. Cuschieri A, Dubois F, Mouiel J, Mouret P, Becker H, Buess G, et al. The European experience with laparoscopic cholecystectomy. Am J Surg. 1991;161:385-7.
34. Peters JH, Ellison EC, Innes JT, Liss JL, Nichols KE, Lomano JM, et al. Safety and efficacy of laparoscopic cholecystec¬tomy. A prospective analysis of 100 initial patients. Ann Surg. 1991;213:3-12.
35. Cuéllar C, Moreno E, Casas C, de Francisco J, Ordóñez H, Riveros R. Colecistectomía laparoscópica. Primera experiencia en Colombia. Rev Colomb Cir. 1991;6:5-12.
36. Abaúnza H, Casas C, Zundel N. Colecistectomía laparoscópica. Trabajo cooperativo de la Sociedad Colombiana de Cirugía. Rev Colomb Cir. 1992;7:2-10.
37. Morales CH, Sierra JM, Ramírez N, Aristizábal JG, Salinas CM, Sierra LS, et al. Colecistectomía videolaparoscópica. II. Evaluación prospectiva de los primeros 328 casos en Medellín. Iatreia. 1994;7:131-4.
38. Litwin DEM, Cahan MA. Laparoscopic cholecystectomy. Surg Clin North Am. 2008;88:1295-313.
39. McMahon AJ, Baxter JN, Anderson JR, Ramsay G, O’Dwyer PJ, Russell IT, et al.. Laparoscopic versus minilaparotomy cholecystectomy: A randomised trial. Lancet. 1994;343:135-8.
40. Zmora O, Weiss EG. Trocar site recurrence in laparoscopic surgery for colorectal cancer. Myth or real concern? Surg Oncol Clin N Am. 2001;10:625-38.
41. Bonjer HJ, Hop WCJ, Nelson H, Sargent DJ, Lacy AM, Castells A, et al. Laparoscopically assisted Vs open colectomy for colon cancer: A meta-analysis. Arch Surg Chic Ill 1960. 2007;142:298- 303.
42. Morgenstern L. The decline and fall of the surgical incision. Surg Innov. 2006;13:207-8.
43. Cantlie, J. On a new arrangement of the right and left lobes in the liver. J Anat Physiol. 1898;32:iv-ix.
44. Rous P, Larimore LD. Relation of the portal blood to liver maintenance : A demonstration of liver atrophy conditional on compensation. J Exp Med. 1920;31:609-32.
45. Belghiti J. The first anatomical right resection announcing liver donation. J Hepatol. 2003;39:475-9.
46. Lortat-Jacob JL, Robert HG.[Well defined technic for right hepatectomy. Presse Med. 1952;60:549-51.
47. Sarmiento JM, Dodson TF. Julian K Quattlebaum, MD: Ameri¬can pioneer of hepatic surgery. J Am Coll Surg. 2008;207:607-11.
48. Sutherland F, Harris J. Claude Couinaud: A passion for the liver. Arch Surg Chic Ill 1960. 2002;137:1305-10.
49. Helling TS, Azoulay D. Ton That Tung’s livers. Ann Surg. 2014;259:1245-52.
50. Fortner JG, Blumgart LH. A historic perspective of liver sur¬gery for tumors at the end of the millennium. J Am Coll Surg. 2001;193:210-22.
51. Bismuth H, Majno PE. Hepatobiliary surgery. J Hepatol. 2000;32(Suppl.):208-24.
52. Guevara O, Eslava-Schamlbach J, Buitrago G, Ovalle D, Belghiti J. When were hepato-pancreato-biliary surgery articles increa¬sed? A bibliometric analysis of an emerging specialty (Abstract). HPB. 2010; 12 (suppl 1): 411
53. Carter DC. The specialty of hepatobiliary surgery. Br J Surg. 1987;74:871-2.
54. Bengmark S. Surgical diseases of the liver, pancreas and biliary tract. Editorial. HPB Surg World J Hepatic Pancreat Biliary Surg. 1988;1:1-2.
55. Belghiti J, Guevara O, Pierangeli F, Sommacale D, Farges O, Sauvanet A. Comparison of the efficacy of the ultrasonic dissec¬tor in cirrhotic and normal liver (Abstract). HPB. 2001;3:107.
56. Pamecha V, Gurusamy KS, Sharma D, Davidson BR. Techniques for liver parenchymal transection: A meta-analysis of randomi¬zed controlled trials. HPB. 2009;11:275-81.
57. Belghiti J, Guevara OA, Noun R, Saldinger PF, Kianmanesh R. Liver hanging maneuver: A safe approach to right hepatectomy without liver mobilization. J Am Coll Surg. 2001;193:109-11.
58. Nitta H, Sasaki A, Otsuka Y, Tsuchiya M, Kaneko H, Waka¬bayashi G. Impact of hybrid techniques on laparoscopic major hepatectomies. J Hepato-Biliary-Pancreat Sci. 2013;20:111-3.
59. Azagra JS, Goergen M, Brondello S, Calmes MO, Philippe P, Schmitz B. Laparoscopic liver sectionectomy 2 and 3 (LLS 2 and 3): Towards the “gold standard.” J Hepatobiliary Pancreat Surg. 2009;16:422-6.
60. Belghiti J, Hiramatsu K, Benoist S, Massault P, Sauvanet A, Farges O. Seven hundred forty-seven hepatectomies in the 1990s: An update to evaluate the actual risk of liver resection. J Am Coll Surg. 2000;191:38-46.
61. Cherqui D, Husson E, Hammoud R, Malassagne B, Stéphan F, Bensaid S, et al. Laparoscopic liver resections: A feasibility study in 30 patients. Ann Surg. 2000;232:753-62.
62. Vibert E, Perniceni T, Levard H, Denet C, Shahri NK, Gayet B. Laparoscopic liver resection. Br J Surg. 2006;93:67-72.
63. Buell JF, Cherqui D, Geller DA, O’Rourke N, Iannitti D, Dagher I, et al. The international position on laparoscopic liver surgery: The Louisville Statement, 2008. Ann Surg. 2009;250:825-30.
64. Soubrane O, Schwarz L, Cauchy F, Perotto LO, Brustia R, Bernard D, et al. A conceptual technique for laparoscopic right hepatectomy based on facts and oncologic principles: The caudal approach. Ann Surg. 2015;261:1226-31.
65. Yoon S-Y, Kim K-H, Jung D-H, Yu A, Lee S-G. Oncological and surgical results of laparoscopic versus open liver resection for HCC less than 5 cm: Case-matched analysis. Surg Endosc. 2015;29:2628-34.
66. Montalti R, Tomassini F, Laurent S, Smeets P, De Man M, Geboes K, et al. Impact of surgical margins on overall and recurrence-free survival in parenchymal-sparing laparosco¬pic liver resections of colorectal metastases. Surg Endosc. 2015;29:2736-47.
67. Wakabayashi G. What has changed after the Morioka consensus conference 2014 on laparoscopic liver resection? Hepatobiliary Surg Nutr. 2016;5:281-9.
68. Ciria R, Cherqui D, Geller DA, Briceño J, Wakabayashi G. Comparative short-term benefits of laparoscopic liver resection: 9000 cases and climbing. Ann Surg. 2016;263:761-77.
69. Wakabayashi G, Cherqui D, Geller DA, Buell JF, Kaneko H, Han HS, et al. Recommendations for laparoscopic liver resection: A report from the second international consensus conference held in Morioka. Ann Surg. 2015;261:619-29.
70. Casas R. Universidad y servicios hospitalarios. Editorial. Rev Fac Med. 1973;33:i-iv.
Correspondencia: Óscar Guevara, MD
Correo electrónico: oaguevarac@yahoo.com
Bogotá, D.C., Colombia
