YADIRA PINTO, MSC, MD*, MILCIADES IBÁÑEZ, MD*, NELSON RANGEL, MSC, MD*,
SANDRA RAMÍREZ, MSC, PHD, MD*, WILLIAM SÁNCHEZ, MD**, DIEGO VANEGAS, MD**,
Palabras clave: cáncer de mama, polimorfismo genético, genes p53, sindromes neoplásicos hereditarios.
Resumen
Introducción: El gen p53 codifica para una proteína de 53 KD con importante función reguladora en procesos celulares como la proliferación, la muerte celular y la preservación del material genético. Se le conoce como el “guardián del genoma” y frecuentemente se encuentra mutado en casi el 50% de los carcinomas humanos. Se han identificado variantes en su secuencia o polimorfismos genéticos (en diferentes regiones del gen), varios estudios han mostrado una asociación entre el riesgo de desarrollar cáncer mamario y la presencia de estas variantes.
El objetivo del presente estudio de casos y controles fue analizar la asociación de los genotipos y las frecuencias alélicas de tres de los polimorfismos del gen p53 con el riesgo de desarrollar cáncer mamario familiar en una población colombiana. Los polimorfismos estudiados fueron: en el exón 4 del gen que corresponde al codón 72 de la proteína, donde puede haber una arginina o una prolina (Arg72Pro); en el intrón 3 (duplicación de 16pb) y en el intrón 6, donde puede encontrarse una guanina o una adenina (G/A).
Materiales y métodos: Se analizaron 186 pacientes con cáncer mamario familiar y 186 individuos como controles, las frecuencias alélicas y genotípicas se determinaron por análisis de RFLPs y se midió la fuerza de asociación mediante la razón de disparidad (Odds ratio: OR), con una significancia de la asociación utilizando el intervalo de confianza del 95% y con el programa estadístico SPSS 11,5.
Resultados: Las frecuencias genotípicas del codón 72 en la población estudiada fueron: 61,3% para Arg/Arg, 32,3% para Pro/Arg y 6,5% para Pro/Pro en los casos y 44,1, 45,7 y 10,2% respectivamente en los controles. La frecuencia alélica obtenida para arginina en los casos fue 77,4 y 67,0% en los controles (P=0,004). Se obtuvo un OR=2,19 con un IC de 95% (1,33-3,63). La frecuencia de los genotipos del intrón 6 fueron entre casos y controles W/W (75,3
frente a 82,3%), W/M (24,2 frente a 15,6%) y M/M (0,5 frente a 2,2%) mientras que los valores de las frecuencias genotípicas del intrón 3 en los casos fueron: 90,3% para W/W, 8,6% para W/M y 1,1% para M/M y en los controles 98,9% para W/W y 0,5% para W/M y M/M.
Las frecuencias alélicas para el alelo silvestre (W) fueron en los casos 94,6% y en los controles 99,2%. Se obtuvo un OR=17,86 con un IC del 95% (2,25-141,84).
Conclusiones: Los resultados obtenidos en la población colombiana estudiada muestran una importante asociación entre el genotipo Arg/Arg del codón 72 (dos veces más) y el genotipo W/M intrón 3 (18 veces más) del gen p53 con el riesgo de desarrollar cáncer mamario familiar.
Introducción
El cáncer de seno es una enfermedad común en países como el Reino Unido y Estados Unidos, donde su prevalencia es 1:12 y 1:8 mujeres, respectivamente (Dunning y cols., 1999). En Colombia, el cáncer mamario ocupa el tercer lugar en incidencia y es la tercera causa de muerte por cáncer después del gástrico y el de cuello uterino (Castro y Martínez, 2003). Del total de casos de cáncer mamario, el 10-15% son de origen familiar, de los cuales el 5% se puede asociar con mutaciones en genes de alta penetrancia y con un rol en la reparación del ADN, como BRCA1 y BRCA2. Adicionalmente, los individuos con antecedentes familiares de la enfermedad presentan un riesgo dos veces mayor de desarrollarla que la población general. Sin embargo, este riesgo no puede ser explicado únicamente por alteraciones en los genes BRCA1/BRCA2, sino que existen variantes genéticas de baja penetrancia que pueden estar asociados con el desarrollo de la enfermedad, como los polimorfismos presentes en genes relacionados con cáncer mamario, como p53 (Coughlin y Piper, 1999; Khaliq y cols., 2000; Suspitsin y cols., 2003).
El gen p53 funciona como supresor de tumor y codifica para una proteína que tiene múltiples funciones, dentro de las que se destacan la regulación de apoptosis o muerte celular programada, el control del ciclo celular y la reparación del ADN, motivo por el cual se le denomina también “guardián del genoma” (Borresen-Dale, 2003; Arrowsmith, 1999).
El p53 posee tres polimorfismos que han sido asociados con el cáncer de seno: en el codón 72 (Arg72Pro), en el intrón 6 (G/A) y en el intrón 3 se ha descrito una inserción de 16 pb (Buyru y cols, 2003;
Coughlin y Piper, 1999; Dunning y cols., 1999; Khaliq y cols., 2000; Papadakis y cols., 2000; Sjalander y cols., 1996; Suspitsin y cols., 2003; Wang-Gohrke y cols., 2002). Sin embargo, muchos de estos estudios no tienen en cuenta el componente étnico, ya que las diferencias entre poblaciones puede determinar la influencia del legado genético en la carcinogénesis; por lo tanto, aunque hay estudios estadísticamente significativos que describen la asociación existente entre los polimorfismos del gen p53 y el cáncer mamario, es importante analizar esta asociación en la población colombiana.
Según datos del Instituto Nacional de Salud, más del 60% de los casos de cáncer mamario que ingresan se encuentran en estadios clínicos tardíos (estadios III y IV) y tan sólo 4,8% lo hacen en estadios tempranos (in situ y I). Por tanto, es importante realizar investigaciones que conduzcan no sólo a la detección temprana de cáncer mamario sino además a la identificación de factores que contribuyan al desarrollo de la enfermedad, especialmente en la población más susceptible como lo es aquélla con antecedentes familiares de cáncer de seno.
Materiales y Métodos
Población de estudio
El estudio realizado es de tipo analítico de casos y controles. Un total de 186 pacientes con cáncer mamario heredofamiliar fueron contactados entre junio de 2004 y octubre de 2005. Igual número de personas sin cáncer (controles) fueron incorporadas al estudio en el mismo periodo, las cuales no tenían antecedentes de cualquier tipo de cáncer familiar en primer o segundo grado.
El rango de edades para ambos grupos estuvo entre 23 y 83 años. Se diseñó una encuesta para obtener información sobre el estilo de vida, características sociodemográficas y antecedentes ginecoobstétricos. Todas las personas incluidas en el estudio diligenciaron el consentimiento informado, aprobado por los comités de ética de las diferentes instituciones participantes.
Extracción de ADN y genotipificación de los polimorfismos del gen p53
En tubos de 5 ml con EDTA se obtuvieron muestras de sangre de cada individuo participante, a partir de las cuales se extrajo el ADN mediante el método PROBE (Briceño, 1988). Con las muestras del ADN obtenido, mediante PCR, se amplificaron las regiones del gen p53 que contienen los tres polimorfismos estudiados.
Polimorfismo exón 4, codón 72 (Arg72Pro): Los primers utilizados para la evaluación de este polimorfismo ubicado en el exón 4 del gen fueron tomados de Fan y cols., 2000 F. 5’-TTGCCGTCCCAAGCAATGGATGA- 3’ R. 5-TCTGGGAAGGGACAGAAGATGAC-3’); 100 – 300 ng de ADN fueron amplificados en un volumen final de 30 µl. La mezcla de PCR final contenía 3 µl de buffer de PCR (1X); 2,4 µl de MgCl2 (2 µM); 1,5 µl de dNTPs (200 µM); 0,75 µl de cada primer (0,25 µM) y 0,4 U de Taq Polimerasa (Promega). Las condiciones de PCR fueron 95°C por 5 min, 30 ciclos a 95°C por 30 seg, 59°C por 30 seg y 72°C por 30 seg, seguido por un paso de extensión final de 72°C por 5 min.
Los productos de PCR fueron digeridos toda la noche a 60ºC con 5U de la enzima BstUI (New England Biolabs) en volumen final de 15 µl. La presencia de un fragmento de 199 pb corresponde al genotipo Pro/Pro, mientras que la presencia de dos fragmentos de 113 pb y 86 pb corresponden al genotipo homocigoto Arg/Arg. Genotipos heterocigotos (Arg/Pro) contienen los tres fragmentos (figura 1a).
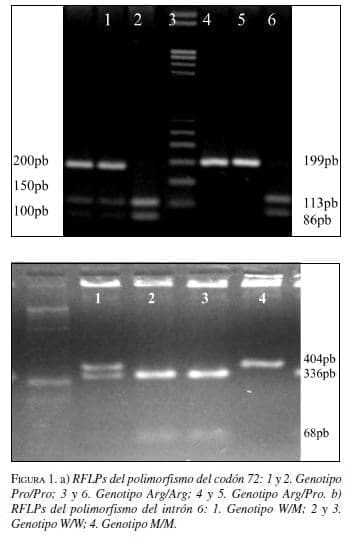
Polimorfismo intrón 6 (G/A): Los primers utilizados para evaluar el polimorfismo fueron F – 5’ TGGCCATCTACAAGCAGTCA 3’, R – 5’ TTGCACATCTCATGGGGTTA 3’ (Wu y cols., 2002).
Las condiciones de PCR utilizadas fueran las mismas del polimorfismo Arg72Pro, excepto por la temperatura de anillaje que fue de 56ºC. Los productos de PCR fueron digeridos toda la noche a 37ºC con 10U de la enzima MspI (New England Biolabs) en volumen final de 15 µl. La presencia de un fragmento de 404 pb corresponde al genotipo A/A (homocigoto mutante, M/M), mientras que la presencia de dos fragmentos de 336 pb y 68 pb corresponde al genotipo G/G (homocigoto silvestre W/W). Genotipos heterocigotos, G/A (W/M) contenían los tres fragmentos (figura 1b).
Polimorfismo intrón 3: El polimorfismo se determinó por la presencia o ausencia de una inserción de 16 pb en los fragmentos analizados. Los primers utilizados fueron F – 5’ TGGGACTGACTTTCTGCTCTT 3’, R – 5’ TCAAATCATCCATTGCTTGG 3’ (Wu y cols., 2002).
Las condiciones de PCR fueron las mismas del polimorfismo Arg72Pro, excepto por la temperatura de anillaje que fue de 57ºC. La presencia de la inserción de 16 pb se detectó mediante la observación de una banda de 196 pb y la ausencia de la misma por la observación de una banda de 180 pb el gel de agarosa.
Todos los productos de PCR y los productos de la digestión enzimática para la evaluación de los polimorfismos del exón 4, intrón 6 e intrón 3 se visualizaron en geles de agarosa al 2% teñidos con bromuro de etidio.
Análisis estadístico
La sistematización de los datos se hizo con la ayuda del paquete estadístico SPSS para Windows versión 11.5. La evaluación de los factores asociados con cáncer mamario heredofamiliar se hizo mediante análisis bivariado, donde se utilizó ji-cuadrado o la prueba exacta de Fisher en valores esperados <5; también se midió la fuerza de asociación mediante la razón de disparidad (Odds ratio: OR) y se evaluó la significancia de la asociación utilizando el intervalo de confianza (IC) de 95%.
La explicación conjunta de los factores y su respectivo control de variables de confusión se hizo inicialmente con el método de estratificación de Cochran-Mantel-Haenzel y finalmente se construyó un modelo de análisis multivariante de regresión logística incondicional para variables dependientes dicotómicas; la evaluación de las variables de confusión se realizó teniendo en cuenta los resultados del análisis bivariado con los OR crudos y se compararon con los obtenidos en el análisis multivariante con los OR ajustados. Las pruebas estadísticas se evaluaron a un nivel de significancia de 5% (p<0,05).
* Laboratorio de Biología celular y molecular. Departamento de
Ciencias Básicas, Facultad de Medicina, Universidad del Rosario,
Bogotá, D.C., Colombia.
** Cirugía General, Hospital Militar Central, Bogotá, D.C.,
Colombia.
Fecha de recibo: Agosto 15 de 2006
Fecha de aprobación: Agosto 30 de 2006
