El curso natural de los paragangliomas del cuerpo carotídeo es motivación para considerar las estrategias que proporcionan la mejor conducta; la cirugía es el procedimiento de preferencia. Hasta no hace mucho, la intervención quirúrgica de estas lesiones era de riesgo importante, con una alta incidencia de morbimortalidad, como consecuencia de las lesiones de los pares craneanos vecinos y de accidentes cerebrovasculares. Sin embargo, este panorama mejoró con los avances técnicos en cirugía vascular; frecuentemente los grandes tumores, para su resección, terminaban con ligadura de la arteria carótida. La mortalidad alcanzaba el 50% y aquellos pacientes que sobrevivían tenían de 15 a 30% de accidentes cerebrovasculares (Mellrad, 1963). Consecuentemente, las complicaciones quirúrgicas, demostraron ser peores que la historia natural de la enfermedad. La resección quirúrgica, ha sido bien documentada como la única manera de obtener una cura definitiva de la neoplasia (Smith, 1988; Hallet, 1998; Krupski, 1982). Aunque la alta mortalidad se ha reducido exitosamente a una cifra insignificante, las lesiones de los pares craneanos ocurren en un 20%, y se relacionan notoriamente con el tamaño del tumor y su localización (Hallet, 1998). La morbilidad es la resultante del formidable desafío que ellos ofrecen al cirujano por su eminente naturaleza vascular, su íntima adherencia a la adventicia arterial, a su localización en la bifurcación carotídea, la cual ensanchan y sobrepasan, y además por su proximidad e inclusión de los nervios craneanos. Por lo tanto, debido a la excesiva pérdida sanguínea, a los accidentes cerebrovasculares y otros déficits neurológicos con significativas incapacidades postoperatorias causadas por disfunción de los pares craneanos, el tratamiento quirúrgico de los grandes paragangliomas del cuerpo carotídeo sigue siendo un riesgo.
Pantonawitz y Mitchel exponen como razón para indicar la cirugía de estos tumores, la experiencia que se tenga en su manejo operatorio, en el riesgo de deterioro de los pares craneanos causado por el progresivo crecimiento de la neoplasia y por la posibilidad de degeneración maligna. Dada la lenta tasa de crecimiento, la política de espera y el intervalo necesario que incluye una RM o TC anual, debe tenerse en cuenta, especialmente en ancianos, el estado general y el curso del tumor (Pantonawitz, 1990; Mitchel, 1996).
Como una alternativa se ha invocado la radioterapia con resultados variables. Sánchez de Guzmán, del Instituto Nacional de Cancerología, publicó la experiencia de 160 pacientes intervenidos en esa institución en un lapso de 38 años, en nueve de los cuales, se incluyó la radioterapia; en tres pacientes como tratamiento primario y en seis como complementario, sin respuesta satisfactoria (Sánchez de Guzmán, 1999).
Otros investigadores (Shamblin, 1971; Warshawski, 1989) sostienen que el tumor no es radiosensible, porque no hay un efecto directo de muerte celular y señalan nuevo crecimiento de la neoplasia, después de haber sido considerada, inicialmente, como reducida por la radiación. Mitchel, sometió a doce pacientes a esta modalidad de tratamiento. De los cuatro paragangliomas del cuerpo carotídeo, dos no mostraron regresión y los dos restantes necesitaron 12 y 18 meses, antes que la respuesta fuese notada. El informe de la Clínica Mayo, en el cual 16 pacientes fueron sometidos a radiación, señala que en un solo caso el tumor disminuyó de tamaño (Mitchel, 1985).
En el manejo de los paragangliomas cervicales la radioterapia no es tenida en cuenta como tratamiento primario (Brackman, 1987), porque la mayoría de los tumores están localizados en sitios más accesibles a la extirpación quirúrgica completa, en comparación con los paragangliomas del hueso timpánico. Actualmente existe mucha controversia por el uso de radiación en el tratamiento primario de los paragangliomas de la base del cráneo.
Angiografía y embolización. Prácticamente a nivel mundial las imágenes no invasivas han desplazado a la angiografía como instrumento radiológico de diagnóstico primario de los paragangliomas de cabeza y cuello (Mafee, 1982; Rao Archana, 1999; Som, 1996). Sin embargo, aún permanece como una parte importante de la valoración prequirúrgica, en especial, cuando se ha escogido la embolización para el manejo de estas lesiones.
La embolización preoperatoria transarterial fue informada por Schick, sugiriendo que con ella se podían reducir las dificultades técnicas de la resección de estas lesiones, altamente vascularizadas, y en esa forma, disminuir la morbilidad perioperatoria. Esta técnica, refinada por radiólogos, generalmente es efectuada en una sola sesión y se facilita por la presencia de vasos dilatados como resultado del alto flujo sanguíneo en el cuerpo carotídeo (Shick, 1980). La embolización arterial es un recurso importante en el manejo de las lesiones vasculares en muchos sitios del organismo. Esta técnica es útil en el tratamiento preoperatorio curativo o paliativo de las lesiones vasculares de cabeza y cuello.
La suplencia vascular de los tumores de cabeza y cuello puede ser mono o multicompartimental (Chambers, 1982); información esencial para la adecuada embolización y tratamiento quirúrgico. En las lesiones multicompartimentales, cada territorio vascular está hemodinámicamente separado y todas las fuentes vasculares de irrigación deben ser identificadas durante la angiografía, para valorar las características vasculares de la lesión. En el caso de las lesiones monocompartimentales, la opacificación de algún pedículo vascular, delinea el tumor completamente (Valavanis, 1985). Por el contrario, si la distribución es multicompartimental se requiere esta maniobra para embolizar cada pedículo vascular, si se desea una adecuada desvascularización del tumor. La mayoría de los paragangliomas de cabeza y cuello son multicompartimentales. Gran parte ellos derivan alguna suplencia vascular de la arteria faríngea ascendente. Otras fuentes vasculares provienen de la maxilar interna, occipital, vertebral o cervical ascendente.
El uso de embolización preoperatoria está bien establecido y experimentado por varios autores. Tikkakoski concluyó que la embolización preoperatoria de paragangliomas de más de 3 cm de diámetro y fue segura y efectiva en reducir la intraoperatoria pérdida de sangre, facilitando el procedimiento quirúrgico y disminuyendo el riesgo (Tikkakoski, 1997); otros autores (DuBois, 1987; Litle, 1996) muestran que la embolización no mejora significativamente el resultado final de la cirugía, en cuanto a las pérdidas sanguíneas, tiempo operatorio y morbilidad perioperatoria. Mencionan complicaciones cerebrales, y sostienen que el plano quirúrgico de disección se puede oscurecer por una respuesta inflamatoria aguda a las partículas embolizadas (Arriaga, 1992). Si se requiere intentar la embolización, se debe efectuar inmediatamente antes de la cirugía.
Técnica Quirúrgica
Durante la extirpación de un paraganglioma del cuerpo carotídeo, la etapa inicial se dirige al control vascular proximal (carótida común) y el distal (carótida interna). La porción distal de la carótida externa se logra por disección ventral en relación con la carótida interna o, en caso de grandes tumores, por disección de sus ramas desde la periferia hacia su sito de origen. El nervio hipogloso (XII) se aísla en la parte superior y lateral del tumor, mientras que el laríngeo superior se puede encontrar medial a la carótida, en la vecindad a la arteria tiroidea superior. El nervio vago (X) se identifica junto a la carótida común y debe seguirse hacia la base del cráneo. El nervio glosofaríngeo (IX) es mucho más difícil de reconocer, generalmente corre hacia el cráneo desde el tumor por detrás del ángulo del maxilar inferior.
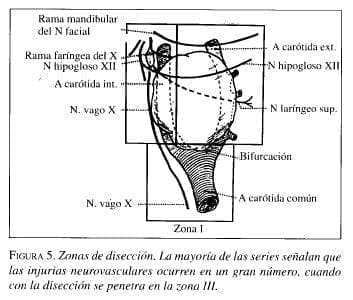
La injuria de los nervios craneanos, asociadas con la resección de este tumor, representa un accidente no resuelto aún hoy en día. El trauma se debe a dos factores posibles: a una falla técnica o a la inclusión de estas fibras nerviosas por el tumor, lo que significa la necesidad de una cuidadosa disección de las mismas. El aspecto que más influye en la agresión neural es la extensión de la masa tumoral. Si recordamos la clasificación de Shamblin, los tumores tipos I y II son de fácil resección. Por el contrario, los tipo III, que ostentan un comportamiento extenso, incluyendo invasión transmural de la pared arterial, comprometerán el territorio de las ramas craneanas ya mencionadas, obligando al cirujano a disecar en la zona III (figura 5), área que como es de esperarse ofrece la mayor incidencia de lesión neural.
La disección periadventicial del tumor (plano de Gordon Taylor) produce un plano de clivaje que facilita las maniobras quirúrgicas. No debe ejercerse tracción sobre la masa, porque una desagradable hemorragia de las venas oscurece el campo operatorio. Se cree que la clave de la extirpación segura de un paraganglioma del cuerpo carotídeo está en el control previo de los vasos nutricios del tumor, usando pequeños lazos. Ya se ha señalado que el más constante de estos es la arteria faríngea ascendente.
Si ocurre una lesión de los vasos carotídeos (carótida común o interna) es seguro heparinizar parcialmente el paciente y obstruir en forma temporal estos vasos, con pequeño riesgo de complicaciones mientras se sutura o se corrige el daño. La derivación interna intraoperatoria no es necesaria durante la reconstrucción vascular. No existen diferencias significativas en la ocurrencia de accidentes cerebrovasculares, con el uso o no de una cánula intraarterial (6.2 vs. 8.8%). El uso rutinario de esta modalidad es desalentador, excepto en pacientes que no toleran la oclusión con balón (Dickinson, 1986; McPherson, 1989). El catéter intravascular puede ocasionar complicaciones como hemorragia, trombosis y embolias, asociadas a lesiones del sistema nervioso central y, aun, mortalidad (Meyer, 1986). Se debe evitar la ligadura de la carótida interna, por la prevalencia de apoplejía en un 66% de los casos.
Abstract
Paragangliomas are neoplasms derivedfrom the neural crest; they are rare lesions, usually benigno Carotid body tumors are the most frequent type in the head and neck region; generally they present as an asymptomatic mass, occurring mainly in people in the 40s and 50s. Etiology seems to be related with life at high altitudes or with chronic pulmonary obstructive disease (chronic hypoxia); there isa group that exhibitsfamily frend. Noninvasive diagnostic imaging (MRl, CT,scintigraphy) are the best methods to confirm the diagnosis. Surgery is recognized as the only approach to achieve cure. With very large tumors there may be complications in the course of surgical intervention. Preoperative arterial embolization has been advised in selected cases with the purpose of reducing the size of the tumor.
Referencias
1. Albert: Cited by Staats EF, Brown RL, Smith RR: Carotid body tumors, benign and malignant. Laryngoscope 1993; 103: 7-15.
2. Albores Saavedra J, Espino Durán M: Association of tyroid carcinoma and chemodectoma. Am J Surg, 1968; 116: 887-90.
3. Arias Stella J, Bustos F: Chronic hipoxia and chemodectomas in bovines at high altitudes. Arch Pathol Lab Med, 1976; 100: 636-9.
4. Arriaga MA, Lo WW, Brackmann DE: Magnetic resonance angiography of synchronous bilateral carotid body paragangliomas and bilateral vagal paragangliomas. Ann Otol Rhinol Laryngol, 1992; 101: 955-7.
5. Batsakis JG: Paragangliomas of the head and neck. 2 ed. Baltimore, Williams and Wilkins, 1979; 369-80.
6. Bozon E, Casas A, De La Hoz J: Tumores del cuerpo carotídeo. Trib Med, 1976; 45: 25-8.
7. Brackman HD, Kinney S, Fuk: Glomus tumor diagnosis and management Head Neck Surg, 1987; 308-11.
8. Brazeau P, Vale W, Burgus R, et al.: Hypothalamic polypeptide that inhibits the secretion of inmunoreactive pituitary growth hormone Science, 1973; 179: 77-9.
9. Brown JW, Burton RC, Dahlin DC: Chemodectoma with skeletal metastasis: report of two cases. Mayo Clin Proc 1967; 42: 351-555.
10. Caplin ME, Buscombe JR, Hilson AJ, et al.: Carcinoid tumors Lancet 1998; 352: 799-805.
11. Carney JA: The triad of gastric epitheliod Leiomy o sarcoma, functioning extra-adrenal paraganglioma, and pulmonary chondroma, cancer, 1979; 43: 374-82.
12. Chambers EF, Norman D, Deds H, Ferrell LD: Primary nasopharyngeal chemodectoma. Neuroradiology, 1982; 23: 285-8.
13. Chambers RG; Mahonay WD: Carotid body tumors. Am J Surg, 1968; 116: 554-8.
14. Chung WB: The carotid body tumour. Can J Surg, 1979; 22: 319-22.
15. De La Hoz J, Brieva J: Tumores carcinoides y síndrome carcinoide. Rev Col Cir, 1996; 11: 337-43.
16. De La Hoz J: Feocromocitoma. Rev Col Cir, 1994; 9: 225-38.
17. Dent TL, Thompson NW, Fry WJ: Carotid body tumors. Surgery, 1976; 80: 365-72.
18. Dickinson PH, Griffin SM, Guy AJ: Carotid body tumor: Thirty years experience. Br J Surg, 1986; 73: 14-6.
19. DuBois J, Kelly W, McMenamin P, et al.: Bilateral carotid body tumors managed with preoperative embolization: A case report and review. J Vasc Surg, 1987; 5: 648-50.
20. Eng C: The RET proto-oncogene in multiple endocrine neoplasia type 2 and Hirschsprung’s disease. N Eng J Med, 1996; 335: 943-51.
21. Farrar T, Kirklin JW, Judd ES. Jr, et al.: Resection of carotid body tumors with preservation of the carotid vassels. Arch Surg, 1956; 72: 595-8.
22. Galland RB: Surgical aspects of carcinoid tumors. In: Surgical Endocrinology. Edited by Lynnand SR Bloom Butterworth- Heinemann Ltd. Oxford, 1993.
23. Glenner GG, Grimley PM: Tumors of the extra-adrenal Paraganglion system (including chemoreceptor). In: Atlas of tumors Pathology Washington DC, Armed Forces Institute of Pathology, 1974; 1-90.
24. Grimley PM, and Genner GG: Histology and ultrastructure of carotid body paragangliomas: Comparison with the normal gland. Cancer, 1967; 20: 1473-88.
25. Gruffermann S, Gillman MW, Pasternak R, et al.: Familial carotid body tumors: Case report and epidemiologic review. Cancer 1980; 46: 2116-22.
26. Gulya AJ: The glomus tumor and its biology. Laryngoscope, 1993; 103: 7-15.
27. Hallet JW Jr, Nora JD, Hollier LH, et al.: Trends in neurovascular complications of surgical management for carotid body and cervical paraganglioma: A 50 years experience with 150 tumors. J Vasc Surg, 1998; 7: 284-91.
28. Hallet JW: Carotid body and cervical chemodectomas: Cure withoud permanent disability. Semin Vasc Surg, 1991; 4: 159-66.
29. Hamberger CA, Hamberger CB, Wersall J, Wagermark J: Malignant catecholamine – producing tumour of the carotid body. Acta Pathol Microbiol Scand, 1967; 69: 489-92.
30. Heath D, Jago R and Smith P: The vascular anatomy of the Carotid Body. Cardiovasc Res, 1983; 17: 33-42.
31. Heath D: The human carotid body. In: Health and disease pathology, 1991; 164: 1-8.
32. Iafrati MD, O’Donell TF: Adjuvant techniques for the management of larger carotid body tumors: A case report and review. Cardiovasc Surg, 1999; 7: 139-45.
33. Krupski WC, Effeney DJ, Ehrenfeld WK, Stoney RJ: Cervical chemodectoma: Technical considerations and management options. Am J Surg, 1982; 144: 215-20.
34. Lack EE: Tumors of the adrenal gland and extra-adrenal paraganglioma. In: Atlas of tumor Pathology series 3, Fase 19. Washington, DC, Armed Forced Institute of Pathology, 1997.
35. Lack EE; Cubilla AL, Woodruff JM, et al.: Paraganglioma of the head and neck region: A clinical study of 69 patients. Cancer, 1977; 39: 397-409.
36. Lechter A, Naar J, Andrade O: Paragangliomas del cuerpo carotídeo. Rev Col Cir, 1992; 7: 86-9.
37. Litle VR, Reilly LM, Ramos TK: Preoperative embolization of carotid. body tumors: When is it appropriate? Ann Vasc Surg, 1996; 10: 464-8.
38. Lustrin E, Palestro C, Vaheesan K. Radiographic evaluation and assessment of paragangliomas. Otolaryngol Clin North Am. 2001;34:881-906
39. McPherson GA, Halliday AW, Mansfield AO: Carotid body tumors and other cervical paragangliomas, diagnosis and management in 25 patients. Br Surg, 1989; 76: 33-6.
40. Mafee M: Dynamic CT and its applications. J Otolaryngol, 1982; 11: 307-18.
41. Maier W, Marangos N, Laszig R: Paraganglioma as a Systemic Syndrome. Pitfalls and strategies. J Laryngol Otol, 1999; 113: 978-82.
42. McCaffrey T, Myssiorek D, Marinan M. Head and neck paragangliomas: Physiology and biochemistry. Otolaryngol Clin North Am, 2001; 34: 837-44.
43. Mellrad DC, Remine WH: Carotid body tumors. Surg Clin North Am, 1963; 43: 1135-44.
44. Meyer FB, Sundt TM Jr, Pearson BW: Carotid body tumors. A subject review and suggested surgical approach. J Neurosurg, 1986; 64: 377-85.
45. Mitchel DC, Clyne CA: Chemodectomas of the neck: The response to radiotherapy. Br J Surg, 1985; 72: 903-5.
46. Monro RS: The natural history of carotid body tumors and their diagnosis and treatment with a report of five cases. Br J Surg, 1960; 37: 445-53.
47. Muhm M, Polteraurer P, Gstottner W, et al.: Diagnostic and therapeutic approaches to carotid body tumors. Review of 24 patients. Arch Surg, 1997; 132: 279-84.
48. Mitchell RO, Richardson JD, Lambert GE: Characteristics, surgical management and outcome in 17 carotid body tumors. Am Surg, 1996; 62: 1034-7.
49. Myssiorek D. Head and neck paragangliomas: An overview. Otolaryngol Clin North Am, 2001; 34: 829-36.
50. Netterville JL, Reilly KM, Robertson D, et al.: Carotid body tumors: A review of 30 patients with 46 tumors. Laryngoscope 1995; 105: 115-26.
51. Nervous Regulation and Rapid Control of arterial pressure. In: Medical Physiology, A.C. Guyton (Ed) W.B. Saunders, Philadelphia, 1991; 194-204.
52. Nora J. Surgical resection of carotid body tumors: Long term survival, recurrence and metastasis. Mayo Clin Proc, 1988; 636: 348-52.
53. Olsen WL, Dilon WP, Kelly WM, et al.: MR imaging of paragangliomas. AJR. Am J Roentgenol, 1987; 148: 201-4.
54. Oszvath RR, Casey SO, Lustrin ES, et al.: Cerebral venography. Comparison of CT and MR projectional Venography. AJR. Am J Roentgenol, 1997; 169: 1699-1707.
55. Pantonawitz D, Davidge-Pitts K, Gaylis H, et al: Are carotid body tumors malignant? S Afr J Surg, 1990; 28: 97-9.
56. Patiño JF: El concepto APUD y los apudomas: unificación patobiológica de diversas neoplasias endocrinas. Hospital General Universitario de la Samaritana y colciencias, Bogotá, 1979.
57. Rao Archana B, et al.: Paragangliomas of the head and neck: Radiologic. Pathologic correlation. Radiographics, 1999; 14: 1605-32.
58. Reisine T: Somatostatin receptors. Am J Physiol, 1995, 269: 813-20.
59. Riegner: Cited by Lahey FH, Warren KW: A long term appraisal of carotid body tumors with remarks on their removal. Surg Gynec Obstet, 1951; 92: 481-6.
60. Reubi JC, Horisberger U, Laissue JA, et al.: High density of somatostatin receptors in veins surrounding human cancer tissue: Role in tumor host interaction? Int J Cancer, 1994; 56: 681-8.
61. Reese HE, Lucas RN, Besgman PA: Malignant carotid body tumor. Ann Surg, 1963; 157: 232-4.
62. Sánchez de Guzmán G.: Paragangliomas del cuerpo carotídeo. Experiencia en el Instituto Nacional de Cancerología. Acta de Otorrinolaringología y Cirugía de Cabeza y Cuello, 1999; 27: 145-52.
63. Saldana MJ, Salen LE, Travezan R: High altitude hipoxia and chemodectomas. Hum Pathol, 1973; 4: 251-63.
64. Schick PM, Hiesima GB, White RA, et al: Arterial cateter embolization followed by surgery for large chemodectoma. Surgery 1980; 87: 459-64.
65. Shamblin WR, ReMine WH, Sheps SG, Harrison EG Jr.: Carotid body tumor (chemodectoma). Clinicopathologic analysis of ninety cases. Am J Surg, 1971; 122: 732-9.
66. Shulak JM, O’Donovan PB, Paushter DM, et al.: Color flow doppler of carotid body paraganglioma. Ultrasound Med 1989; 8: 519-521
67. Smith RF, Shetty PC, Deddy DJ: surgical treatment of carotid paragangliomas presenting unusual technical difficulties. The value of preoperative embolization. J Vasc Surg, 1988; 7: 631-7.
68. Som PM, Curtin HD: Tumors of the temporal bone and the cerebellopontine angle. En: Som PM, Cortin HD (eds): Head and neck imaging, 3 edition, vol. 2. St Louis, Mosby, 1996; 915-51.
69. Steely WM, Davies RS, Brigham RA: Carotid body tumor and hyperparathyroidism: A case report and review of the literature. Am J Surg, 1987; 53: 337-8.
70. Tikkakoski T, Buotonen J, Loeinonen S, et al.: Preoperative embolization in the management of neck paragangliomas. Laryngoscope, 1997; 107: 821-6.
71. Trimas SJ, Mancuso A, de Vries EJ: Avascular carotid body tumor. Otolaryngol Head Neck Surg, 1994; 110: 131-5.
72. Valavanis A: Preoperative embolization of the head and neck. Indications, patient selection goals and precautions. AJNR. Am J Neuroradiol, 1985; 7: 943-52.
73. Van Gils APC, Van der May AGL, Hoogma RPLM, et al.: Iodine – 123 metaiodobenzylguanidine scintigraphy the head and neck region. J Nuc Med, 1990; 31: 873-8.
74. Vogl JJ, Juergens M, Balzer J, et al.: Glomus tumors of the skull base: Combined use of MR angiography and spin echo imaging. Radiology. 1994; 192: 103-10.
75. Warshawski SJ, de Souza FM: The carotid body tumor. J Otolaryngol, 1989; 18: 306-10.
76. Zbaren P, Lehmann W: Carotid body paraganglioma with metastasis. Laryngoscope, 1985; 95: 450-4.
Correspondencia:
Jaime De la Hoz
313 08 00 Cód.: 2876
Bogotá – Colombia

