En un capítulo del Manual de Oncología Quirúrgica (Patiño y col 1991) y en el capítulo correspondiente del texto Lecciones de Cirugía (Patiño 2001), hemos revisado el tema de los tumores del esófago y citamos a Klein y Weinhouse, entre otros autores, quienes hace años señalaron la muy amplia variación geográfica que existe en la incidencia del cáncer del esófago, tal vez la de mayor amplitud entre los tumores humanos. La tasa por 100.000 habitantes oscila en forma notable en las diversas regiones del mundo; se comparan estas diferencias geográficas con la incidencia del carcinoma en esófago de Barrett:

Anteriormente se observaba que más de 95% de los carcinomas del esófago eran carcinomas escamocelulares (epidermoides). Según Ferreira y Ferreira (1996), en el Brasil entre 1981 y 1985, 85,3% eran carcinomas epidermoides.
Es conocido que los adenocarcinomas primitivos del cuerpo del esófago han sido una minoría que se presenta casi exclusivamente en el tercio distal, muchos de éstos generalmente propagados del estómago o de la unión gastroesofágica, y que constituyen una entidad realmente diferente. En la serie de Lira, de Santiago de Chile, los adenocarcinomas representaron menos del 2% del total de 1.684 pacientes con tumores del esófago y cardias atendidos entre 1952 y 1982. En tres grandes series, con un total de 4.173 casos de carcinoma esofágico, la incidencia de adenocarcinoma varió entre 0,8% y 6,9% (DeMeester et al 1988).
Sin embargo, en muchos países se registra ahora una creciente incidencia del adenocarcinoma del esófago (Orringer 1998), así como del carcinoma del cardias, un fenómeno epidemiológico para el cual no existe una explicación clara. La frecuencia del adenocarcinoma ha llegado a representar más del 40% de los carcinomas del esófago en algunos países de Occidente, siendo el esófago de Barrett el principal factor etiológico (Peters & DeMeester 1994).

 |
 |
 |
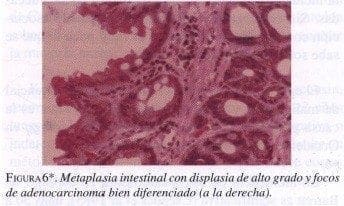 |
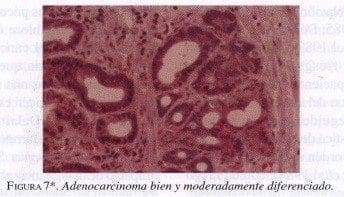
En los Estados Unidos y en Europa el gran incremento del adenocarcinoma esofágico ha llevado a que constituya más del 50% de los casos de neoplasia maligna del esófago (Orringer 1998). Según Swisher y asociados (1995), el cambio del carcinoma escamocelular por adenocarcinoma ocurrió en 1975, y en la actualidad en la Universidad de California en Los Angeles, el adenocarcinoma de la unión gastroesofágica y del esófago es el tipo histológico más frecuente; también señalaron que el porcentaje de adenocarcinomas de Barrett aumentó en forma significativa entre 1970 y 1993, tal vez por un más meticuloso seguimiento de los pacientes con epitelio de Barrett.
Se han planteado diversas hipótesis sobre la etiología del adenocarcinoma del esófago y del adenocarcinoma de la unión gastroesofágica (Patiño 2001) para tratar de explicar este notorio aumento en la incidencia que se registra en las últimas dos décadas. Sin embargo, excepto por su indudable asociación con el esófago de Barrett, es muy poco lo que se sabe sobre su etiología.
El epitelio de Barrett tiene un reconocido potencial de malignidad, y es ampliamente aceptado que es la causa principal de adenocarcinoma en el esófago en Occidente. Por el contrario, es raro en Japón.
La incidencia de adenocarcinoma en esófago de Barrett es significativa (Csendes et al 1983), unas 30 a 40 veces mayor que en la población normal, del orden de 14-15% (Cameron et al 1985; DeMeester & Barlow 1988) hasta 46% (Fekéte y col 1989). Sin embargo no está bien establecido el riesgo de desarrollar adenocarcinoma en aquellos pacientes que no lo tienen en el momento del diagnóstico del esófago de Barrett. Estudios sobre pacientes seguidos por varios años después establecido el diagnóstico de esófago de Barrett, relatan incidencias bajas, del orden de 1/441 (Cameron et al 1985) y 1/175 (Spechler et al 1984), con un rango de 1/56 a 1/441 (Peters & DeMeester 1994) paciente-años.
El American College of Gastroenterology estima una incidencia anual de cáncer en pacientes con esófago de Barrett de 1% a 2% anual, aunque estudios recientes revelan más bien una incidencia de 0,5% por año (Spechler 2001).
El riesgo de desarrollar carcinoma en un esófago de Barrett ha sido comparado con el riesgo de desarrollar carcinoma pulmonar en un fumador empedernido (Peters & DeMeester 1994).
Aunque la mayoría de los pacientes con esófago de Barrett no desarrolla adenocarcinoma (Cameron et al 1985), ello en ninguna forma disminuye la importancia de un seguimiento riguroso mediante endoscopia y citología a intervalos regulares (cada 6 meses a 2 años según los hallazgos histológicos iniciales y otros factores de riesgo individual), con el fin de detectar displasia severa o adenocarcinomas incipientes aún en pacientes sin lesión neoplásica visible.
Actualmente disponemos de pocas medidas para prevenir la aparición de carcinoma en un esófago de Barrett. En general éstas se reducen a tamizaje y a control endoscópico periódico y a esofagectomía profiláctica en presencia de displasia severa. El desarrollo de marcadores epiteliales, de estudios de DNA nuclear y de análisis molecular puede llegar a identificar los pacientes de alto riesgo de degeneración maligna (Pera et al 1994).
Vigilancia y Seguimiento
El seguimiento, o vigilancia, en pacientes con esófago de Barrett permite detectar y tratar lesiones malignas tempranas, con beneficio en cuanto a supervivencia. Pero apenas en unos pocos pacientes, 3,9%, con cáncer de esófago se establece el diagnóstico de Barrett con anterioridad al del cáncer, por lo cual los métodos actuales de vigilancia, que han demostrado ser efectivos, no habrán de lograr una modificación sustancial en la mortalidad por cáncer esofágico (Corley et al 2002). En el estudio de Dalai et al (2002), la prevalencia preoperatoria del Barrett en pacientes con carcinoma de esófago fue apenas 5%, lo cual reafirma el bajo impacto de la vigilancia endoscópica en la salud pública: el beneficio potencial de la vigilancia endoscópica parece estar limitados a unos pocos individuos en riesgo.
Como una entidad que se presenta en enfermos que padecen reflujo gastroesofágico crónico, es perentorio el seguimiento endoscópico durante el manejo de la enfermedad por reflujo gastroesofágico, ERGE. La razón para el seguimiento endoscópico es que a pesar del pronóstico ominoso del cáncer esofágico, la vigilancia endoscópica permite la detección precoz del cáncer o de lesiones precancerosas; la supervivencia a 5 años de un adenocarcinoma esofágico detectado en programas de vigilancia endoscópica es mayor que cuando se lo diagnostica en la fase sintomática, 62% versus 20% (ElKhoury & Sahai 2002).
La recomendación de la American Society for Gastrointestinal Endoscopy (1998) es que durante la vigilancia endoscópica se tome biopsia de cualquier hallazgo macroscópico anormal y que en un epitelio de Barrett de apariencia benigna se tomen biopsias de los cuatro cuadrantes a intervalos de 2 cm, comenzando a 1 cm por debajo de la unión gastroesofágica y hasta 1 cm por encima de la unión escamocolumnar. La frecuencia con que se debe efectuar el examen depende de la severidad de la displasia que se encuentre (ElKhoury & Sahai 2002).
A.J. Cameron (1997), de la Mayo Clinic, ha analizado en un editorial el dilema sobre cuál debe ser el protocolo de vigilancia por endoscopias secuenciales en pacientes con esófago de Barrett. Se refiere a dos estudios, uno por Provenzale et al (1994) y el otro por Drewitz et al (1997).
En el primero, los autores revisan los factores que pueden tener impacto sobre la eficacia de la vigilancia. Tales factores fueron: historia natural del esófago de Barrett y del adenocarcinoma, costos e implicaciones de la endoscopia, costo y morbilidad y mortalidad de la resección del esófago y el efecto de las diversas estrategias de manejo sobre la calidad de vida. La conclusión fue que, al considerar tanto la calidad como la duración de la vida, la endoscopia cada 2 a 3 años sería la más efectiva, aunque costosa. Si el costo es una consideración mayor, la endoscopia cada 5 años aumentaría la expectativa de vida con una efectividad del costo similar a la de otras conductas médicas comunes. Con base en la incidencia de cáncer de 1 por 75 paciente-año, Provenzale y colegas predicen que 27% de los pacientes con Barrett desarrollarían cáncer en el curso de la vida, una tasa que es superior a la de muertes por cáncer en pacientes con esófago de Barrett.
El otro estudio referido por Cameron es por Drewitz y asociados (1997). Es un estudio prospectivo sobre 177 pacientes con esófago de Barrett seguidos por un lapso promedio de 4,8 años. Cuatro desarrollaron adenocarcinoma, lo cual corresponde a una incidencia de 4%, 1 por 208 paciente-año, incidencia que no es significativamente diferente de la informada por Tytgat en una revisión de 18 informes previos, en que el riesgo de cáncer osciló entre 1 en 46 y 1 en 441 paciente-año. Uno de los pacientes de Drewitz tuvo un cáncer que no fue visible en la endoscopia.
Anota Cameron que la vigilancia a corto plazo, o sea, de unos pocos años, puede sobrestimar el riesgo de cáncer a largo plazo. Es posible que adenocarcinomas microscópicos que ya están presentes en el momento de ingreso al protocolo de seguimiento, pueden no ser detectados por una inadecuada toma de la biopsia. Por otra parte, estudios retrospectivos pueden subestimar el riesgo, por cuanto la presencia de células caliciformes (características de la metaplasia intestinal) no eran un requerimiento de ingreso al protocolo, lo cual quiere decir que pacientes calificados como Barrett realmente no lo eran.
Y como lo anota Sprung en un comentario al editorial de Cameron, pacientes con un tumor indolente pueden sobrevivir 5 a 8 años después del diagnóstico, aunque la mayoría muere en los primeros 2 años.
Katz et al (1998), de la Universidad de Wisconsin, recomiendan seguimiento endoscópico cada ž2 años luego de la biopsia inicial, cuando ésta es negativa o indeterminada para displasia, lo cual ha probado ser un método seguro, en su experiencia, y que reduce costos al comparar con el protocolo de seguimiento anual.
La vigilancia endoscópica es costosa. Según Achkar et al (1988) de la Clínica Cleveland, el costo directo del seguimiento de pacientes con epitelio columnar en el esófago es de US$62.000 por cada carcinoma detectado.
DeMeester y DeMeester (2000), quienes preconizan seguimiento endoscópico anual en pacientes con Barrett de cualquier longitud, y cada 3 a 6 meses cuando hay displasia de bajo grado, calculan el costo de la vigilancia con el de la mamografía: el de la endoscopia por cada cáncer de esófago detectado es US$37.928, contra US$54.513 por cada cáncer mamario detectado; por cada vida salvada, la diferencia es dramática: US$4.151 para la endoscopia y US$57.926 para la mamografía.
¿Qué hacer? La recomendación clásica ha sido un seguimiento endoscópico anual. El beneficio de esta conducta ha sido puesto en duda, y el costo es alto. El seguimiento a intervalos de 2 a 5 años podría ser más apropiado en pacientes con un Barrett en que no haya anormalidades focales y no se demuestre displasia en la biopsia. En nuestros servicios de la Fundación Santa Fe de Bogotá seguimos practicando la endoscopia anual como conducta general en todos los pacientes con esófago de Barrett.
Por otra parte, algunos autores han aconsejado un protocolo de seguimiento en displasia de alto grado a fin de evitar la resección quirúrgica (Levine et al 1993). Hoy se acepta universalmente que el seguimiento no está indicado en pacientes con diagnóstico de displasia de alto riesgo, por cuanto un porcentaje muy considerable alberga carcinoma invasor oculto, más del 40%, como se discute más adelante. Por ello, tales pacientes deben ser sometidos a resección “profiláctica”; en el espécimen de resección se halla un alto número de carcinomas que no habían sido detectados en las biopsias preoperatorias (Ferguson & Naunheim 1997; Nigro et al 1999; Peters et al 1994; Reid et al 1988).
El desarrollo de métodos que permitan diferenciar los pacientes de más alto grado de transformación neoplásica permitiría establecer mejores protocolos de seguimiento
La progresión neoplásica se caracteriza por la aparición secuencial de células que asumen, sucesivamente, fenotipos más aberrantes. Tales fenotipos pueden ser detectados mediante técnicas histológicas y de citometría de flujo, en la medida que el proceso avanza de la metaplasia especializada del Barrett negativa para displasia, hacia displasia de bajo grado, displasia de alto grado y adenocarcinoma. La aneuploidia y una mayor población de G2/tetraploidia son precursores de carcinoma en el esófago de Barrett, e indican inestabilidad genómica, según Reid et al (1992), quienes proponen usar una combinación de histología y citometría de flujo para identificar los subgrupos de pacientes que por ser de mayor riesgo, ameriten protocolos de seguimiento más estricto. Evidentemente, la citometría de flujo permite determinar el contenido nuclear de ADN y sus cambios según la progresión de la secuencia metaplasia-displasia-carcinoma (Casson 2002; Guindi & Riddell 2002), como se describió en párrafos anteriores.
R.E. Sampliner (2002), de la Universidad de Arizona, recomienda el siguiente esquema de seguimiento en pacientes con displasia, reconociendo que ésta representa el primer paso en la progresión hacia carcinoma:

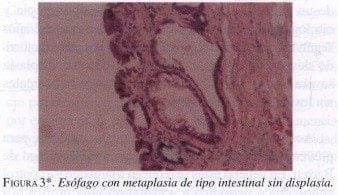
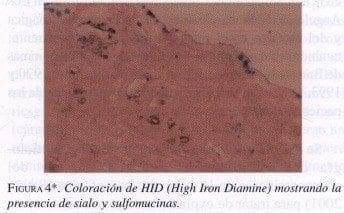
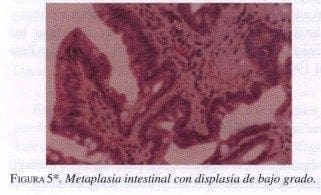
* Microfotografías cortesía del Dr. RAFAELAADRADI; Departamento de Patología, Fundación Santa Fe de Bogotá.