Estudios Experimentales
Evaluación de las Concentraciones Séricas de Enzimas Hepatocelulares
CAMARA NETO R. D., SOUZA A. P, COELHO A. R. B., FERRAZ A. A. B., LIMA FILHO J. F. C., FERRAZ E. M., CAMARA NETO J. B.
Trabajo realizado en el Laboratorio de Cirugía Experimental del Departamento de Cirugía del Centro de Ciencias de la Salud y del Hospital de las Clínicas de la Universidad Federal de Pernambuco, Brasil.
Palabras clave: Hígado, Isquemia, Reperfusión, Descompresión portal, Aspartato aminotransferasa (AST), Alanino aminotransferasa (ALT), Deshidrogenasa láctica (DL), Perros experimentales.
La lesión corriente de isquemia y reperfusión hepáticas normotérmicas ha sido investigada a través de varios modelos experimentales en perros. La intensidad de necrosis hepatocítica ha sido admitida como proporcional al tiempo de isquemia y a la cantidad de hígado desvascularizado. En el presente trabajo, un modelo de isquemia y reperfusión he-páticas en perros fue evaluado a través de enzimas indicativas de necrosis hepatocelular. Veinte perros mestizos con peso corporal de 15.25 ± 1.25 kilos, bajo anestesia general, fueron agrupados de la siguiente manera: 1- Grupo test (n=10), los animales fueron sometidos a desvascularización hepática del 70% durante noventa minutos, con descompresión venosa esplácnica a través de los lóbulos lateral derecho y caudado, seguido de revascularización del hígado.
2- Grupo control (n=10), los perros fueron sometidos a operación simulada. Se determinaron las concentraciones séricas de asparato aminotransferasa, alanino aminotransferasa, deshidrogenasa láctica, 5 minutos antes de la isquemia (To), 5 minutos antes de la revascularización (T1), 1 hora (T2) y 5 horas (T3) después de la revascularización hepática, en la sangre de la vena cava inferior, a nivel de la aurícula derecha. Con una seguridad del 95%, los resultados demostraron que: a) En el período de isquemia no se detectó alteración alguna significativa en las concentraciones de aspartato aminotransferasa, alanino aminotransferasa, deshidrogenasa láctica. b) Después de la reperfusión hepática, hubo aumento significativo y persistente de los niveles de estas enzimas. Los resultados son indicativos de que el tiempo de isquemia y el volumen de hígado desvascularizado fueron capaces de producir la necrosis hepática buscada.
Introducción
La utilización de perros sobre todo cuando se someten a medios de descompresión venosa esplácnica, facilita la investigación de isquemia hepática normotérmica por período de tiempo prolongado (15, 19, 34, 35, 53, 58, 59).
Las lesiones de isquemia y reperfusión hepáticas han sido evaluadas mediante las enzimas comunes de citólisis hepato-celular, tales como: Aspartato aminotransferasa (AST), Alanino aminotransferasa (ALT), y la Deshidrogenasa láctica (DL).
La intensidad de estas lesiones han sido relacionadas no sólo por la cantidad de parénquima hepático sometido a hipoxia tisular, sino también al tiempo de isquemia (14, 47, 53, 58).
El lapso de 90 minutos de isquemia hepática ha sido admitido como suficiente en experimentos in vivo, para ocasionar liberación significativa de enzimas hepatocelulares, indicativas de citólisis, así como también para producir lesión histológica del tipo Necrosis 46. Tal período ha sido admitido como suficiente para la realización de resecciones hepáticas complejas y de anastomosis vasculares durante el trasplante de hígado (4, 31).
En el presente estudio, en el modelo propuesto, la cantidad de tejido hepático sometido a isquemia, estimada entre el 70 y el 75% del total,representada por la suma de los lóbulos hepáticos (LMD, LQ, LME, LLE y PPCC) (13, 22, 41, 42, 44, 54); podría simular guardadas las diferencias en cuanto a la preservación del órgano, situación verificada en el trasplante hepático (2, 7, 8, 10-12, 20, 25, 43, 50, 60).
El presente trabajo, etapa inicial de un proyecto de estudio sobre isquemia y reperfusión hepáticas, pretende en esencia, investigar en un modelo propuesto para perros, resultados de concentración de AST, ALT y DL, antes y después de la inducción de 90 minutos de isquemia, seguida de reperfusión hepática.
Materiales y Métodos
Veinte perros mestizos de ambos sexos con peso corporal de 15.25 ± 1.21 kg, bajo inducción con Tiopental (4 a 6 mgr/kg), fueron intubados y sometidos a respiración controlada con volumen corriente de 15 mL/kg, Fi02 de 21% y frecuencia respiratoria de 16 ciclos/mto. La anestesia gene-ral fue manejada con Cetamina (1 a 2 mg/kg) y Pancuronio (0.1 a 0.2 mg/kg) por vía i.v. Después de abrir la cavidad peritoneal, los animales fueron distribuidos en dos grupos experimentales:
GRUPO TEST (n=10). Los ligamentos hepato-renal, triangular izquierdo, falciforme y gastrohepático fueron des-conectados del hígado. El colédoco, las arterias hepáticas común y gastroduodenal, así como la rama izquierda de la vena porta fueron incluidos, produciéndose de este modo la exclusión vascular normotérmica de los lóbulos medial derecho (LMD), cuadrado (LQ), medial izquierdo (LMI), lateral izquierdo (LLI) y el proceso papilífero del lóbulo caudado (PPLC), por un período de 90 minutos; durante este período, la descompresión del territorio venoso esplácnico fue realizada por la rama derecha de la vena porta, a través del lóbulo derecho y del proceso caudado del lóbulo cuadrado, sometidos apenas a la interrupción del flujo arterial (Figura 1).
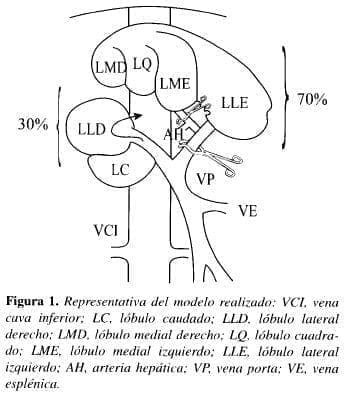
El flujo sanguíneo al hígado era restablecido y, luego de la reperfusión, se procedía a la exclusión vascular de los lóbulos hepáticos utilizados para descompresión esplácnica. Después de esos procedimientos, estos lóbulos eran resecados, cauterizándose la superficie hepática con bisturí de argón.
GRUPO CONTROL (n=10). En este grupo, los animales fueron sometidos solamente a disección y aislamiento de los elementos anatómicos del pedículo hepático.
En todos ellos se investigaron en forma sistemática, niveles de concentración de aspartato aminotransferasa (AST – U/L), alanino aminotrasnfersa (ALT – U/L) y deshidrogensasa láctica (DL – U/L), determinados a 5 minutos de isque-mia (T0), 5 minutos antes de la reperfusión hepática (T1), y 15 minutos (T2), 1 hora (T3), 3 horas (T4) y 5 horas (T5) después de la reperfusión del hígado.
Las concentraciones de las ALT y de las AST fueron dosificadas por el método de Reitman y Frankel, y las concentraciones de las DL por el método de Whitaker, en muestras de sangre obtenidas de la cava inferior a nivel del atrio derecho, siendo los resultados expresados en U/L.
En el análisis estadístico realizado con los datos de AST*, ALT* y DL*, se procedió a la aplicación del Test “t” de Student del modo intragrupo e intergrupo. En todo el estudio estadístico el nivel de confiabilidad escogido fue del 95%.
El experimento fue conducido, aplicándose los principios del código de ética para investigaciones biomédicas en animales, de la OMS**.
Resultados
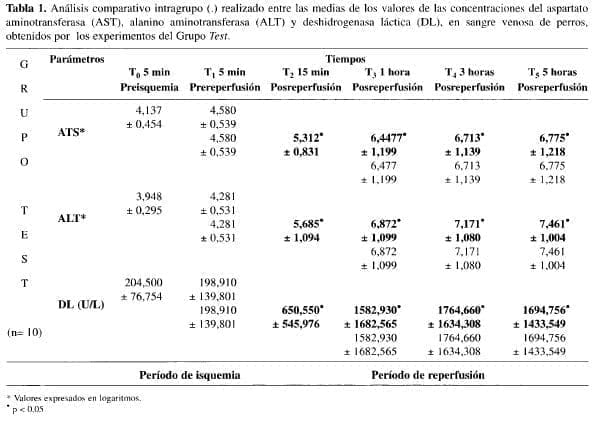
1. Período de isquemia (90 minutos). No se evidenciaron alteraciones significativas entre los niveles medios de las concentraciones de AST, ALT y DL, tanto en el análisis comparativo intragrupo como en aquel realizado entre los grupos, durante el período de isquemia hepática (Tablas 1, 2 y 3).
2. Período de reperfusión (5 horas). En el grupo test, después de la reperfusión hepática, se encontró que a partir del tiempo T2 (15 minutos post-reperfusión) hubo aumento significativo de las concentraciones de AST, ALT y DL, si tomabamos como comparación los niveles medios obtenidos en el tiempo T1 (5 minutos antes de la reperfusión) (Tabla 1). En este mismo cuando se comparó los medios de las concentraciones de estas enzimas, obtenidos en los tiempos T4 y T5, con aquellos verificados en el tiempo T3, no hubo demostración de diferencias estadísticamente significativas (Tabla 1).
En el grupo control, cuando se procedió a la comparación entre los niveles medios de las concentraciones de AST, ALT y DL, obtenidos en los tiempos estudiados después de la reperfusión hepática (T2, T3, T4 y T5) con las medidas de los valores obtenidos antes de la reperfusión (“t”) no se evidenciaron alteraciones estadísticamente significativas. Excepto en relación con AST, en la quinta hora (T5) (Tabla 2).

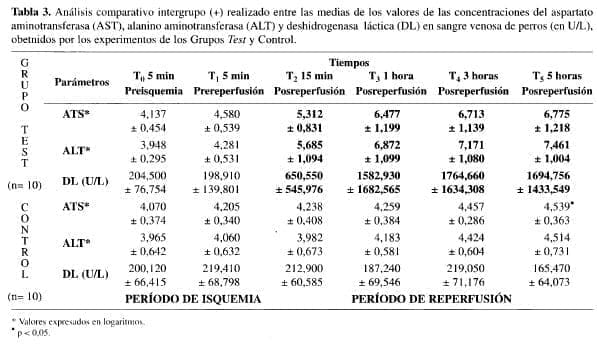
Durante la fase de reperfusión hepática, el análisis comparativo realizado con los experimentos del grupo test, evidenció aumentos significativos de los valores medios de las concentraciones de AST, ALT y DL, cuando se compararon con aquellos determinados, en tiempos correspondientes, en los experimentos del grupo control (Tabla 3).
Discusión
Enzimas citoplasmáticas capaces de expresar lisis celular, han sido estudiadas en modelos experimentales de isquemia y reperfusión hepáticas siendo consideradas, por tal pro-piedad, como marcadores de lesión de reperfusión hepática. Tales estudios incluyen referencias sobre el aspartato aminotransferasa y/o alanino aminotransferasa (1, 5, 6, 8, 11, 14, 17, 28, 21, 24, 26, 27, 29, 30, 33, 36-38, 40, 41, 45, 47, 50, 52, 57, 59, 60, 61, 63), bien sobre la deshidrogenasa láctica (14, 17, 21, 26-28, 35, 36, 52, 57, 60), en grandes resecciones hepáticas practicadas en humanos (16, 31, 32, 41, 51) y en trasplantes de hígado, clínicos o experimentales (3, 9, 23, 37, 39, 40, 44, 48, 49, 56, 62); las aminotransferasas séricas también han sido utilizadas para calificar la intensidad de isquemia ocurrida.
Las aminotrasnferasas, junto con otros indicadores como las bilirrubinas, volumen de bilis producida y disturbios de coagulación, han sido usados con el objeto de valorar la función inmediata del injerto hepático de trasplantes clínicos, reconociéndose que niveles enzimáticos por encima de 3.000 UI/L son indicativos de ausencia de función, y niveles de 2.000 UI/L sugieren disfunción primaria del injerto.
En el presente trabajo, la sangre para determinación de las concentraciones de las enzimas estudiadas, fue tomada de la vena cava inferior supra-hepática de los animales, utilizándose para eso, el catéter de determinación de presión venosa central, pues ha sido recomendado como el más adecuado para la obtención más precisa de componentes del flujo he-pático (10, 12, 60), evitando o minimizando de este modo los inconvenientes propios de las tomas realizadas en sangre pariférica.
Autores: Renato Dornelas Cámara Neto; Ayrton Ponce de Souza; Antonio Roberto de Barros Coelho; Alvaro Antonio Bandeira Ferraz; José Falcão Corrêa Lima Filho; Edmundo Machado Ferraz; José Bezerra Câmara Neto.
Los valores de las medidas de concentraciones del aspartato aminotransferasa y alanino aminotransferasa, fueron inicialmente transformados en logaritmos neperianos para la obtención de distribuciones Gaussianas y ulterior aplicación del test “(“.
** Howard Jones, N. Acioms: Ethical code .!ÍJr animal experimentatioll. WHO Chronide 1985; 39(2): 51-6.
En los grupos experimentales estudiados, cuando el aspartato aminotransferasa, el alanino aminotransferasa y la deshidrogenasa láctica fueron analizados durante el período de 90 minutos de isquemia hepática, mediante comparación entre la media de los valores de esas enzimas obtenidos en el tiempo T1 y la media de los valores obtenidos en el tiempo T0, no se demostró la existencias de diferencias estadísticamente significativas entre ellas, lo que sugiere que las concentraciones de esas enzimas permanecieron inalteradas durante ese período, posiblemente como resultado del flujo sanguíneo inexistente o mínimo en el área del hígado sometida a isquemia (Tablas 1, 2 y 3). Otros autores también hacen referencia de hallazgos de ese tipo (17, 37, 55).
Así Souza y cols, en estudio de necrosis hepática aguda inducida en perros por isquemia vascular en dos tiempos, observaron niveles de aminotransferasa inalterados en la sangre venosa periférica de los animales, atribuyéndose este resultado a probable inexistencia o existencia mínima de flujo sanguíneo hepático, que impediría el transporte de esas enzimas del hígado hacia la vena cava inferior (55). Esos autores sugieren además, que tal posibilidad llegaría a ocu-rrir aun en presencia de vías sanguíneas accesorias al hígado, siempre y cuando que tales vías fuesen de poca importancia en cuanto al flujo sanguíneo en ellas presente, al punto de no estar capacitadas para facilitar el paso de esas enzimas, en cantidades detectables desde el hígado hacia la circulación sistémica, en tiempos cortos de sobrevida (55).
En los experimentos, cuando se procedió al estudio intragrupo entre las medias de los valores de cada enzima estudiada, obtenidos en los tiempos después de la reperfusión hepática, y las medias de los valores de esas enzimas obtenidos 5 minutos antes de la reperfusión (T1), se comprobó que a partir de los 15 minutos de iniciada la reperfusión (T2), ocurrieron aumentos estadísticamente significativos (Tabla 1). En ese mismo grupo, la comparación entre cada una de las medias de los valores de la aminotransferasa obtenidos en el tiempo T4 y T5, y la media de los valores de esas enzimas obtenidos en el tiempo T3, no demostró que ocurrieran diferencias estadísticamente significativas (Tabla 1). El nivel máximo de elevación de esas enzimas ocurrió en el tiempo T3, permaneciendo estable hasta el final de las verificaciones. El mismo estudio en relación con la deshi-drogenasa láctica, demostró que esta enzima presentó resultados semejantes a los obtenidos con las aminotransferasas (Tabla 1).
En el grupo control, el estudio comparativo entre cada una de las medias de los valores de las enzimas analizadas, obtenidos en los tiempos programados para el estudio durante la fase de reperfusión del hígado y la media de los valores de las referidas enzimas obtenidos en el tiempo T1, no demostró diferencias estadísticamente significativas, excepto con relación a la AST en la quinta hora (Tabla 2).
El análisis comparativo realizado entre los experimentos del grupo test y los del grupo control, demostró la ausencia de diferencias estadísticamente significativas entre ellos, con relación a las concentraciones de AST, ALT y DL, durante el período de isquemia hepática, diferente a lo encontrado con relación a este parámetro durante la fase de reperfusión (Tabla 3).
Los aumentos de esas enzimas verificados en los tiempos programados para el estudio durante el período de reperfusión en los experimentos del grupo test (Tabla 1), pudieron haber sido provocados no solamente por el transporte de las referidas enzimas del hígado lesionado hacia la vena cava inferior durante la recirculación del órgano, además de la acción agravante de la propia reperfusión sobre el tejido hepático ya lesionado por la efectiva isquemia inducida. A propósito, Wu y cols, refieren que las enzimas liberadas por el hígado isquémico alcanzan el nivel máximo en la sangre a los 30 minutos después de iniciada la reperfusión, manteniendo valores aún elevados hasta los 120 minutos de este período. Para esos autores esto representaría evidencia de liberación de enzimas producidas durante el período de isquemia hepática (62). Tales observaciones permiten deducir que en esas circunstancias, los altos niveles de en-zimas después de 120 minutos de recirculación del hígado pudieran estar relacionados con la lesión inducida por reperfusión.
El nivel máximo de elevación de las aminotransferasas y de la deshidrogenasa láctica en el modelo experimental de isquemia y reperfusión del hígado, al igual que en la clínica, parece variar de acuerdo con la especie animal utilizada en el estudio, como también con el tipo y la duración de la isquemia inducida. Así, Peng y cols, estudiando el comportamiento de las enzimas citolíticas en ratones sometidos a isquemia y reperfusión hepáticas, encontraron niveles máximos de la concentración de la ALT en la tercera y quinta hora post-perfusión (50). En esos animales los autores comprobaron que no obstante los niveles de esta enzima descen-dieron después de esos tiempos, permanecieron aún elevados 24 horas después de la recirculación (50). Tomizawa y cols., estudiando ese aspecto en perros, obtuvieron niveles máximos de ALT y DL a los 120 minutos después de iniciada la reperfusión hepática (60). Helling y cols, en estudio de isquemia hepática regional efectuado en cerdos, comprobaron que la AST alcanzó elevación máxima a los 30 minutos de iniciada la recirculación del órgano, seguida de caídas a niveles que se mantuvieron elevados hasta por 24 horas de la reperfusión (28).
Los resultados obtenidos en el presente trabajo, en lo que se refiere a las enzimas séricas investigadas, permiten admitir que el modelo experimental propuesto, fue capaz de inducir isquemia hepática, evitando o minimizando la participación de vías colaterales accesorias en el suplemento sanguíneo del hígado, además de la posibilidad de circulación de sangre entre los lóbulos, debido a la disposición anatómica de la vascularización intrahepática. Esto pudo haber contribuido para que la perfusión hepática indeseada no hubiese ocurrido o, en eventualidad diferente ,se hubiese efectuado con flujo máximo, durante el período de isquemia inducida.
Es pertinente mencionar que la presencia de necrosis a la óptica microscópica de manera significativa y progresiva en los hígados de los animales del grupo test, es también indicativa de que haya sido alcanzada la lesión de isquemia y reperfusión hepáticas que se pretendía en la presente investigación.
Conclusiones
En las condiciones de experimentación del presente trabajo, no se encontraron aumentos significativos en las concentraciones de AST, ALT y DL durante el período de isquemia hepática. Después de la reperfusión del hígado ocurrieron aumentos significativos y persistentes en los niveles de estas enzimas.
Abstract
The ordinary ischemic lesion and the reperfusion normo-thermic injury of the liver have been investigated in various canine experimental models. The severity of hepatic necrosis has been shown to be proportional to the time length of ischemia and to the volume of devascularized hepatic tissue.
We have studied a dog model of ischemia and reperfusion by determination of the levels of enzymes related to hepatic necrosis. Twenty mongrel dogs weighing 15.25 +/- 1.25 Kg were subjected to general anesthesia and divided in two groups: 1 – Test group (n=10), comprised by dogs under-going devascularization of 70% of the hepatic parenchyma for a ninety-minute period, with venous splanchic decompression through the right lateral and caudate lobes,
followed by hepatic revascularization. 2- Control group (n=10), dogs undergoing Sham operation. Determination of serum levels of aspartate aminotranspherase, alanine aminotranspherase, and lactic dehydrogenase were done 5 minutes prior to ischemia (T0), 5 minutes before revascula-rization (T1), 1 hour (T2) and 5 hour (T3) following revascularization, in inferior caval blood samples taken at the level of the right atrium. With a 95% confidence level, our results demonstrated that: a) no significant change of enzyme serum levels was detected during the period of ischemia. b) following hepatic reperfusion there was a significant and persistent rise in the enzyme serum levels. These results are indicative that both the time of ischemia and the bulk of devascularized liver parenchyma were capable of producing the expected degree of hepatic necrosis.
Referencias
1. Aril S, Monden, K, Adachi, et al: Patho-genic role of Kupffer cell activation in the reperfusion injury cold-preserved liver. Transplantation 1994; 58 (10): 1072-7
2. Asakawa H, Jeppssonn B, Mack P,et al: Acute ischemic liver failure in the rat: a reproducible model not requiring portal decompression. Eur Surg Res 1989; 21: 42-8
3. Avolio AW, Agnes S, Pelosi G, et al: Intraoperative trends of oxygen consumption and blood lactate as predictors of primary dysfunction after liver transplantation. Transplant Proc 1991; 23 (4): 2263-5
4. Blanot S, Gillon MC, Lopes I, et al: Circulating endotoxins and postreperfusion syndrome during orthotopic liver transplantation 1995; 60 (1): 103-6
5. Brass CA, Nunes F Nagpal R: Increased oxyradical production during reoxygenation of perfused rat liver. Transplantation 1994; 58 (12): 1329-35
6. Buckber GD, Ono H, Joseph WL, et al: Hypotension following revascularization of the anoxic liver: factors influencing its occurrence and prevention. Surgey 1968; 63 (3): 446-58
7. Canada AT, Stein K, Martel D, et al: Biochemical appraisal of models for hepa-tic ischemia – reperfusion injury. Circ Shock 1992; 36: 163-8
8. Chavez – Cartaya RE, Desola GP, Wright L, et al: Regulation of the complement cascade by soluble complement receptor type 1: protective effect in experimental liver ischemia and reperfusion. Transplantation 1995; 59 (7): 1047-52
9. Cherqui D, Emond JC, Pietrabissa A, et al: Segmental liver transplantation from living donors: report of the technique and prelimi-nary results in dogs. H.P.B. Surgery 1990; 2: 189-204
10. Colletti LM, Kunkel SL, Walz A, et al: The role Cytokine networks in the local liver injury following hepatic ischemia reperfusion in the rat. Hepatology 1996; 23 (3): 506-14
11. Colletti LM, Remick GD, et al: Role of tumor necrosis factor- a in the pathophy-siologic alterations after hepatic ische-mia/reperfusion injury in the rat. J Clin Invest 1990, 85: 1936-43
12. Cursio R, Gugenheim J, Tovey M, et al: Protective properties of anti-IFNa/b Anti-bodies in normothermic hepatic ischaemia in the rat. Transplant Proc 1996; 28 (1): 73-4
13. Deweese MS; Lewis Jr. C, Mich AA: Partial hepatectomy in the dog: an experimental study. Surgery 1951; 30 (4):642-51
14. Dhar DK, Nagasue N, Kimoto T, et al: The salutary effect of FK 506 in ischemia-reperfusion injury of the canine liver. Transplantation 1992; 54 (4): 583-8
15. Duchinova SL: Ueber temporäre Abklem-mung des lig. Hepato-duodenale fuer bltlose Operationen an der Leber. Zentra-lorg. Chir 1925; 35: 581-2
16. Emond J, Wachs ME, Renz JF, et al: Total vascular exclusion for major hepatectomy in patients with abnormal liver parenchyma. Arch Surg 1995; 130: 824-31
17. Farkouh EF, Daniel AM, Beaudoin J, et al: Predictive value of liver biochemistry in acute hepatic ischemia. Surg Gynecol Obstet 1971; 132: 832-8
18. Fernandes LP, Rocha MC, Picinato MA, et al: Comportamento enzimatico e funcao mitocondrial hepatica durante isquemia normotermica do figado e apos reperfusao em caes. Anais III Congresso da Associa-ção Brasileira de Transplantes de Órgãos, São Paulo SP-Tema Livre no 068, 1992
19. Fernandes LP, Rocha MC, Silva Jr. OC: Estudo hemodinamico na derivacao veno-venosa passiva durante isquemia e reperfusao hepatica em caes. Acta Cir Bras 1993; 8 (2): 59-62
20. Flye MW, YU S: The synergistic effect superoxide dismutase and adenosine tri-phosphate – MgCl2 on acute hepatic ischemia. Transplant Proc 1987; 19 (1): 1324-6
21. Fukuzawa k, Empre S, Senyuz O, et al: N-acetylcysteine ameliorates reperfusion injury after warm hepatic ischemia. Trans-plantation 1995; 59 (1): 6-9
22. Furnival CM, Mackenzie RJ, Blumgart LH: The mechanism of impaired coagulation after partial hepatectomy in the dogs. Surgs Gynecol Obstet 1976; 143: 81-6
23. García-Valdecasas JC, Rull R., Grande L, et al: Prostacyclin, thromboxane, and oxigen free radicals and postoperative liver function in human transplantation. Transplan-tation 1995; 60 (7): 662-7
24. Harris KA, Wallace C, Wall WJ: Tolerance of the liver to ischemia in the pig. J Surg Res 1982; 33: 524-30
25. Hayashi H, Chaudry IH, Clemens MG, et al: Hepatic ischemia models for determining the effects of ATP-MgCl2 treatment. J Surg Res 1986; 40: 167-75
26. Hayashi T, Nagasue N, Kohno H, et al: Beneficial effect of cyclosporine pretreatment in preventing ischemic damage to li-ver in dogs. Transplantation 1988; 46 (6): 923-4
27. Helling TS, Hacker KA, Kragel PJ, et al: Evidence for cytoprotection by prosta-glandin E1 with normothermic hepatic ischemia. J Surg Res 1994; 56 (4): 309-13
28. Helling TS, Wogahn BM, Olson SA, et al: The effect of prostaglandin E1 on liver Adenine nucleotides and cytoplasmic enzymes in a porcine model of normothermic hepatic ischemia. Hepatology 1995; 22 (5): 1524-8
29. Hirakl S, Nishida M Takao K, et al: Effects of hepatic denervation on ischemia-reper-fusion injury in dogs. Transplant Proc 1996; 28 (3): 1275-8
30. Hirasawa H, Chaudry IH, Baue AE: Improved hepatic funtion and survival with adenosive triphosphate – magnesium chloride after hepatic ischemia. Surgery 1970; 83 (6): 655-2
31. Huguet C, Nordlinger B, Bloch PA, et al: Liver ischemia for hepatic resection: Where is the limit? Surgery 1992; 111: 251-9
32. Huguet C, Nordlinger B, Bloch P, et al: Tolerance of the human liver to prolonget normothermic ischemia. Arch Surg 1978; 113: 1448-51
33. Ikeda T, Yanaga K, Kishikawa K, et al: Ischemic injury in liver transplantation: Difference in injury sites between warm and cold ischemia in rats. Hepatology 1992; 16 (2): 454-65
34. Ishizaki N, Zhu Y, Zhang S, et al: Compa-rison of various lazaroid compounds for protection against ischemic liver injury. Transplantion 1997, 63 (2): 202-8
35. Jin Mb, Yamagishi H, Ochiai T, et al: Protective effect of FK 506 on hepatic energy metabolism in warm ischemic canine livers induced by total hepatic vascular exclusion. Transplant Proc 1996; 28 (2): 1108-10
36. Kahn D, Hickman R, Dent DM, et al: For how long can the liver tolerate ischaemia? Eur Surg Res 1986; 18: 277-82
37. Kamachi H, Nakajima Y, Isai H, et al: Study of liver function in a graft suffering from warm ischemia in porcine liver transplantation. Transplant Proc 1996; 28 (3): 1789-91
38. Kim YI, Kai T, Kitano S, et al: Hepatopro-tection by a PGI2 analogue in complete warm ischemia of the pig liver. Transplantation 1994; 58 (8): 875-9
39. Kusano T, Shiraishi M, Miyaguni T, et al: Organ preserving effect of lidocaine admi-nistration in the model of orthotopic liver transplantation from non-heart-beating donors. Transplant Proc 1996; 28 (3): 1928-9
40. Liu W, Schiob O, Pugmire JE, et al: Glycohydrolases as markers of hepatic ischemia-reperfusion injury and recovery. Hepatology 1996; 24 (1):157-62
41. Mackenzie RJ, Furnival CM, WOOD CB, et al: The effects of prolonged hepatic ischaemia before 70 per cent partial hepatec-
tomy in the dog. Br J Surg 1977; (1): 66-9
42. Maki T, Slapak M: Can a heterotopically placed segmental liver graft be life-supporting? An affirmative finding. Br J Surg 1974; 61: 33-9
43. McCurry KR, Campbell Jr. DA, Scales WE, et al: Tumor necrosis factor, interleukin 6, and the acute phase response following hepatic ischemia/reperfusion. J Surg Res 1993; 55 (1): 49-54
44. Mizumoto R, Yokota T, Ohsawa J, et al: orthotopic partial hepatic transplantation in dog. Jpn J Surg 1974; 4 (2): 121-9
45. Nakamura S, Nishiyama R, Serizawa A, et al: Hepatic release of endothelial after warm ischemia. Transplantation 1995; 59 (5): 679-84
46. Nauta RJ, Tsimoyiannis E, Uribe M, et al: Oxigen-derived free radicals in the hepatic ischemia and reperfusion injury in the rat. Surg Gynecol Obstet 1990; 171: 120-5
47. Nordlinger B, Douvin D, Javaudin L, et al: An experimental study of survival after two hours of normothermic hepatic ischemia. Surg Gynecol Obstent 1980; 150: 859-64
48. Ohkohchi N, Sasaki T, Namiki H, et al: Liver transplantation in dogs after 30 mi-nutes of warm ischemia. Tohoku J Exp Med 1986; 148: 285-94
49. Olson LM, Klintmalm GB, Husberg BS, et al: Superoxide dismutase improves organ preservation in liver transplantation. Transplant Proc 1988; 20 (Suppl. 1): 961-4
50. Peng XX, Currin RT, Thurman RG, et al: Protection by pentoxiflylline against normothermic liver ischemia/reperfusion in rats. Transplantation 1995; 59 (11): 1537-41
51. Pichlmayr R, Grosse H, Hauss J, et al: Technnique and preliminary results of extracorporeal liver surgery (bench procedure) and of surgery on the in situ perfused liver. Br J Surg 1990; 77 (1): 21-6
52. Schön MR, Hunt CJ, Pegg DE, et al: The possibility of resuscitating livers after warm ischemic injury. Transplantation 1993; 56 (1): 24-31
53. Selkurt EE: Effect of acute hepatic ischemia on splanchnic hemodynamics and on BSP removal by liver. Proc Soc Exp Biol NY 1954; 87: 307-12
54. Sigel B: Partial hepatotectomy in the dog. Arch Surg 1963; 87. 100-3
55. Souza AP, Coelho ARB, Câmara-Neto RD, et al: modificação técnica para produção de necrosse hepática aguda em cães por isquemia vascular em dois estágios. Resultados preliminares. Anais da Facul-dade de Medicina, Centro de ciências da Saude-UFPE, Recife PE 1993; 38 (1): 39-45
56. Suehiro T, Boros P, Empre P, et al: Value of caval effluent in predicting early graft function after orthopic liver transplantation. Transplant Proc 1997; 29(1, 2): 469-70
57. Suzuki S, Toledo-Pereyra LH, Rodríguez FJ, et al: Neutrophil infiltration as an important factor in liver ischemia and reperfusion injury. Transplantation 1993; 53 (6): 1265-72
58. Swenson O, Grana L, Inouye T, et al: Immediate and long-term effects of acute hepatic ischemia. Arch Surg (Chicago IL,) 1967 Sep; 95: 451-63
59. Takemoto Y, Uchida M, Nagasue N, et al: Changes in calcium content, of the liver during hepatic ischemia-reperfusion in dogs. J Hepatol 1994;21 (5): 743-7
60. Tomizawa N, Ohwada S, Ohya T, et al: Effects of neutrophil elastase inhibitor on reperfusion injury in the canine liver. Transplant Proc 1996; 28 (3): 1767-8
61. Vollmar B, Glasz J, Leiderer R, et al: Hepatic microcirculatory perfusion failure is as determinant of liver dysfunction in warm ischemia-reperfusion. Am J Pathol (Philadelphia PA) 1994 Dec; 145 (6): 1421-31
62. Wu G, Tomei D, Bathurst IC, et al: Antia-poptotic compound to enhance hypothermic liver preservation. Transplantation 1997; 63 (6): 803-9
63. Yamanol A, Nagasue N, Kohno H, et al: Attenuation of ischemia-reperfusion injury of the liver in dogs by Cyclosporine. A comparative study with allopurinol and methilprednisolone. Transplantation 1991; 52: 27-30.
Correspondencia:
Prof. Edmundo Machado Fecrraz. Rua Dom Debastião Leme, 173/2501 – Graças. CEP-52011-160 – Recife-PE- Brasil. Fax (801) 271-1526 – Fone (081) 423-5394.

