J.C. RAMIREZ, MD, SCC, FRCSC; R. DUEÑAS, MD; R. BUITRAGO, MD, SCC.
El trasplante de órganos se convirtió en una realidad en 1976 con la aparición de la ciclosporina como agente inmunosupresor(1). En 1981 Reitz y col, en Stanford, llevaron a cabo con éxito el primer trasplante de corazón pulmón(2). En 1983, después de varios años de investigación clínica durante la década de los setenta,, el grupo de la Universidad de Toronto llevó a cabo exitosamente el primer trasplante bilateral en bloque, seguidos por el grupo de Toronto(4). Desde entonces el trasplante pulmonar aislado, uni o bilateral, se ha convertido utilizando para el tratamiento de algunos casos seleccionados de enfermedades terminales del pulmón(5).
No obstante los grandes avances obtenidos, el progreso del trasplante pulmonar durante los años siguientes se vio amenazado por la presencia de complicaciones como la dehiscencia de la anastomosis bronquial, la infección y el rechazo. Los grandes adelantos producidos en el curso de la última década se han traducido en criterios más adecuados de selección de donante y receptor, refinamiento de las técnicas quirúrgicas, mejores esquemas de inmunosupresión y disponibilidad de nuevos antibióticos, lo que ha permitido que el trasplante pulmonar sea ahora una opción terapéutica real, asociada con un incremento de la sobrevida y de la función pulmonar. Sin embargo, la aparición de rechazo crónico en forma de bronquiolitis obliterante constituye hoy día el factor limitante más significativo y la causa más importante de mortalidad tardía.
En la actualidad se consideran básicamente tres modalidades de trasplante pulmonar: unilateral, bilateral y de corazón pulmón.
Indicaciones:
Trasplante pulmonar unilateral (TPU):
Inicialmente este procedimiento se indicó en los pacientes con enfermedad pulmonar restrictiva (fibrosis pulmonar) de múltiples etiologías. En estos casos, la poca distensibilidad del pulmón nativo hace que la mayor parte de la ventilación y de la perfusión se dirija preferencialmente hacia el pulmón trasplantado, con la consiguiente mejoría de la función respiratoria. Posteriormente, su aplicación se extendió a los pacientes con efisema y otras formas de enfermedad pulmonar obstructiva crónica con excelentes resultados, particularmente en los pacientes de mayor edad y todos aquellos para quienes la cirugía bilateral entraña un elevado riesgo quirúrgico. El TPU está contraindicado en pacientes con efisema buloso por el riesgo de sobredistensión del pulmón contralateral, desviación del mediastino y comprensión del pulmón trasplantado. La EPOC constituye hoy día indicado este procedimiento en los pacientes con hipertensión pulmonar primaria o secundaria a defectos cardíacos congénitos con la corrección simultánea del defecto.
Trasplante pulmonar bilateral (TPB):
El TPB está indicado en la enfermedad pulmonar séptica (fibrosis quística y bronquiectasis). En estos casos se hace necesaria la remoción de ambos pulmones con el objeto de evitar la infección persistente e incontrolable en un paciente inmunosuprimido. Los pacientes con efisema buloso también requieren trasplante de ambos pulmones. El TPU está contraindicado en estos pacientes debido a que la mayor parte de la ventilación en el postoperatorio se dirige hacia el pulmón nativo, cuya distensibilidad/perfusión y conduce al atrapamiento progresivo de aire en el pulmón nativo, desviación del mediastino y compresión del pulmón trasplantado.
Trasplante de corazón-pulmón (TCP):
Los buenos resultados obtenidos con el trasplante pulmonar aislado y la escasez de donantes han limitado considerablemente la aplicación del trasplante cardiopulmonar a pacientes con enfermedad pulmonar terminal. Algunos centros todavía indican este procedimiento en pacientes con enfermedad pulmonar séptica, enfisema, hipertensión pulmonar y síndrome de Eisenmenger, mientras que otros lo reservan para aquellos casos con daño cardíaco irreversible asociado con la enfermedad pulmonar terminal. La mayoría de autores considera que esta última constituye la indicación fundamental del TCP:
Adicionalmente, en los pacientes que no tienen daño cardíaco irreversible, el trasplante bilateral tiene al ventaja de que evita un trasplante cardíaco innecesario y permite utilizar el corazón para un trasplante cardíaco en otro receptor. Algunos centros donde se practica activamente el TCP vienen utilizando el llamado procedimiento de “Dominó” que consiste en utilizar el corazón del receptor del TCP para un trasplante cardíaco en otro paciente.
Selección del Receptor:
En general, se consideran candidatos para trasplante pulmonar aquellos pacientes con enfermedad pulmonar terminal, cuya expectativa de vida no es mayor de otras enfermedades severas que afecten sistemas distintos al respiratorio o trastornos de tipo psicosocial.
Todos los pacientes son sometidos a una rigurosa evaluación de la función respiratoria, cardiovascular, hepática y renal, así como del estado nutricional. Además deben ser capaces de participar en un estricto programa de rehabilitación funcional pre y postoperatoria.
Inicialmente se consideraba que el antecedente de enfermedad maligna, al edad mayor de 60 años y el tratamiento con esteroides sistémicos eran contraindicaciones absolutas del procedimiento. En la actualidad estos criterios se han modificado y se consideran contraindicaciones relativas (Nomenclatura 1). El tipo de enfermedad pulmonar determina el procedimiento que debe llevarse a cabo.

Evaluación del Donante:
La disponibilidad de órganos constituye un aspecto crítico, especialmente cuando se trata de trasplante pulmonar. La selección del donante y el rescate adecuado del bloque pulmonar constituyen aspectos fundamentales para el éxito del programa. En Norteamérica, la demanda de órganos supera considerablemente la oferta y sólo 1 de cada 15 donantes potenciales satisface los criterios establecidos para la donación pulmonar.
Los criterios empleados para la selección del donante pulmonar son los siguientes: menos de 55 años de edad, ausencia de enfermedad pulmonar previa, radiografía torácica normal y una PaO2 mayor de 300 mmHg con una fracción inspirada de 02 de 1.0 y 5 cm H2O de PEEP. El examen endoscópico de las vías aéreas debe ser normal y no debe encontrarse secreciones pulmonares ni evidencia de broncoaspiración (comida, cuerpos extraños, partículas dentales).
Además de los criterios expuestos, debe existir compatibilidad de tamaño y grupo sanguíneo. Existen informes en la literatura que indican que los receptores de órganos provenientes de donantes con serologías incompatibles para citomegalovirus (CMV) tienen un riesgo elevado de presentar infecciones agudas por este agente en el postoperatorio, particularmente los receptores seronegativos de donantes seropositivos. Teniendo en cuenta que estas infecciones se asocian con una morbimortalidad elevada, algunos grupos consideran que los pacientes con serologías incompatibles no deben trasplantarse. Sin embargo, en la mayoría de los centros no consideran esta una contraindicación y han establecido protocolos especiales de profilaxis con agentes antivirales para prevenir el desarrollo de infección por CMV en estos pacientes. Adicionalmente, las serologías para VIH y hepatitis B deben ser negativas.
Preservación Pulmonar:
Inmediatamente después de la cirugía, el nuevo pulmón debe tener una función suficientemente buena para mantener la vida y permitir un intercambio gaseoso adecuado. En este caso no existe ningún mecanismo artificial que permita sustituir la función del pulmón trasplantado mientras el órgano se recupera.
En consecuencia, para lograr este objetivo el periodo de isquemia desde el momento del rescate hasta la implantación debe ser el mínimo posible. Con las técnicas actuales de preservación, el tiempo de isquemia no debe prolongarse por más de 6 horas.
Actualmente, ha podido demostrarse que tanto el trauma isquémico como el causado por la reperfusión afectan independientemente la función pulmonar. A pesar de casi tres décadas de investigación, no es mucho lo que se ha avanzado en el área de la preservación pulmonar y la mayor parte de las técnicas actualmente utilizadas continúan siendo empíricas. Parece existir acuerdo en que la isquemia hipotérmica es superior a la normotérmica, para el enfriamiento de los pulmones se ha utilizado la hipotermia tópica y la perfusión de la arteria pulmonar con una solución a 4° C. En algunos centros se utiliza la bomba de circulación extracorpórea para el enfriamiento del bloque pulmonar inmediatamente antes de su extracción. Con relación a las soluciones cristaloides y hasta el momento no se ha podido demostrar objetivamente una ventaja clara de una sobre otra.
La técnica de preservación más corrientemente utilizada consiste en la perfusión in situ de la arteria pulmonar con 3 litros de solución de Euro-Collins modificada, a la cual se han agregado 1.000 mcg de prostaglandina E1 (PGE1) y 300 mg de sulfato de magnesio. El bloque pulmonar es subsecuentemente extraído en su estado de insuflación y transportado inmerso en solución de Euro-Collins a 4° C(6).
Los futuros progresos en el área de la preservación pulmonar requieren un conocimiento detallado de los eventos que ocurren a nivel molecular y celular durante el período de isquemia y reperfusión, los que hasta el momento continúan siendo pobremente conocidos. Varios mediadores parecen actuar, entre los cuales cabe mencionar los radicales libres de O2, los metabolitos del ácido araquidónico y el calcio. No obstante, no ha sido posible determinar el papel de cada uno de ellos durante la isquemia y la reperfusión.
Técnica Quirúrgica:
Trasplante unilateral:
La técnica quirúrgica del TPU ha sido bien descrita(7). El paciente es colocado en decúbito lateral. Generalmente se selecciona para el trasplante el pulmón que recibe menos perfusión, de acuerdo con la gamagrafía de perfusión pulmonar. El muslo y la región inguinal deben prepararse e incluirse en el campo quirúrgico en caso de que se requiera circulación extracorpórea. El acceso al tórax se efectúa a través de una toracotomía posterolateral. Se procede a continuación a la liberación de adherencias pleurales y luego a la disección del hilio pulmonar, comenzando por las venas pulmonares, luego la arteria y finalmente el bronquio. Una vez terminada la disección del hilio, se procede al pinzamiento de la arteria pulmonar; si la presión de la arteria se mantiene estable y el intercambio gaseoso es adecuado, la cirugía puede continuarse sin circulación extracorpórea. Si, por el contrario, se produce hipertensión pulmonar y la oxigenación se deteriora, en este momento se coloca al paciente en circulación extracorpórea y se continúa con la neumonectomía, dejando muñones generosos de arteria y vena. La arteria se secciona distalmente al nacimiento de la primera rama. El bronquio es seccionado nivel del nacimiento del bronquio lobar superior puesto que esta maniobra priva al muñón bronquial de irrigación. (Figura 1).
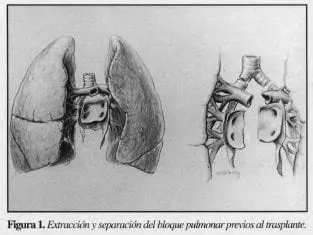
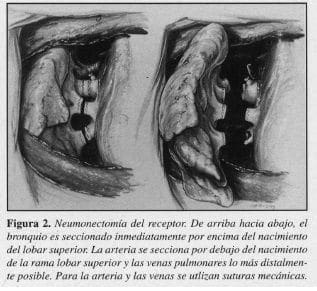
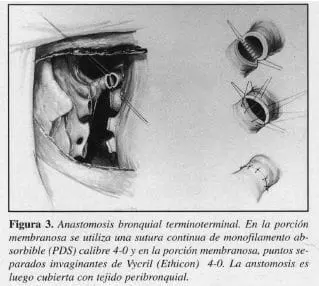
Simultáneamente, otro equipo quirúrgico se encarga de preparar el nuevo pulmón para la implantación (figura 2). Las anastomosis deben ser efectuadas en el siguiente orden: bronquio, arteria pulmonar y aurícula izquierda (Figuras 3 y 4). Esta secuencia evita la manipulación excesiva del pulmón y la utilización de clamps en el bronquio y a la vez permite la aireación de la circulación pulmonar a través de la anastomosis auricular antes de anudar las suturas.
 |
 |
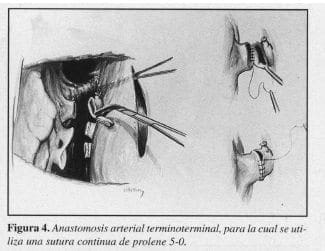
Desde el punto de vista técnico no hay mayor diferencia entre el lado derecho y el izquierdo. No obstante, en los casos que se requiere circulación extracorpórea, el lado derecho ofrece un acceso más fácil a la aurícula derecha para su canulación.
Trasplante bilateral:
La técnica del TPB ha sido significativamente modificada desde su descripción en 1987. Inicialmente esta operación era realizada a través de una esternotomía media, las anastomosis se efectuaban en la tráquea, el tronco principal de la arteria pulmonar y la aurícula izquierda y se requería circulación extracorpórea en todos los casos. El acceso actualmente utilizado en la mayoría de los centros anterolaterales unidas por una esternotomía transversa(8) (Figura 5). Esta incisión proporciona una excelente exposición de ambas cavidades pleurales, corazón y mediastino y una mejor hemostasia. La extracción de los pulmones y la posterior implantación de ambos órganos se efectúa en forma secuencial, a diferencia de la técnica inicialmente descrita en la cual se realizaba el trasplante en bloque de los dos pulmones.
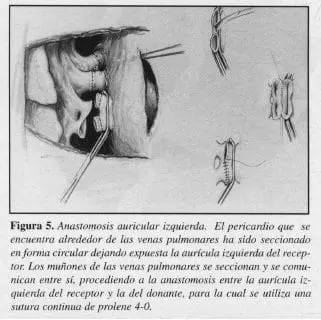
Esta técnica tiene la ventaja adicional de que en la mayoría de lo casos nos e requiere circulación extracorpórea, cuya necesidad depende de la severidad de la inestabilidad hemodinámica y el intercambio gaseoso durante el procedimiento.
Inmunosupresión:
En el curso del primer mes después de trasplante casi todos los pacientes experimentan dos o tres episodios de rechazo agudo. Se estima que 30 a 50% de los pacientes trasplantados desarrollan bronquiolitis obliterante dirigido hacia las vías aéreas.
Se han establecido múltiples protocolos con e objeto de prevenir el rechazo agudo y crónico. Actualmente, la mayoría de los centros de trasplante han establecido esquemas de inmunosupresión basados en tres drogas: ciclosporina A, azatioprina y esteroides. Estas drogas se administran inicialmente por vía endovenosa y luego por vía oral, tan pronto como el paciente esté en condiciones de tomar por esta vía(9) (Tabla 1).

Existe considerablemente controversia con relación al empleo de terapia citolítica (Globulina antilifocítica u OKT3). Estos agentes son utilizados por algunos grupos como terapia de inducción para prevenir el rechazo agudo. Se ha argumentado que el uso de terapia anticitolítica, particularmente el OKT3,s e asocia con un aumento en la incidencia de infecciones por CMV. Sin embargo, este concepto se desarrolló durante la época en que no se tenía en cuenta la serocompatibilidad de donante y receptor y los esquemas de profilaxis anti-CMV no eran utilizados en forma rutinaria(9).
En los primeros años se evitaba el uso de esteroides durante el postoperatorio inmediato, debido a que se pensaba que tenían un efecto adverso sobre la cicatrización bronquial. No obstante, hoy existe evidencia de que su adición puede ser benéfica, por cuanto disminuye inflamatoria e incrementa el flujo sanguíneo a la anastomosis bronquial.
Los episodios de rechazo se tratan con bolos de metilprednisolona, seguidos de un incremento de la dosis de esteroides orales.
Infección:
Las infecciones bacterianas, virales y micóticas continúan siendo la causa más importante de mortalidad y morbilidad en el paciente trasplantado(10). Con el objeto de disminuir su incidencia se han desarrollado varios esquema de profilaxis antibiótica, los cuales varían de acuerdo con la enfermedad de base, los cultivos de esputo en el donante y el receptor, los resultados de las serologías para CMV y los antecedentes de alergias. (Tabla 2).

Resultados:
Desde el punto de vista funcional, ambas modalidades de trasplantes se asocian con excelentes resultados funcionales, con incrementos significativos del VEF1 y la PaO2, que se han mantenido a través de los años en los pacientes que han permanecido libres de rechazo y de infección. Este incremento en las pruebas de función pulmonar se traducen en una dramática mejoría de la capacidad funcional y la tolerancia al ejercicio que han permitido a estos pacientes retornar a sus actividades normales, incluyendo la práctica de deportes. Como es de esperarse, el TPB se asocia con una mejoría más acentuada de las pruebas funcionales y del intercambio gaseoso; no obstante, este incremento no es significativo desde el punto de vista clínico, puesto que la tolerancia al ejercicio es similar en ambos tipos de procedimiento y sólo es evidente en pruebas máximas de ejercicio(11,12).
La enfermedad pulmonar obstructiva crónica es en la actualidad la indicación más frecuente de trasplante pulmonar. Para esta condición se han empleado el TPU y el TPB con excelentes resultados funcionales del TPU versus el TPB en esta enfermedad. Sin embargo, existe controversia con relación a los resultados funcionales del TPU versus el TPB en estado de enfermedad. Aunque los resultados funcionales evaluados en etapas tempranas del postoperatorio sugieren una mínima diferencia entre los dos procedimientos, el TPB parece ofrecer mejores resultados funcionales a largo plazo, que podrían contrarrestar el mayor riesgo quirúrgico asociado con este procedimiento, particularmente cuando se trata de pacientes jóvenes con efisema(9).
En los pacientes con enfermedad vascular pulmonar (hipertensión primaria y Eisenmenger) y aquellas que cursan con hipertensión pulmonar severa como la fibrosis pulmonar, se ha documentado una rápida recuperación de la función ventricular derecha con reducción de la poscarga del ventrículo derecho y cifras normales de presión en la arteria pulmonar. El empleo del TPU se ha asociado con la presencia de inestabilidad hemodinámica severa y cambios bruscos de la presión en la arteria pulmonar en el postoperatorio inmediato. Estas complicaciones son causadas por alteraciones severas de la relación V7Q, puesto que es 90 al 95% del gasto cardíaco se dirigen hacia el pulmón trasplantado mientras que el 50% de la ventilación se dirige hacia el pulmón nativo. Por este motivo, algunos grupos han tenido dificultades en la aplicación del TPU en pacientes con enfermedad vascular pulmonar y recomiendan el TPB en estos casos(13). El trasplante cardiopulmonar, que fuera inicialmente el procedimiento indicado en estos pacientes, continúa siendo practicado en algunos centros, especialmente en el Reino Unido.
De acuerdo con la información suministrada por el Registro Internacional de Trasplante Pulmonar, la sobrevida a 1 año para todos los trasplantes es del 70% y a 5 años es del 43%(14). Al analizar esta información es importante tener en cuenta que el Registro recoge los datos de todos los centros activos del trasplante y que muchos de ellos se encuentran todavía en sus curvas de aprendizaje, lo que puede disminuir las cifras. Algunos centros con la mayor experiencia como el de la Universidad de Washington han informado una mortalidad operatoria del 8% en 131 pacientes consecutivos y una sobrevida a 5 años cercana al 50% (15).
Las causas más frecuentes de mortalidad temprana, de acuerdo con la información del Registro Internacional, son las infecciones bacterianas y la falla primaria del injerto. Las complicaciones relacionadas con la anastomosis bronquial, frecuentemente observadas en los años iniciales como causa de mortalidad, hoy día se presentan con menor frecuencia (14).
Las causas más frecuentes de mortalidad tardía son la infección (29%) y el rechazo crónico manifestado en forma de bronquitis obliterante (28%). La mayor parte de las muertes debidas a infección ocurrieron como resultado de incrementos en los esquemas de inmunosupresión para el tratamiento del rechazo. La bronquitis obliterante constituye el mayor obstáculo para la sobrevida a largo plazo en los pacientes con trasplante pulmonar, por lo cual se requieren en el futuro nuevos agentes y mejores esquemas de inmunosupresión (14).
Abstract
Lung Transplantation
Organ transplantation became a reality with the advent, in 1976, of cyclosporine as an affective immunosuppressive agent (1). Reitz et al performed the first successful heartlung transplantation in 1981 at Stanford University (2). In 1983, following years of clinical investigation, the group at the University of Toronto achieved the first successful transplantation of the isolated lung (3). Three years later, Yacoub at al, in England, performed the first bilateral en bloc trasplant, closely followed by the Toronto group (4). Ever since, transplantation of the isolated lung has been utilized in the treatment of selected cases of terminal pulmonary disease (5). Despite major advances, the progress of lung transplantation in the ensuing years was interferred by complications such as dehiscense of the bronchial anastomosis, infection, and rejection. Major strides achieved over the past decade have led to better criteria for the selection of both donor and recipient, refinement of surgical techniques, better immunosuppressive schemes, and the availability for newer antibiotics, all of which are associated with an increment both in survival and pulmonary function. However, chronic rejection manifested by obliterating bronchiolitis, currently constitutes the most significant limiting factor and the most important cause of late mortality. There are three basic modalities of lung transplantation: unilateral, bilateral, and combined heart-lung.
Referencias
1. Borel JR, Feurer C, Magnee C, et al: Effects of the new antilymphocyte peptide Ciclosporin A in animals. Immunology 1977; 32: 1017-25.
2. Reitz BA, Wallwork JL, Hunt S A, et al: Heart-Lung transplantation: successful therapy for patients with pulmonary vascular disease. N Engl J Med 1982; 306: 557-64.
3. The Toronto Lung Transplant Group. Unilateral lung transplantation for pulmonary fibrosis. N Engl J Med 1986; 313: 1140-5.
4. Cooper JD, Patterson GA, Grossman R. Maurer J, and the Toronto transplant Group. Double lung transplantation for advanced chronic lung disease. Am Rev Respir Dis 1989; 139: 303-7.
5. Theodore J, Lewinston N: Lung transplantation comes to age. N Engl J Med 1990; 322:772-4.
6. Todd TR, Goldberg M, Koshal A, et al: Separate extraction of cardiac and pulmonary grafts from a single organ donor. Ann Thorac Surg 1988; 93:173-81.
7. Cooper JD, Pearson FG, Patterson GA, et al: Technique of successfull lung transplantation in humans. J Thorac Cardiovasc Surg 1987; 93:173-81.
8. Pasque MK, Cooper JD, Kaiser LR, et al: Improved technique for bilateral lung transplantation. Rational and clinical experience. Ann Thorac Surg 1990; 49:7985-91.
9. Patterson GA, Cooper JD: Lung Transplantation. In: Pearson FG, Deslauriers J, Ginsberg RJ, et al, (editors). Thoracic Surgery. Churchill Livingstone; 1995. p. 931..
10. Dauber JH, Paradis IL, Drummer JS: Infectious complications in pulmonary allografts recipients. Clin chest Med 1998; 11:291-308.
11. Ettinger NA: Single Lung Transplantation: Results. In: Patterson GA, Couraud L, (editors) Lung Transplantation. Current topics in General Thoracic Surgery: An International series. Elsevier Science BV; 1995.p. 363.
12. Patterson GA: Results of bilateral lung transplantation. In: Patterson GA, Couraud L (editors): Lung Transplantation. Current Topics in General Thoracic Surgery: An International series. Elsevier BV; 1995. p. 385.
13. Bando K: Current results and indications of single, bilateral and heart and lung transplantation for pulmonary hypertension. J Thorac Cardiovasc Surg 1994; 108; 6: 1056-65.
14. International Lung Transplant Registry. Jan 1997 (Medline).
15. Cooper JD, et al: Results of single and bilateral lung transplantation in 131 consecutive recipients. J. Thorac Cardiovasc Surg 1994; 107:460.
16. Quintero G. A: Manejo actual de la inmunosupresión. Rev Colomb Cirug 1990 jun; 5 (1 Esp.): 56-9.
Doctor Juan Camilo Ramírez. Grupo de Trasplante Pulmonar. Clínica Shaio – Bogotá, Colombia.
Doctores: Juan Camilo Ramírez, Rubén Dueñas y Ricardo Buitrago, Grupo de Trasplante pulmonar, Fundación Clínica Shaio, Santafé de Bogotá, Colombia.
