Casuística de la Fundación Santa Fe de Bogotá
E. LONDOÑO, MD, SCC; S. RESTREPO, MD, SCC; J. ESCALLON, MD, SCC, FACS, FRCS (C);
S. RODRIGUEZ, MD.
Palabras claves: Tumores de tejidos blandos, Sarcomas, Retroperitoneo, Cirugía retroperitoneal.
Los sarcomas retroperitoneales representan únicamente el 15% de todos los sarcomas de tejidos blandos. El 82% de ellos son malignos y un 40% son de origen linfoide. La presentación clínica más frecuente es la presencia de una masa de crecimiento lento, que a medida que el tamaño aumenta produce diversos síntomas principalmente por compresión. El diagnóstico usualmente se establece mediante ayudas diagnósticas como la tomografía axial computarizada y más recientemente la resonancia magnética.
Histológicamente se clasifican de acuerdo con el grado de diferenciación celular. El tratamiento de elección es la resección quirúrgica completa de la masa ya que la radioterapia y la quimioterapia no han dado buenos resultados.Presentamos la experiencia con este tipo de tumores en la Fundación Santa Fe de Bogotá.
Introducción
Los tumores retroperitoneales se manifiestan usualmente alrededor de la quinta década de la vida y la incidencia es igual tanto para hombres como para mujeres. En el 82% de los casos estos tumores son malignos; el 40% de éstos son de origen linfoide o desarrollados a partir de estructuras urogenitales, y el 55% son sarcomas. El 18% restante son tumores benignos (1). Los sarcomas de tejidos blandos representan un 1% de los tumores sólidos, y tienen una incidencia en la población general que varía entre 1 y 4 personas por cada 200.000 habitantes. De estos sarcomas únicamente un 15% se localiza en el retroperitoneo (1-3).
Métodos Diagnósticos
Diagnóstico clínico
En una serie acumulativa en la que se incluyeron 675 pacientes, la presentación clínica más frecuente (80-90%) fue la presencia de una masa no dolorosa. Un 40 a 70% de los pacientes acusan una sensación de “abombamiento” o un aumento del diámetro abdominal. Una tercera parte de ellos desarrollan signos y síntomas neurológicos debidos a compresión de una raíz nerviosa o a invasión directa de la médula espinal a través de los forámenes espinales. En sólo un lOa 15% se desarrolla ascitis o se presentan signos de obstrucción intestinal (1). En el 7% se observa pérdida de peso por encima del 10% del peso usual, en menos de l mes (4). Cuando ocurre necrosis tumoral, principalmente en masas de gran volumen y de crecimiento rápido, se puede presentar fiebre y leucocitosis. Si el tumor erosiona una víscera hueca, el paciente puede desarrollar una hemorragia digestiva en forma aguda o puede sangrar crónicamente. En muy raras ocasiones el paciente manifiesta hipoglicemia ya que algunos sarcomas pobremente diferenciados producen sustancias similares a la insulina o porque la actividad metabólica del tumor es muy alta y hay un gasto acelerado de las reservas de glucosa.
Como se aprecia, la sintomatología inicial en la mayoría de los pacientes es muy vaga y por esto no consultan tempranamente sino cuando el tumor ha alcanzado un tamaño considerable o cuando la infiltración del tumor afecta otros
órganos adyacentes (5).
Diagnóstico imaginológico
La tomo grafía axial computadorizada (TAC) es el método de elección en el estudio de los tumores primarios del retroperitoneo (Fig. 1). Estos se presentan generalmente como masas grandes, dado lo tardío de sus manifestaciones clínicas y el amplio espacio anatómico con que cuentan para crecer en el retroperitoneo. El liposarcoma retroperitoneal es el tumor maligno primario más frecuentemente desarrollado en este compartimiento. Friedman y col, mencionan cómo los liposarcomas pueden tener tres patrones escanográficos: sólido, quístico o pseudoquístico (6). En los Iiposarcomas pobremente diferenciados se identifica muy poca o ninguna grasa con la TAC, encontrándose coeficientes de atenuación mayores a las 20 UH.
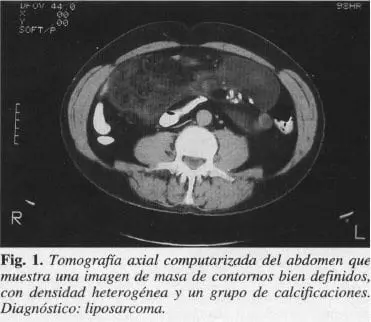
Las lesiones mixtas se presentan con áreas focales de baja densidad, con coeficientes de atenuación entre las -40 y -20 UH (Fig. 2). En el subtipo pseudoquístico, los tejidos sólido y graso promedian sus densidades creando áreas con densidades alrededor de O UH, las cuales dan un aspecto de zonas focales hipodensas que simulan lesiones quísticas de contenido líquido; ante la presencia de una masa retroperitoneal con coeficientes de atenuación negativos en la TAC, debe pensarse en la posibilidad de un liposarcoma.
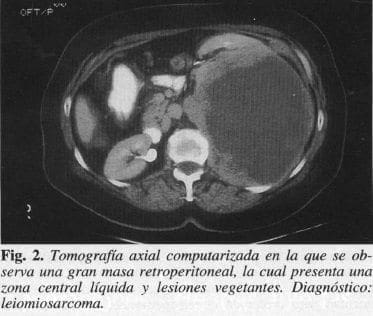
La TAC usualmente puede diferenciar un tumor primario de un linfoma. Los tumores retroperitoneales primarios tienden a tener una densidad heterogénea mientras que los linfomas habitualmente son homogéneos. Excepto el liposarcoma que posee las características específicas ya enunciadas, en los otros tipos de tumores retroperitoneales primarios no es posible diferenciar unos tipos histológicos de otros por imágenes diagnósticas. Todos tienden a producir masas grandes, extensas, de más de 10 cm de diámetro en el momento del diagnóstico, con características tisulares inespecíficas (7).
Los tumores retroperitoneales primarios se pueden originar en la grasa, en el tejido vascular o nervioso, en el tejido linfático o en remanentes embrionarios. Los estudios por imágenes diagnósticas son útiles para hacer el diagnóstico diferencial con tumores primarios de los riñones, páncreas o del tracto digestivo.
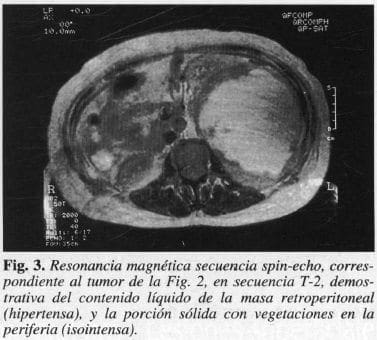
La resonancia magnética nuclear (RMN) no es suficientemente específica para lograr diferenciar la variedad histopatológica de la lesión, por cuanto se obtienen únicamente la morfología, la intensidad de la lesión o los tiempos de relajación tisular. La especificidad para el diagnóstico de estos tumores por RMN es del 24% (8) (Fig. 3). Los lipomas son de los pocos tumores en los que las lesiones se pueden caracterizar. Los liposarcomas presentan un aspecto variable tanto por RMN como por TAC, dependiendo de su contenido graso, matriz mucinosa y pleomorfismo celular. Se han informado liposarcomas sin grasa detectable imaginológicamente. Además, cuando los tumores retroperitoneales alcanzan un gran tamaño en el momento del diagnóstico, es imposible determinar el sitio o el órgano de origen de la masa. La TAC y la
ecografía, permiten además realizar una punción con aguja fina del tumor y de esta manera obtener material para estudio citológico (9).
Histología y estadificación
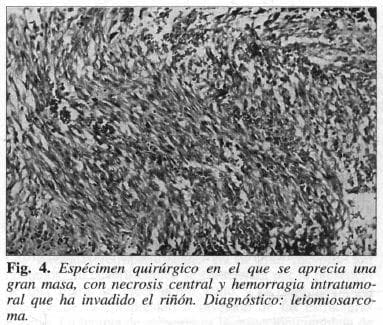
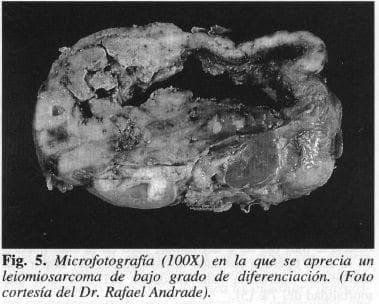
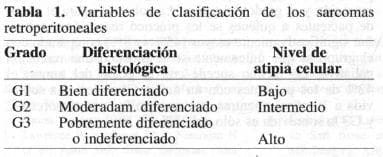
Los sarcomas retroperitoneales más frecuentes son los lipa sarcomas (23%) seguidos por los fibrosarcomas (19%) y los leiomiosarcomas (16%). Sinembargo, no es la variedad del tumor sino el grado de malignidad el que determina el pronóstico final del paciente (Fig. 4). Los sarcomas se clasifican por grados de acuerdo con el nivel de atipia celular, número de mitosis, presencia o no de necrosis y extensión de ésta. Los tumores grado 1 (G1) son los bien diferenciados; los grado 2 (G2) los de nivel intermedio o moderadamente diferenciados; y los grado 3 (G3) los pobremente diferenciados (Tabla 1) (Fig. 5). De acuerdo con su tamaño, los tumores se clasifican en TI «Scm), T2 (> S cm) y T3 que son los que invaden hueso, raíces nerviosas o estructuras vasculares (2). Actualmente, y como regla general, el grado histopatológico del tumor determina el estado. Los pacientes con tumores G 1 tienen un estado 1; aquellos con un tumor TI «S cm) se subclasificarían como un subestado A y los de mayor tamaño, como B. Los pacientes con metástasis linfáticas se clasificarían como un estado IV B (1). Otros autores aún prefieren utilizar la clasificación TNM para estos tumores (2).
 |
 |
Tratamiento
A. Quirúrgico
La tasa de resecabilidad de estos tumores es variable (SO a 7S%) (1, 2,4). Luego de una evaluación exhaustiva y establecido el diagnóstico, se debe proceder al tratamiento quirúrgico; sinembargo, en un S% de los casos no es posible confirmar un diagnóstico histológico eoperatorio, pero se debe realizar inicialmente una biop .a a cielo abierto. Durante este procedimiento es importante proteger los bordes de la herida quirúrgica; la porción más sólida del tumor debe aislarse del resto del campo operatorio y la cápsula del mismo se ircide cuidadosamente. Se obtiene una cuña de 1 a 2 cm de tejido y luego se procede al cierre de la cápsula. Es necesario prevenir el desarrollo de un hematoma intratumoral con lo que se evita la contaminación del medio circundante con células tumorales. Este tejido debe enviarse de inmediato para que el patólogo pueda tomar impresiones en fresco y luego proceder al estudio por congelación que, a pesar de que la muestra sea representativa, en algunos casos es imposible establecer el diagnóstiCo definitivo (1).
Cuando se ha decidido intervenir al paciente se debe utilizar una vía de acceso abdominal, bien sea por laparotomía mediana o por vía subcostal bilateral y, si es necesario, se puede ampliar la incisión mediante una toracotomía. Como se sabe, estos tumores son altamente vascularizados debido al gran número de vasos nutricios que los irrigan, en la mayoría de los casos a partir de la aorta, de la arteria renal o de las ramas musculares del psoas o del cuadrado lumbar; es necesario establecer, tan pronto sea posible, un control vascular del tumor sobre la línea media. Existen ciertas maniobras que se deben practicar para establecer la resecabilidad del tumor; la primera consiste en realizar una disección en el plano subadventicial a lo largo de la aorta y de la vena cava inferior que se extiende dorsalmente entre la columna vertebral y el plano de los músculos psoas y cuadrado lumbar; la segunda maniobra consiste en incidir el retroperitoneo lateralmente para obtener un plano de disección posterior a los procesos espinosos.
Si en este punto de la disección el cirujano puede tocar sus dedos a través de las disecciones sin que exista evidencia de tumor, éste se considera resecable. Si existe invasión a órganos vecinos se debe practicar, de ser posible, resección en bloque con la víscera comprometida (1). El riñón es el órgano que con mayor frecuencia se encuentra invadido por el tumor (46%), seguido por el colon, el páncreas, los grandes vasos y el bazo (2, 4, S). De acuerdo con Jaques y col, la resección en bloque con el órgano comprometido fue necesaria en un 83% de los casos. En el 53% de los pacientes se practicó la resección de un órgano adyacente, mientras que el 30% requirieron la resección de más de un órgano en el momento de la cirugía radical. En aproximadamente el 7% de los casos se encuentran metástasis sincrónicas con una incidencia similar tanto en el hígado como en el pulmón. En esta misma serie del MemorialSloan-Kettering Cáncer Center, los criterios de irresecabilidad en 43 pacientes fueron: invasión vascular, en el 43%; implantes peritoneales, en el 28%; metástasis a distancia, en el 19%; enfermedad extensa, en el 17%; invasión de la raíz del mesenterio, en el 8%; e invasión de la médula espinal, en el 6%. En este grupo de pacientes, el 63% tenía tumores de alto grado de malignidad, y un tamaño de más de 20 cm en el 60% de los casos (4). Se considera como cirugía paliativa aquella en la que puede resecarse más del 80% del tumor, pero en la cual quedan en la zona operada residuos microscópicos del tumor. La morbilidad operatoria está alrededor del 24% con una mortalidad del 7% (5).
B. Complementario
Los resultados del tratamiento complementario en este tipo de patología han sido pobres. En la actualidad se utilizan la quimioterapia, la radioterapia intraoperatoria en combinación con la radioterapia externa o esta última solamente, la terapia fotodinámica intraoperatoria y la hipertermia.
La utilidad de la quimioterapia aún está discutida. En un estudio prospectivo del Instituto Nacional de Salud en Bethesda, EE.UU, el uso de terapia coadyuvante con base en adriamicina y ciclofosfamida no mejoró ni la sobrevida ni el tiempo libre de enfermedad en este grupo de pacientes (11). Sinembargo, este esquema aún se utiliza como terapia adyuvante o de rescate.
La radioterapia intraoperatoria ha sido utilizada clínicamente pero tiene sus dificultades técnicas y sus limitaciones. Un estudio prospectivo de comparación entre el uso de radioterapia intraoperatoria (2.000 rads) conjuntamente con radioterapia externa (3.500-4.000 rads) frente al uso de sólo radioterapia externa (5.000-5.500 rads), no demostró ninguna diferencia significativa con respecto al tiempo de sobrevida, al tiempo libre de enfermedad, a la incidencia de recidiva local o al control del área del campo quirúrgico. Aunque disminuyó la incidencia de enteritis postirradiación en el grupo sometido a radioterapia intraoperatoria, la incidencia de neuropatía periférica fue mayor. Al considerar las dificultades técnicas de este método intraoperatorio y los pobres resultados, no parece ser una terapia indicada en este grupo de pacientes (4, 12). A pesar del uso de la radioterapia externa postoperatoria hasta 5.400 rads, el abdomen es el sitio de recidiva local en el 69% de los casos (12), lo cual es semejante a lo que sucede con pacientes que no reciben radioterapia en el postoperatorio (4-6, 13, 14).
La terapia fotodinámica intraoperatoria consiste en administrar al paciente un derivado de la hematoporfirina o dihematoporfirina en el preoperatorio. Durante la operación el área del tumor se expone y si no existen metástasis he páticas el tumor se reseca completamente. Al finalizar la operación se utiliza una lámpara de luz ultravioleta para buscar áreas de fluorescencia; si existen estas áreas se procede a resecar quirúrgicamente el tejido que macroscópicamente se observe fluorescente y luego se ilumina el campo operatorio con una fuente de luz de 630 nm con un poder de densidad de 50 a 200 um/cm2 durante 20 minutos hasta una dosis total de luz de 30 a 288 Joule/cm . El paciente luego del procedimiento debe protegerse del sol durante 4 semanas. A pesar de parecer un tratamiento prometedor aún no se conocen series con un número adecuado de pacientes para sacar conclusiones sobre su efectividad (15). En los últimos años se ha empleado la hipertermia como tratamiento complementario; sinembargo, aún los resultados son controvertidos y se requieren nuevos estudios aleatorios para confirmar su efectividad (16).
Recurrencia
La tasa de recurrencia del tumor es del 43 al 82%, incluyendo pacientes a quienes se les ha practicado una resección radical considerada como curativa (2). En la serie del Sloan-Kettering, el 49% de los pacientes a quienes se les había practicado una resección curativa, presentaban recurrencia local luego de un período de seguimiento de 31 meses. De este grupo de pacientes el 50% fueron sometidos a una nueva resección curativa, pero el 90% de ellos presentó una nueva recurrencia local (4). Haciendo una recopilación de las diferentes series, se acepta un índice de recurrencia local del 72% de los casos a 2 años y del 94% a 5 años (1-5).
Pronóstico
La sobrevida a 2, 5 y 10 años es del 56%, 34% y 18% respectivamente. Los únicos factores que intervienen en el pronóstico de estos pacientes son la extensión de la resección y el grado del tumor. La sobrevida para el grupo de pacientes a quienes se les practicó resección curativa, fue significativamente mayor (45% vs 8%) comparado con el grupo al que únicamente se le practicó una resección paliativa. Lo mismo sucede con el grado del tumor; el 42% de los pacientes con un tumor Gl tienen una sobrevida a 10 años, mientras que en aquellos con tumores G2 y G3 la sobrevida es sólo del 11% (1, 10).
Casuística de la Fundación Santa Fe de Bogotá
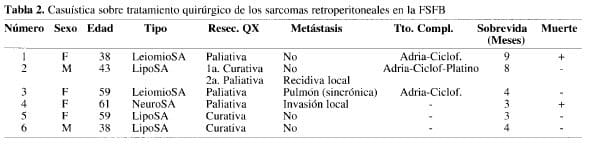
Durante los últimos 10 años, en la Fundación Santa Fe de Bogotá, han sido tratados 6 pacientes con sarcomas retroperitoneales, 5 de ellos en el último año; pero, como puede apreciarse, 1 paciente ya requirió una segunda intervención por recidiva local y en otra paciente a quien se le extirpó un leiomiosarcoma en bloque con el riñón izquierdo, se confirmaron metástasis pulmonares sincrónicas, y 1 año después se ha observado por TAC, recidiva local del tumor (Tabla 2).
Conclusiones
Los sarcomas retroperitoneales en su gran mayoría son malignos. Su cuadro clínico se caracteriza por la presencia de una masa de crecimiento lento y la sintomatología depende de la compresión o invasión de las estructuras vecinas. La terapia de elección es la resección completa de la masa, con lo cual mejora la sobrevida a 5 años.
Abstract
Retroperitoneal sarcomas represent only 15% of the soft tissue sarcomas. Eighty two percent to these are malig nant and 40% are lymphoid in orlgln. The most frecuent clinical presentation is the presence of a slow growing mass that, as it increases its size, produces diverse symptoms, primarly by compression of adjacent structures. The diagnosis is usual!y established by auxilliary diagnostic procedures such as Computarized Tomography and most recently Magnetic Resonance.
Histologically these tumors are classified according to its cell differentiation. The mnost indicated treatment is a complete resection of the mass; radiotherapy or chemotherapy have shown very poor results. The experience obtained with these type of tumors at the Fundación Santa Fe de Bogotá is presented.
Referencias
1.Slorm F K, Mahvi D M: Diagnosis and managemenl of retropcritoncal soft-tissue sarcoma. Ann Surg 1991; 214: 2-10
2. Dalton R R, Donohue J H, Mucha P el al: Management 01′ retropcritoneal sarcomas. Surgcry 1989; 106: 725-33
3. Lawrence W, Donegan W L, Natarajan N et al: Adult soft tissue sarcomas. Ann Surg 1987; 205: 349-59
4. Jaques D P, Coil D G, Hajdu S 1, Brennan M F: Managemenl of primary and recurrent soft-tissue sarcoma of the relroperiloneum. Ann Surg 1990; 212: 52- 9
5. McGrath P C, Neifeld J P, Lawrence W et al: lmproved survival following complete excision 01′ retroperiloneal sarcomas. Ann Surg 1984; 200: 200-4
6. Friedman A C, Hartman D S, Sherman J et al: Computed tomography 01′ abdominal fatty masses. Radiology 1981; 139: 415
7. Lane R H, Stephen D H, Reiman H M: Primary retroperitoneal neoplasms: CT findings in 90 cases with clinical and pathologic correlatio. AJR 1989; 152: 83-6
8. Kransforf M J, Jelinek J S, Moser R P et al: Soft tissue masses: diagnosis using MR lmaging. AJR 1989; 153: 541-7
9. Waligore M P, Stephens D H, Sou1e E H: Lipomatous tumors of the abdominal cavity: CT appearance and patho10gic correlation. AJR 1981; 137: 539-45
lO. Bevilacqua R G, Rogatko A, Hajdu S 1, Brennan M F: Prognostic factors in primary retroperitoneal soft-tissue sarcomas.Arch Surg 1991; 126: 328-34
1I. Glenn J, Sinde1ar W F, Kinsella T et al: Results of multimodality therapy of resectable soft-tissue sarcomas of the retroperitoneum. Surgery 1985; 97: 316-25
12. Kinsella T J, Sindelar W K, Lack E etal: Preliminary results of a randomized study of adjuvant radiation therapy in resectablc adult retroperitoneal soft tissue sarcomas. J Clin Oncol 1988; 6: 18-25
13. Cody H S, Tumbull A D, Fortner J G, Hajdu S 1: The continuing challange of retroperitoneal sarcomas. Cancer 1981; 47: 2147-52
14. Kara10usis C P, Vélez A F, Ernrich L J: Management 01′ retroperitoneal sarcomas and patient survival. Am J Surg 1985; 150: 376-80
15. Nambisan R N, Karakousis C P, Holyoke E D, Dougherty T J: lntraoperative photodynamic therapy 01′ retroperitoneal sarcomas. Cancer 1988; 61: 1248-52
16. Hirao1a M, Jo S, Akuta K etal: Radiofrequency capacitive hyperthermia for deep-seated tumors. Cancer 1987; 60: 121-7
Doctores: Eduardo Londoño, Santiago Restrepo, Jaime Escallón y Sandra Rodríguez, de los Departamentos de Cirugía e 1mágenes Diagnósticas de la Fundación Santa Fe de Bogotá, Bogotá, D.C., Colombia.

Buenos Dias una inquietud si el tumor es identificado en el retroperitoneo y el mismo tiene metastasis en higado y pulmones es posible la cirugia o solo el cuidado paliativo? gracias
Edwin buen día, este es un portal únicamente de consulta. No tenemos personal capacitado para dar respuesta a tu pregunta. Lo sentimos, feliz día!
Mi padre vive en Venezuela, quirúrgicamente no están preparados para realizar una operación de tumor retroperitoneal, me gustaría saber como presento el caso en un hospital o clínica en Colombia, necesita ser operado urgentemente. Toda información es de gran ayuda! gracias
Ariana lamentamos mucho tu situación, lamentablemente somos un portal de contenido, y no contamos con la respuesta a tu pregunta. Esperamos puedas solucionar, un saludo!
Mi señora fue diagnosticada con ca del endometrio despúes de una histerectomía,posteriormente a los once meses nueva cirugía encontrando gran tumor maligno en el retroperitoneo,falleciendo a los ocho meses de la última intervención.